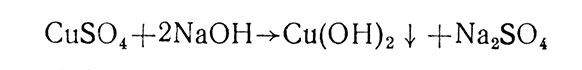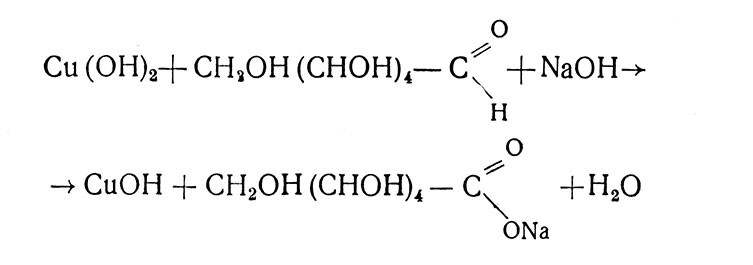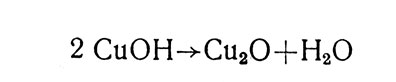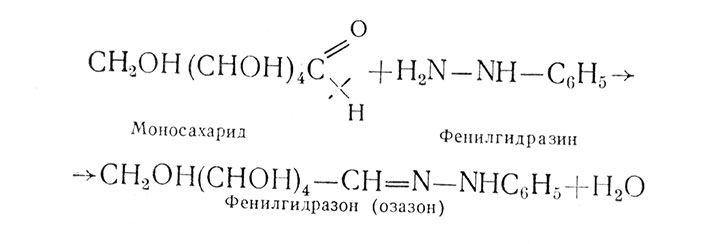какое соединение можно обнаружить реакцией троммера
Реакция Троммера
Качественные реакции на углеводы
Лабораторная работа №4
Многие качественные реакции углеводов основаны на восстанавливающих свойствах свободных карбонильных групп (свободного гликозидного гидроксила) сахаров. Эти же реакции применяются для большинства количественных методов определения углеводов.
Моносахариды обладают свойствами как спиртов, так и карбонильных соединений. При восстановлении карбонильной группы металлами (серебро, медь, висмут, железо и др.) в щелочной среде образуются многоатомные спирты. При окислении в первую очередь окисляется карбонильная группа, превращаясь в карбоксильную, а затем возможно окисление спиртовых гидроксилов. Металлы при этих реакциях восстанавливаются из окисной формы в закисную или даже до свободного состояния. На способности моносахаридов восстанавливать различные соединения основаны методы качественного и количественного определения моносахаридов.
Фруктоза также дает реакции восстановления металлов, хотя она имеет не альдегидную, а кетонную группу, которой не свойственно окисляться слабыми окислителями. Это объясняется тем, что в щелочной среде фруктоза легко превращается в глюкозу, которая и проявляет восстанавливающие свойства.
Определение содержания глюкозы в крови и обнаружение ее в моче играет важную роль в клиническом исследовании.
Дисахариды, имеющие свободный глюкозидный гидроксил (мальтоза, лактоза, целлобиоза), дают реакции восстановления металлов. Дисахариды сахароза и трегалоза, не имеющие свободного глюкозидного гидроксила, не дают этих реакций.
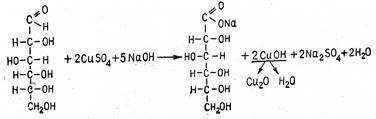
Реакция обусловлена окислением моносахарида и восстановлением гидрата окиси меди в гидрат закиси или закись меди. Схематично реакция может быть изображена следующим образом:
В пробирку наливают 1 мл раствора глюкозы и 1 мл 10% раствора гидроксида натрия. К смеси прибавляют при встряхивании по каплям 5% раствор сульфата меди до появления неисчезающей голубой мути гидроксида меди (II). Осторожно нагревают верхнюю часть содержимого пробирки. Появляется желтое окрашивание, характерное для гидроксида меди (I), переходящее в красное, характерное для оксида меди (I), что указывает на положительную реакцию Троммера.
Параллельно поставить ту же пробу с раствором фруктозы, сахарозы, мальтозы.
Избыток медной соли маскирует реакцию, так как гидроксид меди (II) при нагревании теряет воду и дает черный оксид меди (II).
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Проба Троммера: для чего используется и методика проведение
Проба Троммера – специфический метод определения наличия моносахаридов в жидкости.
Навигация по статье
Применение пробы Троммера
Проба применяется в медицинской диагностике для установления наличия глюкозы в моче.
Суть метода основана на реакции восстановления гидрата окиси меди при взаимодействии с сахаридами, открытой химиком А.К. Троммером. Ученому удалось установить, что моносахариды способны окисляться и образовывать кислоты, которые в свою очередь способны восстанавливать соли металлов. Такая реакция происходит благодаря наличию свободной кетоновой и альдегидной групп.
Проба Троммера активно применяется не только в медицине, но и в пищевой промышленности. С помощью этой реакции определяют наличие моносахаридов в молоке, различных пищевых жидкостях.
Проведение пробы Троммера
Суть пробы Троммера заключается в добавлении к биологической жидкости 10 капель щелочи (10%), после чего в пробирку добавляется раствор сульфата меди (2,5%), пока в пробирке не образуется мутно-голубой раствор, содержащий следы оксида меди в виде нерастворенного осадка. Полученную жидкость нагревают горелкой, не доводя до кипения и не сбалтывая содержимое пробирки.
Если в биологической жидкости присутствует сахар, то из голубого цвета при нагревании жидкость превратится в смесь желтого цвета, образуя из окиси меди гидрат закиси меди.
Возможно также образование красного оттенка содержимого пробирки при образовании Cu2О, а при избыточном содержании в смеси сульфата меди цвет может быть изменен на черный.
При недостаточном количестве CuS04 в растворе возможно образование бурого цвета жидкости в пробирке.
Реакция Троммера



Восстанавливающие свойства углеводов
Углеводы, в составе которых имеются свободные карбонильные группы, дают ряд реакций, основывающихся на окисляемости этой группы.
В основе реакции Троммера лежит окислительно-восстановительный процесс: в щелочной среде при нагревании альдегидная группа сахара окисляется, а гидрат окиси меди (осадок голубого или синего цвета) восстанавливается в гидрат закиси меди (кирпично-красный осадок).
Углевод при этом дает различные продукты окисления, так как при окислении в щелочной среде моносахариды претерпевают глубокие изменения с расщеплением углеродной цепи. Среди продуктов окисления не удается выделить кислоту с тем же числом атомов углерода, как у исходного сахара (в отличие от окисления обычных альдегидов). Сахара, не имеющие свободной альдегидной группы, пробу Троммера не дают.
Окислительно-восстановительную реакцию можно представить в виде следующей схемы:
Гидрат окиси окисления Гидрат закиси
меди (голубой осадок) глюкозы меди (желтый осадок)

Гидрат окиси окисления Закись меди
меди (голубой осадок) глюкозы (кирпично-красный осадок)
Реактивы: 0,5 %-ные растворы глюкозы, фруктозы, сахарозы, мальтозы и крахмала, 2 н раствор NaOH, 0,2 н раствор CuSO4.
Оборудование: пробирки, пипетки, спиртовка.
ХОД РАБОТЫ. В пробирку наливают раствора глюкозы и 6-8 капель 2н NaOH. Затем по каплям добавляют 0,2 н раствор CuSO4 до образования нерастворимого голубого осадка. Осторожно нагревают пробирку на спиртовке. Голубой, не растворимый в воде осадок гидрата окиси меди (II) постепенно переходит в желтый, а затем в красный осадок закиси меди (I). Это указывает на положительную реакцию Троммера.
Аналогичный опыт проводят с сахарозой, мальтозой, фруктозой и крахмалом. Делают заключение о восстанавливающих свойствах этих углеводов.
Избыток медной соли маскирует реакцию, так как гидроокись меди (II) при нагревании теряет воду и дает черный оксид меди (II).
Какое соединение можно обнаружить реакцией троммера
Реакция Троммера
Эта реакция основана на восстанавливающих свойствах свободных карбонильных групп сахаров. Такие группы имеются у всех моносахаридов, у большинства дисахаридов (например, мальтозы, лактозы, целлобиозы) и трисахаридов. В щелочной среде эти сахара восстанавливают металлы из окисной формы в закисную.
Такие дисахариды, как сахароза, в которых обе карбонильные группы связаны, а также полисахариды этой реакции не дают.
При реакции Троммера происходит восстановление окиси меди в закись. Для проведения этой реакции используется медный купорос и гидроокись натрия, которые при взаимодействии образуют гидрат окиси меди, вступающий в реакцию с сахарами:
При нагревании голубой гидрат окиси меди восстанавливается сахарами в желтый гидрат закиси меди:
Гидрат закиси меди при дальнейшем нагревании, теряя воду, переходит в красную закись меди, выпадающую в виде кристаллов:
Применение медного купороса и щелочи в этой реакции может привести к нежелательному образованию побочных продуктов, так как если сахара недостаточно, чтобы восстановить весь образовавшийся гидрат окиси меди, то его избыток разлагается (под действием нагревания) на окись меди и воду. Черные кристаллы окиси меди маскируют реакцию.
Этого недостатка реакции Троммера можно избежать, используя в качестве реактива фелингову жидкость, в которой ион двухвалентной меди находится в комплексном соединении с виннокислой солью (сегнетова соль).
1) 7%-ный раствор медного купороса.
2) 50%-ный раствор гидроокиси натрия или гидроокиси калия,
3) Фелингова жидкость.
Приготовление фелинговой жидкости. Раствор А: 20 г сегнетовой солю и 15 г гидроокиси натрия или гидроокиси калия растворить в 100 мл воды. Раствор Б: 4 г медного купороса растворить в 100 мл воды. Перед употреблением слить растворы А и Б в равных объемах (можно на предметном стекле).
Проведение реакции Троммера с медным купоросом и едкой щелочью
1. Поместить срез в 7%-ный раствор медного купороса на 1-5 мин (в часовом стекле).
2. Быстро ополоснуть водой.
3. Перенести срез на предметное стекло в кипящую каплю 50%-ного раствора гидроокиси натрия (или калия) и накрыть покровным стеклом.
4. Наблюдать появление коричнево-красных кристаллов закиси меди.
Проведение реакции Троммера с фелинговой жидкостью
1. Поместить срез в фелингову жидкость на предметное стекло и накрыть покровным стеклом.
2. Осторожно подогреть.
3. Наблюдать выпадение кристаллов закиси меди.
Результаты реакции (табл. 1)
Обе модификации этой реакции дают аналогичные результаты. В присутствии восстанавливающих сахаров появляются коричнево-красные кристаллы закиси меди.
После длительного кипячения дисахарид сахароза, гидролизуясь, превращается в моносахарид, и реакция начинается снова.
Препарат следует рассматривать в отраженном свете, так как выпавшие кристаллы непрозрачны.
При любом увеличении микроскопа видно, что эпидермис, паренхимные клетки листа капусты, а также живые клетки проводящих пучков забиты коричневыми кристаллами закиси меди. Так как клеточный сок, содержащий сахара, вытекает из разрезанных клеток, то кристаллы закиси меди легко перемещаются из одной клетки в другую, препятствуя установлению истинной локализации сахара. Однако, по-видимому, кристаллов в паренхиме пучков, флоэме и камбии несколько меньше, чем в паренхиме листа, где клетки особенно богаты клеточным соком.
Реакция с фенилгидразином (озазоновая) по Э. Фишеру
Преимуществом этой реакции по сравнению с вышеописанными является то, что она позволяет более точно установить локализацию сахара и, кроме того, различить вид сахара.
Определение основано на образовании кристаллов озазона при взаимодействии уксуснокислого фенилгидразина с моносахаридами. Уксуснокислый фенилгидразин получается при взаимодействии солянокислого фенилгидразина с уксуснокислым натрием. Реакция с уксуснокислым фенилгидразином протекает так:
Сахароза, предварительно превращенная в моносахарид нагреванием в глицерине, также дает эту реакцию.
Готовят два препарата из одного и того же материала. Чтобы отличить моносахариды от дисахаридов, один препарат оставляют при комнатной температуре, другой подогревают на водяной бане.
Если кристаллы озазона выпадают при 10-минутном подогревании или без подогревания в течение нескольких часов (дней), следовательно, в препаратах присутствуют моносахариды. При этом в течение первого часа реагирует фруктоза, глюкоза выявляется через несколько дней.
При более длительном нагревании препарата (около полутора часов) под воздействием глицерина происходит расщепление сахарозы на моносахара. Усиление реакции в этом случае указывает на присутствие сахарозы.
Форма выпадающих кристаллов озазона зависит от вида сахара, а также от условий реакции. При комнатной температуре озазон выпадает обычно в виде мелких сферокристаллов. При нагревании появляются золотисто-желтые игольчатые кристаллы, собранные в пучки, снопики, звезды, а также мелкие сферокристаллы.
Перед проведением реакции реактивы смешать в равных объемах (можно на предметном стекле). При приготовлении растворов оба вещества измельчить в порошок и растворить в глицерине на водяной бане в течение 1 ч. Реактивы хранить в темных склянках и в темноте.
1. На предметное стекло нанести каплю солянокислого фенилгидразина и добавить к ней каплю уксуснокислого натрия.
2. Поместить срез в реактив и накрыть покровным стеклом.
3. Один препарат оставить на холоде, другой поместить на водяную баню.
4. Наблюдать выпадение кристаллов озазона.
Результаты реакции (табл. 2, 3)
Без подогревания в листе капусты на 3-й день выпадают довольно мелкие сферокристаллы. Иногда их кристаллическая природа едва заметна и они имеют вид золотистых глыбок неправильной формы, например, при выпадении в мелких клетках пучка. Выпадение кристаллов без подогревания свидетельствует о наличии глюкозы во всех живых клетках листа капусты.
При кратковременном нагревании препарата также выпадают сферокристаллы и мелкие игольчатые кристаллы. После длительного нагревания количество выпадающих кристаллов увеличивается за счет сахарозы. Иногда удается обнаружить картины постепенного укрупнения сферокристаллов и перекристаллизации их в игольчатую форму. Размеры игольчатых кристаллов могут во много раз превышать диаметр клетки.
Разнообразие формы и размеров кристаллов озазона объясняется, по-видимому, трудностью создания совершенно одинаковых условий протекания реакции.
Таким образом, лист капусты содержит как моносахариды, так и дисахариды.
Опыт 22. Реакция Троммера



Благодаря наличию свободной альдегидной группы в молекуле лактозы (в остатке глюкозы) и мальтозы (у второго остатка глюкозы) эти дисахариды обладают восстанавливающими свойствами.
Опыт 23. Реакция на сахарозу
К 2 мл 2% раствора сахарозы приливают 1 мл 5% раствора NaOH. Далее к смеси добавляют 5 капель 2% раствора Co(NO3)2. Проделывают реакцию с глюкозой, лактозой. Наблюдают появление окраски и делают выводы. Написать реакции.
Опыт 24. Реакция Мальфатти на лактозу
К 1 мл 2% раствора лактозы прибавляют 2 капли 10% раствора NaOH. Далее к смеси приливают 0.5 мл концентрированного NH4OH. Пробирку помещают в водяную баню на 15 мин. Наблюдают окрашивание и делают выводы. Написать реакцию.
Опыт 25. Инверсия сахарозы
Реактивы: Сахароза, крахмал, инулин 1-2%-ные растворы, соляная кислота, концентрированная, едкий натр, 10-15%-ный раствор Реактивы для реакций Троммера, Бенедикта, Ниландера, Селиванова
ПОЛИСАХАРИДЫ
Опыт 26. Реакция крахмала с иодом
При взаимодействии крахмала с иодом образуется комплексное адсорбционное соединение, окрашенное в синий цвет. При нагревании окраска исчезает, но появляется опять при охлаждении, что свидетельствует об образовании нестойкого комплекса крахмала с иодом. Реакцией пользуются для выявления активности ферментов, гидролизующих крахмал. Окраску имеет комплекс йода с крахмалом, образование которого объясняют способностью молекул I2 помещаться в длинных полостях между витками спиралей, образованных молекулой крахмала. Полости заполнены плотно, и взаимодействия между молекулами достаточно сильны, чтобы обеспечить появление интенсивного окрашивания даже при очень низких концентрациях йода. Моносахариды и некоторые дисахариды, имеющие свободную карбонильную группу, обладают способностью восстанавливать в щелочной среде металлы из их оксидов. Этим свойством пользуются для обнаружения глюкозы в крови и моче. Привести структуру комплекса.
Опыт 27. Кислотный гидролиз крахмала.
В большую пробирку с пипеткой помещают 1 мл 0,1%-го раствора крахмала и 20 капель 2 н. раствора серной кислоты. Нагреть на водяной бане в течение 10 мин, отбирая пипеткой каждые 2 мин в маленькие пробирки 3-4 капли гидролизата и добавляя в них по 1 капле йода. Обратить внимание на изменение окраски гидролизата с йодом в ходе гидролиза. К последней пробе в большой пробирке добавить 2 капли 2 н. раствора сульфата меди, а затем добавлять по каплям 2 н. раствора гидроксида натрия до образования растворимого темно-синего соединения. О чем говорит эта реакция? Далее полученный раствор нагреть (реакция Троммера). Появляется желто-красное окрашивание (положительная реакция Троммера). О чем говорит эта реакция? По результатам реакций сделать заключение о строении крахмала.
Опыт 28. Выделение гликогена из печени.
Опыт 29. Разделение и идентификация углеводов с помощью бумажной хроматографии.