какое представление о строении атома верно большая часть массы атома сосредоточена
Презентация-тест по физике «Опыт Резерфорда. Строение атома»
Описание разработки
В опыте Резерфорда a-частицы рассеиваются
1. Электростатическим полем ядра атома
2. Электронной оболочкой атомов мишени
3. Гравитационным полем ядра атома
Ядро состоит из
1. Нейтронов и электронов
2. Протонов и нейтронов
3. Протонов и электронов
На основании исследования явления рассеяния альфа-частиц при прохождении через тонкие слои вещества Резерфорд сделал вывод, что
1. Альфа-частицы являются ядрами атомов гелия
2. Альфа-распад является процессом самопроизвольного превращения ядра одного химического элемента в ядро другого элемента
3. Внутри атомов имеются положительно заряженные ядра очень малых размеров, вокруг ядер обращаются электроны
Какое представление о строении атома соответствует модели атома Резерфорда?
1. Ядро – в центре атома, заряд ядра положителен, большая часть массы атома сосредоточена в электронах.
2. Ядро – в центре атома, заряд ядра отрицателен, большая часть массы атома сосредоточена в электронной оболочке.
3. Ядро – в центре атома, заряд ядра положителен, большая часть массы атома сосредоточена в ядре.
4. Ядро – в центре атома, заряд ядра отрицателен, большая часть массы атома сосредоточена в ядре.
В нейтральном атоме суммарный заряд электронов
1. Отрицательный и всегда больше по модулю заряда ядра
2. Отрицательный и равен по модулю заряду ядра
3. Положительный и равен по модулю заряду ядра
4. Может быть положительным или отрицательным, но равным по модулю заряду ядра.
Можно утверждать, что ядра атомов. А) являются мельчайшими неделимыми частицами материи. Б) имеют электрический заряд
Какое представление о строении атома верно большая часть массы атома сосредоточена
Опыты Э. Резерфорда по рассеянию α-частиц показали, что
А. почти вся масса атома сосредоточена в ядре.
Б. ядро имеет положительный заряд.
Какое (-ие) из утверждений правильно (-ы)?
Отзыв
Вопрос 2
Текст вопроса
Какое представление о строении атома соответствует модели атома
Резерфорда?
Отзыв
Ядро – в центре атома, заряд ядра положителен, бóльшая часть массы
атома сосредоточена в ядре.
Вопрос 3
Текст вопроса
Каков заряд ядра 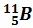
Отзыв
Вопрос 4
Текст вопроса
AFBCEA Какое представление о строении атома соответствует модели атома Резерфорда?
Отзыв
Вопрос 5
Текст вопроса
668ECF Какое представление о строении атома верно?
Бóльшая часть массы атома сосредоточена
Отзыв
в ядре, заряд электронов отрицателен
Вопрос 6
Текст вопроса
FD4549 Планетарная модель атома обоснована опытами по
Отзыв
рассеянию α частиц
Вопрос 7
Текст вопроса
964633 Планетарная модель атома обоснована
Отзыв
Вопрос 8
Текст вопроса
1A1499 На рисунке изображены схемы четырех атомов. Черными точками обозначены электроны. Атому B соответствует схема
Отзыв
Вопрос 9
Текст вопроса
5B3DFD В опыте Резерфорда a-частицы рассеиваются
Отзыв
электростатическим полем ядра атома
Вопрос 10
Текст вопроса
861E7A В опыте Резерфорда бóльшая часть α-частиц свободно проходит сквозь фольгу, практически не отклоняясь от прямолинейных траекторий, потому что
Отзыв
ядро атома имеет малые (по сравнению с атомом) размеры
Вопрос 11
Текст вопроса
C5B22F Какое представление о строении атома соответствует модели атома Резерфорда?
Отзыв
Вопрос 12
Текст вопроса
59E457 На рисунке изображены схемы четырех атомов. Черными точками обозначены электроны. Атому 6 4Be соответствует схема
Отзыв
Вопрос 13
Текст вопроса
(5C3EA3) Будем считать, что потенциальная энергия взаимодействия протона с электроном равна нулю, если расстояние между ними неограниченно велико. Тогда энергия взаимодействия ядра и электрона в атоме водорода
Какое представление о строении атома верно?
Какое представление о строении атома верно?
Бóльшая часть массы атома сосредоточена
1) в ядре, заряд электронов положителен
2) в ядре, заряд ядра отрицателен
3) в электронах, заряд электронов отрицателен
4) в ядре, заряд электронов отрицателен.
Заряд ядра атома магния + 12, а заряд ядра атома кальция + 20?
Заряд ядра атома магния + 12, а заряд ядра атома кальция + 20.
Определите, на сколько больше электронов в атоме кальция, чем в атоме магния.
В нейтральном атоме суммарный заряд электронов 1) положительный и равен по модулю заряду ядра 2) отрицательный и равен по модулю заряду ядра 3 )может быть положительным или отрицательным, но равным по?
В нейтральном атоме суммарный заряд электронов 1) положительный и равен по модулю заряду ядра 2) отрицательный и равен по модулю заряду ядра 3 )может быть положительным или отрицательным, но равным по модулю заряду ядра 4) отрицательный и всегда больше по модулю заряда ядра.
1. В ядре атома углерода содержится 12 частиц?
1. В ядре атома углерода содержится 12 частиц.
Вокруг ядра движутся 6 электронов.
Сколько в ядре этого атома протонов и сколько нейтронов?
(С решением пожалуйста) 2.
От атома гелия отделился один электрон.
Как называется оставшаяся частица?
Определить для атома натрия23, 11 зарядовое число, заряд ядра(в элементарных электрических зарядах), число электронов, массовое число ядра?
Определить для атома натрия23, 11 зарядовое число, заряд ядра(в элементарных электрических зарядах), число электронов, массовое число ядра.
В ядре атома олота 197 частиц, из них 118 нейтронов?
В ядре атома олота 197 частиц, из них 118 нейтронов.
Сколько протонов содержится в ядре золота и сколько электронов движется вокруг ядра этого атома?
Выразить заряд ядра золота в кулонах.
В атоме бора 5 электронов?
В атоме бора 5 электронов.
Б) Атом бора электрически нейтрален В) заряд атома отрицателен Г) Масса электронов составляет больше половины массы атома.
Определите число протонов в ядре атома бора и число электронов в атоме.
Суммарный заряд протонов в ядре нейтрального атома 1) отрицательный и равен по модулю суммарному заряду электронов?
Суммарный заряд протонов в ядре нейтрального атома 1) отрицательный и равен по модулю суммарному заряду электронов.
2)положительный и равен по модулю суммарному заряду электронов.
3) может быть положительным и отрицательным, но разным по модулю суммарному заряду электронов.
4) положительный и всегда больше по модулю суммарного заряда электронов.
Электронная оболочка электронейтального атома кислорода содержит 8 электронов?
Электронная оболочка электронейтального атома кислорода содержит 8 электронов.
Сколько протонов в ядре атома кислорода?
Каков заряд ядра атома кислорода& ;
Все нефтепродукты представляют собой смеси углеводородов. Среднюю плотность нефтепродукта определяют по правилу смешения и аддитивности : 30 / ро керосин + 70 / ро мазут = 100 / ро смесь тоесть V керосина + V мазута = V смесь.
P = Fv F = P / v F = 70000 / 20 = 3500 Н.
P = 600кПа = 600000Па g = 10Н / кг p(плотность) = 1000кг / м3 p = pgh h = p : gp h = 600000Па : 10Н / кг * 1000кг / м3 = 60м.
1) Упало в два раза (управление состояния при неизменной температуре : произведение давления на объём константа) 2) Увеличилось. Вода выталкивает брусок, брусок толкает воду, создаёт давление.
Тест «Физика атома и атомного ядра»
Ищем педагогов в команду «Инфоурок»
Физика атома и атомного ядра
А1. Какое представление о строении атома верно?
Большая часть массы атома сосредоточена в ядре, заряд ядра отрицателен
Большая часть массы атома сосредоточена в электронах, заряд электронов отрицателен
Большая часть массы атома сосредоточена в ядре, заряд электронов положителен.
Большая часть массы атома сосредоточена в ядре, заряд электронов отрицателен
А2. Чему равна величина заряда α-частицы.
13 протонов, 27 нейтронов
13 протонов, 14 нейтронов
27 протонов, 13 нейтронов
14 протонов, 13 нейтронов
А4. Что представляет собой β-излучение?
1. поток ядер водорода. 3. поток быстрых электронов.
2. поток ядер гелия. 4. поток квантов электромагнитного излучения.
3. Гравитационные, электростатические и ядерные.
4. Ядерные и гравитационные.
1. 236 Th 2. 234 U 3. 238 Am 4. 242 Cm
1. 235 Th 2. 239 Ra 3. 240 U 4 . 239 Np
А8. Какое определение соответствует понятию термоядерная реакция?
Способность некоторых ядер самопроизвольно превращаться в другие ядра, испуская при этом различные частицы.
Минимальная энергия, необходимая для полного расщепления ядра на отдельные нуклоны.
Устройство, в котором осуществляется управляемая цепная реакция ядерного деления.
Реакция слияния легких ядер, протекающая при очень высокой температуре.
А9. Какие вещества обычно используются в ядерных реакторах в качестве ядерного топлива?
1. уран, плутоний. 3. вода, графит.
2. кадмий, бор. 4. Бетон с железным наполнителем.
Физика атома и атомного ядра
А1. Какое представление о планетарной модели атома верно?
В центре атома ядро, состоящее из протонов и нейтронов, вокруг ядра вращаются электроны. Количество протонов рано количеству электронов.
Атом представляет собой шар, заполненный протонами, нейтронами и электронами в равных количествах.
В центре атома ядро, состоящее из протонов и электронов, вокруг ядра вращаются нейтроны. Количество нейтронов равно количеству электронов и протонов
Атом состоит из положительных протонов и такого же числа отрицательных электронов.
А2. Чему равна величина заряда β-частицы.
1 0 протонов, 2 2 нейтронов
1 2 протонов, 1 0 нейтронов
2 2 протонов, 1 0 нейтронов
1 0 протонов, 1 2 нейтронов
А4. Что представляет собой β-излучение?
1. поток ядер водорода. 3. поток быстрых электронов.
2. поток ядер гелия. 4. поток квантов электромагнитного излучения.
3. Гравитационные, электростатические и ядерные.
4. Ядерные и гравитационные.
1. 235 Th 2. 234 U 3. 238 Am 4. 242 Cm
1. 205 Hg 2. 83 209 Bi 3. 210 Pb 4. 210 Po
А8. Какое определение соответствует понятию радиоактивность?
Способность некоторых ядер самопроизвольно превращаться в другие ядра, испуская при этом различные частицы.
Минимальная энергия, необходимая для полного расщепления ядра на отдельные нуклоны.
Устройство, в котором осуществляется управляемая цепная реакция ядерного деления.
Реакция слияния легких ядер, протекающая при очень высокой температуре.
А9. Какие вещества обычно используются в ядерных реакторах в качестве теплоносителя?
1. уран, плутоний. 3. вода, жидкий натрий.
2. кадмий, бор. 4. Бетон с железным наполнителем.
Физика атома и атомного ядра
А1. Какое представление о строении атома соответствует модели Резерфорда?
Ядро в центре атома, большая часть массы атома сосредоточена в электронах, заряд ядра положителен
Ядро- в центре атома, большая часть массы атома сосредоточена в электронной оболочке, заряд ядра отрицателен.
Ядро- в центре атома, большая часть массы атома сосредоточена в ядре, заряд ядра положителен
Ядро- в центре атома, большая часть массы атома сосредоточена в ядре, заряд ядра отрицателен.
А2. Чему равна величина заряда γ-частицы.
А3. Чему равно число протонов и число нейтронов в изотопе кобальта 27 59 Со?
59 протонов, 27 нейтронов
32 протона, 27 нейтронов
27 протонов, 32 нейтрона
27 протонов, 59 нейтронов
А4. Что представляет собой γ-излучение?
1. поток ядер водорода. 3. поток быстрых электронов.
2. поток ядер гелия. 4. поток квантов электромагнитного излучения.
2. Электростатические и гравитационные.
3. Гравитационные, электростатические и ядерные.
4. Ядерные и гравитационные.
А6. Изотоп какого химического элемента образуется при α-распаде бериллия 242 Вк?
1. 236 Th 2. 234 U 3. 238 Am 4. 242 Cm
1. 235 Th 2. 239 Ra 3. 240 U 4 . 239 Np
А8. Какое определение соответствует понятию энергия связи?
Способность некоторых ядер самопроизвольно превращаться в другие ядра, испуская при этом различные частицы.
Минимальная энергия, необходимая для полного расщепления ядра на отдельные нуклоны.
Устройство, в котором осуществляется управляемая цепная реакция ядерного деления.
Реакция слияния легких ядер, протекающая при очень высокой температуре.
А9. Какие вещества обычно используются в ядерных реакторах в регулирующих стержнях?
1. уран, плутоний. 3. вода, графит.
2. кадмий, бор. 4. Бетон с железным наполнителем.
Курс повышения квалификации
Дистанционное обучение как современный формат преподавания
Курс профессиональной переподготовки
Физика: теория и методика преподавания в образовательной организации
Курс повышения квалификации
Современные педтехнологии в деятельности учителя
Тест по теме «Физика атома и атомного ядра» предназначен для проверки знаний учащихся девятых и одиннадцатых классов. Тест состоит из десяти заданий с выбором ответа и позволяет проверить знания по следующим вопросам:
Работа составлена в трех вариантах, поэтому один вариант можно разобрать всем классом, а два других для проверки знаний. Ответов нет: преподаватель физики без труда выполнить работу, а учащиеся не смогут найти ответы по Интернету
Номер материала: 439524
Международная дистанционная олимпиада Осень 2021
Не нашли то что искали?
Оставьте свой комментарий
Авторизуйтесь, чтобы задавать вопросы.
Безлимитный доступ к занятиям с онлайн-репетиторами
Выгоднее, чем оплачивать каждое занятие отдельно
В школе в Пермском крае произошла стрельба
Время чтения: 1 минута
В Приамурье начнут пускать на занятия только привитых студентов
Время чтения: 0 минут
Вузам Москвы и Подмосковья рекомендовали с 8 ноября ввести смешанный формат обучения
Время чтения: 1 минута
Жириновский предложил ввести в школах уроки полового воспитания
Время чтения: 1 минута
В Москве разработают дизайн-код для школ и детсадов
Время чтения: 1 минута
Роспотребнадзор продлил действие санитарных правил для школ
Время чтения: 1 минута
Подарочные сертификаты
Ответственность за разрешение любых спорных моментов, касающихся самих материалов и их содержания, берут на себя пользователи, разместившие материал на сайте. Однако администрация сайта готова оказать всяческую поддержку в решении любых вопросов, связанных с работой и содержанием сайта. Если Вы заметили, что на данном сайте незаконно используются материалы, сообщите об этом администрации сайта через форму обратной связи.
Все материалы, размещенные на сайте, созданы авторами сайта либо размещены пользователями сайта и представлены на сайте исключительно для ознакомления. Авторские права на материалы принадлежат их законным авторам. Частичное или полное копирование материалов сайта без письменного разрешения администрации сайта запрещено! Мнение администрации может не совпадать с точкой зрения авторов.
Строение атома
История открытия. Демокрит. Начала атомистики
Уже в древности философы задумывались, из чего же состоит природа вокруг них. Демокрит первым из античных ученых предположил, что все в мире состоит из крошечных неделимых частиц. Эту частицу он назвал атом, что в переводе с греческого означает «неделимый».
К сожалению, возможности ученых в те времена были весьма ограничены. Каких-либо приборов, позволяющих исследовать строение вещества, у них не было. Но значение Демокрита в зарождении атомистики невозможно сбросить со счетов истории.
Атомно-молекулярное учение. Строение атома
Практически до середины XVIII века, пока М.В. Ломоносов не принес в химию количественные эксперименты, учение об атомах оставалось лишь прерогативой философских размышлений. Михаил Васильевич считал, что лишь знание физических законов поможет правильно истолковать результаты химических опытов.
В своих исследованиях ученый выделил в веществе крупные частицы — «корпускулы», и мелкие — «элементы», или как мы называем их сейчас — атомы.
Ломоносов считал, что каждая молекула по своему составу идентична всему веществу, а также, что различные по химическому строению элементы имеют и разные по составу молекулы. Ученый предполагал, что вещества имеют особенности не только из-за отличий в составе молекул, но и благодаря различному расположению атомов в молекуле.
Следующий шаг в изучении атомов сделал английский естествоиспытатель Джон Дальтон. Проводя различные эксперименты с растворением газов в жидкостях, ученый открыл главное физическое качество атомов: эти мельчайшие частицы имеют вес. Но поскольку атом до сих пор никто не видел, Дальтон назвал вес частицы относительным. Он установил, что самым легким элементом является водород и предложил его вес принять за единицу.
Открытие Дальтона стало прорывом в химии. Ведь теперь к любому химическому соединению можно было подойти с измерительным прибором. Это исследование позволило приблизиться к современной записи химических формул и уравнений. И именно Дальтон придумал первые обозначения для известных химических элементов.
До конца XIX века, несмотря на все старания ученых, химическое строение атома по-прежнему оставалось лишь гипотезой.Ученым не хватало оборудования, чтобы постичь тайну мельчайшей частицы.
Открытие Дальтона дало толчок дальнейшим опытам, в ходе которых ученые вычислили относительную атомную массу разнообразных химических элементов, что позволило их классифицировать, а Д.И.Менделееву – сформулировать периодический закон и представить научному миру Периодическую систему химических элементов.
Протоны и нейтроны
Обнаружение катодных лучей немецким ученым-физиком Юлиусом Плюккером в 1859 году и создание прототипа электронной трубки Ульямом Круксом в 1879 году положили новый виток исследованиям в атомистике.
Однако потребовалось еще несколько десятков лет, чтобы строение атомов химических элементов приоткрыло свои тайны. на заре XX века в одном журнале появились две публикации, которые пытались объяснить структуру атома. Одна из публикаций принадлежала английскому ученому Д.Д. Томсону, автором другой был японский физик Хантаро Нагаока.
При создании своей атомной структуры Нагаока использовал разработанную Максвеллом в 1856 году теорию устойчивости колец Сатурна. Японский ученый был убежден, что опираясь на «сатурнианскую» модель ядра в будущих исследованиях, можно прояснить все основные свойства материи.
Исследователь ошибся, однако два постулата его теории впоследствии подтвердились:
Томсон выдвинул гипотезу о том, что атом напоминает шарообразную, электронейтральную сферу диаметром около 10 –10 м, где положительный заряд равномерно распределен по всей структуре атома, а электроны хаотично расположены в этом поле. Поэтому, можно сказать, что атом напоминает микроскопическую булочку с изюмом.
Опыты продолжались в разных странах. В лаборатории Резерфорда проходили испытания, которые смогли доказать, что в центре атома расположено крупное ядро с диаметром около —10 —15 м, в котором содержится более 99,95 % его массы, а заряд его положительный.
В 1932 году и Джеймс Чедвик обнаружил нейтрон — третий недостающий элемент атома.
Атомное взаимодействие обеспечивает тесную связь протонам и нейтронам в ядре атома. Протоны и нейтроны имеют общее название — нуклоны. Ученые считают, что их характеристики достаточно подобны, чтобы отнести эти частицы к одному семейству, как биологи относят в один вид собак и волков.
Казалось бы, вот оно – тайна ядра разгадана. Но нет, в современной физике считается, что нуклоны состоят из еще более мелких частиц, которые называют кварками, и кварковая модель является ведущей в современной науке.
Эксперименты по исследованию атома и его ядра не прекращаются, и в 2010 году международная группа физиков при исследовании протонов в мюонном водороде установила, что размер радиуса протона меньше на 4%, чем считалось до этого.
Так в фундаментальную физику ворвалась загадка протонного радиуса, почему измерение одной и той же величины в обычном и в мюонном водороде дает разные результаты — и, несмотря на усилия сотен специалистов, она до сих пор не решена.
Изотопы
Работая в лаборатории Резерфорда, Фредерик Содди экспериментально установил, что встречаются атомы одного химического элемента с различной атомной массой. А поскольку к этому времени уже было известно, что количество протонов для ядра постоянно, соответственно, отличались они количеством нейтронов.
Содди предложил термин изотоп (от греческих слов изос — «равный» и топос — «место») для обозначения веществ, идентичных по химическим свойствам, но отличающихся атомной массой и определенными физическими свойствами.
При графической записи изотоп выглядит как знак химического элемента, которому он соответствует. А что бы обозначить разницу, в массовом числе используют индекс слева вверху: ( 12 C, 222 Rn)
Протий, дейтерий, и тритий — исторические собственные названия изотопов водорода.
Электронное строение атома
Исследование таинственного микромира продолжается. Изучение движения электронов и внутриатомных взаимодействий выделилось в отдельную область физики — квантовую механику. Главный постулат квантовой механики — все волны обладают свойствами частиц, а микрочастицы имеют волновую природу.
В макромире физическое тело всегда находится в какой-то конкретной точке пространства. Даже если вы сфотографируете летящую муху и на фотографии она будет в виде черной полосы, вы все равно будете уверены, что в конкретный момент времени она была в определенном месте.
В мире атома все иначе. Легкий подвижный электрон находится одновременно во всех точках околоядерного пространства. Если провести аналогию с макромиром, больше всего это напомнит неплотный клубок мягкой пушистой шерсти.
И именно эта зона пространства, где существует вероятность встретить электрон, называется электронным облаком. Плотность электронного облака неравномерна.
В электронном облаке выделяют зону, где вероятность встречи с электроном более 90% — эта область обозначена как атомная или электронная орбиталь.
Все электроны в атоме обладают определенной энергией. Чтобы описать состояние электрона, ученые используют квантовые числа. Всего их четыре. Целое число n, которое определяет энергию электронов на конкретном энергетическом уровне, называют главным квантовым числом.
На одной электронной оболочке находятся атомные орбитали с единым значением главного квантового числа n.
У невозбужденного атома электроны расположены на орбиталях 4-х видов: s, p, d и f.
Но почему нельзя было обозначить буквами по алфавиту a, b, c? Все не так просто, для обозначения атомных орбиталей ученые решили использовать начальные буквы от прилагательных, описывающих спектральные линии в атомных спектрах:
Чтобы графически представить расположение электронов на уровнях и подуровнях атомной оболочки, ученые ввели электронные формулы. Это такие численно-буквенные комбинации, где подуровень обозначен строчной латинской литерой, а цифровой индекс вверху справа обозначает количество электронов на подуровне.
Несмотря на свои способности быть одновременно в любой точке пространства, электроны при заполнении орбиталей соблюдают определенный порядок:
У этого правила есть еще одно мнемоническое название — правило троллейбуса. Расположение электронов напоминает рассадку в общественном транспорте. Если есть свободные места и человек входит один, он сядет на свободное сиденье, и только если нет свободных сидений, подсядет к кому-то на свободное место.
Итак, подведем выводы, на которые ученым понадобилось более сотни лет опытов, исследований, научных дискуссий и даже трагедий.
Чтобы проверить насколько хорошо усвоен материал, предлагаем вашему вниманию тест на тему «Строение атома» для 8-11 классов:





















