Какое количество синапсов может образовывать один нейрон
Неврология. Общие данные. Нейрон. Нейроцит. Синапс.
Одним из основных свойств живого вещества является раздражимость. Каждый живой организм получает раздражения из окружающего его мира и отвечает на них соответствующими реакциями, которые связывают организм с внешней средой. Протекающий в самом организме обмен веществ в свою очередь обусловливает ряд раздражений, на которые организм также реагирует. Связь между участком, на который падает раздражение, и реагирующим органом в высшем многоклеточном организме осуществляется нервной системой.
Проникая своими разветвлениями во все органы и ткани, нервная система связывает все части организма в единое целое, осуществляя его объединение, интеграцию.
Следовательно, нервная система есть «невыразимо сложнейший и тончайший инструмент сношений, связи многочисленных частей организма между собой и организма как сложнейшей системы с бесконечным числом внешних влияний» (И. П. Павлов).
Основным анатомическим элементом нервной системы является нервная клетка, которая вместе со всеми отходящими от нее отростками носит название нейрона, или нейроцита. От тела клетки отходят в одну сторону один длинный (осевоцилиндрический) отросток — аксон, или нейрит, в другую сторону — короткие ветвящиеся отростки — дендриты.
Передача нервного возбуждения внутри нейрона идет в направлении от дендритов к телу клетки от нее к аксону; аксоны проводят возбуждение в направлении от тела клетки. Передача нервного импульса с одного нейрона на другой осуществляется посредством особым образом построенных концевых аппаратов, или синапсов (от греч. synapsis — соединение). Различают аксосоматические связи нейронов, при которых разветвления одного нейрона подходят к телу клетки другого нейрона, и филогенетически более новые аксодендритические связи, когда контакт осуществляется с дендритами нервных клеток.
Какое количество синапсов может образовывать один нейрон
Цитоархитектоника головного мозга человека организована таким образом, что более чем 10 млрд. нервных клеток, занимая относительно небольшое пространство и будучи сформированными в специализированные структуры, обеспечивают специфические функции мозга, связанные с восприятием, переработкой и проведением информации, в соответствии с которой осуществляется взаимодействие организма с внешней средой на основе высокой нейрональной специфичности и пластичности.
Основной структурной единицей нервной системы является нейрон. Различные типы нейронов дифференцируются по величине и форме тела клетки, а также по длине и степени ветвистости ее отростков.
Клеточное тело по своим размерам варьирует очень широко — от 5 до 100 мкм в диаметре. Оно содержит следующие органеллы: ядро, митохондрии, эндоплазматический ретикулум (гладкий и шероховатый), расположенные на цистернах эндоплазматического ретикулума и в свободном пространстве рибосомы и полисомы, комплекс Гольджи и различные внутриклеточные включения (гранулы гликогена, липидные капли, скопления частиц пигмента в особых нейронах и др.), везикулы, а также лизосомы. Группы параллельно расположенных цистерн шероховатого эндоплазматического ретикулума в виде ограниченных мембраной удлиненных цистерн с прикрепленными к ним рибосомами образуют субстанцию (тельца) Ниссля (тигроидное вещество). В цитоплазме имеются также нейрофиламенты и нейротрубочки (рис. 3).
Все перечисленные ультраструктурные органеллы клетки несут определенные функции. Ядро является субстратом основных генетических процессов в клетке. Митохондрии обеспечивают энергетический обмен — в них происходит окислительное фосфорилирование, приводящее к продукции энергии в виде молекул АТФ. Эндоплазматический ретикулум с прикрепленными на его цистернах рибосомами, а также свободно расположенные рибосомы и их комплексы (полисомы) имеют отношение к белковому обмену и синтетическим процессам в клетке. Лизосомам приписывается обменно-выделительная роль. Нейротрубочки и нейрофиламенты обеспечивают транспорт внутриклеточных веществ, имеющих отношение к проведению нервного импульса. Долгое время считали, что комплекс Гольджи, состоящий из параллельно расположенных цистерн и скоплений пузырьков на их концах, выполняет неопределенные обменно-выделительные функции. Хотя об этом комплексе известно далеко не все, привлекают к себе накопленные многими исследователями данные, свидетельствующие о том, что он играет главную роль в процессах обновления клеточной мембраны и ее генетически обусловленной специализации. Известно, что в комплексе Гольджи может происходить первичная сборка специализированных участков мембраны (рецепторов), которые в виде пузырьков транспортируются к наружной клеточной оболочке и встраиваются в нее. Такие исследования были обобщены А.А.Милохиным (1983).
От тела нейрона отходят основной отросток — аксон и многочисленные ветвящиеся отростки — дендриты. Длина аксонов различных нейронов колеблется от 1 мм до почти 1 м (нервное волокно). Вблизи окончания аксон разделяется на терминали, на которых расположены синапсы, контактирующие с телом и дендритами других нейронов. Синапсы вместе с нейрофиламентами и нейротрубочками являются субстратом проведения нервного импульса.

Рис. 3. Основные ультраструктурные компоненты нейрона.
Л — лизосомы; ШЭР — шероховатый эндоплазматический ретикулум (цистерны с прикрепленными рибосомами); М — митохондрии; НФ — нейрофиламенты; НТ — нейротрубочки; P — рибосомы; П — полисомы (комплексы рибосом); КГ — комплекс Гольджи; Я — ядро; ЦЭР — цистерны эндоплазматического ретикулума; ЛГ — липидные гранулы; ЛФ — липофусцин.
Кроме нейронов, в ткани мозга имеются различные виды глиальных клеток — астроглия, олигодендроглия, микроглия. Астроглия играет большую роль в обеспечении функции нейрона и формировании реакции мозговой ткани на вредоносные воздействия (инфекция, интоксикация и др.) — принимает участие в воспалительных процессах и ликвидации их последствий (заместительный глиоз). Олигодендроглия, как известно, обеспечивает миелинизацию нервного волокна и регулирует водный обмен (дренажная глия). Функции микроглии не до конца изучены, но ее значение подчеркивается размножением этих клеток при некоторых специфических процессах (участие в формировании сенильных бляшек; существует предположение о выработке микроглиальными клетками амилоидных фибрилл и т.п.).
Особые клеточные структуры характерны для желудочковых поверхностей головного мозга и его сосудистого сплетения. Желудочковая поверхность мозга покрыта клетками эпендимы с многочисленными микроворсинками и ресничками, принимающими участие в ликворообращении; сосудистое сплетение представлено «гроздьями» ворсинок, состоящих из капилляров, покрытых эпителиальными клетками. Их основная функция связана с обменом веществ между кровью и цереброспинальной жидкостью.

Типичный синапс состоит из пресинаптической терминали, постсинаптической области и расположенной между ними синаптической щели. Пресинаптическая терминаль является окончанием аксона. Она содержит нейрофиламенты, нейротрубочки, митохондрии и синаптические пузырьки, скопления которых видны около пресинаптической мембраны. Через последнюю переносятся содержащиеся в пузырьках нейротрансмиттеры. Постсинапс характеризуется наличием постсинаптического утолщения. Постсинаптическое утолщение представлено мембраной клетки с расположенными на ней рецепторами, входящими в структуру самой мембраны. Синапс представлен на рис. 4, а его электронно-микроскопическая картина на рис. 5.

Синапс может быть расположен на теле (соме) клетки — аксосоматический синапс, на дендрите — аксодендритный, на шипике дендрита — аксошипиковый (рис. 6) и на аксоне другой клетки — аксо-аксональный. Аксошипиковые синапсы несколько отличаются по своему строению от типичного синапса, что определяется строением шипика, имеющего в составе постсинапса особый шипиковый аппарат.
Взаимодействие пресинапса и постсинапса обеспечивается благодаря переносу нейротрансмиттера через синаптическую щель. Выделяясь из пресинапса, нейротрансмиттер (медиатор) может связываться с рецептором постсинаптической мембраны, инактивироваться в синаптической щели и частично вновь захватываться пресинаптической мембраной (процесс обратного захвата — reuptake ). Если рецептор постсинаптической мембраны заблокирован, то возможны оба последних процесса, а также избыточное накопление медиатора и связанное с этим развитие гиперчувствительности рецепторов (см. рис. 4).
Более подробно эти процессы рассматриваются в разделе «Нейрохимические системы мозга».
Рецепторы нейронов — это белковые структуры, расположенные на внешней поверхности мембраны клеток. Они способны «распознавать» и связывать биологически активные вещества — нейротрансмиттеры, различные эндогенные вещества, а также экзогенные соединения, в том числе психофармакологические средства. Соединения, которые могут связывать рецепторы, называются лигандами. Лиганды бывают эндогенными и экзогенными.
Распознавание лиганда рецептором обеспечивается специальными структурными элементами, или сайтами. Специфичность связывания лиганда происходит благодаря структурному соответствию молекул лиганда и рецептора, когда они подходят друг к другу по типу «ключ к замку». Реакция связывания является моментом запуска каскада внутриклеточных реакций, приводящих к изменению функционального состояния нейрона. В зависимости от «силы» и «прочности» связывания лиганда с рецептором употребляют понятие аффинности (сродства) лиганда по отношению к рецептору.
При связывании рецептора с лигандом может происходить как активация, так и блокада рецептора. В связи с этим говорят об агонистах и антагонистах рецепторов, а также о частичных агонистах (рис. 7).
Максимальную эффективность в отношении активации рецептора имеет полный агонист, минимальную (практически нулевую) — антагонист. Между ними находятся вещества, называемые частичными агонистами. Последние действуют значительно мягче, чем полные агонисты. Частичные агонисты, кроме того, занимая определенное пространственное положение в молекуле рецептора, могут предотвращать избыточное действие полного агониста, т.е. действуют частично как антагонисты. В этом случае употребляют понятие агонист/антагонист.
Высокой аффинностью могут обладать как агонисты, так и антагонисты рецептора. Агонист активирует рецептор, вызывая соответствующий физиологический эффект, в то время как антагонист, связываясь с рецептором, блокирует его и предотвращает развитие физиологического эффекта, выявляемого агонистами. Примером антагонистов могут служить нейролептики, которые предотвращают эффекты дофамина на уровне дофаминового рецептора.
При связывании лиганда с рецептором происходит изменение конфигурации последнего (рис. 7).
Многие вещества, как эндогенные, так и экзогенные, реагируют не с одним, а с несколькими типами рецепторов — «семейством» их, которое подразделяется на отдельные типы. Примером могут служить многие нейротрансмиттеры, реагирующие с несколькими типами специфических рецепторов (например, Д1—Д5-типы дофаминовых рецепторов). Существование нескольких рецепторов к одному лиганду носит название гетерогенности рецепторов.
Представление о функции рецепторов было бы неполным, если не представить внутриклеточные процессы, развивающиеся после связывания рецептора соответствующим веществом, и механизмы, обеспечивающие трансформацию внешнего сигнала в процессы, приводящие к появлению нервного импульса. Связывание лиганда с рецептором может приводить либо непосредственно к открытию (или закрытию) соответствующих ионных каналов (см. рис. 7), либо к активации вторичных мессенджерных систем (в качестве первичного мессенджера рассматривается вещество, реагирующее с рецептором).


Позднее были открыты и другие вторичные мессенджеры. Сейчас выделяют среди них 3 класса: 1) циклические нуклеотиды (цАМФ, циклический гуанозинмонофосфат — цГМФ); 2) ионы кальция (Са 2+ ); 3) метаболиты фосфолипидов — инозитол-1,4,5-трифосфат (1Р 3 ), диглицерин (ДАГ), арахидоновую кислоту. В отличие от других вторичных мессенджеров Са 2+ транспортируется в нейрон из внутриклеточного пространства.
Строение нейрона и синапса
Нейроны — главные кирпичики нервной системы. Их основная функция — передача сигналов по маленьким соединениям (синапсам). Хотя нейроны бывают разных видов, их строение и функции в целом схожи между собой.
Наш мозг — это приблизительно полтора килограмма ткани, которая содержит порядка 1,1 триллиона клеток, в том числе 100 миллиардов нейронов. В среднем каждый нейрон образует около пяти тысяч соединений с другими нейронами — так называемых синапсов.
Клеточное тело нейрона выпускает отростки, которые называются дендритами. Они получают нейромедиаторы от других нейронов (некоторые нейроны взаимодействуют друг с другом через электрические импульсы.)
Давайте представим один типичный нейрон. Он выделяет нейромедиатор под названием серотонин.
Этот маленький нейрон является частью нервной системы, но и сам по себе он — сложная система, для работы которой требуется взаимодействие нескольких подсистем. Когда нейрон возбуждается, усики на кончиках его аксонов вбрасывают молекулы на синапсы — соединения, которые наш нейрон создал с другими нейронами.
Если же это синапсы-получатели, то через них нейрон получает от других нейронов сигналы (обычно в форме химических элементов, которые называют нейротрансмиттерами). Сигнал указывает нейрону, возбуждаться или нет.
Возбуждение нейрона зависит в основном от сочетания сигналов, получаемых в каждый конкретный момент. Когда же нейрон возбуждается, он начинает по синапсам посылать сигналы другим нейронам, передавая им сообщение: возбуждаться или нет.
Обычный нейрон возбуждается 5–50 раз в секунду. За время, которое потребуется вам на прочтение этого текста, у вас в голове будут переданы в буквальном смысле квадриллионы сигналов.
На каждом нейроне порядка двухсот небольших пузырьков, везикул, полных серотонина. Каждый раз, когда нейрон возбуждается, открываются от пяти до десяти везикул. Если в среднем нейрон возбуждается десять раз в секунду, каждый усик опустошается раз в несколько секунд.
Как следствие, маленькие молекулярные машинки должны либо производить новый серотонин, либо перерабатывать свободный серотонин, который плавает вокруг нейрона. После этого им нужно построить везикулы, наполнить их серотонином, довести до места действия на кончике каждого отростка.
Согласитесь, здесь не обойтись без поддержания баланса между многими процессами, а значит, многие процессы могут пойти не так. И не будем забывать, что метаболизм серотонина — это лишь одна система из тысяч, функционирующих в вашем теле.
Сильно упрощая, можно сказать, что общее возбуждение нейрона зависит от суммы всех возбуждающих и тормозящих сигналов, которые он получает в каждую миллисекунду.
Когда нейрон возбуждается, по его аксону (отростку, по которому передаются сигналы) проходит электрохимическая волна. Она высвобождает нейротрансмиттеры, которые попадают на синапсы к нейронам-получателям и вызывают либо торможение, либо возбуждение.
Скорость передачи нервных сигналов увеличивается благодаря миелину — жировой субстанции, изолирующей аксоны.
Серое вещество мозга по большей части состоит из клеточных тел нейронов. В состав белого вещества входят аксоны и глиальные клетки.
Глиальные клетки осуществляют метаболическую поддержку — способствуют образованию миелиновой оболочки на аксонах и перерабатывают неиспользованные нейромедиаторы.
Функционально клеточные тела нейронов похожи на сто миллиардов переключателей «Вкл./Выкл.», соединенных проводами-аксонами в сложнейшую сеть прямо в вашей голове.
Каждый нервный сигнал — это бит информации. Нервная система перемещает информацию по вашему организму так же, как сердце качает кровь.
Количество возможных комбинаций возбуждения или торможения сотни миллиардов нейронов составляет 10 в миллионной степени (то есть единица и еще миллион нулей). По сути, это и есть число возможных состояний вашего мозга. Чтобы лучше понять значение этого числа, сравним его с количеством атомов во Вселенной — «всего лишь» десять в восьмидесятой степени.
Сознательные психические события основываются на временных комбинациях синапсов, которые формируются и распадаются (обычно в течение пары секунд), как вихри в потоке. Также нейроны способны создавать долгосрочные нервные цепи, соединения в которых усиливаются каждый раз, когда происходит определенная психическая активность.
Richard Mendius, Rick Hanson. The Practical Neuroscience of Happiness, Love & Wisdom. 2010
Мозг, общение нейронов и энергетическая эффективность
По всей видимости, в эволюции сформировались энергетически эффективные механизмы кодирования и передачи информации в мозге. Подпись: «Усердно пытаюсь минимизировать энергозатраты».
Автор
Редакторы
Статья на конкурс «био/мол/текст»: Клеточные процессы, обеспечивающие обмен информацией между нейронами, требуют много энергии. Высокое энергопотребление способствовало в ходе эволюции отбору наиболее эффективных механизмов кодирования и передачи информации. В этой статье вы узнаете о теоретическом подходе к изучению энергетики мозга, о его роли в исследованиях патологий, о том, какие нейроны более продвинуты, почему синапсам иногда выгодно не «срабатывать», а также, как они отбирают только нужную нейрону информацию.
Конкурс «био/мол/текст»-2017
Эта работа опубликована в номинации «Свободная тема» конкурса «био/мол/текст»-2017.

Генеральный спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.

Спонсором приза зрительских симпатий и партнером номинации «Биомедицина сегодня и завтра» выступила фирма «Инвитро».

Происхождение подхода
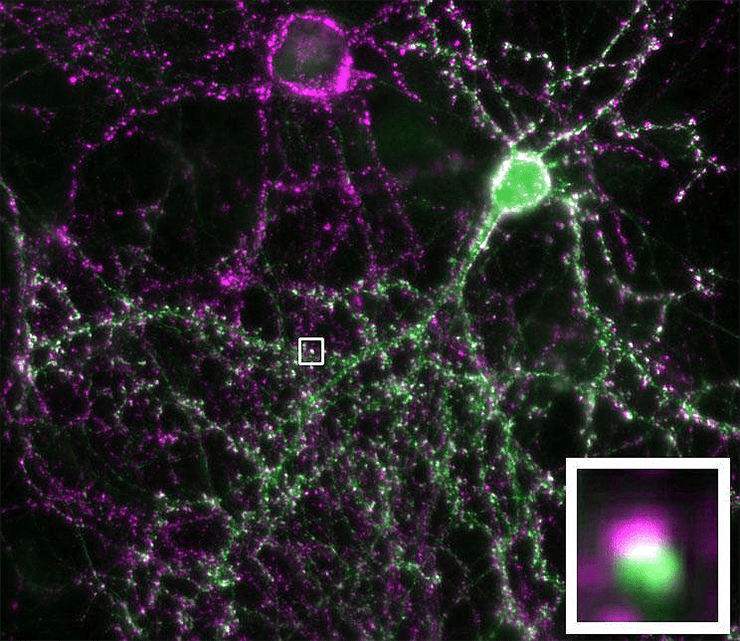
С середины ХХ века известно, что головной мозг потребляет значительную часть энергоресурсов всего организма: четверть всей глюкозы и ⅕ всего кислорода в случае высшего примата [1–5]. Это вдохновило Уильяма Леви и Роберта Бакстера из Массачусетского технологического института (США) на проведение теоретического анализа энергетической эффективности кодирования информации в биологических нейронных сетях (рис. 1) [6]. В основе исследования лежит следующая гипотеза. Поскольку энергопотребление мозга велико, ему выгодно иметь такие нейроны, которые работают наиболее эффективно — передают только полезную информацию и затрачивают при этом минимум энергии.
Это предположение оказалось справедливым: на простой модели нейронной сети авторы воспроизвели экспериментально измеренные значения некоторых параметров [6]. В частности, рассчитанная ими оптимальная частота генерации импульсов варьирует от 6 до 43 имп./с — почти так же, как и у нейронов основания гиппокампа. Их можно подразделить на две группы по частоте импульсации: медленные (
40 имп./с). При этом первая группа значительно превосходит по численности вторую [7]. Аналогичная картина наблюдается и в коре больших полушарий: медленных пирамидальных нейронов (
4—9 имп./с) в несколько раз больше, чем быстрых ингибиторных интернейронов (>100 имп./с) [8], [9]. Так, видимо, мозг «предпочитает» использовать поменьше быстрых и энергозатратных нейронов, чтобы те не израсходовали все ресурсы [6], [9–11].
Рисунок 1. Представлены два нейрона. В одном из них фиолетовым цветом окрашен пресинаптический белок синаптофизин. Другой нейрон полностью окрашен зеленым флуоресцентным белком. Мелкие светлые крапинки — синаптические контакты между нейронами [12]. Во вставке одна «крапинка» представлена ближе.
Группы нейронов, связанных между собой синапсами, называются нейронными сетями [13], [14]. Например, в коре больших полушарий пирамидальные нейроны и интернейроны образуют обширные сети. Слаженная «концертная» работа этих клеток обусловливает наши высшие когнитивные и другие способности. Аналогичные сети, только из других типов нейронов, распределены по всему мозгу, определенным образом связаны между собой и организуют работу всего органа.
Что такое интернейроны?
Нейроны центральной нервной системы разделяются на активирующие (образуют активирующие синапсы) и тормозящие (образуют тормозящие синапсы). Последние в значительной степени представлены интернейронами, или промежуточными нейронами. В коре больших полушарий и гиппокампе они ответственны за формирование гамма-ритмов мозга [15], которые обеспечивают слаженную, синхронную работу других нейронов. Это крайне важно для моторных функций, восприятия сенсорной информации, формирования памяти [9], [11].
Интернейроны отличаются способностью генерировать значительно более высокочастотные сигналы, чем другие нейроны. Они также содержат больше митохондрий, главных органелл энергетического метаболизма, «фабрик» по производству АТФ. Последние к тому же содержат большое количество белков цитохром-с оксидазы и цитохрома-с, являющихся ключевыми для метаболизма. Так, интернейроны являются крайне важными и, в то же время, энергозатратными клетками [8], [9], [11], [16].
Работа Леви и Бакстера [6] развивает концепцию «экономии импульсов» Горация Барлоу из Университета Калифорнии (США), который, кстати, является потомком Чарльза Дарвина [17]. Согласно ей, при развитии организма нейроны стремятся работать только с наиболее полезной информацией, фильтруя «лишние» импульсы, ненужную и избыточную информацию. Однако эта концепция не дает удовлетворительных результатов, так как не учитывает метаболические затраты, связанные с нейрональной активностью [6]. Расширенный подход Леви и Бакстера, в котором внимание уделено обоим факторам, оказался более плодотворным [6], [18–20]. И энергозатраты нейронов, и потребность в кодировании только полезной информации являются важными факторами, направляющими эволюцию мозга [6], [21–24]. Поэтому, чтобы лучше разобраться в том, как устроен мозг, стоит рассматривать обе эти характеристики: сколько нейрон передает полезной информации и сколько энергии при этом тратит.
За последнее время этот подход нашел множество подтверждений [10], [22], [24–26]. Он позволил по-новому взглянуть на устройство мозга на самых разных уровнях организации — от молекулярно-биофизического [20], [26] до органного [23]. Он помогает понять, каковы компромиссы между выполняемой функцией нейрона и ее энергетической ценой и в какой степени они выражены.
Как же работает этот подход?
Положим, у нас есть модель нейрона, описывающая его электрофизиологические свойства: потенциал действия (ПД) и постсинаптические потенциалы (ПСП) (об этих терминах — ниже). Мы хотим понять, эффективно ли он работает, не тратит ли неоправданно много энергии. Для этого нужно вычислить значения параметров модели (например, плотность каналов в мембране, скорость их открывания и закрывания), при которых: (а) достигается максимум отношения полезной информации к энергозатратам и в то же время (б) сохраняются реалистичные характеристики передаваемых сигналов [6], [19].
Поиск оптимума
Эти «оптимальные» значения параметров затем нужно сравнить с измеренными экспериментально и определить, насколько они отличаются. Общая картина отличий укажет на степень оптимизации данного нейрона в целом: насколько реальные, измеренные экспериментально, значения параметров совпадают с рассчитанными. Чем слабее выражены отличия, тем нейрон более близок к оптимуму и работает энергетически более эффективно, оптимально. С другой стороны, сопоставление конкретных параметров покажет, в каком конкретно качестве этот нейрон близок к «идеалу».
Далее, в контексте энергетической эффективности нейронов рассмотрены два процесса, на которых основано кодирование и передача информации в мозге. Это нервный импульс, или потенциал действия, благодаря которому информация может быть отправлена «адресату» на определенное расстояние (от микрометров до полутора метров) и синаптическая передача, лежащая в основе собственно передачи сигнала от одного нейрона на другой.
Потенциал действия
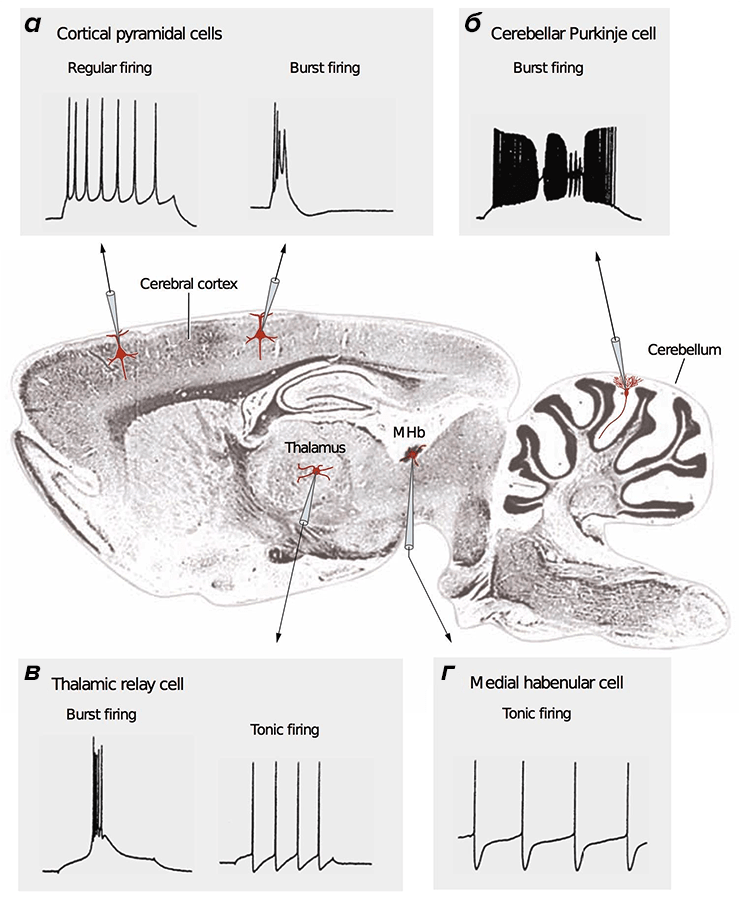
Потенциал действия (ПД) — сигнал, которые отправляют друг другу нейроны. ПД бывают разные: быстрые и медленные, малые и большие [28]. Зачастую они организованы в длинные последовательности (как буквы в слова), либо в короткие высокочастотные «пачки» (рис. 2).
Большое разнообразие сигналов обусловлено огромным количеством комбинаций разных типов ионных каналов, синаптических контактов, а также морфологией нейронов [28], [29]. Поскольку в основе сигнальных процессов нейрона лежат ионные токи, стоит ожидать, что разные ПД требуют различных энергозатрат [20], [27], [30].
Что такое потенциал действия?
ПД — это относительно сильное по амплитуде скачкообразное изменение мембранного потенциала.
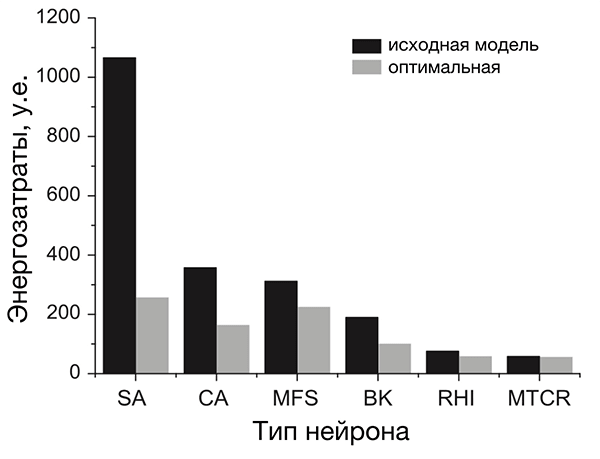
Анализ разных типов нейронов (рис. 4) показал, что нейроны беспозвоночных не очень энергоэффективны, а некоторые нейроны позвоночных почти совершенны [20]. По результатам этого исследования, наиболее энергоэффективными оказались интернейроны гиппокампа, участвующего в формировании памяти и эмоций, а также таламокортикальные релейные нейроны, несущие основной поток сенсорной информации от таламуса к коре больших полушарий.
Рисунок 4. Разные нейроны эффективны по-разному. На рисунке представлено сравнение энергозатрат разных типов нейронов. Энергозатраты рассчитаны в моделях как с исходными (реальными) значениями параметров (черные столбцы), так и с оптимальными, при которых с одной стороны нейрон выполняет положенную ему функцию, с другой — затрачивает при этом минимум энергии (серые столбцы). Самыми эффективными из представленных оказались два типа нейронов позвоночных: интернейроны гиппокампа (rat hippocampal interneuron, RHI) и таламокортикальные нейроны (mouse thalamocortical relay cell, MTCR), так как для них энергозатраты в исходной модели наиболее близки к энергозатратам оптимизированной. Напротив, нейроны беспозвоночных менее эффективны. Условные обозначения: SA (squid axon) — гигантский аксон кальмара; CA (crab axon) — аксон краба; MFS (mouse fast spiking cortical interneuron) — быстрый кортикальный интернейрон мыши; BK (honeybee mushroom body Kenyon cell) — грибовидная клетка Кеньона пчелы.
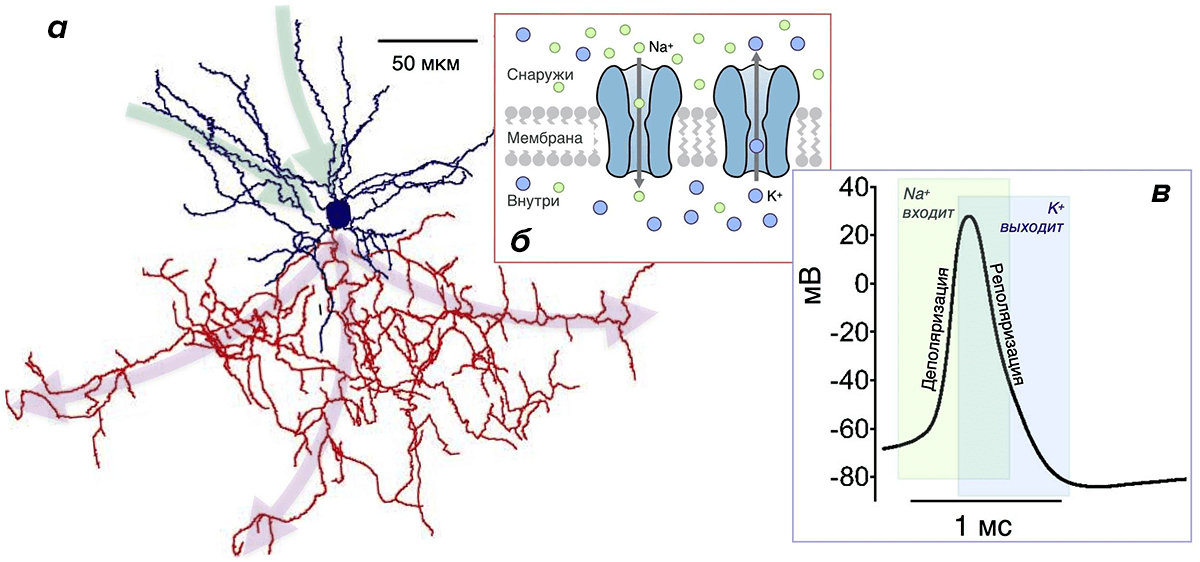
Почему они более эффективны? Потому что у них малó перекрывание Na- и К-токов. Во время генерации ПД всегда есть промежуток времени, когда эти токи присутствуют одновременно (рис. 3в). При этом переноса заряда практически не происходит, и изменение мембранного потенциала минимально. Но «платить» за эти токи в любом случае приходится, несмотря на их «бесполезность» в этот период. Поэтому его продолжительность определяет, сколько энергетических ресурсов растрачивается впустую. Чем он короче, тем более эффективно использование энергии [20], [26], [30], [43]. Чем длиннее — тем менее эффективно. Как раз в двух вышеупомянутых типах нейронов, благодаря быстрым ионным каналам, этот период очень короткий, а ПД — самые эффективные [20].
Кстати, интернейроны гораздо более активны, чем большинство других нейронов мозга. В то же время они крайне важны для слаженной, синхронной работы нейронов, с которыми образуют небольшие локальные сети [9], [16]. Вероятно, высокая энергетическая эффективность ПД интернейронов является некой адаптацией к их высокой активности и роли в координации работы других нейронов [20].
Синапс
Передача сигнала от одного нейрона к другому происходит в специальном контакте между нейронами, в синапсе [12]. Мы рассмотрим только химические синапсы (есть еще электрические), поскольку они весьма распространены в нервной системе и важны для регуляции клеточного метаболизма, доставки питательных веществ [5].
Чаще всего, химический синапс образован между окончанием аксона одного нейрона и дендритом другого. Его работа напоминает. «переброс» эстафетной палочки, роль которой и играет нейромедиатор — химический посредник передачи сигнала [12], [42], [44–48].
На пресинаптическом окончании аксона ПД вызывает выброс нейромедиатора во внеклеточную среду — к принимающему нейрону. Последний только этого и ждет с нетерпением: в мембране дендритов рецепторы — ионные каналы определенного типа — связывают нейромедиатор, открываются и пропускают через себя разные ионы. Это приводит к генерации маленького постсинаптического потенциала (ПСП) на мембране дендрита. Он напоминает ПД, но значительно меньше по амплитуде и происходит за счет открывания других каналов. Множество этих маленьких ПСП, каждый от своего синапса, «сбегаются» по мембране дендритов к телу нейрона (зеленые стрелки на рис. 3а) и достигают начального сегмента аксона, где вызывают открывание Na-каналов и «провоцируют» его на генерацию ПД.
Такие синапсы называются возбуждающими: они способствуют активации нейрона и генерации ПД. Существуют также и тормозящие синапсы. Они, наоборот, способствуют торможению и препятствуют генерации ПД. Часто на одном нейроне есть и те, и другие синапсы. Определенное соотношение между торможением и возбуждением важно для нормальной работы мозга, формирования мозговых ритмов, сопровождающих высшие когнитивные функции [49].
Как это ни странно, выброс нейромедиатора в синапсе может и не произойти вовсе — это процесс вероятностный [18], [19]. Нейроны так экономят энергию: синаптическая передача и так обусловливает около половины всех энергозатрат нейронов [25]. Если бы синапсы всегда срабатывали, вся энергия пошла бы на обеспечение их работы, и не осталось бы ресурсов для других процессов. Более того, именно низкая вероятность (20–40%) выброса нейромедиатора соответствует наибольшей энергетической эффективности синапсов. Отношение количества полезной информации к затрачиваемой энергии в этом случае максимально [18], [19]. Так, выходит, что «неудачи» играют важную роль в работе синапсов и, соответственно, всего мозга. А за передачу сигнала при иногда «не срабатывающих» синапсах можно не беспокоиться, так как между нейронами обычно много синапсов, и хоть один из них да сработает.
Еще одна особенность синаптической передачи состоит в разделении общего потока информации на отдельные компоненты по частоте модуляции приходящего сигнала (грубо говоря, частоте приходящих ПД) [50]. Это происходит благодаря комбинированию разных рецепторов на постсинаптической мембране [38], [50]. Некоторые рецепторы активируются очень быстро: например, AMPA-рецепторы (AMPA происходит от α-amino-3-hydroxy-5-methyl-4-isoxazolepropionic acid). Если на постсинаптическом нейроне представлены только такие рецепторы, он может четко воспринимать высокочастотный сигнал (такой, как, например, на рис. 2в). Ярчайший пример — нейроны слуховой системы, участвующие в определении местоположения источника звука и точном распознавании коротких звуков типа щелчка, широко представленных в речи [12], [38], [51]. NMDA-рецепторы (NMDA — от N—methyl-D—aspartate) более медлительны. Они позволяют нейронам отбирать сигналы более низкой частоты (рис. 2г), а также воспринимать высокочастотную серию ПД как нечто единое — так называемое интегрирование синаптических сигналов [14]. Есть еще более медленные метаботропные рецепторы, которые при связывании нейромедиатора, передают сигнал на цепочку внутриклеточных «вторичных посредников» для подстройки самых разных клеточных процессов. К примеру, широко распространены рецепторы, ассоциированные с G-белками. В зависимости от типа они, например, регулируют количество каналов в мембране или напрямую модулируют их работу [14].
Различные комбинации быстрых AMPA-, более медленных NMDA- и метаботропных рецепторов позволяют нейронам отбирать и использовать наиболее полезную для них информацию, важную для их функционирования [50]. А «бесполезная» информация отсеивается, она не «воспринимается» нейроном. В таком случае не приходится тратить энергию на обработку ненужной информации. В этом и состоит еще одна сторона оптимизации синаптической передачи между нейронами.
Что еще?
Энергетическая эффективность клеток мозга исследуется также и в отношении их морфологии [35], [52–54]. Исследования показывают, что ветвление дендритов и аксона не хаотично и тоже экономит энергию [52], [54]. Например, аксон ветвится так, чтобы суммарная длина пути, который проходит ПД, была наименьшей. В таком случае энергозатраты на проведение ПД вдоль аксона минимальны.
Снижение энергозатрат нейрона достигается также при определенном соотношении тормозящих и возбуждающих синапсов [55]. Это имеет прямое отношение, например, к ишемии (патологическому состоянию, вызванному нарушением кровотока в сосудах) головного мозга. При этой патологии, вероятнее всего, первыми выходят из строя наиболее метаболически активные нейроны [9], [16]. В коре они представлены ингибиторными интернейронами, образующими тормозящие синапсы на множестве других пирамидальных нейронов [9], [16], [49]. В результате гибели интернейронов, снижается торможение пирамидальных. Как следствие, возрастает общий уровень активности последних (чаще срабатывают активирующие синапсы, чаще генерируются ПД). За этим немедленно следует рост их энергопотребления, что в условиях ишемии может привести к гибели нейронов.
При изучении патологий внимание уделяют и синаптической передаче как наиболее энергозатратному процессу [19]. Например, при болезнях Паркинсона [56], Хантингтона [57], Альцгеймера [58–61] происходит нарушение работы или транспорта к синапсам митохондрий, играющих основную роль в синтезе АТФ [62], [63]. В случае болезни Паркинсона, это может быть связано с нарушением работы и гибелью высоко энергозатратных нейронов черной субстанции, важной для регуляции моторных функций, тонуса мышц. При болезни Хантингтона, мутантный белок хангтингтин нарушает механизмы доставки новых митохондрий к синапсам, что приводит к «энергетическому голоданию» последних, повышенной уязвимости нейронов и избыточной активации. Все это может вызвать дальнейшие нарушения работы нейронов с последующей атрофией полосатого тела и коры головного мозга. При болезни Альцгеймера нарушение работы митохондрий (параллельно со снижением количества синапсов) происходит из-за отложения амилоидных бляшек. Действие последних на митохондрии приводит к окислительному стрессу, а также к апоптозу — клеточной гибели нейронов.
Еще раз обо всем
В конце ХХ века зародился подход к изучению мозга, в котором одновременно рассматривают две важные характеристики: сколько нейрон (или нейронная сеть, или синапс) кодирует и передает полезной информации и сколько энергии при этом тратит [6], [18], [19]. Их соотношение является своего рода критерием энергетической эффективности нейронов, нейронных сетей и синапсов.
Использование этого критерия в вычислительной нейробиологии дало существенный прирост к знаниям относительно роли некоторых явлений, процессов [6], [18–20], [26], [30], [43], [55]. В частности, малая вероятность выброса нейромедиатора в синапсе [18], [19], определенный баланс между торможением и возбуждением нейрона [55], выделение только определенного рода приходящей информации благодаря определенной комбинации рецепторов [50] — все это способствует экономии ценных энергетических ресурсов.
Более того, само по себе определение энергозатрат сигнальных процессов (например, генерация, проведение ПД, синаптическая передача) позволяет выяснить, какой из них пострадает в первую очередь при патологическом нарушении доставки питательных веществ [10], [25], [56]. Так как больше всего энергии требуется для работы синапсов, именно они первыми выйдут из строя при таких патологиях, как ишемия, болезни Альцгеймера и Хантингтона [19], [25]. Схожим образом определение энергозатрат разных типов нейронов помогает выяснить, какой из них погибнет раньше других в случае патологии. Например, при той же ишемии, в первую очередь выйдут из строя интернейроны коры [9], [16]. Эти же нейроны из-за интенсивного метаболизма — наиболее уязвимые клетки и при старении, болезни Альцгеймера и шизофрении [16].
В общем, подход к определению энергетически эффективных механизмов работы мозга является мощным направлением для развития и фундаментальной нейронауки, и ее медицинских аспектов [5], [14], [16], [20], [26], [55], [64].
Благодарности
Искренне благодарен моим родителям Ольге Наталевич и Александру Жукову, сестрам Любе и Алене, моему научному руководителю Алексею Браже и замечательным друзьям по лаборатории Эвелине Никельшпарг и Ольге Слатинской за поддержку и вдохновение, ценные замечания, сделанные при прочтении статьи. Я также очень благодарен редактору статьи Анне Петренко и главреду «Биомолекулы» Антону Чугунову за пометки, предложения и замечания.