Удлинение интервала qt на экг у ребенка что это
• Для синдрома удлиненного интервала QT характерны 2 признака: удлинение интервала QT (длительность расчетного интервала QT превышает 0,44 с) и желудочковая тахикардия с обмороками.
• В дополнение к этим признакам отмечаются высокая волна U, уплощенный или отрицательный зубец Т, а также синусовая тахикардия.
• Врожденная форма данного синдрома встречается реже и является генетически гетерогенным заболеванием, приобретенная форма часто бывает обусловлена антиаритмической терапией.
• Врожденную форму синдрома удлиненного интервала QT лечат блокаторами бета-адренергических рецепторов, а при отсутствии эффекта от медикаментозной терапии при необходимости имплантируют кардиовертер/дефибрил-лятор. При приобретенной форме следует, прежде всего, отменить препараты, которые могли стать причиной удлинения интервала QT.
Синдром удлиненного интервала QT (синоним: синдром QT) делят на врожденную, генетически гетерогенную, форму и приобретенную, или медикаментозную, форму. Врожденная форма встречается крайне редко (1 случай на 10 000 новорожденных). Клиническое значение синдрома QT состоит в том, что как врожденная, так и приобретенная его форма проявляется желудочковой тахикардией.
I. Врожденный синдром удлиненного интервала QT (синдромы Джервелла-Ланге-Нильсена и Романо-Уорда)
В патогенезе врожденного синдрома QT играют роль мутации генов, кодирующих белки ионных каналов, приводящие к недостаточной активности калиевых каналов или повышенной активности натриевых каналов. Синдром удлиненного интервала QT может проявляться в форме синдрома Джервелла-Ланге-Нильсена и синдрома Романо-Уорда.
При синдроме Романо-Уорда глухонемоты нет.
Первые клинические проявления врожденного синдрома QT появляются уже в детском возрасте. Характерны повторные эпизоды обмороков, появляющиеся на фоне симпатикотонии, например, когда ребенок плачет, испытывает стресс или кричит.
К важнейшим ЭКГ-признакам синдрома QT относятся:
• удлинение интервала QT, т.е. длительность расчетного интервала QT превышает 0,44 с (в норме он равен 0,35-0,44 с)
• желудочковая тахикардия (пируэтная тахикардия: быстрая и полиморфная форма)
• синусовая брадикардия в покое и при нагрузке
• уплощенный или отрицательный зубец Т
• высокая или двухфазная волна U и слияние зубца Т и волны U
• зависимость продолжительности интервала QT от ЧСС
При измерении интервала QT следует проявить внимательность, чтобы не включить в интервал волну U (корригированный интервал QT; интервал QTC по Базетту). Относительный интервал QT (например, по Лепешкину или Хегглину и Гольцману) измерить проще, но значение его при этом менее точное. В норме оно составляет 100±10%.
При синдроме QT отмечается неравномерное удлинение фазы реполяризации, что облегчает механизм повторного входа волны возбуждения, способствуя появлению желудочковой тахикардии (torsade de pointes, пируэтная тахикардия) и фибрилляции желудочков.
Лечат синдром QT блокаторами бета-адренергических рецепторов, а в случае резистентности к этим препаратам имплантируют кардиовертер/дефибриллятор.
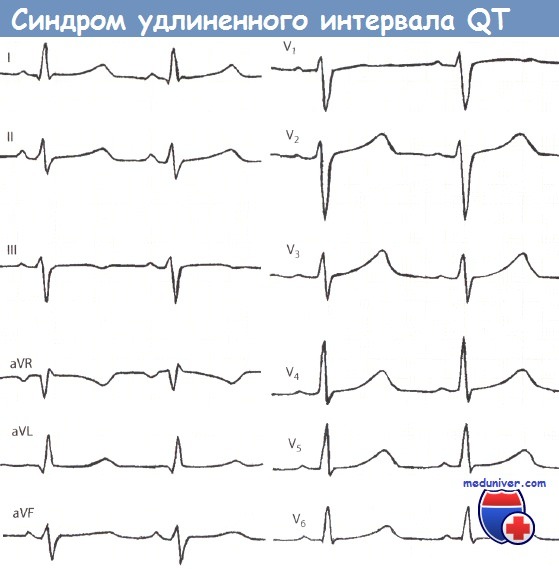
ЧСС 90 ударов в минуту, длительность QT 0,42 с, относительная длительность интервала QT составляет 128%, откорректированный интервал QTC удлинен и равен 0,49 с.
II. Приобретенный синдром удлиненного интервала QT
Причины, вызывающие приобретенный синдром удлиненного интервала QT, могут быть разные. Ниже перечислены только имеющие наибольшее клиническое значение:
• антиаритмические препараты (например, хинидин, соталол, амиодарон, аймалин, флекаинид)
• нарушение электролитного баланса (например, гипокалиемия)
• блокада ножки ПГ и уширение комплекса QRS
• гипотиреоз
• ИБС
• антибиотикотерапия (например, эритромицином)
• злоупотребление алкоголем
• миокардит
• церебральное кровоизлияние
В типичных случаях приобретенный синдром QT бывает связан с приемом антиаритмических препаратов, особенно хинидина и соталола. Клиническое значение данного синдрома велико, учитывая, что, как и при врожденной форме, приобретенный синдром QT сопровождают приступы желудочковой тахикардии.
Частота возникновения приступов желудочковой тахикардии у больных с приобретенным синдромом удлиненного интервала QT составляет 2-5%. Типичным примером являются так называемые хинидиновые обмороки. Изменения на ЭКГ такие же, как при врожденном синдроме QT.
Лечение подразумевает, прежде всего, отмену «причинного» препарата и введение, помимо прочего, раствора лидокаина.
Особенности ЭКГ при синдроме удлиненного интервала QT:
• Изменение интервала QT (в норме интервал QTC
Учебное видео оценки комплекса QRS на ЭКГ в норме и при патологии
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
— Вернуться в оглавление раздела «Кардиология.»
Удлинение интервала QT
Статья посвящена врождённому и приобретённому ЭКГ-синдрому удлинённого интервала QТ, а также Амиодарону, как наиболее частой медикаментозной причине данного состояния.
Синдром удлинения QT интервала представляет собой сочетание удлиненного интервала QT стандартной ЭКГ и угрожающих жизни полиморфных желудочковых тахикардий (torsade de pointes – «пируэт»). Пароксизмы желудочковых тахикардий типа «пируэт» клинически проявляются эпизодами потери сознания и нередко заканчиваются фибрилляцией желудочков, являющихся непосредственной причиной внезапной смерти.
Длительность интервала QT зависит от частоты сердечных сокращений и пола пациента. Поэтому используют не абсолютную, а корригированную величину интервала QT (QTc), которую рассчитывают по формуле Базетта:
где: RR – расстояние между соседними зубцами R на ЭКГ в сек. ;
К = 0, 37 для мужчин и К = 0, 40 для женщин.
Удлинение интервала QT диагностируют в том случае, если длительность QTc превышает 0, 44 с.
Установлено, что как врожденные, так и приобретенные формы удлинения интервала QT являются предикторами фатальных нарушений ритма, которые, в свою очередь, приводят к внезапной смерти больных.
Так, отсутствует единое мнение о верхней границе нормальных значениях дисперсии корригированного интервала QT. По мнению одних авторов, предиктором желудочковых тахиаритимий является QTcd более 45, другие исследователи предлагают считать верхней границей нормы QTcd 70 мс и даже 125 мс.
Cуществуют два наиболее изученных патогенетических механизма аритмий при синдроме удлиненного QT интервала. Первый – механизм «внутрисердечных нарушений» реполяризации миокарда, а именно, повышенная чувствительность миокарда к аритмогенному эффекту катехоламинов. Второй патофизиологический механизм – дисбаланс симпатической иннервации (снижение правосторонней симпатической иннервации вследствие слабости или недоразвития правого звездчатого ганглия). Эта концепция подтверждается на моделях с животными (удлинение QT интервала после правосторонней стеллэктомии) и результатами левосторонней стеллэктомии в лечении резистентных форм удлинения QT интервала.
Частота выявления удлинения интервала QT у лиц с пролапсами митрального и/или трикуспидального клапанов достигает 33%. По мнению большинства исследователей, пролапс митрального клапана является одним из проявлений врожденной дисплазии соединительной ткани. Среди других проявлений «слабости соединительной ткани» – повышенная растяжимость кожи, астенический тип телосложения, воронкообразная деформация грудной клетки, сколиоз, плоскостопие, синдром гипермобильности суставов, миопия, варикозное расширение вен, грыжи. Рядом исследователей выявлена взаимосвязь увеличенной варибельности QT интервала и глубины пролабирования и/или наличия структурных изменений (миксоматозная дегенерация) створок митрального клапана. Одной из главных причин формирования удлинения интервала QT у лиц с пролапсом митрального клапана является генетически предопределенный или приобретенный дефицит магния
Приобретенное удлинение QT интервала может возникнуть при атеросклеротическом или постинфарктном кардиосклерозе, при кардиомиопатии, на фоне и после перенесенного мио– или перикардита. Увеличение дисперсии интервала QT (более 47 мс) может также являться предиктором развития аритмогенных синкопальных состояний у больных с аортальными пороками сердца.
Удлинение интервала QT может наблюдаться и при синусовой брадикардии, атриовентрикулярной блокаде, хронической цереброваскулярной недостаточности и опухоли головного мозга. Острые случаи удлинения интервала QT могут также возникать при травмах (грудной клетки, черепно–мозговых).
Автономная нейропатия также увеличивает величину интервала QT и его дисперсию, поэтому данные синдромы имеют место у больных сахарным диабетом I и II типов.
Удлинение интервала QT может иметь место при нарушениях электролитного баланса с гипокалиемией, гипокальциемией, гипомагнезиемией. Подобные состояния возникают под воздействием многих причин, например, при длительном приеме диуретиков, особенно петлевых (фуросемид). Описано развитие желудочковой тахикардии типа «пируэт» на фоне удлинения интервала QT cо смертельным исходом у женщин, находившихся на малобелковой диете с целью снижения массы тела.
Общеизвестно удлинение QT при острой ишемии миокарда и инфаркте миокарда. Стойкое (более 5 дней) увеличение интервала QT, особенно при сочетании с ранними желудочковыми экстрасистолами, прогностически неблагоприятно. У этих пациентов выявлено значительное (в 5–6 раз) повышение риска внезапной смерти.
В патогенезе удлинения QT при остром инфаркте миокарда, несомненно, играет роль гиперсимпатикотония, именно этим многие авторы объясняют высокую эффективность b–блокаторов у этих пациентов. Кроме того, в основе развития данного синдрома лежат и электролитные нарушения, в частности, дефицит магния. Результаты многих исследований свидетельствуют о том, что до 90% больных с острым инфарктом миокарда имеют дефицит магния. Выявлена также обратная корреляционноая взаимосвязь уровня магния в крови (сыворотке и эритроцитах) с величиной интервала QT и его дисперсией у пациентов с острым инфарктом миокарда.
У пациентов с идиопатическим пролапсом митрального клапана лечение следует начинать с применения пероральных препаратов магния (Магнерот по 2 табл. 3 раза в день в течение не менее 6 месяцев), поскольку тканевой дефицит магния считают одним из основных патофизиологических механизмов формирования как синдрома удлинения QT интервала, так и «слабости» соединительной ткани. У этих лиц после лечения препаратами магния не только нормализуется величина интервала QT, но и уменьшаются глубина пролабирования створок митрального клапана, частота желудочковых экстрасистол, выраженность клинических проявлений (синдрома вегетативной дистонии, геморрагических симптомов и др. ). Если лечение пероральными препаратами магния через 6 месяцев не оказало полного эффекта показано добавление b–блокаторов.
Другой важной причной удлинёния интервала QT является приём специальных медикаментов, одним из таких препаратов, чаще всего используемых в клинической практике является Амиодарон (Кордарон).
Амиодарон относится к III классу антиаритмических препаратов (класс ингибиторов реполяризации) и обладает уникальным механизмом антиаритмического действия, так как помимо свойств антиаритмиков III класса (блокада калиевых каналов) он обладает эффектами антиаритмиков I класса (блокада натриевых каналов), антиаритмиков IV класса (блокада кальциевых каналов) и неконкурентным бета-блокирующим действием.
Кроме антиаритмического действия у него имеются антиангинальный, коронарорасширяющий, альфа- и бета-адреноблокирующий эффекты.
Антиаритмические свойства:
— увеличение продолжительности 3-ей фазы потенциала действия кардиомиоцитов, в основном за счет блокирования ионного тока в калиевых каналах (эффект антиаритмика III класса по классификации Вильямса) ;
— уменьшение автоматизма синусового узла, приводящее к уменьшению частоты сердечных сокращений;
— неконкурентная блокада альфа- и бета- адренергических рецепторов;
Описание
— замедление синоатриальной, предсердной и атриовентрикулярной проводимости, более выраженное при тахикардии;
— отсутствие изменений проводимости желудочков;
— увеличение рефрактерных периодов и уменьшение возбудимости миокарда предсердий и желудочков, а также увеличение рефрактерного периода атриовентрикулярного узла;
— замедление проведения и увеличение продолжительности рефрактерного периода в дополнительных пучках предсердно-желудочкового проведения.
Другие эффекты:
— отсутствие отрицательного инотропного действия при приеме внутрь;
— снижение потребления кислорода миокардом за счет умеренного снижения периферического сопротивления и частоты сердечных сокращений;
— увеличение коронарного кровотока за счет прямого воздействия на гладкую мускулатуру коронарных артерий;
— поддержания сердечного выброса за счет снижения давления в аорте и снижения периферического сопротивления;
— влияние на обмен тиреоидных гормонов: ингибирование превращения Тз в Т4 (блокада тироксин-5-дейодиназы) и блокирование захвата этих гормонов кардиоцитами и гепатоцитами, приводящее к ослаблению стимулирующего влияния тиреоидных гормонов на миокард.
Терапевтические эффекты наблюдаются в среднем через неделю после начала приема препарата (от нескольких дней до двух недель). После прекращения его приема амиодарон определяется в плазме крови на протяжении 9 месяцев. Следует принимать во внимание возможность сохранения фармакодинамического действия амиодарона в течение 10-30 дней после его отмены.
Каждая доза амиодарона (200 мг) содержит 75 мг йода.
Показания к применению
Профилактика внезапной аритмической смерти у больных группы высокого риска
Для больных хронической сердечной недостаточностью амиодарон является единственным разрешенным к применению антиаритмиком. Это связано с тем, что прочие препараты у этой категории пациентов или увеличивают риск внезапной середечной смерти, или угнетают гемодинамику.
При наличии ишемической болезни сердца препаратом выбора является соталол, на 1/3 являющийся, как известно, b–адреноблокатором. Но при его неэффективности в нашем распоряжении вновь только амиодарон. Что же касается больных с артериальной гипертензией, то из их числа, в свою очередь, выделяются пациенты с выраженной и невыраженной гипертрофией левого желудочка. Если гипертрофия невелика (в Руководстве 2001 г. – толщина стенки левого желудочка менее 14 мм), препарат выбора – пропафенон, но при его неэффективности – как всегда, амиодарон (наряду с соталолом). Наконец, при выраженной гипертрофии левого желудочка, как и при хронической сердечной недостаточности, амиодарон – единственный возможный препарат.
Источник: Остроумова О. Д. Удлинение интервала QT. РМЖ №18 2001 С 750-54
Статья добавлена 11 апреля 2015 г.
Проблемы диагностики синдрома удлиненного интервала QT у новорожденных детей
Представлены два клинических случая наблюдения новорожденных детей с удлиненным интервалом QTс. Первый отражает успешную терапевтическую тактику при высоком риске неблагоприятного исхода. Второй случай демонстрирует тревожные симптомы и условия развития ж
Two clinical cases of observation of newborn children with prolonged QTс interval were presented. The first one reflects successful therapeutic strategy in high risk of adverse outcome. The second case demonstrates dangerous symptoms and conditions for development of life-threatening state in neonatal period, which requires preventive treatment with beta-blocker to prevent irreversible outcomes.
В течение 30 лет синдром удлиненного интервала QT (СУИQT) активно изучается, происходит накопление клинических данных, выявление генетических мутаций и полиморфизмов генов в различных комбинациях, детерминирующих гетерогенность фенотипических проявлений каналопатии.
Представленные P. J. Schwartz с соавт. в 1998 г. результаты электрокардиографического (ЭКГ) скрининга у новорожденных детей, определившие связь с внезапной смертью младенцев [1–4], во многом изменили представления о наблюдении новорожденных и детей раннего возраста. В ряде работ было показано, что ЭКГ-скрининг позволяет выявить группу риска — новорожденных детей с брадикардией и/или изменениями на электрокардиограмме. Кроме того, установлено увеличение вероятности идиопатического СУИQT по мере удлинения периода реполяризации: так, у новорожденных с продолжительностью интервала QTc более 470 мсек, а также их бессимптомных родственников в 43% случаев выявляются мутации генов, подтверждающие клинический диагноз [1, 5, 6].
Новорожденные дети являются наиболее сложной категорией пациентов для своевременного выявления СУИQT. Причиной этому является широкий спектр перинатальных состояний и заболеваний, оказывающих негативное влияние на функции центральной нервной системы. С одной стороны, данные состояния маскируют нарушения сознания на фоне жизнеугрожающих состояний, с другой — могут инициировать раннюю манифестацию заболевания.
В то же время известно, что патология перинатального периода способна индуцировать вторичные нарушения электрических функций миокарда с развитием жизнеугрожащих состояний. Исследование вторичного СУИQT установило, что он может быть транзиторным, но иметь такие же серьезные последствия, как и генетически детерминированные заболевания ионных каналов. Выявлена причастность повреждений миокарда, гипотермии, гипотиреоза, гипокальциемии к развитию вторичных нарушений электрических функций сердца и жизнеугрожающих аритмий [7].
Мы представляем клинические случаи наблюдения новорожденных детей, родившихся в марте-апреле 2016 г. в Перинатальном центре КККЦОМД, с целью обратить внимание неонатологов и детских кардиологов на проблему своевременной диагностики СУИQT и возможность профилактического назначения терапии. Электрокардиограмма у новорожденных оценивалась согласно рекомендациям, корригированный интервал QT рассчитывался по формуле Базетта [8, 9].
Клинический случай 1. Пациент Н., родился на 38–39 неделе гестации, плановое кесарево сечение (по причине рубца на матке после аналогичных операций в 2010, 2014 гг.) с массой 3470 г, оценкой по шкале Апгар 8/9 баллов. Маме 32 г., хроническая железодефицитная анемия I ст.; отцу 37 лет, здоров. Предыдущие беременности — первая в 2005 г. — срочные роды, девочка развивается по возрасту, здорова; вторая в 2009 г. — срочные роды ребенка с массой 4200 г (Апгар — 8–9 баллов) — мальчик умер на седьмые сутки жизни; третья в 2010 г. — срочные роды ребенка (тазовое предлежание) с массой 3700 г — мальчик умер на седьмые сутки жизни; четвертая в 2014 г. — срочные роды, масса при рождении 2300, мальчик умер на четвертые сутки. Все случаи смерти новорожденных в данной семье произошли на дому и в родильном доме Республики Таджикистан — без выявленной причины, квалифицированы как синдром внезапной смерти младенцев (СВСМ).
Учитывая семейный анамнез, принято решение дообследовать ребенка в условиях стационара. С пятых суток жизни начал прибавлять в массе по 15,0–30,0 г в сутки. В раннем неонатальном периоде отмечена желтуха с гипербилирубинемией до 250 мкмоль/л на вторые сутки и снижением на фоне фототерапии до 168 мкмоль/л. По данным эхокардиографии отмечено некоторое расширение правых отделов сердца, функционирующие фетальные коммуникации — аневризма межпредсердной перегородки с дефектом по типу овального окна 5,0 × 6,0 мм и артериальный проток размером 2,0 × 2,0 мм с лево-правым сбросом, недостаточность трикуспидального клапана I ст., среднее давление в легочной артерии (СДЛА) — 30 мм рт. ст. В течение 11 дней значение СДЛА снизилось до 20 мм рт. ст., документировано закрытие артериального протока, но сохраняется прежних размеров межпредсердный дефект с некоторым увеличением правых отделов.
По данным электрокардиографии на вторые сутки жизни отмечается синусовый ритм с ЧСС 143–156 в минуту, длительность корригированного интервала QT — 520–616 мсек, неполная блокада правой ножки пучка Гиса (рис.). Анализ холтеровского мониторирования ЭКГ в течение суток установил синусовый ритм (средняя ЧСС — 136 в минуту, максимальная — 176 в минуту при проведении процедуры санитарной обработки), эпизоды брадикардии ниже критических цифр для периода новорожденности — 65 в минуту во время сна, длительность корригированного интервала QT в течение всего времени наблюдения — 460–500 мсек.
За 12 дней наблюдения эпизодов нарушения сознания и каких-либо других неврологических симптом выявлено не было, мониторинг ритма не зафиксировал желудочковых тахикардий. Электролитных нарушений также не выявлено: натрий — 141 ммоль/л, калий — 4,6 ммоль/л, глюкоза — 4,6 ммоль/л.
Оценка симптомов по критериям Шварца для данного пациента была следующей: длительность спонтанного QTc > 480 мсек у пациента мужского пола — 3 балла, случаи внезапной необъяснимой смерти в семье — 0,5 балла, получена сумма ≥ 3,5 балла, то есть отмечается высокий риск идиопатического СУИQT.
Учитывая неблагоприятный семейный анамнез и критическое удлинение корригированного интервала QT, на вторые сутки жизни ребенку назначен бисопролол в дозе 0,3 мг (0,08 мг/кг в сутки) в сутки однократно под контролем артериального давления. На фоне терапии отмечено снижение артериального давления до 60–56/37 мм рт. ст. в первые двое суток терапии, что потребовало коррекции режима введения препарата — перевода на введение суточной дозы в два приема. Это привело к стабилизации артериального давления на уровне 65–72/40 мм рт. ст., ребенок был выписан под наблюдение участкового педиатра и детского кардиолога.
В настоящее время ребенку 5 месяцев, проводится постоянная поддерживающая терапия бета-блокатором, которая переносится удовлетворительно. Состояние стабильное: адекватные прибавки в массе, интеллектуальное развитие и нормальный темп формирования двигательных навыков, жизнеугрожающих состояний не зафиксировано. В возрасте 1 месяца интервал QTc на электрокардиограмме составляет 463 мсек, в 3 месяца — 457 мсек, то есть прослеживается позитивная клиническая динамика. Продолжается наблюдение педиатра и детского кардиолога, взят под наблюдение аритмолога ФЦССХ г. Красноярска. Проведен забор венозной крови для выделения ДНК и проведения молекулярно-генетического исследования у ребенка, сибса (сестры) и родителей.
Помимо драматичного семейного анамнеза, рассматриваемый клинический случай интересен чрезмерным удлинением корригированного интервала QT при полном клиническом «благополучии» пациента. В литературе описана ассоциация удлинения QTc более 600 мсек с летальным исходом в первую неделю жизни [10]. Вероятно, у данного пациента раннее начало терапии бета-блокатором оказало позитивное влияние на симпатическую регуляцию сердечного ритма, позволило избежать развития жизнеугрожающих нарушений сердечного ритма и не повторить судьбы трех предыдущих сибсов.
Клинический случай 2. Пациентка В., от преждевременных третьих родов в 35 недель. Отягощенный медико-социальный и акушерский анамнез — курение матери во время беременности, рубец на матке после кесарева сечения в 2009, 2001 гг., угроза разрыва матки по рубцу, умеренная тромбоцитопения без геморрагического синдрома, экстренное кесарево сечение. Масса при рождении — 2170 г, длина тела — 49 см, оценка по шкале Апгар — 7/8 баллов. На 8-й минуте жизни стала подстанывать, появились бледность и акроцианоз, экскурсия грудной клетки снижена, одышка до 60 в минуту с втяжением межреберных мышц, проводные хрипы. Симптом «бледного пятна» — 3 секунды. Сердечные тоны ритмичные, достаточной громкости, с ЧСС — 138 в минуту. Живот доступен глубокой пальпации, печень выступает на 1,5 см из-под края реберной дуги. Был выставлен диагноз «транзиторное тахипноэ новорожденного», девочка переведена в отделение патологии новорожденных.
В динамике появились крепитирующие хрипы, нарастание дыхательной недостаточности, АД — 57/26 мм рт. ст., артериальная гипоксемия (SaO2 — 87%, рН — 7,162, рСО2 — 62,6 мм рт. ст., рО2 — 59,8 мм рт. ст.). По данным эхокардиографии выявляются функционирующие фетальные коммуникации — артериальный проток 2 мм и овальное окно 3 мм, СДЛА — 40 мм рт. ст. Состояние ребенка квалифицируется как респираторный дистресс-синдром. Начата респираторная поддержка (респиратор SLE 5000, режим SIMV, параметры: pip 16 см Н2О, peep 5 см Н2О, МАР 9 см Н2О, FiO2 0,3, f 60 мин, Tin 0,33 сек). Установлен катетер (линия, v. saphena) для проведения антибактериальной терапии — ампициллин (0,11 г дважды в сутки) и нетромицин (100 мг/мл — 0,0098 мл однократно в сутки). Введен Куросурф (80 мг/мл суспензия 1,5 мл) 480 мг однократно.
Через 15 минут реанимационных мероприятий (интубация трахеи, ИВЛ, медикаментозная терапия, непрямой массаж сердца) зафиксированы сердечные сокращения более 100 уд. в мин. Начата интенсивная терапия, направленная на лечение постреанимационной болезни: ИВЛ в режиме нормовентиляции, иммобилизация головного мозга, инотропная стимуляция, инфузионная терапия 120 мл/кг, антибактериальная терапия в прежнем режиме. На фоне массивной медикаментозной седации — кома 3, после отмены — появление двигательной активности, постепенное восстановление рефлексов. Диагноз при выписке: «Аноксическое поражение головного мозга, тяжелое. Перивентрикулярная лейкомаляция в стадии образования кист. Синдром удлиненного интервала QT, вероятно вторичный (на фоне транзиторной гипокальциемии). Транзиторное тахипноэ новорожденного».
Особенностью данного клинического случая является то, что с одинаковой вероятностью причинами клинической смерти ребенка могли быть как транзиторное удлинение интервала QTc на фоне гипокальциемии и развитие аритмии под влиянием болевого стресса, так и генетически детерминированное заболевание ионных каналов кардиомиоцитов (mutation de novo).
Таким образом, представленные клинические случаи демонстрируют настороженность педиатров и неонатологов при наличии семейного анамнеза внезапной необъяснимой смерти детей, оперативность и правильность диагностики СУИQT, а также успешность терапии. С другой стороны, необходимо усилить внимание к комбинации таких условий, как нарушение электролитного баланса, брадикардия, нарушение реполяризации на электрокардиограмме у новорожденных и избегать создания стрессовых ситуаций (в том числе лечебных и диагностических манипуляций) без коррекции указанных симптомов.
Литература
* ГБОУ ВПО КрасГМУ им. проф. В. Ф. Войно-Ясенецкого МЗ РФ, Красноярск
** КГБУЗ КККЦОМД, Красноярск
*** КГБУЗ КМДКБ № 1, Красноярск


.jpg)



