Удаление гонад что это
Этиологические факторы первичной аменореи достаточно разнообразны. Как было сказано выше, к четырем основным причинам первичной аменореи относятся следующие:
• дисгенезия гонад (почти половина всех случаев);
• мюллерова агенезия (например, врожденное отсутствие матки и влагалища);
• гипоталамические расстройства, в том числе связанные с избыточной физической нагрузкой и нарушениями питания;
• конституциональная задержка полового созревания. К другим, более редким причинам первичной аменореи относятся анатомические особенности (неперфорированная девственная плева или поперечная перегородка влагалища), синдром тестикулярной феминизации, а также врожденные дефекты синтеза гонадотропинов или врожденная резистентность яичников к гонадотропинам. Некоторые из перечисленных нарушений рассмотрены в данной статье.
Дисгенезия гонад как причина первичной аменореи
Термин «дисгенезия гонад» в общем используют для описания всех форм нарушения развития гонад у пациентов с нормальным кариотипом (46ХХ; 46XY), а также ряда аномальных или мозаичных нарушений, наиболее частое из которых — синдром Тернера (45X0). Гонады в таких случаях представляют собой функционирующие фиброзные тяжи.
Чистая форма дисгенезии гонад. Для чистой формы дисгенезии гонад характерны: женский фенотип, наличие гонад в виде фиброзных тканей, наружные половые органы, развитые по женскому типу, нормально развитые мюллеровы структуры и кариотип 46XY (синдром Суайра) или 46ХХ. Это гетерогенное состояние может быть результатом структурных нарушений в Y-хромосоме, мутации гена SRY (мутации в участке Y-хромосомы, при которой происходит нарушение половой дифференцировки у мальчиков) или мутации аутосомного гена.
Смешанная дисгенезия гонад. Смешанная дисгенезия гонад развивается вследствие хромосомного мозаицизма. В кариотипе у таких больных отмечают частичную моносомию по половым хромосомам с отсутствием или аномалией второй половой хромосомы, причем кариотип чаще всего 45X0/46XY.
Фенотипически это могут быть и женщины, и мужчины, и псевдогермафродиты — в зависимости от отношения доли клеток с кариотипом 45X0 к клеткам с нормальным (46ХХ или 46XY) кариотипом в каждой из гонад. У этих пациентов обнаруживают нарушение половой дифференцировки.
Возможны варианты наличия фиброзированной половой железы с одной стороны и недостаточно развитой или нормальной — с другой в сочетании с ипсилатеральным развитием вольфова протока или мюллеровых структур. Большинство таких пациентов имеют низкий рост, а у одной трети выявляют признаки синдрома Тернера.
У большинства пациенток с дисгенезией гонад никогда не бывает менструаций. Эта группа больных составляет около 40% всех случаев первичной аменореи, и у 40% из них обнаруживают аномалии кариотипа. При нарушениях кариотипа синдром Тернера (46,Х0) диагностируют в 50% случаев, мозаичный кариотип X0/XY — в 25%.
Больных с дисгенезией гонад и нормальным кариотипом необходимо также обследовать для исключения нейросенсорной тугоухости и синдрома инактивированной Х-хромосомы. Поиск этих клинических связей особенно важен, если в семейном анамнезе есть случаи преждевременной яичниковой недостаточности (ПЯН).
Лечение дисгенезии гонад
Подростки с дисгенезией гонад нуждаются в гормональной терапии с целью стимуляции роста и своевременного полового развития. В течение первого года применяют эстрогены в низких дозах (0,25-0,3 мг/сут) иногда в сочетании с гормоном роста, чтобы индуцировать нормальное половое развитие, минимизировать эффекты раннего закрытия эпифизов костей и обеспечить нормальный рост. Приблизительно через год терапии эстрогенами подключают препараты прогестерона (например, медроксипрогестерон по 5 мг/сут или иную форму прогестерона), который используют во второй половине месяца.
Дозы эстрогенов постепенно увеличивают, чтобы за 2-3 года больные достигли половой зрелости.
Для поддерживающей терапии используют 2 мг/сут эстрадиола или 1,25 мг/сут конъюгированных эстрогенов. Если назначено лечение гормоном роста, эстрогены можно назначить раньше. Если же гормон роста не используется, начало лечения эстрогенами может быть отсрочено до 14-15 лет, но не позже. Применение этинилэстрадиола повышает риск артериальной гипертензии у больных с синдромом Тернера. Больным с Y-хромосомой с целью предотвращения малигнизации показана гонадэктомия.
Благодаря возможности использования донорской яйцеклетки у больных может наступать беременность. Однако повышенные требования, которые беременность предъявляет к сердечно-сосудистой системе (с учетом того, что распространенность ее аномалий у этих больных достигает 25-50%), становятся у таких больных существенным фактором риска. В докладе ASRM говорится, что риск развития расслаивающей аневризмы аорты и ее разрыва составляет 2% и выше, а риск смерти во время беременности повышается в 100 раз.
Выявление любых тяжелых аномалий сердечно-сосудистой системы необходимо рассматривать как противопоказание для донации ооцитов. Даже при отсутствии подобных аномалий сохраняется риск расслаивающей аневризмы аорты во время беременности.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Синдром Свайера – это нарушение формирования пола, характеризующееся кариотипом 46XY, врождённой дисгенезией гонад при первично сформированных прочих женских гениталиях – влагалище, матке, фаллопиевых трубах. К признакам патологии относятся первичная аменорея, маскулинное телосложение, половой инфантилизм. Диагноз выставляется на основании анамнестических данных, результатов общего и гинекологического осмотра, интроскопических методов исследования органов малого таза, гормонального и молекулярно-генетического анализа. Лечение состоит из двух этапов – удаления неразвитых половых желёз и длительного применения заместительной гормональной терапии.
МКБ-10
Общие сведения
Синдром Свайера (полную, или «чистую» дисгенезию гонад) можно кратко охарактеризовать как женский фенотип при мужском генотипе. Заболевание названо по имени британского эндокринолога Джералда Свайера, описавшего его в 1955 году как случай мужского псевдогермафродитизма. Полная форма дисгенезии является несиндромальной (не сопровождается экстрагенитальными пороками развития), исключает двойственность полового развития (наличие мужских первичных половых признаков наряду с женскими), психологическое развитие происходит по женскому типу. Врождённая патология встречается в одном случае на 20 000 индивидов с мужским кариотипом и регистрируется чаще иных форм XY-дисгенезии гонад.
Причины
Этиология синдрома Свайера изучена недостаточно. На сегодняшний день известно, что чаще всего возникновение патологии связано с отсутствием или мутацией гена SRY, расположенного на коротком плече хромосомы Y и большей частью отвечающего за контроль формирования тестикул. Судя по наблюдениям семейных случаев заболевания, возможна причастность пока неизвестных X-сцепленных или аутосомных генов.
Факторы риска тоже до конца не установлены. Кроме общих мутагенных воздействий (ионизирующего излучения и интоксикаций, вирусных инфекций, несбалансированного или пониженного питания) и уже упомянутого наследственного отягощения предполагается, что вероятность патологии может находиться в прямой зависимости от возраста отца. Чаще всего проследить связи между каким-либо воздействием на организм во время гестации и развитием синдрома Свайера не удаётся.
Патогенез
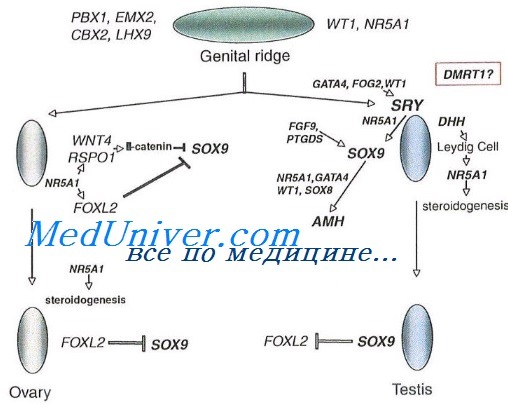
Формирование репродуктивных органов происходит из мюллерова протока у женщин и вольфова – у мужчин. У эмбриона с мужским генотипом синтез мужских стероидных гормонов клетками Лейдига в эмбриональных семенниках обусловлен воздействием материнского хорионического гонадотропина. Клетки Сертоли стимулируют дифференцировку клеток Лейдига и прочих, продуцируют антимюллеров гормон, способствующий атрофии мюллерова протока. Их нормальная деятельность обуславливает развитие индивида мужского пола – с адекватной дифференцировкой тестикул, атрофией мюллерова протока.
Выраженные сбои этого механизма приводят к формированию из бипотентных зачатков женских репродуктивных органов, развитие которых не требует столь сложной регуляции. Созревание мужского эмбриона контролируется геном SRY. При его отсутствии или мутации нарушается деятельность клеток Сертоли, дифференцировка гонад не происходит, что влечёт развитие синдрома Свайера – фенотипически женского организма без полноценных яичников, способных в дальнейшем стимулировать развитие вторичных половых признаков, но с бесполезными, склонными к малигнизации зачатками желёз.
Симптомы
В допубертатном периоде патология протекает без каких-либо субъективных проявлений. В период пубертата для синдрома Свайера характерно отсутствие признаков полового созревания. Может отмечаться лишь скудное оволосение в области лобка и подмышек, однако нередко отсутствует и оно. Менархе не наступает, молочные железы не развиваются или выражены очень слабо. Тип телосложения при овариальной дисгенезии мужской – с широкими плечами, объёмной грудной клеткой, узким тазом.
У женщин с синдромом Свайера чаще наблюдается нормальный или выше среднего рост, развитая мускулатура, «тяжёлая» нижняя челюсть. Иногда возникает незначительная гипертрофия клитора, хотя обычно наружные гениталии несколько недоразвиты. Больные жалуются на первичное бесплодие, ощущение дискомфорта или боли ввиду недостаточного развития вагины при половом акте или гинекологическом осмотре.
Осложнения
Частым (у 20-60% пациенток) осложнением синдрома Свайера является развитие опухолей, по большей части исходящих из рудиментарного полового тяжа, которым, по сути, представлены дисгенетичные гонады – дисгермином, андробластом. Эти неоплазии нередко имеют злокачественный характер, возникают с обеих сторон (синхронно или метахронно), регистрируются в раннем репродуктивном, подростковом и детском возрасте.
К последствиям нелеченного синдрома Свайера также можно отнести раннее появление патологий, обусловленных дефицитом эстрогена у женщин – остеопороза, сердечно-сосудистых заболеваний (артериальной гипертензии, ишемической болезни сердца). Кроме того, для многих больных диагноз становится источником тяжёлого психологического страдания по поводу «утраты женственности», а у замужних женщин – и боязни распада семьи.
Диагностика
Диагностика синдрома Свайера осуществляется гинекологом при участии медицинского генетика. Чаще всего диагноз устанавливается в 14-15 лет при обращении к врачу по поводу отсутствия полового развития, иногда – позднее, по причине бесплодия. В некоторых случаях первым признаком заболевания и основанием для углублённого исследования является опухолевое образование рудиментарных половых желёз, случайно обнаруженное врачом или самой больной. Диагностические мероприятия включают:
Синдром Свайера дифференцируют с другими формами дисгенезии гонад – синдромом Шерешевского-Тёрнера, мозаицизмом 45,X/46,XY, синдромом Морриса (синдромом тестикулярной феминизации), а также с задержкой полового развития гипоталамо-гипофизарного, конституционального, идиопатического генеза. При подозрении на опухоль необходима консультация онкогинеколога, а для выявления центральных форм задержки полового созревания – эндокринолога.
Лечение синдрома Свайера
Консервативная терапия
Лечение заболевания направлено на предупреждение осложнений, нормализацию психоэмоционального статуса пациентки, по возможности – на реализацию репродуктивной функции. После установления диагноза осуществляется хирургическая операция (удаление рудиментарных гонад), затем назначается гормональная терапия. Раннее (с подросткового периода) начало лечения синдрома Свайера повышает вероятность вынашивания ребёнка.
При достаточном развитии матки возможно применение программы ЭКО с имплантацией донорских ооцитов, оплодотворённых спермой супруга пациентки. На протяжении вынашивания плода женщине назначается сначала поддерживающая, затем сохраняющая гормонотерапия. Родоразрешение осуществляется оперативно. В современных репродуктологии и акушерстве уже накоплен успешный опыт ведения беременности у больных с дисгенезией гонад (в том числе синдромом Свайера).
Хирургическое лечение
Оперативное вмешательство в объёме удаления рудиментарных гонад и маточных труб выполняется непосредственно после диагностики этой формы врождённой овариальной агенезии. Хирургическое лечение проводится с целью предотвращения новообразований, источником которых являются клетки дисгенетичных половых желёз. Консервативное лечение не рекомендуется начинать до хирургической операции, поскольку гормональная терапия повышает риск развития онкологических осложнений.
Прогноз и профилактика
При своевременно начатом рациональном лечении синдрома Свайера прогноз относительно продолжительности и качества жизни благоприятный. Некоторые пациентки могут реализовать детородную функцию с помощью вспомогательных репродуктивных технологий, описаны случаи повторных успешных беременностей. Первичная профилактика рождения девочек с XY-дисгенезией включает здоровый образ жизни во время беременности, исключение профессиональных и бытовых вредностей. Для раннего выявления и лечения заболевания следует подвергать генетическому обследованию монозиготных близнецов больных.
Что такое синдром Морриса? Причины возникновения, диагностику и методы лечения разберем в статье доктора Литвинова В. В., репродуктолога со стажем в 38 лет.
Определение болезни. Причины заболевания
Синдром Морриса (синдром тестикулярной феминизации) — это врождённое генетическое заболевание, при котором у людей мужского пола ткани-мишени не чувствительны к мужским половым гормонам — андрогенам. Человек с синдромом Морриса генетически является мужчиной (имеет кариотип 46 XY), но выглядит как женщина.
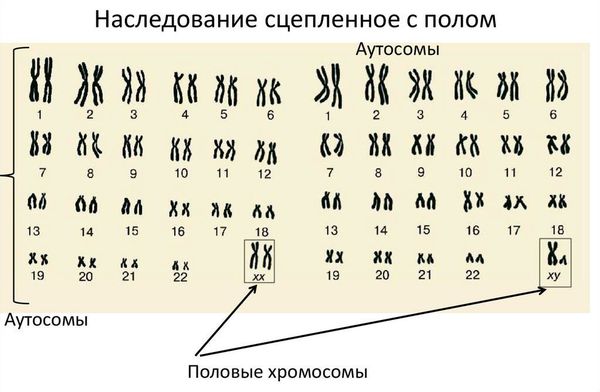
Кариотип — это набор хромосом, который передаётся ребёнку от матери и отца. Кариотип позволяет определить характеристики индивида, включая пол. В норме у человека в генетическом наборе присутствует 46 хромосом, из них 22 пары аутосомных (не определяющих пол) и одна пара половых хромосом, которая определяет гендерную принадлежность ребёнка. Половые хромосомы женщины обозначаются как ХХ, мужчины — ХY. То есть нормальный женский кариотип — 46 XX, мужской — 46 XY.
Часто мужчины с синдромом Морриса даже не догадываются о своём биологическом поле (как и их родители) и живут как девочки/женщины. Это объясняется тем, что данная патология больше никак себя не проявляет, кроме проблем с фертильностью (способностью к зачатию) во взрослом возрасте.
Симптомы синдрома Морриса
Как правило, люди с синдромом тестикулярной феминизации имеют женский фенотип, т. е. внешне выглядят как женщины. Однако есть некоторые признаки, по которым можно определить наличие заболевания.
Патогенез синдрома Морриса
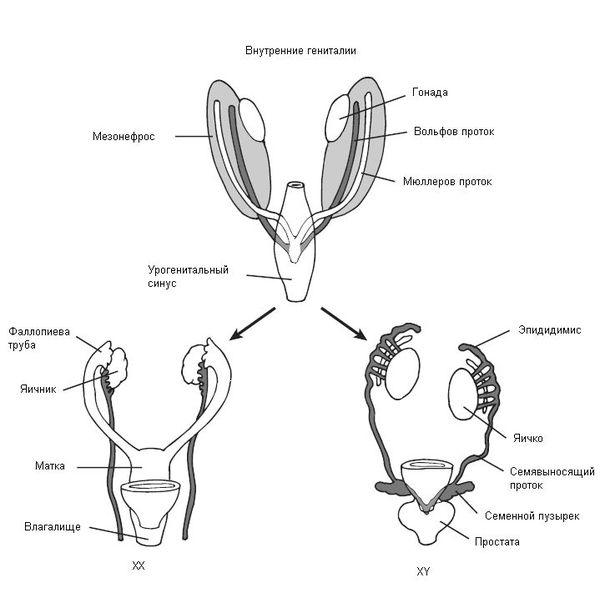
В начале эмбрионального развития у зародышей вне зависимости от хромосомного набора, образовавшегося при оплодотворении яйцеклетки сперматозоидом, половая система закладывается одинаково и предоставляет возможности для развития как женской, так и мужской половой системы. В частности, у зародыша одновременно формируются вольфов и мюллеров протоки, которые потом превращаются в семявыносящие протоки у мужчин и матку с фаллопиевыми трубами и влагалищем у женщин. Половые железы эмбриона (гонады) не дифференцированы и содержат первичные половые клетки (гаметы), которые могут превратиться как в клетки яичников (женские гонады), так и в клетки семенников (мужские гонады).
Таким образом, эмбрион до 6 недель является нейтральным по полу (имеет признаки и мужского, и женского пола). Далее процесс формирования половых признаков и в дальнейшем организма происходит под строгим контролем гормонов: у эмбриона мужского пола — под влиянием тестостерона (влагалище атрофируется), у эмбриона женского пола — под влиянием эстрадиола и прогестерона (влагалище трансформируется из «слепого мешка» и формируется шейка матки и матка). Тестостерон и эстрадиол вырабатываются как у мужчин, так и у женщин, только их соотношение разное. В норме у мальчиков соотношение мужского гормона к женскому 4\1, а в случае СТФ — 0\1. У девочек соотношение мужского гормона к женскому, прямо противоположное — 1\4.
Классификация и стадии развития синдрома Морриса
Синдром тестикулярной феминизации делят на две формы — полный и неполный. Дети с полной формой нечувствительности к мужским гормонам имеют однозначно женский внешний вид. При этом состоянии чувствительность организма к мужскому половому гормону (тестостерону) отсутствует полностью. Рождается здоровая «девочка», не имеющая, на первый взгляд, каких-либо отклонений в развитии.
Осложнения синдрома Морриса
Диагностика синдрома Морриса
Лечение синдрома Морриса
Лечение синдрома тестикулярной феминизации должно осуществляться междисциплинарной командой врачей, которая состоит из хирурга, гинеколога, генетика, эндокринолога и клинического психолога или психиатра.
Операция эффективна в 100 % случаев. Но так как удаляемые гонады мягкие и не имеют чёткой формы и структуры, возможны случаи неполного их удаления. Тогда оставшаяся ткань яичка может возобновить свою работу, что проявляется повышением тестостерона в крови и визуализацией на УЗИ гонады/гонад. В этом случае необходима повторная операция. Однако это случается очень редко.
Прогноз. Профилактика
Дисгенезия
МКБ-10: Q99.1 — 46,XX истинный гермафродит.
Дисгенезия – это группа врожденных нарушений развития репродуктивной системы, в частности гонад. Дисгенезия характеризуется прогрессирующей потерей зародышевых клеток на развивающихся гонадах эмбриона, что приводит к недоразвитию половых желез, главным образом, состоящим из волокнистой ткани.
Стаж работы 13 лет.
Это форма аплазии, при которой яичник заменяется бесфункционной тканью. Сопровождающая дисгенезию гормональная недостаточность также препятствует развитию вторичных половых признаков в обоих полах, что приводит к появлению сексуально инфантильной женской внешности и бесплодию.
Различают три формы дисгенезии:


Причины
Половое созревание у мужчин и женщин требует функциональных гонад, которые будут работать в гармонии с гипоталамусом, гипофизарной железой для адекватного производства гормонов.
Существует несколько основных причин дисгенезии:

Симптомы
Обычно патология проявляется сразу же при рождении ребенка. Классические симптомы дисгенезии у малышей — аномалия почек, врожденный порок сердца, крыловидная шея и отечность лимфоузлов на конечностях.
Также дисгенезия отличается такими клиническими признаками:
Диагностика
Основная задача диагностики дисгенезии — определить гормональный статус, половой хроматин, кариотип. Обычно подозрения возникают при нарушениях менструального цикла у женщин, первичной аменорее.
Также в план диагностических мероприятий входит:
Лечение
Как правило, лечение дисгенезии требует комплексного подхода. Тактика курса терапии зависит от индивидуальных особенностей клинической картины.
Медики применяют такие методики лечения:
Y-хромосомы и антиген H-Y характеризуются высоким риском злокачественного преобразования, может потребоваться хирургическое лечение. Чтобы улучшить кровоснабжение органов малого таза назначаются физиопроцедуры. Врачи также рекомендуют прием витаминных комплексов и психотерапевтическое воздействие. По скорости развития вторичных половых признаков специалисты оценивают эффективность лечебного курса.
Пациентки, имеющие этот диагноз, зачастую страдают неизлечимым бесплодием. В случае беременности, необходимо проводить генетическое исследование. Если у вас обнаружены проблемы генетического характера, не отчаивайтесь. Квалифицированные специалисты клиники «АльтраВита» постараются вам помочь родить здорового ребенка путем ЭКО с использованием донорских яйцеклеток. Мы располагаем всеми необходимыми ресурсами для успешного результата.
Данная статья не может быть использована для постановки диагноза, назначения лечения и не заменяет прием врача.
Лечение пороков развития яичников
Заболевания женской половой системы многообразны, но отдельное место среди них занимают различные аномалии развития половых органов – яичников, матки, влагалища, маточных труб. Аномалии развития яичников – это нарушение роста, расположения и строения яичников, возникающее, как правило, еще во время внутриутробного развития. Чаще всего встречаются следующие виды пороков развития половых органов:
К счастью, пороки развития яичников встречаются в практике довольно редко, однако данные медицинской статистики подтверждают, что за последние несколько десятилетий частота таких патологий возросла до 2 %. Клиника Современной Медицины – один из лучших медицинских центров Москвы, специализирующийся на гинекологических заболеваниях, включая патологии развития яичников и других женских половых органов.
Передовая диагностическая база и уникальный опыт лечения патологий такого типа позволяют нам быстро выявить характер нарушения и провести эффективную терапию, подобранную с учетом формы заболевания, тяжести клинических проявлений, возраста пациентки и других факторов.
Причины аномалий развития яичников
В современной гинекологии выделяют три основные группы причин, провоцирующих пороки развития яичников:
Как правило, аномалии развития яичников обусловлены хромосомными нарушениями и зачастую сопровождаются патологическими изменениями всех репродуктивных органов, а нередко и других систем организма.
Аномальное развитие яичников возникает вследствие нарушения внутриутробного развития, на стадии закладки и дифференцирования тканей половых органов девочки. Главными причинами развития патологии являются:
Аномалии развития яичников сопряжены с врожденным дефектом развития половых желез или их полным отсутствием в генотипе (так называемая дисгенезия гонад в генотипе). Данные патологии проявляются в четырех вариантах: чистая, типичная (синдром Шерешевского-Тернера), смешанная и стертая. Размеры половых желез значительно отстают от возрастной нормы, а их морфологическая структура, генеративная и эндокринная функции неполноценны (яйцеклетки дегенерируют, фолликулы не достигают зрелости и т. д.).
Симптомы патологий развития яичников
Яичники (ovaria) – это парная половая железа, расположенная в малом тазу женщины. Именно в яичнике созревают яйцеклетки, принимающие участие в зачатии, и синтезируются женские половые гормоны, поступающие затем непосредственно в кровеносную систему.
В норме яичники взрослой здоровой женщины имеют овальную форму, толщину 1-1,5 см, длину 2,5-3,5 см, ширину 1,5-2,5 см и массу 5-8 г. При этом правый яичник имеет чуть большие размеры, чем левый. Первичные половые железы у зародыша закладываются уже на 3-й неделе внутриутробного развития и включительно до 6-7 недели не имеют никаких половых различий. Только с 7-8 недели беременности гонады начинают дифференцироваться в яичники (у зародышей с женским набором хромосом) и к 25 неделе формирование морфологических структур яичников заканчивается.
Симптомы аномалий развития яичников зависят от формы болезни. Как правило, для таких патологий характерно:
Для смешанной формы характерно увеличение клитора и присутствие рудиментарной матки.
Какие бывают пороки развития яичников
Аномалии развития яичников довольно разнообразны. Реже всего встречается полное отсутствие одного или обоих яичников. Более часто у женщин диагностируется наличие дополнительной половой железы, состоящей из островков яичниковой ткани, прилегающих или прикрепленных непосредственно к яичнику. Также нередко встречаются гипертрофированные яичники, значительно превышающие размерами норму. Такие изменения происходят из-за увеличения фолликулярного слоя и практически не оказывают влияния на нормальную функциональную деятельность половой железы.
Очень редкой патологией являются раздвоенные яичники разного или одинакового размера, расположенные один за другим. Возникает такая патология вследствие редупликации первичных гонад. Также к порокам развития яичников относится опущение яичника с образованием грыж, из-за которых орган смещается в тот или иной грыжевой мешок.
Аномалии развития яичников и пороки половых путей взаимно не обусловлены и могут не комбинироваться, поскольку половые протоки и половые железы формируются не синхронно и из разных эмбриональных зачатков. Аномальные яичники зачастую располагаются в несвойственных для них местах, к примеру, в паховом канале. Пороки развития яичников нуждаются в обязательном лечении и максимально пристальном внимании, поскольку в тканях таких половых желез довольно нередко образуются очаги бластоматозного роста, что угрожает не только здоровью, но и жизни женщины.
Диагностика
Диагностическое исследование пороков развития яичников включает:
Необходимы консультации генетика и онколога. После проведения дифференциальной диагностики ставится диагноз и определяется тип патологии. В Клинике Современной Медицины работают лучшие акушеры-гинекологи, эндокринологи, онкологи и генетики Москвы, имеющие уникальный опыт работы в диагностике и лечении пороков развития органов репродуктивной системы, что дает возможность быстро установить характер нарушения кариотипа, досконально исследовать яичники с минимумом дискомфорта.
Лечение аномалий развития яичников
Лечение пороков развития яичников может быть как консервативным, так и оперативным. Метод терапии врач подбирает индивидуально, на основании полученных при обследовании данных. Объем и способ лечения напрямую зависит от характера патологии, формы дисгенезии гонад, выраженности клинических проявлений и других факторов.
Полное излечение аномалий развития яичников невозможно. Симптоматическое лечение заключается в назначении заместительной гормонотерапии с целью предотвращения метаболических нарушений. Нередко патология требует оперативного лечения, которое заключается в удалении аномальной половой железы.
Клиника Современной Медицины обладает передовой лечебно-диагностической базой для определения типа дисгенезии гонад и оснащена прогрессивным оборудованием для выполнения сложных микрохирургических операций. Большой опыт работы в данной области позволяет нашим специалистам быстро определить характер патологии, провести тщательное, всестороннее обследование яичников с минимальным стрессом для пациентки и назначить грамотное и результативное лечение.
Наш медицинский центр оказывает самый широкий спектр услуг. Вы всегда можете обратится к нам по вопросам лечения гинекологических заболеваний. Мы готовы оказать вам услуги лечения сальпингита и лечения сальпингоофорита.