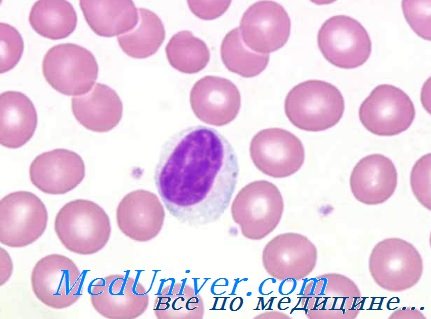
Тяжелый комбинированный иммунодефицит что это
Тяжелый комбинированный иммунодефицит что это
Больные с комбинированными нарушениями гуморального и клеточного иммунитета страдают тяжелыми, часто оппортунистическими инфекциями, которые без трансплантации костного мозга приводят к смерти в грудном возрасте. Считается, что распространенность таких дефектов невелика. Однако их истинная частота неизвестна, так как скрининг новорожденных на какое-либо из этих нарушений не проводится. Не исключено, что многие случаи смерти от инфекций в грудном возрасте связаны именно с комбинированными нарушениями иммунитета.
В основе синдромов тяжелого комбинированного иммунодефицита (ТКИД) лежат мутации различных генов, приводящие к выпадению всех адаптивных иммунных реакций, а в некоторых случаях и к отсутствию NK-клеток. Для этих синдромов характерны наиболее тяжелые нарушения иммунитета.
Патогенез тяжелого комбинированного иммунодефицита
В типичных случаях тимус очень маленький и весит менее 1 г. Обычно он остается в области шеи, содержит крайне мало клеток, граница между корковым и мозговым веществом в нем неразличима, тельца Гассаля отсутствуют. Эпителий тимуса сохранен. В фолликулярной и паракортикальной областях селезенки лимфоциты практически отсутствуют. Лимфатические узлы, миндалины, аденоиды и пейеровы бляшки либо отсутствуют, либо в значительной степени недоразвиты.
Клинические проявления тяжелого комбинированного иммунодефицита. Уже в первые месяцы жизни у больных возникают понос, пневмония, средний отит, сепсис и кожные инфекции. Вначале ребенок растет нормально, но понос и инфекции приводят к его резкому истощению. Такие оппортунистические инфекции, как Candida albicans, P. carinii, ветряная оспа, корь, парагрипп 3, ЦМВ, вирус Эпштейна-Барр, аденовирус и БЦЖ, оказываются смертельными.
Чужеродные ткани у больных не отторгаются, что создает опасность реакции «трансплантат против хозяина», обусловленной проходящими через плаценту материнскими Т-лимфоцитами, а также Т-лимфоцитами, присутствующими в необлученных препаратах крови или аллогенном костном мозге.
С самого рождения отмечается лимфопения (
Иммунодефицит
Содержание статьи
Читая об иммунодефицитных состояниях, многие люди неверно понимают, что значит данное заболевание, считая, что это более частые простуды и общее недомогание. В реальности иммунодефицит у взрослого – это серьезная, достаточно тяжелая патология, при которой перестают работать одно или несколько звеньев иммунной защиты организма от инфекций. Причем, это не одно единственное заболевание, а целая группа процессов, имеющих разные причины и симптомы болезни, тяжесть и прогнозы.
Опасность иммунодефицитов в том, что на фоне серьезных изменений иммунная система перестает надежно защищать организм от агрессии возбудителей, в силу чего вирусные и бактериальные инфекции протекают тяжело, с осложнениями и могут грозить неблагоприятными исходами. Источник:
М. Есеналиев. Синдром приобретенного иммунодефицита – главная проблема общественного здравоохранения // Вестник АГИУВ, 2013, №1, с.64-65.
Классификация иммунодефицитов
С точки зрения причин и патогенеза иммунодефицитов их можно разделить на три большие группы.
Физиологические иммунодефициты, возникающие на определенном этапе жизни, связанные с особенностями работы иммунной системы. Самые известные виды – это младенческие, возникающие в период новорожденности и раннего детства, изменения иммунной системы в период беременности, а также старческое снижение иммунной защиты. Они не требуют лечения, но инфекции могут возникать чаще и протекают несколько тяжелее.
Первичный иммунодефицит (ПИД) связан с дефектами в генах. Его признаки проявляются с самого рождения, связаны с поломкой определенного гена, который отвечает за активность того или иного звена иммунитета (отсутствие определенных клеток, защитных белков). На сегодняшний день известно более 200 вариантов ПИД, в целом до 6 млн людей в мире страдают этим состоянием, и у большей части состояние своевременно не выявляется. В РФ каждый 500 ребенок рождается с определенным дефектом иммунитета первичного характера, на сегодняшний день под наблюдением врачей находится более 3000 пациентов.
Вторичные иммунодефициты возникают в течение жизни. Самый известный из них – это патология, вызванная заражением ВИЧ-инфекцией, которая по мере прогрессирования вызывает так называемый синдром приобретенного иммунодефицита (СПИД). Но известны и другие вирусы иммунодефицита у взрослого, которые приводят к повреждениям иммунной системы и отказу одного из звеньев защиты организма. Помимо вирусных инфекций провокаторами могут становиться различные методы терапии онкологических заболеваний и сами эти патологии, прием медикаментов при лечении серьезных патологий Источник:
Ю.Н. Фёдоров, В.И. Клюкина, М.Н. Романенко, О.А. Богомолова, А.Н. Денисенко. Стратегия и принципы иммунокоррекции и иммуномоделирующей терапии. и т.д.
Причины возникновения
В отношении первичных иммунодефицитов точной причины, вызывающей повреждения генов не определено. Возможно влияние тератогенных факторов во время беременности, изначальные дефекты в половых клетках родителей, нарушения во время внутриутробного развития, вызванные перенесенными инфекциями, приемом лекарств или проблемами здоровья матери.
Вторичными причинами могут стать вирусы, поражающие иммунные клетки, облучение, химиопрепараты,тяжелые инфекции и т.д.
Признаки иммунодефицитов
При иммунодефицитах основными проявлениями становятся тяжело протекающие бактериальные, грибковые или вирусные инфекции. Речь идет не о банальных простудах, а о серьезных состояниях: постоянные синуситы, рецидивирующие пневмонии, множественные абсцессы, грибковые поражения кожи, слизистых и кишечника, герпетические высыпания. Чем тяжелее стадия иммунодефицита, тем серьезнее проявления.
Врачи выделяют пять групп ПИД в зависимости от поражения того или иного звена иммунитета:
Заподозрить ПИД можно по набору определенных признаков, но диагноз подтверждается лабораторно, по данным иммунограммы, а при ВИЧ – выявляя антитела к иммунодефициту человека. Среди ключевых признаков можно отметить:
Задачи иммунологических обследований:
Проведение иммунотерапии
После того как выполнена полная диагностика и определен тип иммунодефицита, врач-иммунолог подбирает индивидуальную схему лечения.
Применение иммунотерапии (препаратов для коррекции иммунитета) направлено на усиление работы иммунной системы, коррекции нарушенного баланса иммунных реакций, подавление агрессии аутоиммунитета, патологически активных процессов. Важно также стимулировать именно нарушенные у конкретного пациента звенья иммунитета.
Тяжелый комбинированный иммунодефицит
Общая информация
Краткое описание
Тяжелый комбинированный иммунодефицит (тяжелая комбинированная иммунная недостаточность-ТКИН) – генетически обусловленный иммунодефицит, характеризующийся практически полным отсутствием зрелых Т-лимфоцитов при наличии или отсутствии В- и НК-лимфоцитов, что ведет к ранним, крайне тяжелым инфекциям вирусной, бактериальной и оппортунистической природы и в отсутствие патогенетической терапии смерти в первые два года жизни.
Общая частота ТКИН 1:50000 новорожденных. Среди больных преобладают лица мужского пола.
Соотношение кодов МКБ-10 и МКБ-9
| МКБ-10 | МКБ-9 | ||
| Код | Название | Код | Название |
| D81.0 | Тяжелый комбинированный иммунодефицит с ретикулярным дисгенезом | 86.10 | Диагностические процедуры на коже и подкожных тканях |
| D81.1 | Тяжелый комбинированный иммунодефицит с низким содержанием Т и В- клеток | 86.11 | Биопсия кожи и подкожных тканей |
| D81.2 | Тяжелый комбинированный иммунодефицит с низким и нормальным содержанием В-клеток | 40.11 | Биопсия лимфатической структуры |
| D81.3 | Дефицит аденозиндезаминазы | ||
| D81.4 | Синдром Незелофа | ||
| D81.5 | Дефицит пуриннуклеозидфосфорилазы | ||
| D81.6 | Дефицит молекул класса I главного комплекса гистосовместимости | ||
| D81.7 | Дефицит молекул класса IIглавного комплекса гистосовместимости | ||
| D81.8 | Другие комбинированный иммунодефициты | ||
| D81.9 | Комбинированный иммунодефицит неуточненный | ||
Дата разработки/пересмотра протокола: 2016 год.
Пользователи протокола: врачи общей практики, педиатры, неонатологи, детские онкологи/гематологи, иммунологи, аллергологи.
Категории пациентов: дети 0-2 года.
Шкала уровня доказательности:
| A | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты которых могут быть распространены на соответствующую популяцию. |
| B | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| C | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+). Результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D | Описание серии случаев или неконтролируемое исследование или мнение экспертов. |
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
В зависимости от измененного гена выделяют аутосомно-рецессивный и Х-сцепленный тип наследования [2].
Диагностика (амбулатория)
ДИАГНОСТИКА НА АМБУЛАТОРНОМ УРОВНЕ [1-3,5,7]
Диагностические критерии
Жалобы и анамнез: разнообразие жалоб связано с многообразием клинических проявлений осложнений тяжелого комбинированного иммунодефицита и уровнем дефекта. Преимущественные жалобы на затяжные пневмонии, отставание массы тела, частый жидкий стул, длительный кашель, затяжные лихорадки, появление частых гнойных выделений из различных локусов, упорный афтозный стоматит, снижение аппетита, рвота, длительный кашель [3,5].
При сборе семейного анамнеза надо обращать внимание на случаи повторных тяжелых инфекций и смертей детей в раннем возрасте с клиникой инфекционных заболеваний. Смерти мальчиков в нескольких поколениях в семье позволяет предполагать Х-сцепленный характер заболевания. Близкородственный брак у родителей увеличивает вероятность аутосомно-рецессивной патологии [2, 5-7].
Клиническая симптоматика:
· отставание ребенка в возрасте до 1 года в весе и росте;
· поствакцинальные осложнения (БЦЖит диссеминированный, полиомиелит паралитический и др.);
· перенесенные не менее 2 раз тяжелые инфекции, такие как: менингит, остеомиелит, целлюлит, сепсис;
· частые гнойные отиты — не менее 3-4 раз в течение одного года;
· упорная молочница и грибковые поражения кожи;
· гнойное воспаление придаточных пазух носа 2 и более раз в течение года;
· рецидивирующие гнойные поражения кожи;
· рецидивирующие типичные бактериальные инфекции, протекающие в тяжелой форме, с необходимостью использования множественных курсов антибиотиков (до 2 месяцев и дольше);
· оппортунистические инфекции (например: Pneumocystic carini), вирусами герпес группы, грибками, проявляются в очень тяжелой, хронической форме или не поддаются стандартному лечению, (необходимо внутривенное введение антибиотиков);
· рецидивирующие (повторные) диареи; мальабсорбция;
· отсутствие/увеличение лимфатических узлов;
· увеличение печени и селезенки;
· наличие в семье больных ПИД;
· наличие в семейном анамнезе смерти ребенка раннего возраста с клиникой инфекционного заболевания;
· изменения в анализе крови: очень часто анемия, в лейкоформуле снижение количества лимфоцитов, эритроцитов, реже тромбоцитов;
· абсцессы внутреннего органа;
· рецидивирующие абсцессы подкожной клетчатки;
· тяжелое или длительное проявление бородавок, контагиозный моллюск.
Физикальное обследование
· рост и вес ребенка. У детей с ТКИН часто отмечается задержка развития;
· лимфатическая система: периферические лимфатические узлы уменьшены или отсутствуют, реже лимфаденопатия (чрезмерная);
· увеличение печени и селезенки;
· кожные покровы и слизистые: кандидоз кожи и слизистых при отсутствии предрасполагающих факторов (лечения антибиотиками или кортикостероидами, инфицирование при кормлении грудью). Изъязвления языка, слизистой рта и перианальной области. Гнойные инфекции кожи и подкожной клетчатки. Возможна сыпь по типу себорейного дерматита. Конъюнктивит, вызванный Haemophilus influenzae;
· заболевания ЛОР органов: хронические гнойные отиты, сопровождающиеся рубцовыми имениями барабанной перепонки;
· неврологические нарушения: энцефалопатии;
· позднее отпадение пуповины, омфалиты.
Инструментальные исследования:
· УЗИ органов брюшной полости, щитовидной железы и других органов (по показаниям);
· УЗИ вилочковой железы;
· Рентгенография органов грудной клетки (по показаниям);
· Рентгенография грудной клетки в двух проекциях (дополнительно размер вилочковой железы).
Диагностический алгоритм: (схема) 
Диагностика (стационар)
ДИАГНОСТИКА НА СТАЦИОНАРНОМ УРОВНЕ [2,4] (УД – В)
Диагностические критерии: см. амбулаторный уровень.
Лабораторные исследования:
· общий анализ крови + лейкоформула ручным методом;
· биохимический анализ крови: ферритин сыворотки, железо сыворотки, трансферрин, АЛТ, АСТ, билирубин общий/фракции, щелочная фосфатаза, гамма‐глутамилтранспептидаза, общий белок, определение белковых фракций, уровень иммуноглобулинов A,M,G,E, креатинин, мочевина, электролиты;
· развернутая иммунограмма : подсчет субпопуляционного состава Т-, В-лимфоцитов, NK-клеток, HLA DR+CD3+, HLADR+CD3-, CD25+, CD95+;
· CD4+8+, уровень сывороточных иммуноглобулинов (с подтипами G1,2,3,4, sIgA), кислородзависимый и кислороднезависимый фагоцитоз, определение активности компонентов комплемента, тесты функциональной активности Т-лимфоцитов, цитокиновый статус, интерфероновый статус, экспрессия рецепторов цитокинов;
· определение TREG [2];
· исследование крови на ВИЧ;
· HLA-типирование ребенка и его ближайших родственников (сибсов и родителей) [2];
· микробиологические исследования – посевы биоматериала (на флору и грибы) с определением антибиотикочувствительности со слизистых, из очагов инфекции (включая кровь, мочу, кал, бронхоальвеолярный лаваж, ликвор и биопсийный материал) [2];
· при наличии вакцинации БЦЖ микроскопия материала на кислотоустойчивые бактерии, а также выявление M.bovii методом ПЦР;
· молекулярно- генетический анализ с помощью ПЦР и последующего секвенирования;
· ИФА и ПЦР на цитомегаловирусную, Эпштейн-Барр вирусную, герпес-инфекцию, токсоплазмоз;
· при подозрении на Т-В- ТКИН – АДА недостаточность необходимо цитохимическое исследование: определение АДА в эритроцитах и лимфоцитах;
· морфологическое исследование пунктата костного мозга с целью дифференциальной диагностики;
· гистологическое исследование кожи, лимфоузлов и ткани тимуса при подозрении на синдром Омен [4].
Инструментальные исследования [2]:
· УЗИ брюшной полости и забрюшинного пространства для оценки вовлеченности внутренних органов;
· УЗИ вилочковой железы;
· компьютерная томография грудной клетки с контрастированием сосудов даже при отсутствии указаний на подтвержденные пневмонии в анамнезе;
· рентгенография грудной клетки;
· рентгенография придаточных пазух носа в динамике.
Диагностический алгоритм: (схема)
Перечень основных диагностических мероприятий:
· общий анализ крови + лейкоформула ручным методом;
· пунктат костного мозга (миелограмма);
· биохимический анализ крови;
· определение белковых фракций;
· развернутая иммунограмма : подсчет субпопуляционного состава Т-,В-лимфоцитов, NK-клеток, HLA DR+CD3+, HLADR+CD3-, CD25+, CD95+, CD4+8+, уровень сывороточных иммуноглобулинов (с подтипами G1,2,3,4, sIgA), кислородзависимый и кислороднезависимый фагоцитоз, определение активности компонентов комплемента, тесты функциональной активности Т-лимфоцитов, цитокиновый статус, интерфероновый статус, экспрессия рецепторов цитокинов;
· общий анализ мочи;
· исследование крови, других сред на стерильность, грибы;
· бак посев из зева на стерильность, грибы;
· ИФА на цитомегаловирус, вирусы простого герпеса;
· ПЦР (кровь, моча, слюна) на цитомегаловирус, ВПГ, ВЭБ, вирус Зостер;
· ИФА на грибковые инфекции;
· ПЦР (кровь, отделяемого из различных локусов) на грибковую инфекцию;
· копрология, исследование кала на яйца глист и простейших;
· УЗИ органов брюшной полости и забрюшинного пространства;
· УЗИ вилочковой железы;
· рентгенография грудной клетки в 2-х проекциях;
· компьютерная томография грудной клетки с контрастированием сосудов;
· молекулярно-генетическое исследование с целью выявления причинной генетической мутации;
· исследование крови на ВИЧ;
· HLA типирование пациента (в качестве реципиента ТГСК) и его сиблингов ( в качестве потенциальных доноров).
Тяжелый комбинированный иммунодефицит
Причины, диагностика, лечение тяжелого комбинированного иммунодефицита – заболевания, которое при отсутствии лечения приводит к смерти на первом году жизни.
Новорожденный ребенок защищен от инфекций благодаря иммунитету, который он получает от матери. В первые месяцы жизни иммунная система ребенка развивается и приобретает способность бороться с инфекциями. Однако иммунная система некоторых детей не способна самостоятельно защитить организм от инфекций: у таких детей развивается иммунодефицит.
Симптомы иммунодефицита зависят от того, какое звено иммунной системы вовлекается в патологический процесс, и варьируются от слабо выраженных до угрожающих жизни. Тяжелый комбинированный иммунодефицит является одним из угрожающих жизни иммунодефицитов.
Тяжелый комбинированный иммунодефицит – это редкое заболевание, для которого существуют методы лечения, если оно выявлено своевременно. При отсутствии лечения ребенок погибает на первом году жизни.
Что такое тяжелый комбинированный иммунодефицит?
Тяжелый комбинированный иммунодефицит – это целая группа наследственных заболеваний, характеризующихся серьезными нарушениями работы иммунной системы. Эти нарушения заключаются в уменьшении количества или изменении функции T- и B-лимфоцитов – специализированных лейкоцитов, которые образуются в костном мозге и защищают организм от инфекций. Из-за нарушения работы иммунной системы организм не может бороться с вирусами, бактериями и грибами.
Термин «комбинированный» означает, что в патологический процесс вовлекаются оба вида лимфоцитов, тогда как при других заболеваниях иммунной системы поражается только один вид клеток. Существует несколько форм комбинированного иммунодефицита. Самая распространенная форма заболевания связана с мутацией гена X-хромосомы и встречается только у мужчин, так как они наследуют одну X-хромосому. Поскольку женщины наследуют две X-хромосомы (одну патологическую и одну нормальную), они являются только носителями заболевания, иммунные нарушения у них при этом отсутствуют.
Причиной другой формы заболевания является дефицит фермента аденозиндеаминазы. Остальные формы заболевания связаны с различными генетическими мутациями.
Диагностика
Основным симптомом тяжелого комбинированного иммунодефицита является повышенная восприимчивость к инфекциям и задержка физического развития (как следствие перенесенных инфекций).
У ребенка с тяжелым комбинированным иммунодефицитом наблюдаются рецидивирующие бактериальные, вирусные или грибковые инфекции, имеющие тяжелое течение и плохо поддающиеся лечению. К таким инфекциям относятся инфекции уха (острый средний отит), синуситы, кандидоз (грибковая инфекция) полости рта, инфекции кожи, менингит и пневмония. Кроме того, у детей наблюдается хроническая диарея. При наличии перечисленных симптомов врач должен заподозрить тяжелый комбинированный иммунодефицит и провести соответствующее обследование.
Будущим родителям, имеющим наследственную предрасположенность к иммунодефициту, рекомендуется пройти генетическое консультирование. Ребенку, родившемуся от таких родителей, следует как можно раньше сделать анализ крови, поскольку ранняя диагностика позволяет своевременно начать лечение и улучшить прогноз заболевания. При наличии данных о генетической мутации у родителей или их ближайших родственников заболевание можно диагностировать еще во время беременности. Чем раньше начать лечение, тем больше шансов на выздоровление.
При отсутствии данных о наследственной предрасположенности заболевание удается диагностировать только в возрасте 6 месяцев или позже.
Лечение
После того как у ребенка диагностируют тяжелый комбинированный иммунодефицит, его направляют к детскому иммунологу или детскому инфекционисту.
Важную роль в лечении заболевания играет профилактика инфекций, поэтому врач назначает ребенку антибиотики и советует родителям не находиться с ребенком в местах скопления людей и изолировать его от больных людей.
Детям с тяжелым комбинированным иммунодефицитом ни в коем случае нельзя вводить живые вирусные вакцины (против ветряной оспы, а также кори, паротита и краснухи). Попадание даже ослабленного вакцинного вируса в организм ребенка представляет опасность для его здоровья.
Кроме того, детям внутривенно вводят иммуноглобулины, которые помогают организму бороться с инфекциями.
Наиболее эффективным методом лечения тяжелого комбинированного иммунодефицита является пересадка стволовых клеток. Стволовые клетки – это клетки костного мозга, из которых образуются все виды клеток крови. Их вводят в организм ребенка с целью формирования новых клеток иммунной системы.
Наилучших результатов удается достичь, если для пересадки использовать костный мозг брата или сестры больного ребенка. Если у ребенка нет братьев и сестер, используется костный мозг родителей. Для некоторых детей не удается найти подходящего донора среди ближайших родственников – в этом случае используются стволовые клетки человека, не состоящего с ребенком в родственных связях. Вероятность благоприятного исхода увеличивается, если пересадка стволовых клеток выполняется в течение первых месяцев жизни ребенка.
Некоторым пациентам перед пересадкой стволовых клеток проводится химиотерапия. Химиопрепараты разрушают клетки костного мозга, освобождая место для донорских клеток и предотвращая реакцию на их введение. Химиотерапия не проводится пациентам, у которых мало иммунных клеток. Решение о необходимости проведения перед пересадкой стволовых клеток химиотерапии принимается с учетом нескольких факторов: тяжести иммунодефицита, формы заболевания, донора, у которого будут взяты стволовые клетки, и места проведения пересадки.
Если причиной тяжелого комбинированного иммунодефицита является отсутствие фермента, пациенту каждую неделю вводят соответствующий фермент. Данный метод не позволяет вылечить заболевание, поэтому пациенты должны получать фермент пожизненно.
В настоящее время изучается еще один метод лечения – генная терапия. Суть метода заключается в получении клеток больного ребенка, внедрении в них новых генов и введении в организм ребенка. После того как эти клетки попадут в костный мозг, они дадут начало новым иммунным клеткам.
Уход за ребенком
После пересадки костного мозга детям назначают антибиотики или иммуноглобулины.
До тех пор пока иммунная система не начнет работать в полную силу, ребенок должен носить маску, что позволит снизить риск развития инфекций. Кроме того, маска является сигналом, указывающим на то, что ребенку требуется защита.
Детям с тяжелым комбинированным иммунодефицитом приходится пройти через большое количество болезненных процедур и госпитализаций. Это может стать испытанием для всей семьи. К счастью, существуют группы взаимопомощи, социальные работники и друзья, которые всегда готовы помочь и не дадут родителям ребенка остаться наедине с бедой.
В каком случае следует обратиться к врачу
Родителям следует проконсультироваться с врачом в том случае, если их ребенок болеет чаще, чем другие дети. Если у ребенка тяжелая инфекция, необходимо немедленно обратиться за медицинской помощью.
Чем раньше начать лечение, тем больше шансов на выздоровление и восстановление работы иммунной системы. Если у ребенка диагностирован тяжелый комбинированный иммунодефицит, следует обратиться к врачу при появлении любой инфекции.