Кафедра факультетской хирургии им. И.И. Грекова – сто лет в движении.
В апреле 2013 года «молодая» кафедра факультетской хирургии им. И.И. Грекова, появившаяся при объединении в 2011 году кафедры хирургии им. В.А. Оппеля СПбМАПО и кафедры хирургических болезней МПФ СПбГМА им. И.И. Мечникова, стала инициатором проведения в СЗГМУ им. И.И. Мечникова международной конференции, посвященной хирургии поджелудочной железы. По приглашению зав. кафедрой проф. В.П. Земляного в Петербург приехал один из самых авторитетных мировых специалистов в этой области хирургии проф. Ганс Бегер – автор оригинальной операции при хроническом панкреатите, когда производится резекция поджелудочной железы с сохранением двенадцатиперстной кишки. Авторитет корифея мировой хирургии и кафедры факультетской хирургии им. И.И. Грекова в этой области, позволили собрать в нашем университете, пожалуй, всех ведущих специалистов в хирургии поджелудочной железы из России, стран СНГ и Германии. Конференция позволила напомнить наш приоритет в этой области, ведь еще в 1913 году основатель нашей кафедры проф. Иван Иванович Греков в статье «К хирургии pancreas», описывал случай успешной резекции поджелудочной железы при опухоли в ее головке, с сохранение тонкой полоски ткани поджелудочной железы на двенадцатиперстной кишке.
15 февраля 1915 года В.М. Бехтерев приглашает И.И. Грекова организовать кафедру хирургии психо-неврологического института. Можно ли говорить, что только мы являемся продолжателями школы Грекова. Пожалуй нет. Наверно, вся хирургия России, СССР XX века развивалась под его влиянием. Он был инициатором оживления работы хирургического общества Пирогова, которое практически перестало работать в годы Первой мировой войны, а так же возродил издание «Вестника хирургии и пограничных областей» главным редактором которого он был 12 лет (ныне журнал носит его имя). В речи на гражданской панихиде, московский проф. В.Н. Розанов сказал: «Греков так же популярен, как и Обуховская больница. Грекова не нужно было называть, достаточно было сказать – Иван Иванович, и всякий знал, что это предложил, сказал профессор И.И. Греков, чьи работы известны не только хирургам, но и любому образованному врачу».
Родился Греков 5 марта 1867 года в семье донского казака в Воронежской губернии. Отец его умер рано, поэтому жил он в стесненных обстоятельствах. В 1885 году Иван Иванович поступил на историко-филологический факультет Московского университета. В 1890 году за участие в уличных выступлениях Греков был заключен в Бутырскую тюрьму и исключен из университета. В последующем он получил возможность вернуться в университет, но уже не в Московский, а на медицинский факультет в Юрьевский. После университета в 1895 году Иван Иванович поступил работать в качестве экстерна в Обуховскую больницу, в которой и проработал всю жизнь, дойдя до должности главного врача. На тот момент Обуховская больница была одной из самых крупных в Петербурге и включала два самостоятельных учреждения – мужскую и женскую больницы с особой администрацией в каждой. Мужским хирургическим отделением заведывал А.А. Троянов, женским – А.А. Кадьян. Считается, что А.А. Троянов был создателем «обуховской» школы хирургов, из которой вышли ряд других крупных хирургов. Штат хирургического отделения был ограничен и включал заведующего и одного помощника, что объяснялось обилием экстернов, работавших бесплатно. В качестве экстерна Греков проработал 8 лет. Хоть и трудные в материальном плане – эти годы, позволили Ивану Ивановичу накопить огромный опыт лечения гнойных заболеваний и неотложных заболеваний органов брюшной полости и грудной клетки. В 1905 году А.А. Троянов ушел из Обуховской больницы, его место занял Цейдлер, а И.И. Греков возглавил женское хирургическое отделение. Хоть больница и имела собственное гинекологическое отделение Греков, так же активно интересовался лечением гнойников малого таза. Операция эвагинации сигмовидной кишки (Греков I) была выполнена в качестве импровизации, когда его позвали для помощи в гинекологическую операционную больной с повреждением сигмовидной кишки вследствие криминального аборта. С 1912 года он заведовал мужским отделением, а в 1926 году мужское и женское отделения были объединены под его началом.
В 1915 году на базе Обуховской больницы развертываются кафедры психо-неврологического института, хирургическую клинику которого возглавил И.И. Греков. На съездах хирургов России, инициатором возрождения которых (с 1922 года) он и был, Греков и его сотрудники выступают с программными докладами по лечению перитонита. Иван Иванович был сторонником широкого применения тампонирования брюшной полости, что не нашло широкого распространения в будущем, а вот подходы Грекова к лечению ранению груди остаются актуальными поныне. В 1931 году была произведена реконструкция Обуховской больницы и на ее базе открывают III медицинский институт. Умер И.И. Греков внезапно 11 февраля 1934 года на заседании в ЛГИУВе.
Удивительно, но исторические пути обеих объединившихся кафедр пересеклись при самом своем основании. Известно, что II кафедру хирургии ЛГИУВа проф. В.А. Оппель основывает 13 февраля 1928 года на базе хирургического отделения больницы им. И.И. Мечникова, которой он тогда заведовал. Владимир Андреевич работал во многих ведущих клиниках нашего города, однако заботы по созданию крупного хирургического отделения будущей основной клинической базы нашего университета, стали одними из самых значимых событий в его жизни. Сам он так говорит об этом:
«История получения мной в заведывание хирург. Отделения б. Мечникова такова. В 1920 г. больница Петра Великого – так называлась тогда б. Мечникова – была закрыта. Весной 1924 г. Лининградский Губздрав решил не только больницу открыть, но и достроить. В илюле 1924 г. т. Адуевский пригласил меня посмотреть на достраивающееся хирург. отделение. Я пришел в полный восторг: было совершенно ясно, что хирург. отделению предстоит огромная работа. Все отделение должно было располагать 250 хирургическими койками. Операционный корпус имел 4 операционные и совершенно обособленное послеоперационное отделение на 50 коек. Меня крайне удивило, что от заведывания таким отделением отказывались некоторые хирурги. С большим удовольствием принял я предложение т. Адуевского заведывать этим отделением. Лучшего отделения я себе представить не мог – я лучшего отделения до сих пор не видел. В своем решении я не раскаиваюсь и сейчас. ».
Проф. В.А. Оппель отмечал, что заняв место заведующим большим (на 250 коек) хирургическим отделением б. Мечникова, он поставил себе задачу содействовать уничтожению границ между «клиническим» и «больничным» подходом к больным, что и является основной отличительной чертой университетской хирургической клиники.
Сердце любой хирургической клиники – операционная. Один из операционных залов кафедры факультетской хирургии не обычен – он окрашен в черный цвет – черный пол, черные стены, черный потолок. Это операционная Оппеля. Почему Владимир Андреевич решил выбрать столь необычный цвет, ассоциирующийся скорее со смертью, чем с жизнью. В то время было принято все больничные помещения красить в белый цвет, как свидетельство чистоты и опрятности. В то же время, яркий белый свет утомляет глаза, что может приводить к усталости во время операции. В.А. Оппель пришел к идее пойти на столь необычный шаг так:
Можем подтвердить на основании наших наблюдений мнение Оппеля, что больные даже под местной анестезией спокойно оперируются в черной операционной, не испытывая страха. Интересно, что известный хирург из лейпцига Heller, узнав от Э.Р. Гессе о черной операционной Оппеля, завел у себя зеленую операционную.
Мы не можем рассматривать историю кафедры в отрыве от культурной среды России первой половины XX века. 17 декабря 1915 года на выставке супрематического исскуства, был представлен черный квадрат Каземира Малевича. Это была в некотором смысле революция в искусстве, создание нового алфавита цветоформ, нового языка в живописи. Любопытно, что Малевич проводил научные исследования по влиянию цветовой среды на людей, в частности на трудоспособность. На основании своих исследований он пришел к заключению, что белый цвет стен и предметов в больницах опасен и вреден, и рекомендовал для хирургических костюмов использовать зеленый цвет, он же предложил оранжевый цвет для одежды сотрудников ремонтных и спасательных служб.
Удивительно, но черная операционная оказалась очень удобна для новых медицинских технологий – эндовидеохирургических операций, когда создается оптимальная световая среда для выполнения лапароскопических операций.
В 1932 году проф. В.П. Оппель передает II кафедру хирургии ЛГИУВа своему помощнику по работе в хирургическом отделении больницы Мечникова – Николаю Николаевичу Самарину, который одним из первых в СССР начал выполнять панкреато-дуоденальные резекции.
В эти же годы кафедра госпитальной хирургии 2-го ЛМИ получает в качестве клинической базы 15 пав. больницы Мечникова. К сожалению, очень короткий период с 1934 года по 1936 г. кафедрой руководил Э.Р. Гессе, подготовивший 2-х томное руководство по хирургии, считавшееся одним из лучших в свое время. В 1937 году Эрик Романович был расстрелян по ложному доносу.
Говоря о формировании хирургической школы кафедры факультетской хирургии им. И.И. Грекова следует упомянуть имя основателя желчной хирургии в России С.П. Федорова. Владимир Андреевич Оппель 6 лет работал под руководством проф. Федорова. Другой ученик Сергея Петровича Федорова – проф. Александр Васильевич Смирнов приглашается в 1937 году на заведывание кафедрой госпитальной хирургии 2-го ЛМИ. Проф. А.В. Смирнов длительное время руководил кафедрой вплоть до 1965 г., оставаясь научным консультантом до 1972 года. Александр Васильевич активно развивает желчную хирургию, хирургию поджелудочной железы. На базе хирургической клиники 15 павильона больницы Мечникова работал всесоюзный центр по лечению заболеваний гепато-панкреато-дуоденальной зоны. В 1972 году выходит его монография «Хирургическое лечение заболеваний поджелудочной железы и периампулярной области», объединившая весь накопленный за предыдущие годы в этой области опыт. Совместно с зав. II хирургической кафедрой ЛГИУВа проф. Г.А. Гомзяковым, А.В. Смирнов обобщает опыт, накопленный за годы войны в атласе огнестрельных ранений – «Огнестрельные ранения таза и мочеполовой системы», 1953 год.
В связи с необходимостью организации преподавания торакальной и сосудистой хирургии в 1971 в ЛСГМИ приглашается на заведование кафедрой проф. М.И.Бурмистров, выполнивший первое протезирование митрального клапана в Ленинграде. В это время, направление работы клиники меняется, ведущее значение придается разделам торакальной и сосудистой хирургии. Данные направления развивали проф. Ф. В. Баллюзек, К.Н. Сазонов, С.М. Лазарев. Стоит отметить, что после работы в ЛСГМИ Ф.В. Баллюзек возглавлял кафедру сосудистой хирургии ЛГИУВа.
Высокая актуальность и сложность лечения острого панкреатита определили интерес возглавлявших в 90-е годы кафедру хирургических болезней №2 ЛСГМИ проф. В.И. Ковальчука и заведующего кафедрой неотложной хирургии СПб МАПО проф. А.С. Шугаева к этой сложной проблеме. Разрабатываются классификации острого панкреатита, оригинальные подходы к его лечению, в том числе определение хирургической тактики.
В 2011 году объединенную кафедру возглавил заслуженный врач России, проф. Вячеслав Петрович Земляной. Освоив под руководством проф. А.М. Гранова все нюансы хирургии печени и панкреато-дуоденальной зоны, Вячеслав Петрович организует первое в истории хирургическое отделение в инфекционной больнице, что позволяет накопить уникальный опыт лечения хирургических осложнений инфекционных заболеваний.
МЕХАНИЧЕСКАЯ ЖЕЛТУХА: диагностический алгоритм и лечение
Cреди хирургических заболеваний печени и внепеченочных желчных путей наиболее тяжелыми могут быть признаны те, которые сопровождаются стойкой непроходимостью магистральных желчных протоков с последующим развитием механической желтухи (МЖ). Проблемы диагн
Cреди хирургических заболеваний печени и внепеченочных желчных путей наиболее тяжелыми могут быть признаны те, которые сопровождаются стойкой непроходимостью магистральных желчных протоков с последующим развитием механической желтухи (МЖ). Проблемы диагностики и дифференциальной диагностики причин обтурации желчных путей не потеряли актуальности и в настоящее время. Хирургические вмешательства у больных МЖ, выполняемые по экстренным показаниям, сопровождаются большим числом осложнений, а летальность достигает 15-30%, что в 4 раза выше, чем в тех случаях, когда МЖ удается ликвидировать до операции [3, 7]. Огромный опыт, накопленный зарубежными и отечественными хирургами, показывает, что синдром МЖ возникает у 15-40% больных с желчнокаменной болезнью (ЖКБ) и у всех больных, имеющих опухолевое поражение желчных путей [1, 5, 9]. Декомпрессия билиарной системы является одной из главных целей и важнейшим компонентом лечебных мероприятий у этих пациентов.
Людей, страдающих МЖ, следует относить к группе пациентов с острыми хирургическими заболеваниями. В настоящее время большинство зарубежных и отечественных авторов считают оптимальным проведение лечения больных МЖ в два этапа [1, 2, 3, 7, 9, 10]. На первом этапе выполняют временную наружную или внутреннюю декомпрессию билиарных путей с помощью различных методов желчеотведения, а на втором, после ликвидации МЖ, при плановой операции стараются устранить причину, вызвавшую МЖ. Такая тактика лечения позволяет добиться уменьшения количества послеоперационных осложнений и снижения уровня общей летальности.
Вместе с тем в ходе разработки способов желчеотведения у больных МЖ возникает ряд проблем и спорных вопросов. Тяжелыми осложнениями МЖ являются холангит и печеночная недостаточность (ПН). Ведущие факторы в патогенезе холангита — холестаз с последующим присоединением инфекции.
В последнее время для декомпрессии желчных путей используют малоинвазивные эндоскопические или чрескожные чреспеченочные методы желчеотведения под контролем рентгенологического аппарата, ультразвукового аппарата (УЗИ), компьютерного томографа (КТ) или лапароскопа [2, 4, 6, 8, 10]. В 2001 году исполнилось 75 лет с начала применения чрескожных методов контрастирования билиарной системы (Burckhardt H., Muller W., 1921) и 40 лет — чрескожного чреспеченочного желчеотведения у больных МЖ (Remolar I. et al., 1956).
Узловыми вопросами в лечении МЖ остаются сроки и виды декомпрессивных вмешательств, методы профилактики и лечения послеоперационной ПН. Кроме того, оценки эффективности, преимуществ и недостатков различных «закрытых» и «открытых» методов декомпрессии желчных путей при МЖ не проводилось. Поэтому проблема выбора инструментальной дооперационной декомпрессии желчных протоков при МЖ и гнойном холангите остается предметом дискуссии.
Итак, основная цель хирургического вмешательства при МЖ — декомпрессия желчевыводящих путей, устранение обтурации, ликвидация желтухи и профилактика возникновения или прогрессирования ПН. В настоящее время арсенал желчеотводящих методов при МЖ достаточно велик и включает в себя:
МЖ может быть доброкачественного (наблюдается у 45-55% больных) и злокачественного генеза. Среди МЖ доброкачественного генеза наиболее часто встречается холедохолитиаз, в остальных случаях речь идет о рубцовых стриктурах внепеченочных желчных путей, панкреатитах, паразитарных заболеваниях гепатобилиарной зоны, дивертикулах и доброкачественных опухолях большого дуоденального сосочка (БДС). Опухолевая природа заболевания обусловлена раком головки поджелудочной железы (ПЖ), БДС, желчного пузыря, гепатикохоледоха, ворот печени и метастазами рака другой локализации в печень.
Накопленный опыт лечения больных МЖ позволил нам разработать и внедрить новый алгоритм диагностики и лечения данной категории больных. В алгоритм диагностики МЖ кроме стандартного клинико-лабораторного исследования входят УЗИ, эзофагогастродуоденоскопия (ЭГДС), ЭРХПГ, КТ, ЧЧХГ и лапароскопия. Каждое исследование при необходимости можно превратить из диагностической процедуры в лечебную. При разработке алгоритма мы исходили из того, что МЖ должна быть ликвидирована как можно раньше от начала заболевания из-за опасности развития холангита и ПН. При этом процесс диагностики МЖ не должен отодвигать сроки начала ее лечения. Целесообразно диагностику и лечение МЖ проводить одновременно, хотя нередко лечение опережает по времени дифференциальную диагностику причины и уровня обтурации желчных путей.
Лечение больных с МЖ должно носить комплексный характер. Консервативные мероприятия кроме нормализации гомеостаза и инфузионной терапии включают следующие мероприятия:
Все существующие малоинвазивные методы декомпрессии билиарной системы можно разделить на две группы: эндоскопические (без нарушения целостности кожного покрова) и чрескожные. К первой группе относятся ЭРХПГ с ЭПСТ, назобилиарное дренирование, различные варианты эндопротезирования желчных путей. ЭРХПГ с ЭПСТ на протяжении многих лет остается основным методом эндоскопического лечения холедохолитиаза. Этот метод позволяет в 85-90% случаев удалять конкременты из общего желчного протока и восстанавливать желчеотток. ЭРХПГ дает возможность не только контрастировать протоки, но и визуально оценить состояние БДС, а также периампулярной области. С этой точки зрения возможности ЭРХПГ, безусловно, шире по сравнению с другими методами исследования желчевыводящих путей. При наличии крупных фиксированных камней по ходу магистральных желчных протоков к ретроградному контрастированию последних прибегать не следует, ограничившись проведением УЗИ или КТ. Ретроградное контрастирование в этом случае ведет к ухудшению состояния больного в связи с увеличением гипертензии во внутрипеченочных протоках, инфицированием и затрудненной эвакуацией контрастного вещества и желчи. В такой ситуации показана чрескожная чреспеченочная декомпрессия желчных путей. Если размер камня больше диаметра образованного устья общего желчного протока, прибегают к внутрипротоковому разрушению камня с помощью ретроградной механической литотрипсии. Эта методика, по данным многих зарубежных авторов, может быть признана высокоэффективной. Иногда ЭРХПГ с ЭПСТ недоступна — после резекции желудка по Бильрот-II, наличие крупных дивертикулов и непреодолимых препятствий в устье общего желчного протока.
Необходимость во временном эндопротезировании гепатикохоледоха и назобилиарном дренировании вызвана наличием у пациентов выраженной желтухи и холангита в условиях, когда санация гепатикохоледоха оказалась неполной и желчеотток не был окончательно восстановлен. Назобилиарное дренирование в этих случаях помимо желчеотведения позволяет также промывать желчные пути растворами антибиотиков, что способствует быстрой ликвидации холангита и дает возможность выполнять рентгеноконтрастные исследования для контроля за отхождением фрагментов разрушенного камня и мелких конкрементов.
Транспапиллярное эндопротезирование гепатикохоледоха нами выполняется в основном при опухолях панкреатобилиарной зоны, стриктурах. Для этой цели используются стандартные эндопротезы фирм «Olimpus» (Япония) и «Willson-Cook» (США), сроки функционирования которых составляют 4-5 месяцев. Перед эндопротезированием выполняется ЭПСТ в целях профилактики острого панкреатита, который может возникнуть при обтурации устья панкреатического протока концом эндопротеза.
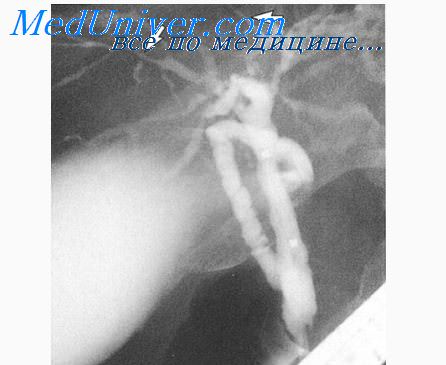
Ко второй группе малоинвазивных методов декомпрессии желчных путей относят ЧЧХГ с ЧЧХС, чрескожную чреспеченочную холецистостомию под контролем УЗИ, КТ или лапароскопа. Несмотря на совершенствование УЗИ диагностики и КТ, объективная информация о патологии желчных протоков, достаточная для принятия решения о методе декомпрессии, может быть получена только при прямом контрастировании желчных путей. В последние 10 лет широкое распространение получили методы чрескожных чреспеченочных эндобилиарных вмешательств [2, 5, 7, 8, 10]. Их удается осуществить независимо от уровня и протяженности обтурации желчных путей. Осложнения и летальность при них составляют от 3 до 10%. На начальном этапе ЧЧХГ проводили в целях дифференциальной диагностики МЖ, определения уровня блока желчных протоков, решения вопроса о возможности выполнения наружного дренирования. Абсолютными противопоказаниями к ЧЧХГ мы считаем непереносимость контрастных препаратов и выраженные нарушения свертывающей системы крови.
С внедрением в клиническую практику УЗИ, КТ потребность в выполнении ЧЧХГ сократилась. В настоящее время мы выполняем ЧЧХГ у больных с незначительной дилятацией желчных протоков, а также при подозрении на доброкачественную стриктуру желчных протоков и вентильный камень дистального отдела гепатикохоледоха у пациентов, которым невозможно выполнить ЭРХПГ.
В последние годы наложение чрескожной чреспеченочной холецистостомы под контролем УЗИ, КТ или лапароскопа стало наиболее распространенным методом, позволяющим не только сразу установить характер и место обтурации желчных путей, но и осуществить их декомпрессию. Рентгенологический вид блока при заболеваниях, вызывающих обтурационную желтуху, не является строго специфичным, что может быть объяснено различной распространенностью процесса, наличием мелких включений, замазкоподобных масс и воспалительного отека. Противопоказания к чрескожным чреспеченочным вмешательствам — множественные метастазы в печень, крайне тяжелое состояние больных с некорригируемой ПН, выраженная гипокоагуляция с угрозой кровотечения.
Целесообразность применения каждого метода декомпрессии определяется несколькими факторами, основными из которых являются:
Преимущественное значение, определяющее лечебный результат, имеют два первых фактора.
С учетом накопленного нами опыта мы рекомендуем придерживаться следующей схемы лечебно-диагностических малоинвазивных инструментальных вмешательств при МЖ: клинико-лабораторные данные, УЗИ, КТ Ѓ ЭРХПГ или ЧЧХГЃ ЭПСТ или ЧЧХС или холецистостомия Ѓ лапаротомия.
Если возможности малоинвазивных методов декомпрессии желчных протоков исчерпаны или ограничены, то в срочном порядке больному показана лапаротомия с выполнением одного из методов интраоперационного желчеотведения.
Адекватность декомпрессии оценивается нами путем изучения функционального состояния печени и изменения пейзажа микрофлоры. О степени нарушения функционального состояния печени позволяют судить данные радиоизотопной гепатографии, антипириновой и биливердиновой проб, которые выявляют снижение поглотительно-выделительной и обезвреживающей функций печени, повышение уровня билирубина в крови. Для выявления степени инфицированности желчи и определения эффективности антибактериальной терапии проводится изучение микрофлоры и количественного бактериологического анализа желчи методом газовой хроматографии и масс-спектрометрии.
Таким образом, малоинвазивные эндоскопические и чрескожные чреспеченочные декомпрессионные вмешательства представляют собой эффективный способ восстановления желчеоттока при обструкции билиарной системы. Эти методики позволяют достаточно быстро и эффективно ликвидировать МЖ и холангит, дают возможность проводить хирургические вмешательства в наиболее благоприятных условиях, в плановом порядке, а у больных пожилого возраста с тяжелой сопутствующей патологией могут служить альтернативой хирургическому лечению. Эти вмешательства малотравматичны и сопровождаются небольшим числом осложнений. Применение этих методов позволяет значительно улучшить результаты лечения больных МЖ.
Литература
1. Данилов М. В., Глабай В. П., Кустов А. Е. и др. Хирургическое лечение больных механической желтухой опухолевой этиологии //Анналы хир. гепатологии. 1997. Т. 2. С. 110-116.
2. Ившин В. Г., Якунин А. Ю., Макаров Ю. И. Чрескожные чреспеченочные диагностические и лечебные вмешательства у больных с механической желтухой //Анналы хир. гепатологии. 1996. Т. 1. С. 121-131.
3. Каримов Ш. И. Эндобилиарные вмешательства в диагностике и лечении больных с механической желтухой. Ташкент: Издательство им. Ибн Сины, 1994. 239 с.
4. Прокубовский В. И., Капранов С. А. Чреспеченочное эндопротезирование желчных протоков //Хирургия. 1990. № 1. С.18-23.
5. Савельев В. С., Прокубовский В. И., Филимонов М. И. и др. Чрескожное чреспеченочное дренирование желчных путей при механической желтухе //Хирургия. 1988. № 1. С. 3-7.
6. Хрусталева М. В. Современные эндоскопические транспапиллярные методы лечения механической желтухи //Анналы НЦХ РАМН. 1997. С. 39-42.
7. Шаповальянц С. Г., Цкаев А. Ю., Грушко Г. В. Выбор метода декомпрессии желчных путей при механической желтухе //Анналы хир. гепатологии. 1997. Т. 2. С. 117-122.
8. Cotton P. B. Endoscopic management of biliary strictures //Annu gastrointes. endoscopy. 1993. P. 6.
9. Guschieri A., Buess G., Perissat J. Operative manual of endoscopic surgery //Springer-Verlag. 1993. V. 2. P. 273.
10. Murai R., Hashig Ch., Kusujama A. Percutaneus stenting for malignant biliary stenosis //Surgical endoscopy. 1991. V. 5. P. 140.
Перемежающуюся желтуху можно объяснить тест
Любое поражение печеночной паренхимы может стать настолько тяжелым, что печень не в состоянии даже в наименьшей степени обеспечить необходимые для жизни функции, а это клинически выражается в картине печеночной комы. По всей вероятности, ведущую роль при этом играет содержание аммиака в крови2. Поступающий из кишечника аммиак не превращается печенью с достаточной быстротой в мочевину. Диагностически важно обратить внимание на то, что, помимо тяжести поражения печеночной паренхимы, возникновению печеночной комы может способствовать также повышенное образование аммиака вследствие избыточного введения белка, кишечных кровотечений, приемов хлористого аммония или мочевины, а также инфекций, кровопусканий, пункций асцита и применения чрезмерно сильных седативных средств.
Во всяком случае определение содержания аммиака в сыворотке крови не оказалось надежным показателем тяжести печеночной недостаточности. Клинически печеночная кома иногда сопровождается острым, напоминающим истерию, состоянием возбуждения и некоординированным психическим поведением. Опытный врач распознает печеночную кому по характерному печеночному запаху. Перкуторно часто можно определить уменьшение размеров печени, что говорит об ее атрофии. Другим признаком начинающейся печеночной комы являются резко положительные функциональные пробы печени. В этом отношении особенно оправдало себя определение концентрации протромбина. Если концентрация протромбина падает ниже 30% и не повышается после введения больших доз витамина К (приблизительно 100 мг), то надо считать, что имеется тяжелейшее нарушение функции печени.
Содержание холестеринэстеров уменьшается. На ЭКГ появляется характерное удлинение интервала Q — T с широким зубцом Т (гепато-кардиальный синдром).Электрофоретически отмечается увеличение у-глобулинов за счет а-глобулинов. В моче могут быть обнаружены кристаллы лейцина и тирозина. Проба Миллона резко положительна.
Перемежающаяся юношеская желтуха — Icterus juvenilis intermittens Мейленграхта (Meulengracht). Практически важны дискинезии желчных путей (v. Bergmann), которые надо отличать от легких рецидивирующих поражений паренхимы печени. Они, по-видимому, идентичны перемежающейся юношеской желтухе Мейленграхта и простой семейной холемии Жильбера (cholemie simple familiale Gilbert). Поражаются молодые люди с повышенной возбудимостью вегетативной нервной системы. Желтуха, никогда не превышающая субиктеричности, усиливается после психических или физических напряжений. Она сопровождается в большинстве случаев повышенной утомляемостью, приводящей больных к врачу. В некоторых случаях на передний план выступают болевые ощущения в области печени.
Желтуха может рецидивировать в течение ряда лет. Результаты всех исследований (пальпация, функциональные исследования печени, дуоденальное зондирование, осмотическая резистентность эритроцитов и т. д.) отрицательны. Патогенез еще окончательно не выяснен. Согласно более новым исследованиям (Arias), заболевание, по всей вероятности, обусловлено понижением активности ферментов, принимающих участие в образовании билирубин-глюкуронида. Клинически эта ферментная недостаточность еще не доступна распознаванию. Диагноз, таким образом, ставится преимущественно путем исключения других поражений печени при нормальных показателях функциональных проб и данных биопсии печени. Диагноз подкрепляет семейное возникновение заболевания.
Dubin и Johnson выделили недавно близко стоящую к юношеской желтухе картину болезни на основе обнаружения аморфного коричневого пигмента в печеночных клетках (при пункции печени). Но, по-видимому, речь идет о заболевании, идентичном гипербилирубинемии после гепатита (Kalk). Клинически эта особая хроническая, идиопатическая желтуха (Dubin и Johnson) дифференцируется от холемии Жильбера на основании следующих признаков: а) темная моча, б) более часто встречающееся выделение билирубина с мочой, в) билирубин сыворотки всегда дает прямую реакцию ван ден Берга, г) выделение бромсульфалеина часто задержано, д) рентгенологически не удается получить изображения желчного пузыря, е) имеется характерная пигментация печеночных клеток (биопсия или пункция печени).
Хронический гепатит является обычно следствием перенесенного эпидемического гепатита. Вероятно, между хроническим гепатитом и билирубинемией после гепатита (Kalk) имеются лишь количественные различия.
О хроническом гепатите говорят в тех случаях, когда при симптомах, описанных выше, можно обнаружить, помимо билирубинемии, объективные признаки заболевания (набухание печени, увеличение селезенки, положительные результаты функциональных проб печени). Решающее значение для диагноза имеют гистологические данные исследования материала, полученного при пункционной биопсии печени (круглоклеточные инфильтраты, изменения паренхиматозных клеток).
Хотя окончательно решить вопрос о положении этих часто наблюдаемых клинических картин болезни — гипербилирубинемии после гепатита и хронического гепатита — еще невозможно из-за малочисленности гистологических исследований, все же представляется вероятным, что речь идет об идентичных, лишь количественно разнящихся проявлениях одного и того же патологического процесса в печеночных клетках.