о молекуле можно сказать что она имеет агрегатное состояние массу запах
Основные агрегатные состояния вещества
Агрегатные состояния вещества
Чтобы разобраться с тем, какими бывают агрегатные состояния, предлагаю по ходу чтения статьи заполнять таблицу.
Агрегатные состояния
Свойства
Расположение молекул
Расстояние между молекулами
Движение молекулы
Лед, вода и водяной пар — это все три агрегатных состояния одного вещества. Лед — твердое состояние, вода — жидкая, пар — газообразное. Для каждого вещества существует три состояния.
Твердое состояние
Его очень легко представить — это любой предмет, который мы встречаем в жизни. В этом состоянии тело сохраняет форму и объем. Расстояние между молекулами, приблизительно равно размеру самих молекул, которые, в свою очередь, расположены очень структурированно.
Такая структура называется кристаллической решеткой — из-за четкой структуры молекулам сложно двигаться, и они просто колеблются около своих положений.
Заполняем нашу табличку
Агрегатные состояния
Свойства
Расположение молекул
Расстояние между молекулами
Движение молекулы
сохраняет форму и объем
в кристаллической решетке
соотносится с размером молекул
колеблется около своего положения в кристаллической решетке
Жидкое состояние
В этом состоянии сохраняется объем, но не сохраняется форма. Например, если перелить молоко из кувшина в стакан, то молоко, имевшее форму кувшина, примет форму стакана. Кстати, в корове у молока тоже была другая форма.
Расстояние между молекулами в жидком состоянии чуть больше, чем в твердом, но все равно невелико. При этом частицы не собраны в кристаллическую решетку, а расположены хаотично. Молекулы почти не двигаются, но при нагревании жидкости делают это более охотно.
Вспомните, что происходит, если залить чайный пакетик холодной водой — он почти не заваривается. А вот если налить кипяточку — чай точно будет готов.
Агрегатные состояния
Свойства
Расположение молекул
Расстояние между молекулами
Движение молекулы
сохраняет форму и объем
в кристаллической решетке
соотносится с размером молекул
колеблется около своего положения в кристаллической решетке
близко друг к другу
малоподвижны, при нагревании скорость движения молекул увеличивается
Газообразное состояние
В жизни мы встречаем газообразное состояние вещества, когда чувствуем запахи. Запах очень легко распространяется, потому что газ не имеет ни формы, ни объема (он занимает весь предоставленный ему объем), состоит из хаотично движущихся молекул, расстояние между которыми больше, чем размеры молекул.
Агрегатные состояния
Свойства
Расположение молекул
Расстояние между молекулами
Движение молекулы
сохраняет форму и объем
в кристаллической решетке
соотносится с размером молекул
колеблется около своего положения в кристаллической решетке
близко друг к другу
малоподвижны, при нагревании скорость движения молекул увеличивается
занимают предоставленный объем
больше размеров молекул
хаотичное и непрерывное
С агрегатными состояниями разобрались, ура! Но до сих пор неясно, каким образом у каждого вещества их целых три, и как одно переходит в другое. Для этого узнаем, что такое фазовые переходы.
Фазовые переходы: изменение агрегатных состояний вещества
При изменении внешних условий (например, если внутренняя энергия тела увеличивается или уменьшается в результате нагревания или охлаждения) могут происходить фазовые переходы — изменения агрегатных состояний вещества.
Фазовые переходы интересны тем, что все живое не Земле существует лишь благодаря тому, что вода умеет превращаться в лед или пар. С кристаллизацией, плавлением, парообразованием и конденсацией связаны многие процессы металлургии и микроэлектроники.
На схеме — названия всех фазовых переходов:
Переход из твердого состояния в жидкое — плавление;
Переход из жидкого состояния в твердое — кристаллизация;
Переход из газообразного состояния в жидкое — конденсация;
Переход из жидкого состояния в газообразное — парообразование;
Переход из твердого состояния в газообразное, минуя жидкое — сублимация;
Переход из газообразного состояния в твердое, минуя жидкое — десублимация.
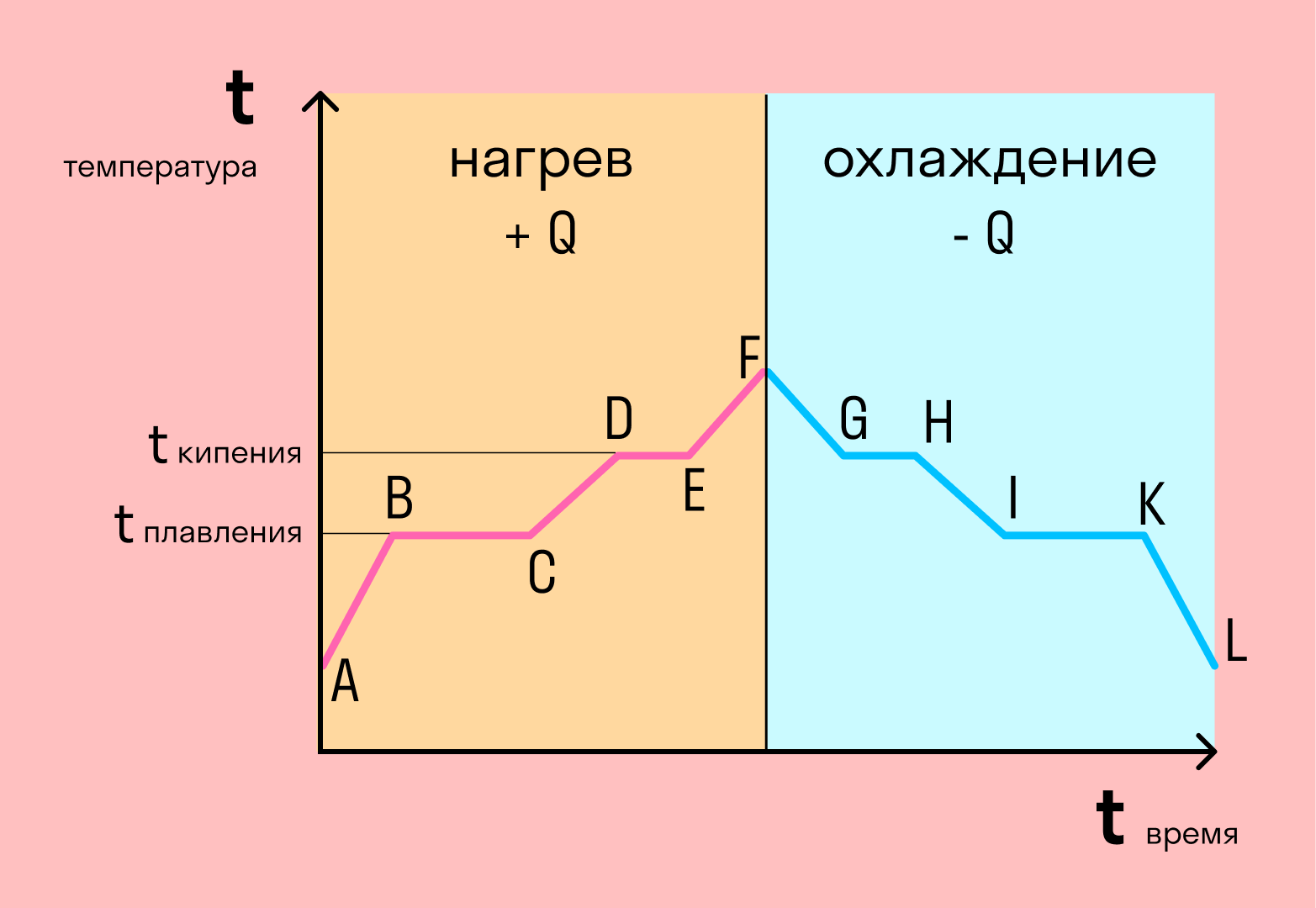
График фазовых переходов
Если взять процесс превращения льда в воду, воды — в пар, и обратные действия, то мы получим очень информативный график.
Разбираемся по шагам. Сначала взяли лед, конечно, при отрицательной температуре, потому что при нуле лед начинает плавиться. Нагрели лед до температуры плавления (до 0 градусов).
После того, как лед нагрелся до температуры плавления, он начинает плавиться. Плавление происходит при постоянной температуре тем дольше длится, чем больше масса плавящегося вещества. Еще этот процесс зависит от свойств самого вещества, но об этом немного позже.
Расправившись вещество уже в жидком состоянии снова начинает нагреваться, и температура увеличивается, пока не достигает температуры кипения. В данном случае нагревается вода — это значит, что ее температура кипения равна 100 градусам Цельсия.
При 100 градусах вода кипит, пока не выкипит целиком. В данном случае процесс аналогично плавлению происходит при постоянной температуре. Данный процесс нельзя путать с испарением, потому что парообразование происходит при конкретной температуре, а испарение — при любой.
Далее полученный пар нагревается, но путем нагревания невозможно дойти до другого фазового перехода — можно пойти только обратно.
Первый шаг в обратную сторону — охлаждение до температуры кипения.
Дойдя до температуры кипения (в данном случае 100 градусов), пар начинает переходить в жидкое состояние. Этот процесс также происходит при постоянной температуре.
Сконденсировавшись, вода охлаждается, пока не начнет замерзать.
Кристаллизуется (замерзает) вода при той же температуре, что и плавится лед — 0 градусов. Кристаллизация также происходит при постоянной температуре.
После кристаллизации лед охлаждается.
С нагреванием и охлаждением все совсем просто — мы либо передаем теплоту телу (веществу), и оно идет на увеличение температуры, либо тело отдает тепло и охлаждается.
В остальных процессах температура не меняется. Это связано с тем, что количество теплоты не всегда зависит от температуры. Формулы для всех процессов выглядят так:
Нагревание
Охлаждение
Q — количество теплоты [Дж]
c — удельная теплоемкость вещества [Дж/кг*˚C]
m — масса [кг]
tконечная — конечная температура [˚C]
tначальная — начальная температура [˚C]
Плавление
Кристаллизация
Q — количество теплоты [Дж]
λ — удельная теплота плавления вещества [Дж/кг]
m — масса [кг]
Парообразование
Конденсация
Q — количество теплоты [Дж]
L — удельная теплота парообразования вещества [Дж/кг]
m — масса [кг]
Решение задач по фазовым переходам
С теорией разобрались — а теперь давайте практиковаться!
Задачка раз. Температура медного образца массой 100 г повысилась с 20 °С до 60 °С. Какое количество теплоты получил образец? Удельную теплоёмкость меди считать равной 380 Дж/(кг умножить на °С)
Q = 380 * 0,1*(60-20) = 1520 Дж
Ответ: образец получил 1520 Дж
Задачка два. Какое количество теплоты необходимо для плавления 2,5 т стали, взятой при температуре плавления? Удельная теплота плавления стали λ=80кДж/кг. Теплопотерями пренебречь.
80 кДж/кг = 80000 Дж/кг
Q = 80000*2500 = 200 000 000 Дж = 200 МДж
Ответ: для плавления 2,5 т стали необходимо 200 МДж теплоты.
Сублимация и десублимация
Мы уже рассказали про такие процессы, как сублимация и десублимация.
Примерчики из жизни🤓
Про принтеры. Цветные принтеры (только не лазерные) печатают путем сублимации. Вот как это работает: частицы краски быстро переходят из твердого состояния в газообразное и оседают на бумаге — так получается цветная картинка.
Рисуночки на окнах. Если вы решите проехаться на автобусе в холодную погоду — увидете на стеклах чудесные узоры. Из-за огромной разницы температур между улицей и автобусом, мы можем наблюдать процесс десублимации в виде красивых рисунков на стеклах. Иней образуется похожим способом — резкое похолодание приводит к десублимации воздуха.
Влажность воздуха: испарение и конденсация
Такие процессы, как испарение и конденсация, становятся более логичными и простыми, если их рассмотреть на примере влажности воздуха.
Влажность воздуха говорит нам о том, сколько в воздухе содержится водяного пара. Любое количество пара в воздух не запихнешь, поэтому, во-первых, его там очень мало, а во-вторых, при избыточном количестве водяного пара происходит конденсация — это когда образуется роса.
Как влажность влияет на человека
Для человека влажность очень важна, потому что мы состоим из воды на 90%. Если окружающей среде нечего испарять, она будет испарять нас. Поэтому при низкой влажности мы чувствуем сухость во рту, а при высокой — волосы впитывают влагу, разбухают и начинают виться. На этом принципе построены некоторые гигрометры — приборы для измерения влажности. Они так и называются — волосяные гигрометры. Только внутри не человеческий волос, а конский, но принцип от этого не меняется.
При высокой влажности холод и тепло воспринимаются более чувствительно. Это связано с потливостью человека при высокой температуре. Такой механизм помогает нам бороться с жарой, но при высокой влажности пот не может испариться. При испарении пота мы теряем избыточное тепло, а в данном случае этого не происходит.
При низкой влажности происходит нечто похожее. Как ни странно, в мороз мы тоже потеем (намного меньше, но все-таки это происходит). Если влажность на улице низкая, то пот испарится из-под куртки и нам будет комфортно, а при высокой влажности — он там задержится и будет проводить тепло наружу, забирая у нас драгоценные Джоули тепла. Поэтому зимой в Петербурге холоднее, чем в Москве.
Влажностью можно управлять. Существуют мешочки с шариками адсорбентами, которые кладут в коробки с обувью, чтобы впитать лишнюю влагу. Чтобы окна не запотевали, можно насыпать в рамы соль, которая также впитает влагу. А если вам наоборот нужно больше влаги — берем увлажнитель воздуха (классная вещь!): он добавляет в воздух водяной пар.
Контрольная работа по теме «Первоначальные понятия» (химия, 8 класс)
Ищем педагогов в команду «Инфоурок»
Вид контролируемой деятельности
Уровень усвоения знаний
Простые и сложные вещества
Простые и сложные вещества
Вещества, свойства веществ
Вещества, свойства веществ
Чистые вещества и смеси
Вещество, химический элемент
Понятие о химическом элементе
Структура Периодической Системы
Структура Периодической Системы
Явления физические и химические
Устанавливать причинно-следственные связи
Относительная молекулярная масса. Массовая доля химического элемента
Вещества и физические тела. Физические свойства. Физические и химические явления. Основы атомно-молекулярного учения
Количество вещества. Моль. Молярная масса
Количество вещества. Моль. Молярная масса
Количество вещества. Моль. Молярная масса
Контрольная работа по теме «Первоначальные химические понятия»
Часть А Из предложенных вариантов выберите 1 правильный ответ:
А) молекул Б) химических элементов В) веществ Г) атомов
2. О молекуле можно сказать, что она имеет
А) массу Б) агрегатное состояние В) запах Г) температуру кипения
3. Из приведенных утверждений:
А) Атомы – это мельчайшие химически неделимые частицы вещества
Б) Простые вещества состоят из атомов разных элементов
А) верно только А Б) верно только Б В) верно А и Б Г) оба утверждения неверные
4. Сложным является каждое из двух веществ:
А) KNO 3 и Cl 2 Б) P и О 3 В) KOH и А r Г) CO 2 и NH 3
5. Свойством вещества не является
А) горючесть Б) цвет В) агрегатное состояние Г) плотность
6. О веществе можно сказать:
А) большое Б) круглое В) твердое Г) длинное
7. Для очистки воды от растворенных в ней минеральных солей используется
А) отстаивание Б) дистилляция В) фильтрование Г) выпаривание
8. О простом веществе железо идет речь в выражении
А) железо входит в состав стали Б) железо входит в состав ржавчины
В) железо входит в состав железного купороса Г) железо притягивается магнитом
9. О химическом элементе кислороде идет речь в выражении
А) кислород входит в состав воздуха Б) кислород входит в состав воды
В) кислород хранится в стальном баллоне Г) кислород растворяется в воде
10. В V группе 2 периода находится элемент __________, порядковый номер которого равен _____, атомная масса _______.
11. Укажите элемент, атомная масса которого равна 56 а.е.м.. Укажите номер группы, номер периода, порядковый номер данного элемента
12. Запишите химические формулы веществ, если известно, что их молекулы состоят:
А) из двух атомов азота и пяти атомов кислорода
Б) из двух атомов водорода, одного атома кремния и трех атомов кислорода
В) из одного атома алюминия, одного атома фосфора, четырех атомов кислорода
13. Растения поглощают углекислый газ и воду, а в процессе фотосинтеза вырабатывают кислород и органические вещества. Из этого следует,
А) кислород – простое вещество Б) фотосинтез – химическая реакция
В) вода и углекислый газ – сложные вещества Г) молекулы воды состоят из атомов кислорода и водорода
14. На какой диаграмме распределение массовых долей элементов соответствует 
15. Допишите схемы реакций, расставьте коэффициенты
1. Дополните определения:
1. Физические явления – процессы, в ходе которых….
2. Вещество – вид материи, …
2. Напишите формулы соединений с кислородом для следующих элементов:
А) лития Б) углерода (валентность IV ) В) фосфора (валентность III ) Г) серы (валентность II )
3. Установите соответствие между уравнением реакции и типом
А) реакция соединения
Б) реакция замещения
Г) реакция разложения
4. Расставьте коэффициенты, преобразовав схемы 5 задания в уравнения реакций
Рассчитайте число молекул, которое содержится в 7 моль MgO
Фосфор массой 2 г прореагировал с кислородом. Какая масса кислорода вступила в реакцию? Какая масса оксида фосфора Р 2 О 5 образовалась в ходе реакции?
Известно, что 140 г некоторого металла содержат 2,5 моль атомов этого элемента. О каком металле идет речь?
Контрольная работа по теме «Первоначальные химические понятия»
Часть А Из предложенных вариантов выберите 1 правильный ответ:
А) молекул Б) химических элементов В) веществ Г) атомов
2. Об атоме можно сказать, что он имеет
А) массу Б) агрегатное состояние В) запах Г) температуру кипения
3. Из приведенных утверждений:
А) Атомы состоят из молекул
Б) сложные вещества состоят из простых веществ
А) верно только А Б) верно только Б В) верно А и Б Г) оба утверждения неверные
4. Простым является каждое из двух веществ:
А) KNO 3 и Cl 2 Б) P и О 3 В) KOH и А r Г) CO 2 и NH 3
5. Свойством вещества не является
А) текучесть Б) цвет В) агрегатное состояние Г) электропроводность
6. О веществе нельзя сказать:
А) большое Б) ковкое В) твердое Г) растворимое
7. Для очистки воды от древесных опилок используется
А) отстаивание Б) дистилляция В) фильтрование Г) выпаривание
8. О простом веществе медь идет речь в выражении
А) проволока сделана из меди Б) медь входит в состав оксида меди
В) медь входит в состав малахита Г) медь входит в состав бронзы
9. О химическом элементе азоте идет речь в выражении
А) азот является составной частью воздуха Б) взрывчатое вещество тротил содержит азот
В) азот имеет меньшую плотность, чем кислород Г) жидкий азот иногда используется для замораживания продуктов
10. В III группе 2 периода находится элемент __________, порядковый номер которого равен _____, атомная масса _______.
11. Укажите элемент, атомная масса которого равна 48 а.е.м.. Укажите номер группы, номер периода, порядковый номер данного элемента
12. Запишите химические формулы веществ, если известно, что их молекулы состоят:
А) из двух атомов мышьяка и пяти атомов кислорода
Б) из двух атомов водорода, одного атома серы и трех атомов кислорода
В) из трех атома калия, одного атома фосфора, четырех атомов кислорода
13. Растения поглощают кислород, в процессе дыхания образуется углекислый газ, вода и другие продукты обмена. Из этого следует,
А) кислород – простое вещество Б) дыхание – химическая реакция
В) вода и углекислый газ – сложные вещества Г) молекулы воды состоят из атомов кислорода и водорода
14. На какой диаграмме распределение массовых долей элементов соответствует 
15. Допишите схемы реакций, расставьте коэффициенты
1. Дополните определения:
1. Химические реакции – процессы, в ходе которых….
2. Молекула – наименьшая частица веществ _________________строения. Молекулы образованы ….
2. Напишите формулы соединений с водородом для следующих элементов:
А) лития Б) углерода (валентность IV ) В) фосфора (валентность III ) Г) серы (валентность II )
3. Установите соответствие между уравнением реакции и типом
А) реакция соединения
Б) реакция замещения
Г) реакция разложения
4. Расставьте коэффициенты, преобразовав схемы 5 задания в уравнения реакций
Рассчитайте число молекул, которое содержится в 5 моль Na 2 O
Кальций массой 2 г прореагировал с кислородом. Какая масса кислорода вступила в реакцию? Какая масса оксида кальция СаО образовалась в ходе реакции?
Известно, что 5 моль двухатомных молекул некоторого неметалла имеют массу 140 г. О каком неметалле идет речь?