нимесулид при панкреатите можно или нет
Сравнительная оценка влияния нимесулида на верхние отделы желудочно-кишечного тракта
Показано, что нимесулид оказывает значительно меньшее негативное влияние на верхние отделы желудочно-кишечного тракта, чем другие неселективные нестероидные противовоспалительные препараты (диклофенак, кетопрофен и индометацин).
Nimesulide has significantly less negative impact on the upper gastrointestinal tract than other non-selective non-steroidal anti-inflammatory drugs (diclofenac, ketoprofen and indomethacin).
Нимесулид — один из наиболее популярных в России представителей группы нестероидных противовоспалительных препаратов (НПВП). Это лекарство имеет в нашей стране репутацию эффективного и достаточно безопасного анальгетика и широко используется в различных отраслях медицины (прежде всего, в ревматологии, неврологии и травматологии), в которых имеется необходимость борьбы с острой или хронической болью [1–3].
Одной из главных особенностей российского опыта применения нимесулида является нередкое использование его продолжительными курсами. В большинстве стран мира нимесулид рассматривается прежде всего как ургентное обезболивающее средство; учитывая ограничения контролирующих органов, он назначается лишь на короткое время, обычно менее двух недель [4]. В нашей стране, напротив, нимесулид часто рекомендуют больным с хроническими заболеваниями, такими как остеоартроз (ОА), ревматоидный артрит (РА) и анкилозирующий спондилоартрит (АС). При этой патологии суммарный срок приема нимесулида у российских пациентов может достигать многих месяцев и даже лет.
Такая практика дает большой материал для оценки достоинств и недостатков лекарства, прежде всего, его безопасности.
Как известно, главной проблемой НПВП является риск развития побочных эффектов со стороны желудочно-кишечного тракта (ЖКТ) и сердечно-сосудистой системы [5, 6]. При этом основным достоинством нимесулида считается хорошая гастроинтестинальная переносимость, что, собственно, определяет основное преимущество этого препарата в сравнении со многими другими НПВП [1–4, 7].
Однако четких доказательств, подтверждающих низкий риск серьезных ЖКТ-осложнений (таких как кровотечения и клинически выраженные язвы) при использовании нимесулида, относительно немного. Имеются лишь немногочисленные работы, в которых специально изучалась частота таких опасных побочных эффектов, и отдельные исследования, организованные в соответствии с жесткими современными критериями «доказательной медицины», — двойные слепые, рандомизированные и контролируемые [7–9].
В этом случае большое значение приобретает анализ частоты осложнений, которые отмечаются в реальной клинической практике. Так, в клинику ФГБУ НИИР им. В. А. Насоновой РАМН ежегодно поступает для стационарного лечения большое число пациентов с различными ревматическими заболеваниями (РЗ) — ревматоидным артритом (РА), остеоартрозом (ОА), серонегативными спондилоартритами (ССА) и др., которые в течение длительного времени принимают НПВП, в т. ч. нимесулид. В данном учреждении функционирует собственный эндоскопический кабинет, основным направлением работы которого является выявление патологии верхних отделов ЖКТ. Результаты обследования больных РЗ, которые находятся в архиве кабинета эндоскопии, позволяют получить достаточно большой материал для оценки частоты патологии верхних отделов ЖКТ, возникающей на фоне приема НПВП.
Целью настоящего исследования было оценить сравнительную частоту и характер изменений верхних отделов ЖКТ у больных РЗ, регулярно принимавших нимесулид.
Материал и методы исследования
Мы провели ретроспективный анализ результатов всех эндоскопических исследований верхних отделов ЖКТ (эзофагогастродуоденоскопия (ЭГДС)), выполненных за период 2011–2013 гг. в клинике ФГБУ НИИР им. В. А. Насоновой РАМН больным РЗ, которые не менее 1 месяца до проведения данной процедуры получали нимесулид. В качестве контроля были использованы результаты ЭГДС, проведенных в тот же период всем больным, не менее месяца получавшим другие неселективные НПВП.
Все пациенты были направлены на эндоскопическое исследование лечащими врачами в связи с наличием определенных показаний: для исключения патологии верхних отделов ЖКТ из-за наличия симптомов гастроэзофагеального рефлюкса, гастралгии или диспепсии, наличия в анамнезе язвы желудка или двенадцатиперстной кишки (ДПК), для поиска источника анемии, для проведения онкопоиска, при необходимости взятия биопсии слизистой оболочки ДПК на амилоид и др.
Критериями отбора больных для проведения анализа являлся возраст старше 18 лет и зафиксированный в медицинской документации факт регулярного использования НПВП в течение не менее 1 месяца до момента до проведения ЭГДС.
В анализ не включались данные эндоскопического исследования у больных системными РЗ, при которых поражение ЖКТ может быть проявлением висцеральной патологии: системной склеродермией, поли/дерматомиозитом, системной красной волчанкой, болезнью Бехчета и системными васкулитами. В контрольную группу также не были включены пациенты, использовавшие мелоксикам, целекоксиб и эторикоксиб; принимавшие участие (на момент проведения ЭГДС) в клинических исследованиях, в которых изучалась безопасность НПВП; направленные на ЭГДС для контроля результатов курсового лечения язвы желудка, и/или ДПК, или эрозивного эзофагита.
Суммарно за три года ЭГДС была выполнена 1048 больным, соответствующим критериям отбора и принимавшим нимесулид, а также 816 больным, использовавшим другие неселективные НПВП. Этими препаратами были в основном диклофенак, кетопрофен, индометацин, ацеклофенак и ибупрофен; лишь единичные больные регулярно принимали пироксикам, теноксикам, кеторолак или метамизол.
Клиническая характеристика больных в исследуемых группах представлена в таблице.
Как видно, большинство пациентов были женщины среднего возраста, страдавшие ревматоидным артритом. В целом исследуемые группы были сопоставимы — правда, в контрольной группе было достоверно больше пациентов, страдающих ССА (преимущественно анкилозирующим спондилоартритом). Этот факт объясняет более высокую долю лиц мужского пола в контрольной группе. Следует отметить, что больные, принимавшие нимесулид, чаще имели язвенный анамнез, чаще принимали глюкокортикоиды (ГК) и достоверно реже — ингибиторы протонной помпы (ИПП).
При анализе результатов ЭГДС мы учитывали выявление эрозий, под которыми подразумевался поверхностный дефект слизистой, не имеющий видимой глубины, и язв — локального повреждения стенки ≥ 5 мм, имеющего видимую глубину. При обнаружении менее 10 эрозий они описывались как «единичные», а при выявлении ≥ 10 — как «множественные».
Электронная база данных была создана с помощью программы Microsoft Office Excel 2007, статистический анализ проводился с помощью программы SPSS 10.0. Приведенные в статье цифровые значения представлены в виде M ± m. Для оценки значимости отличия количественных параметров использован t-тест Стьюдента, для качественных параметров — χ 2 или точный тест Фишера.
Результаты
Общее число больных с эрозиями или язвами в группе 1 составило 244 (23,3%), в группе 2 — 272 (33,3%), р 65 лет) на частоту язв желудка и/или ДПК.
Оказалось, что язвы значительно чаще выявлялись у лиц, имевших язвенный анамнез. Так, в группе 1 у больных с этим фактором риска суммарная частота язв желудка и/или ДПК оказалась 11,5%, без — 3,1% (р 65 лет, принимавших нимесулид, частота язв составила 9,9%, более молодого возраста — 3,5% (р 65 лет) частота язв была намного ниже, чем в целом по группе. Тем не менее, язвы существенно чаще выявлялись в группе 2. Так, в группе 1 у 752 больных без факторов риска язвы были выявлены лишь у 16 (2,1%), а в контрольной группе — у 48 из 568 (8,5%), р 65 лет). Так, применение ИПП было отмечено у 16,2% больных из группы 1, имевших вышеуказанные факторы риска, и лишь у 5,3% не имевших; аналогично, в группе 2 эти препараты получали 26,2% и 5,6%.
Отдельным объектом нашего анализа стала оценка частоты патологии пищевода. Эрозивный эзофагит был выявлен лишь у небольшого числа больных (в сравнении с патологией желудка и ДПК). Тем не менее, эрозивный эзофагит достоверно реже выявлялся у пациентов в группе 1 — у 15 (1,4%), в сравнении с 26 (3,1%) в группе 2, р = 0,03.
Такие факторы риска, как пожилой возраст и ГК, не ассоциировались с более высокой частотой патологии пищевода ни в группе 1, ни в группе 2. В то же время эрозивный эзофагит достоверно чаще выявлялся у пациентов в группе 2, получавших НДА (но не в группе 1). Прием бисфосфонатов оказался однозначно важным фактором риска — и в группе 1, и группе 2, при использовании этих препаратов эрозивный эзофагит определялся достоверно чаще (p
А. Е. Каратеев, доктор медицинских наук, профессор
ФГБУ НИИР им. В. А. Насоновой РАМН, Москва
Нимесулид в лечении хронических заболеваний суставов
Заболевания суставов различной локализации являются одной из самых частых причин обращения к врачу наряду с артериальной гипертензией. Заболевания суставов являются социально значимыми болезнями.
Заболевания суставов различной локализации являются одной из самых частых причин обращения к врачу наряду с артериальной гипертензией. Заболевания суставов являются социально значимыми болезнями.
Во-первых, эти заболевания поражают значительную часть населения. Наиболее распространенным заболеванием суставов является деформирующий остеоартроз (ОА), особенно у лиц старше 65 лет, когда его распространенность достигает 97% населения. Среди хронических воспалительных заболеваний суставов наиболее частым является ревматоидный артрит (РА) — заболевание, практически облигатно приводящее к инвалидизации больных уже через 3–5 лет от дебюта болезни.
Во-вторых, эти заболевания характеризуют развитие стойкого болевого синдрома, который может быть связан с различными причинами. Наиболее частая причина боли при патологии суставов — развитие синовиита. Однако при ОА развитие боли может быть связано и с другими патогенетическими звеньями болезни. В норме болевые окончания имеют все структуры сустава, за исключением хряща. Но при ОА происходит частичная васкуляризация и иннервация хряща. Истончение и повреждение хряща снижает его амортизационные свойства, увеличивается нагрузка на субхондральную кость с развитием ее отека и боли. Кроме того, фибрилляция хряща также индуцирует боль и воспаления.
Данные, полученные при изучении влияния боли на прогноз при ОА, свидетельствуют:
Нестероидные противовоспалительные препараты (НПВП) обладают анальгетическим, противовоспалительным и жаропонижающим эффектами. Поэтому они являются незаменимыми в лечении артрологических заболеваний. Быстрое развитие обезболивающего эффекта и определяет облигатность их применения в лечении суставной патологии. Позитивный лечебный эффект НПВП связан с ингибицией ЦОГ-2. Этот фермент, участвующий в каскаде распада поврежденных при воспалении и других поражениях клеточных мембран, отвечает за выделение провоспалительных простагландинов и других медиаторов воспаления не только в суставах, но и в других органах и тканях, в первую очередь в стенках сосудов. Исходя из вышесказанного, становится ясно, что использование селективных ингибиторов ЦОГ-2 имеет важное клиническое и социальное значение.
В клинической практике селективные ингибиторы ЦОГ-2 заняли прочное место, хотя до сих пор не весь потенциал их возможностей используется практическими врачами. Нередко возникают «мифы» об их потенциальной токсичности, в первую очередь в отношении сердечно-сосудистой системы. В западной литературе была опубликована информация о гепатотоксичности нимесулидов, основанная на единичных и плохо документированных клинических случаях. Эти аспекты хотелось особо обсудить в данном сообщении, взяв в качестве примера препарат «Найз».
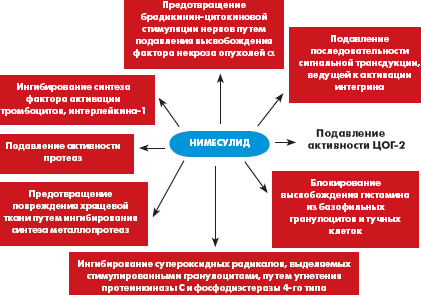
Препарат «Найз» относится к селективным ингибиторам ЦОГ-2, что доказано в исследованиях in vivo [7] и in vitro на молекулярных моделях [6]. Кроме того, препарат обладает еще несколькими важными механизмами действия (рис.). Наибольший опыт применения препарата «Найз» в ревматологической практике в Российской Федерации накоплен в лечении больных с ОА. Больные ОА, как правило, имеют высокий риск развития желудочно-кишечных осложнений в связи с возрастом, частым наличием сопутствующей сосудистой, кардиальной, ренальной патологии и необходимостью использовать сопутствующую терапию. Найз обычно используется этой категорией больных в суточной дозе 200 мг/сутки. Это обеспечивает достижение клинического эффекта у 87% [8] — 93% [9] больных при хорошей переносимости Найза в отношении желудочно-кишечного тракта, как по отечественным данным (табл. 1), так и по данным зарубежных контролируемых исследований, постмаркетингового изучения переносимости нимесулида в 17 странах у 118 831 385 больных [10–13].
В нашем исследовании участвовало 40 больных с ОА (32 больных) и с РА (8 больных), в возрасте от 49 до 79 лет (58,8 ± 18,3 года), страдающих артериальной гипертензией более чем 5 лет, получающих стабильную дозу антигипертензивных препаратов в течение не менее 6 месяцев, без явных проявлений сердечной недостаточности. Большинство больных получали ингибиторы АПФ (эналаприл 10–30 мг/сутки) — 28 больных, β-адреноблокаторы (пропранолол 20–40 мг/сутки) — 12 больных. Всем больным после 3-дневного периода перерыва в приеме НПВП (ибупрофен, мелоксикам, кетопрофен, диклофенак) назначался рандомизировано либо диклофенак в дозе 100–150 мг/сутки, либо Найз в дозе 200–400 мг/сутки на 20 дней. АД регистрировалось 6 раз в сутки: после пробуждения, перед первым приемом антигипертензивных или нитратных препаратов, через 2 часа после их приема и далее еще 3 раза с равными промежутками в течение всего периода «отмывки», первую и последнюю неделю приема НПВП, в остальное время исследования АД регистрировалось 4 раза в сутки каждые 3 часа с момента пробуждения. Пациенты в течение периода исследования вели дневник с указанием АД, приема антигипертензивных препаратов и нежелательных реакций. Статистическая обработка проводилась методом сопряженных пар.
Практически у всех больных обеих групп к концу периода «отмывки» отмечалось увеличение среднесуточного АД (табл. 2). Тем не менее, в течение 1-й недели лечения (табл. 2), различия в среднем систолическом давлении были достоверно больше при приеме диклофенака, а на фоне Найза практически не отличались от исходного (p 0,05). Известно, что изменение систолического АД (САД) является более важным фактором риска кардиоваскулярной патологии, чем изменение ДАД [19]. Уменьшение уровня САД на 12 мм рт. ст. снижает риск развития инфаркта миокарда на 27%, усугубления застойной сердечной недостаточности на 55% и инсульта на 56% [19, 20].
Аналогичные результаты продемонстрированы в исследовании В. И. Мазурова и соавт. [21], сравнивших гемодинамические показатели у больных ОА (n = 40), имеющих (23 пациента) или не имеющих (17 пациентов) сопутствующую артериальную гипертензию (АГ), при назначении Найза или диклофенака на 1 месяц. Пациенты всех подгрупп были сопоставимы по локализации ОА, рентгенологической стадии. Пациенты, имевшие ОА в сочетании с АГ, были примерно на 10 лет старше больных с нормальным уровнем АД. Доза Найза составляла 200 мг/сутки и диклофенака — 100 мг/сутки. Для лечения АГ всем больным второй подгруппы был назначен Ренитек (эналаприл) по 5–10 мг 2 раза в сутки. Всем больным до назначения НПВП и через 1 месяц помимо клинического осмотра и оценки боли (по шкале ВАШ) проводились ЭКГ, суточное мониторирование АД, импедансометрическая кардиография (ИМК), определение уровня десквамированных эндотелиоцитов в периферической крови по методике Hladovec J. и соавт. (1978), определение состояния эндотелий-зависимой и эндотелий-независимой (проба с нитроглицерином) вазодилятации (ЭЗВД, ЭНВД соответственно) плечевой артерии с помощью ультразвука высокого разрешения.
Через один месяц лечения статистически значимых различий в уменьшении боли по ВАШ на фоне приема Найза или диклофенака не отмечено (p > 0,05). Данные средних параметров суточного мониторирования АД представлены в табл. 3 и 4. При назначении Найза больным ОА без АГ (группа 1А) среднее суточное САД и среднее дневное САД и ДАД повышались в пределах нормальных значений без субъективных ощущений. В группе 1Б, получавшей диклофенак, отмечено более значимое увеличение систолического и ДАД, как среднесуточного, так и среднедневного (p
Н. В. Чичасова, доктор медицинских наук, профессор
Г. Р. Имаметдинова
Е. Л. Насонов, доктор медицинских наук, профессор, академик РАМН
ММА им. И. М. Сеченова, Москва
Современные возможности терапии хронического панкреатита
Хронический панкреатит — длительно протекающее воспалительное заболевание поджелудочной железы, проявляющееся необратимыми морфологическими изменениями, которые вызывают боль и/или стойкое снижение функции поджелудочной железы. При хроническом панкреатит
Хронический панкреатит — длительно протекающее воспалительное заболевание поджелудочной железы, проявляющееся необратимыми морфологическими изменениями, которые вызывают боль и/или стойкое снижение функции поджелудочной железы. При хроническом панкреатите морфологические изменения поджелудочной железы сохраняются после прекращения воздействия этиологического агента. В настоящее время распространенность хронического панкреатита, по данным аутопсий, составляет от 0,01 до 5,4%, в среднем — 0,3-0,4%, при этом за последние 40 лет заболеваемость выросла примерно в два раза, что связывают с тем, что население стало употреблять больше алкогольных напитков, а также с воздействием вредных факторов окружающей среды (см. диаграмму 1).
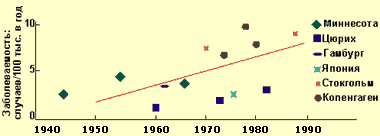 |
| Диаграмма 1. Заболеваемость ХП в 1945—1985 гг. (Worning H., 1990) |
В патогенезе хронического панкреатита важную роль играют несколько факторов. Одним из основных является обструкция главного панкреатического протока при конкрементах, воспалительном стенозе или опухолях. При алкогольном панкреатите повреждение поджелудочной железы связано с повышением содержания белка
в панкреатическом секрете, что приводит к возникновению белковых пробок и обструкции мелких протоков железы. Другим фактором, влияющим на патогенез алкогольного панкреатита, является изменение тонуса сфинктера Одди: его спазм вызывает внутрипротоковую гипертензию, а релаксация способствует рефлюксу дуоденального содержимого и внутрипротоковой активации панкреатических ферментов.
Разрушение экзокринной части поджелудочной железы вызывает прогрессирующее снижение секреции бикарбонатов и ферментов, однако клинические проявления нарушения переваривания пищи развиваются лишь при деструкции более 90% паренхимы органа. В первую очередь возникают проявления недостаточности липазы в виде нарушения всасывания жиров, жирорастворимых витаминов: A, D, E и K, что нечасто проявляется поражением костей, расстройствами свертывания крови. У 10–30% больных хроническим панкреатитом развивается сахарный диабет, обычно на поздних стадиях заболевания, нарушение толерантности в глюкозе наблюдается гораздо чаще. Для таких больных характерно развитие гипогликемических реакций на инсулин, недостаточное питание или злоупотребление алкоголем. Кетоацидоз развивается редко, что связано с одновременным снижением продукции инсулина и глюкагона.
Приступ хронического панкреатита проявляется иррадиирующими в спину болями в верхней половине живота, развивающимися после приема пищи, которые могут продолжаться в течение многих часов или нескольких дней. Нередко наблюдается тошнота, рвота, у 30–52% пациентов — снижение веса, у 16–33% — желтуха. Преходящая желтуха возникает вследствие отека железы при обострениях хронического панкреатита, постоянная — связана с обструкцией общего желчного протока вследствие фиброза головки поджелудочной железы. При разрывах протоков поджелудочной железы, на месте предыдущего некроза ткани происходит скопление секрета, что приводит к формированию псевдокист. Кисты могут быть бессимптомными или вызывать боли в верхней половине живота. При длительном течении заболевания, при уменьшении объема функционирующей паренхимы до 10% от нормы появляются признаки мальабсорбции (полифекалия, жирный стул, похудание).
В течении хронического панкреатита можно выделить несколько стадий (Lankisch P.G., Moessner Y.), умение различать которые важно для правильного подбора терапии. Так, на первой стадии заболевания клиническая симптоматика отсутствует: в этот период характерные для ХП изменения данных КТ или ЭРХПГ выявляются лишь при случайном обследовании.
На второй стадии возникают начальные проявления, характеризующиеся частыми эпизодами обострения ХП (которые могут быть ошибочно расценены как острый панкреатит). Заболевание видоизменяется от повторных приступов боли в животе до постоянных умеренных болей и похудания. С течением времени рецидивы становятся менее тяжелыми, но симптоматика сохраняется в периоды между приступами. На этой стадии может существенно ухудшаться качество жизни. Вторая стадия обычно продолжается на протяжении четырех—семи лет. Иногда заболевание быстро прогрессирует, развивается атрофия ПЖ, и нарушается функция органа.
У больных на третьей стадии постоянно присутствует симптоматика ХП, прежде всего — абдоминальная боль. Пациенты могут стать зависимыми от анальгетиков, значительно сокращают объем принимаемой пищи из-за опасения усиления боли. Появляются признаки экзокринной и эндокринной панкреатической недостаточности.
Особенность панкреатита на четвертой стадии — это атрофия ПЖ, развитие экзокринной и эндокринной недостаточности, что проявляется стеатореей, похуданием и сахарным диабетом. Снижается интенсивность боли, прекращаются острые приступы заболевания, могут развиваться тяжелые системные осложнения ХП и аденокарцинома поджелудочной железы.
Терапия панкреатита проводится по нескольким направлениям: отказ от употребления алкоголя; соблюдение диеты с низким содержанием жира (до 50–75 г/сут) и частым приемом небольших количеств пищи; купирование боли; ферментная заместительная терапия, борьба с витаминной недостаточностью; лечение эндокринных нарушений.
Лечение приступа хронического панкреатита, а также острого панкреатита проводиться по аналогичной схеме. Обязательные компоненты терапии: внутривенное введение растворов электролитов и коллоидов, голодная диета (полное голодание до двух дней) и анальгезия (например, меперидин). Рекомендуется введение свежезамороженной плазмы или альбумина. Диуретики не показаны большинству больных: олигурия разрешается при исчезновении гиповолемии и нормализации перфузии почек. Для облегчения рвоты, купирования пареза желудочно-кишечного тракта и уменьшения стимуляции поджелудочной железы может быть использована аспирация содержимого желудка через назогастральный зонд. Коагулопатия, возникающая при панкреатите, обычно требует назначения гепарина, свежей плазмы. В последние годы при остром панкреатите показана эффективность антагониста тромбоцит-активирующего фактора лексипафанта (60–100 мг/сут), однако его действие при хроническом панкреатите еще нуждается в уточнении.
Применение ингибиторов протеолитических ферментов (например, апротинина, габексата) является спорным. Исследования показывают, что при остром панкреатите не наблюдается дефицита ингибиторов протеаз, кроме того, проведенные клинические исследования не выявили преимуществ этих препаратов по сравнению с плацебо. Однако существуют данные, что габексат, низкомолекулярный ингибитор трипсина, эффективно используется для профилактики развития острого панкреатита, связанного с ЭРХПГ.
Ингибиторы секреции поджелудочной железы: глюкагон, соматостатин, кальцитонин, ингибиторы карбоангидразы, вазопрессин, изопреналин, также было предложено применять для лечения острого панкреатита, однако их эффективность к настоящему времени не получила достаточного подтверждения. Препараты пищеварительных ферментов можно использовать для лечения как в разгар заболевания с целью подавления панкреатической секреции, так и в период выздоровления, когда пациент снова получает возможность принимать пищу орально.
При билиарном обструктивном панкреатите должна быть проведена своевременная эндоскопическая декомпрессия желчных путей. Выполняется папиллосфинктеротомия, дилатация или стентирование панкреатического протока. Хирургическое лечение обструктивного панкреатита, безусловно, является основным методом, в то же время целесообразность проведения вмешательства в первые сутки после развития тяжелого приступа должна быть признана спорной. После стихания остроты воспаления целесообразно проведение холецистэктомии.
Схему длительной терапии при хроническом панкреатите можно разделить на две основные части, в соответствии с ведущими клиническими синдромами (см. диаграмму 2).
Боль могут облегчить большие дозы панкреатических ферментов. Попадание ферментов поджелудочной железы (прежде всего — трипсина) в двенадцатиперстную кишку по механизму отрицательной обратной связи вызывает снижение панкреатической секреции, снижение внутрипротокового давления и уменьшает боль. Традиционно для этой цели использовались порошок или таблетированные препараты панкреатина.
Если болевой синдром резистентен к терапии, при расширении главного протока более 8 мм, у 70–80% пациентов облегчение может принести латеральная панкреатоеюностомия. В случаях, когда панкреатический проток не расширен, показано проведение дистальной панкреатэктомии (при преимущественном поражении хвоста железы) или операция Уиппла (Whipple) (при поражении в основном головки железы). Альтернативой операции является чрезкожная денервация солнечного сплетения введением алкоголя, однако эффект этой процедуры сохраняется лишь в течение нескольких месяцев. Весьма перспективно эндоскопическое лечение под контролем эндоскопического УЗИ (дренирование псевдокист, невролиз солнечного сплетения).
Показаниями для заместительной терапии экзокринной панкреатической недостаточности являются исключительно клинические показатели: похудание, стеаторея, метеоризм. Классическая рекомендация, предусматривающая определение содержания жира в кале перед назначением лечения, в настоящее время потеряла свое значение из-за трудоемкости и низкой чувствительности данного метода. Для купирования внешнесекреторной панкреатической недостаточности используют различные препараты экстрактов поджелудочной железы (см. таблицу 1).
При выборе препарата для заместительной терапии следует учитывать следующие показатели:
Способность препарата активироваться только в щелочной среде — очень важное свойство, которое резко повышает эффективность ферментов; так, при использовании препарата, имеющего энтеросолюбильную оболочку, всасывание жиров повышается в среднем на 20% по сравнению с такой же дозой обычного средства. Однако при хроническом панкреатите происходит значительное снижение продукции бикарбонатов, что приводит к нарушению щелочной среды в двенадцатиперстной кишке. Это создает несколько проблем. Первая касается нарушения активации частиц ферментного препарата, покрытых энтеросолюбильной оболочкой. Вторая проблема заключается в том, что в кислой среде происходит преципитация желчных солей и нарушение эмульгации жира, что делает его малодоступным для расщепления липазой. Поэтому эффективность ферментной терапии (см. рисунок 1) может быть повышена благодаря одновременному назначению антацидов за 30 мин до и через 1 ч после еды или антисекреторных препаратов (Н2-блокаторы, омепразол), но необходимо помнить, что антациды, содержащие кальций или магний, ослабляют действие ферментных препаратов. Возможно использование препаратов, содержащих протеолитические ферменты растительного происхождения, которые сохраняют активность в гораздо более кислой среде, чем животные.
Значительное снижение качества жизни больного панкреатитом связано с такой проблемой, о которой обычно забывают, как стойкое вздутие живота. Нередко вздутие не купируется даже при приведении заместительной терапии высокими дозами ферментов. В этом случае к проводимой терапии необходимо добавить адсорбенты (симетикон, диметикон) или использовать комбинированные ферментные препараты, содержащие адсорбирующие вещества.
Разовая доза ферментов, которая рекомендуется для лечения внешнесекреторной панкреатической недостаточности, должна содержать не менее 20–40 тыс. ед. липазы. Обычно пациенту назначают две—четыре капсулы препарата (по 20—25 тыс. ед. липазы) при основных приемах пищи и по одной-две капсуле (по 8—10 тыс. ед. липазы) или таблетки панкреатина при употреблении небольшого количества пищи. При клинически выраженной панкреатической недостаточности обычно не удается полностью устранить стеаторею даже с помощью высоких доз препаратов, поэтому критериями адекватности подобранной дозы пищеварительных ферментов являются: прибавка веса, нормализация стула (менее трех раз в день), снижение вздутия живота.
Причины неэффективности заместительной терапии могут быть связаны как с неточной диагностикой заболевания, так и с неадекватным назначением терапии больному (см. рисунок 2).
Побочные эффекты ферментной терапии (см. рисунок 3) обычно не носят тяжелого характера, наиболее известный опасный побочный эффект — развитие фиброзирующей колопатии — возникает при длительном приеме очень высоких доз ферментов в виде микротаблеток: более 50 тыс. ед. липолитической активности на 1 кг веса тела в сутки.
Таким образом, терапия хронического панкреатита должна проводиться дифференцированно, в зависимости от ведущего клинического синдрома и стадии заболевания. Заболевание, которое удается обнаружить на первой стадии, как правило, не требует медикаментозной коррекции, в этом случае обычно достаточно изменения образа жизни и диетотерапии. Лечение ХП на второй стадии включает назначение таблетированного панкреатина, антисекреторных препаратов и спазмолитиков. Третья стадия обычно требует использования всего арсенала средств, которые имеются у врача для купирования панкреатической боли: микрогранулы панкреатина, антисекреторные препараты, октреотид, спазмолитики, мощные анальгетики, психотропные препараты. На последней, четвертой, стадии лечение основывается, прежде всего, на использовании микрогранул панкреатина в высокой дозе с целью проведения заместительной терапии.
По вопросам литературы обращайтесь в редакцию
А. В. Охлобыстин, кандидат медицинских наук
Э. Р. Буклис, кандидат медицинских наук
ММА им. И. М. Сеченова, Москва
_575.gif)