нейронтин и нейромидин можно ли вместе
Нейромидин при грыже позвоночника: описание препарата, механизм воздействия
Нейромидин – это особый препарат, который не относится ни к миорелаксантам, ни к обезболивающим, ни к противовоспалительным средствам. Его нет ни в одном международном и отечественном протоколе лечения острой боли в спине, и тем более – когда боль вызвана дискогенными осложнениями остеохондроза (протрузиями и грыжами). Стоимость Нейромидина достаточно высока, и превышает 1000 рублей. Разберемся: применение Нейромидина при грыже позвоночника действительно помогает, или же это просто трата денег впустую?
Вопрос этот далеко не праздный. Межпозвонковые протрузии и грыжи имеют все признаки «удобных» заболеваний для знахарей и шарлатанов. Вот эти признаки:
Таким образом, вариантов консервативно «полечить» грыжу есть множество: мази, кремы, кинезиотерапия и краниосакральное воздействие, массаж и физиотерапия, мануальные техники и блокады. Следует помнить одно: все эти методы лечения не имеют отношения к грыже, как к дефекту межпозвонкового диска. Они помогают устранить неприятные симптомы, которые вызвала грыжа, «натирая» нервные корешки, связки и мышцы.
Все без исключения консервативные способы лечения помогают только лишь снять боль и увеличить объем движений в спине, но при этом — это не свидетельство радикального излечения. Это результат уменьшения воспаления, боли и отека, улучшения кровоснабжения окружающих тканей и снижения мышечного тонуса. Грыжа вновь проявит себя, возможно, она увеличится, и эти методы консервативного лечения перестанут помогать. Тогда спасет только операция.
Современная спинальная нейрохирургия
Лишь современное малоинвазивное оперативное вмешательство (например, видеоэндоскопическая микродискэктомия, или лазерная вапоризация и нуклеопластика) может удалить сам грыжевой дефект, или воспрепятствовать его появлению в случае наличия протрузии. Однако, российский пациент прекрасно знает, что такое операция. Это больно. Это надолго выводит из нормальной жизни. Это может быть опасно. Таких «но» набирается так много, что операцию считают последним видом лечения, когда перестают помогать массажисты, сеансы карбокситерапии, «мануальщики» и кинезитерапевты.
К счастью, в странах Европы, Израиле, США – подход совсем другой. Если есть показания, то пациент оперируется без боли, и зачастую в тот же день, или на следующий, покидает стационар на собственных ногах. Качество жизни у него сохраняется. Ему не запрещается сидеть в течение многих дней, и он не вынужден справлять большую нужду стоя. Поэтому там современную операцию считают лучшим, быстрейшим и эффективным средством радикального лечения. Кстати, врачи многих страны Восточной Европы, например, Чехии, показывают отличные результаты лечения грыж оперативным путем при довольно скромных затратах.
В России же предпочитают не удалять сразу грыжевое выпячивание, а многие годы бороться с его последствиями и осложнениями – периодически лечить воспаление, боли и отек корешков, которые упорно возникают снова и снова. И в этом отношении отечественный пациент напоминает несчастного водителя, который вместо того, чтобы, наконец, поменять проколотое колесо, вынужден накачивать его через каждые полчаса езды. Только в отличие от водителя, пациент, длительно «лечащий» грыжу, подчас тратит в несколько раз больше денег, чем стоила бы операция.
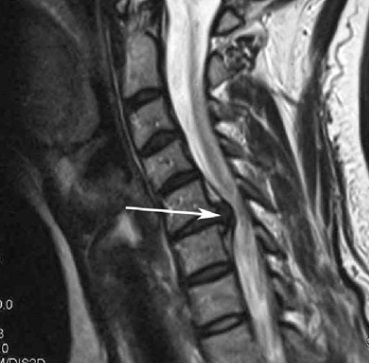
Грыжа шейного отдела на МРТ.
Но даже в ряду лекарств для снятия отека, боли в спине, избыточного мышечного напряжения Нейромидин не «числится». Однако, его иногда назначают при грыжах, и совершенно неоправданно. Ситуация усугубляется невообразимо большим количеством сайтов, которые написаны с потрясающей медицинской безграмотностью. Ибо если есть запрос «Нейромидин при грыжах как принимать», то тут же появится услужливая, но безграмотная статья, которая даже может нанести вред здоровью. Как принимать Нейромидин при грыжах? Никак не принимать. Но обо всем по порядку….
Механизм действия препарата
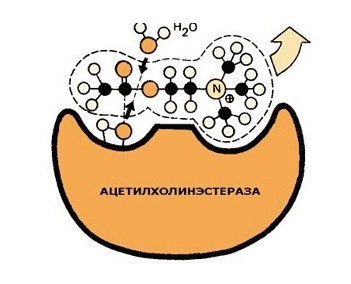
Известно, что от нервов приказ мышцам на сокращение отдает ацетилхолин, который выбрасывается в синаптическую щель – место связи нерва с мышцей. Ацетилхолин, если его не убрать вовремя, будет держать мышцу в длительном сокращении. Поэтому «очистка» синаптической щели от ацетилхолина очень важна, и им занимается фермент ацетилхолинэстераза. Так вот, Нейромидин ее угнетает, и ацетилхолин дольше циркулирует в синаптической щели, и импульс становится ярче, продолжительнее, активнее. Он влияет на уровне каналов калия. В итоге улучшается нейромышечная передача, сократимость гладкой мускулатуры.
Показания к применению: можно ли применять при грыжах?
Поэтому применять Нейромидин следует там, где есть дефект нейромышечной передачи (например, слабость и вялость мышц, когда есть наследственный дефицит ацетилхолина). Это миастения и различные мистеноподобные синдромы.
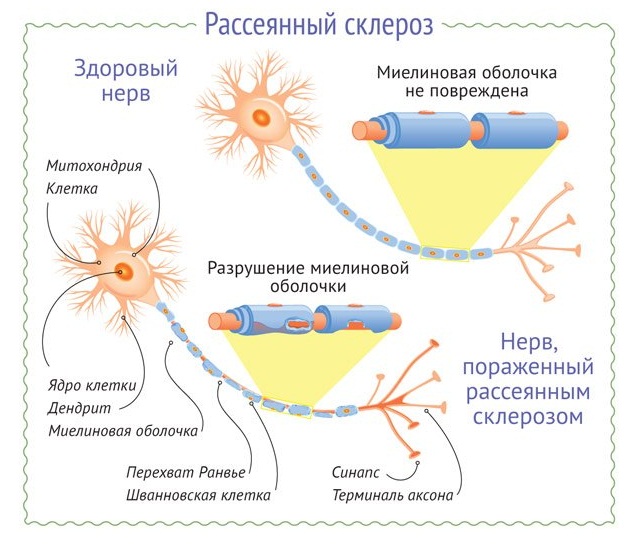
Второе показание – это собственно плохие нервы, по которым импульс проводится плохо, с потерями. Это полинейропатия, например, при сахарном диабете, или алкогольная полинейропатия. В последнем случае многолетнее употребление алкоголя привело к разрушению нервов, а в первом случае – высокий уровень сахара. Сюда же примыкают и демиелинизирующие заболевания, например, рассеянный склероз, когда миелиновая оболочка нервов дефектная, и часто возникает «короткое замыкание» и нарушение передачи импульса вследствие плохой изоляции.
Обширная группа показаний – это различные параличи и парезы, когда нейроны очень плохо генерируют импульс, и тогда нужно на периферии, в месте подхода аксона нерва к мышце хоть как-то его усилить. Это бульбарные параличи, парезы с двигательным дефицитом.
Наконец, вследствие влияния на гладкую мускулатуру Нейромидин показан при низком тонусе кишечника и для лечения атонических запоров.
Нужна ли улучшенная нейромышечная передача при грыжах?
Конечно, нет. Вспомним, что:
И, наконец, «вишенка на торте»: ацетилхолин – это медиатор парасимпатической нервной системы, и он не имеет ну никакого отношения к мышцам туловища или поясничного отдела. Нейромидин стимулирует такие эффекты, как:
Кроме этого, ацетилхолин является нервным медиатором внутри центральной нервной системы, и циркулирует внутри головного мозга. Его дефицит может вызвать болезнь Альцгеймера, и поэтому Нейромидин может ещё применяться, как препарат, помогающий замедлить прогрессирование симптомов этого заболевания.
Как видно, никакого отношения к грыже межпозвонковых дисков это средство не имеет, и иметь не может. Его механизм действия лежит вне влияния на воспаление, боль, отек и мышечный спазм, который и имеет место при протрузиях и грыжах.
Побочные эффекты и противопоказания
Нейромидин — это серьезный препарат. Если его применять в высоких дозах, то может быть боль за грудиной, рвота, головокружение, головная боль. У женщин может повышаться тонус матки. Поскольку стимулируются мускариновые холинорецепторы, то в качестве симптомов передозировки у пациентов может быть диарея, потливость, сердцебиение, появится избыточное отхождение мокроты, вплоть до признаков бронхоспазма, могут возникать даже и судороги.
Перечень противопоказаний для приёма Нейромидина также достаточно внушительный. Это беременность, период грудного вскармливания, а также детский и подростковый возраст, включая 18 лет. Препарат категорически запрещен у пациентов с:
Существует и перечень заболеваний, когда Нейромидин применять по показаниям можно, но с большой осторожностью. Это различные обструктивные заболевания легких, бронхит и, тиреотоксикоз, болезни сердечно-сосудистой системы, при наличии панических атак, и кардионевроза, поскольку препарат может снижать порог судорожной готовности.
Категорически запрещается употреблять в процессе лечения алкоголь, поскольку количество побочных эффектов препарата совместно с этиловым спиртом усиливается. На фоне лечения Нейромидином пациент не должен водить автотранспорт, а также работать на производстве при наличии факторов риска, поскольку препарат не может гарантировать быстроту психомоторных реакций и хорошей концентрации внимания
Взаимодействия с другими лекарствами
Также Нейромидин может взаимодействовать с другими лекарственными средствами. Он усиливает свой седативный эффект, если вы применять с препаратами, угнетающими центральную нервную систему, например со снотворными препаратами, транквилизаторами из группы бензодиазепинов или совместно с барбитуратами. Напомним, что известный представитель барбитуратов — фенобарбитал входит в состав Валокордина и Корвалола, которые продаются без рецепта. Если сочетать прием Нейромидина с бета-адреноблокаторами, которые уменьшают частоту сердечных сокращений и работу сердца, то возникает риск брадикардии, коллаптоидного и обморочного состояния.
Формы выпуска и аналоги
Нейромидин содержит действующее вещество — ипидакрин, выпускается он в виде таблеток, а также раствора для инъекций. Таблетки продаются в упаковке по 20 мг № 50, а раствор для инъекций – в виде двух дозировок. Первая — 5 мг на миллилитр, а вторая втрое более концентрированная: 15 мг на миллилитр ипидакрина. В одной упаковке находятся 10 ампул.
Применять Нейромидин при полинейропатии желательно, в среднем, по одной таблетке от одного до 3 раз в день, курс лечения — от одного до 2 месяцев. В случае тяжелых миастенических кризов вводят внутривенно Нейромидин по одному или два мл, то есть до 30 мг раствора 1,5%, а затем переходят на таблетированную форму.
При тяжелых параличах пациенту назначают по 1 таблетке 3 раза в сутки длительным курсом, до 6 месяцев. При наличии атонии кишечника дозировка такая же, одна таблетка 2-3 раза в сутки, но курс короткий — не более 2 недель. Максимальная суточная доза не должна составлять более 10 таблеток, Или 200 мг.
Сам Нейромидин стоит недешево: одна упаковка таблеток, которую хватит на две недели применения (1 таблетка 3 раза в день) стоит, в среднем 1350 руб. Производит Нейромидин латвийская компания Олайнфарм.
Аналогом является словацкий (НВМ-фарма) препарат Ипигрикс (1100 рубля за такую же упаковку), а также отечественный Аксамон. Выпускает его Пик – фарма, по средней цене 1263 руб. за упаковку в 50 табл.
Заключение
Таким образом, нет никаких показаний к применению Нейромидина при остеохондрозе и его осложнених дискогенного характера, которыми являются протрузии и грыжи. Механизм действия Нейромидина совсем иной. Он не влияет на тонус поперечно-полосатой мускулатуры, на асептическое воспаление, которое вызывано постоянным трением грыжей мягких тканей.
Он не влияет на боль, на отёк, на выброс биогенных аминов в зоне компрессии грыжей нервных структур. В этом случае необходимо воспользоваться теми препаратами, которые непосредственно разрывают патологический каскад реакций. Отек снимают нестероидные противовоспалительные средства, например, Мовалис или Кетонал, а с мышечным спазмом Успешно борется Мидокалм или Сирдалуд. Назначать при грыжах Нейромидин — это примерно то же самое, как лечить голод сном.
А затем возникает ситуация, при которой болевой синдром при протрузии или грыжи постепенно уменьшается сам с собой. Пациент принимает это за чудодейственный эффект Нейромидина. Кроме этого, человек так устроен, что потратив больше 1000 руб. за лекарство, он внушает себе, что такой дорогой препарат не может «не работать».
Лечение болевой формы диабетической полинейропатии
Диабетическая дистальная симметричная сенсорно-моторная полинейропатия (ДПН) — самый частый вариант диабетической нейропатии, который выявляется более чем у 50% больных с сахарным диабетом (СД) 1-го и 2-го типа.
Диабетическая дистальная симметричная сенсорно-моторная полинейропатия (ДПН) — самый частый вариант диабетической нейропатии, который выявляется более чем у 50% больных с сахарным диабетом (СД) 1-го и 2-го типа [1]. ДПН является второй по частоте встречаемости причиной нейропатической боли (НБ). Распространенность ДПН варьирует в зависимости от используемых диагностических критериев. Частота нейропатии, диагностируемой на основании симптомов, составляет около 25%, а при проведении электронейромиографического исследования — 100% у больных СД [2].
Диагноз ДПН основывается на тщательно собранном анамнезе, неврологическом обследовании, электрофизиологическом исследовании. Типичными симптомами являются ощущение «бегания мурашек», жжения, боли в голенях и стопах, ночные судороги мышц. При неврологическом обследовании выявляются ослабление ахилловых рефлексов, нарушение чувствительности по типу «носков» и «перчаток», снижение проприоцептивной чувствительности. При несвоевременно начатом лечении и неэффективности терапии развиваются такие осложнения ДПН, как язвы стоп, которые могут приводить к некрозу, гангрене (диабетическая стопа) и часто к ампутациям. Пациенты с СД нуждаются в ежегодном неврологическом и клиническом обследовании стопы [3].
Общепризнано, что основной причиной развития ДПН является повышенный уровень глюкозы [4]. Соответственно, единственным подтвержденным методом лечения, способным замедлять и даже в некоторой степени обращать прогрессирование ДПН, является хороший контроль уровня гликемии у больных с инсулинзависимым СД. У пациентов с интенсивной терапией СД (3 или более инъекции инсулина в день либо выполнение непрерывной подкожной инфузии инсулина с помощью дозатора инсулина (уровень HbA1c в диапазоне 6,5–7,5)) наблюдалось достоверное снижение риска развития микрососудистых осложнений и нейропатии [5]. Интенсивное лечение сульфонилмочевинами пациентов с инсулинонезависимым типом СД также приводило к снижению частоты и прогрессирования нейропатии [6]. Однако только достижение нормогликемии не способно быстро ликвидировать клинические проявления ДПН. В связи с этим требуется дополнительное патогенетическое и симптоматическое лечение, особенно для купирования болевого синдрома.
К препаратам патогенетического действия относится альфа-липоевая (тиоктовая) кислота (Эспа-липон, Тиоктацид, Тиогамма, Тиолепта). Эти препараты являются золотым стандартом патогенетического лечения ДПН. Альфа-липоевая кислота является мощным липофильным антиоксидантом. Тиоктовая кислота, накапливаясь в нервных волокнах, снижает содержание свободных радикалов; увеличивает эндоневральный кровоток; нормализует содержание NO, регулятора расслабления сосудистой стенки (если его много, как при СД, то он начинает действовать как свободный радикал); улучшает эндотелиальную функцию; снижает уровень общего холестерина, увеличивает уровень антиатерогенной фракции липопротеинов высокой плотности. В ряде исследований показано, что применение альфа-липоевой кислоты в дозе 600 мг/день в/в или перорально в течение от трех недель до шести месяцев уменьшает в клинически значимой степени главные симптомы ДПН, включая боль, парестезии и онемение [7, 8]. Оптимальным считается назначение в начале лечения внутривенного капельного введения альфа-липоевой кислоты (600 мг на 200 мл физиологического раствора) в течение 3 недель (15 капельниц) с последующим приемом 600 мг препарата в виде таблеток (один раз в день за 30–40 минут до еды) в течение 1–2 месяцев.
К препаратам, которые улучшают метаболизм пораженных нервных структур, традиционно относятся витамины группы B, что обусловлено их нейротропными свойствами. Витамин B1 участвует в синтезе ацетилхолина, а В6 — в синтезе нейромедиаторов, передаче возбуждения. Витамин В12 улучшает трофику периферических нервов. Показана высокая эффективность препарата Мильгамма драже в комплексном лечении ДПН. В его состав входят 100 мг бенфотиамина и 100 мг пиридоксина. Препарат назначается по одному драже 2–3 раза в сутки в течение 3–5 недель. Важно, что Мильгамма содержит бенфотиамин, липидорастворимость которого является причиной достижения высокой концентрации тиамина в крови и тканях.
Данные об эффективности и профиле безопасности позволяют рассматривать альфа-липоевую кислоту и бенфотиамин как препараты первой линии патогенетически ориентированной терапии диабетической полинейропатии [9].
В двух мультицентровых плацебо-контролируемых исследованиях 1335 пациентов с ДПН показано, что прием ацетил-L-карнитина в дозе 1000 мг 3 раза в день в течение 6 и 12 месяцев значительно уменьшал симптоматику ДПН [10].
Направление патогенетической терапии является чрезвычайно важным и во многом предопределяет прогноз. Однако лечение проводится длительными курсами и не всегда сопровождается быстрым очевидным клиническим улучшением. В то же время даже при негрубой ДПН может иметь место выраженный болевой синдром, приводя к нарушениям сна, депрессии, тревоге и социальной дезадаптации. Именно поэтому параллельно с патогенетической терапией чрезвычайно важно проводить своевременную симптоматическую терапию НБ.
Хочется сразу подчеркнуть, что простые анальгетики и нестероидные противовоспалительные препараты в лечении болей при ДПН не рекомендуются из-за их неэффективности [11]. К сожалению, в мире более 60% больных с НБ по-прежнему получают эти препараты, что недопустимо и чрезвычайно опасно при длительном применении (осложнения со стороны желудочно-кишечного тракта (ЖКТ), печени и крови). Основными группами препаратов для лечения НБ при ДПН являются: антидепрессанты, антиконвульсанты, опиоиды, антиаритмические средства, средства местного действия.
Трициклические антидепрессанты (ТЦА) стали одними из первых препаратов, которые продемонстрировали свою эффективность в лечении пациентов с НБ [12]. Тем не менее в России зарегистрирован только один ТЦА — амитриптилин, который используется для лечения НБ (постгерпетическая невралгия, ДПН). Считается, что обезболивающее действие ТЦА связано с ингибированием ими обратного захвата серотонина и норадреналина, следствием чего является усиление нисходящей активности норадренергических и серотонинергических систем, оказывающих тормозящее влияние на проведение болевых импульсов по ноцицептивным путям в ЦНС.
Помимо блокирования обратного захвата серотонина и норадреналина ТЦА блокируют альфа1-адренергические, Н1-гистаминовые, М-холинергические рецепторы, что обусловливает целый ряд противопоказаний и побочных эффектов, ограничивающих их применение. Среди побочных эффектов наблюдаются нарушение зрения, сухость во рту, синусовая тахикардия, запор, задержка мочи, спутанность сознания и/или нарушение памяти (антихолинергические эффекты); седативный эффект, сонливость, увеличение веса (Н1-гистаминовые эффекты); ортостатическая гипотензия, головокружение, тахикардия (альфа1-адренергические эффекты) [13]. ТЦА противопоказаны больным с острым и подострым инфарктом миокарда, с нарушением внутрижелудочковой проводимости, с закрытоугольной глаукомой, принимающими ингибиторы моноаминоксидазы (ИМАО). Эти препараты следует применять с осторожностью пациентам с ишемической болезнью сердца (ИБС), аритмией, артериальной гипертонией, после инсульта, а также с задержкой мочи или вегетативной недостаточностью. Данное обстоятельство существенно ограничивает применение ТЦА в общемедицинской практике.
Эффективность применения ТЦА (амитриптилин, дезипрамин, кломипрамин, имипрамин) при лечении болевой формы ДПН показана в ряде рандомизированных плацебо-контролируемых исследований [14]. Наиболее распространенными препаратами этой группы, применяемыми для лечения болевых полинейропатий, являются амитриптилин и имипрамин [15]. Наиболее широко используется амитриптилин. Начальная доза препарата составляет 10–12,5 мг на ночь, затем дозу постепенно увеличивают на 10–25 мг каждые 7 дней до достижения эффекта (максимально до 150 мг/сут). Суточную дозу принимают однократно на ночь или дробят на 2–3 приема. При сопутствующей депрессии обычно требуется назначение более высоких доз препарата. При непереносимости амитриптилина возможно назначение других ТЦА, например имипрамина или кломипрамина. Пробное лечение антидепрессантами должно продолжаться как минимум 6–8 недель, при этом максимально переносимую дозу пациент должен принимать не менее 1–2 недель. Хотя амитриптилин эффективен примерно у 70% больных с НБ, выраженные побочные эффекты ограничивают его применение. Перед назначением любого ТЦА обязательно предварительное проведение ЭКГ, особенно у лиц старше 40 лет.
При плохой переносимости ТЦА возможно применение тетрациклических антидепрессантов (например, мапротилина, 25–100 мг/сут) или селективных ингибиторов обратного захвата серотонина и норадреналина (СИОЗСН) (венлафаксина, 150–225 мг/сут, или дулоксетина, 60–120 мг/сут) [16]. Эффективность венлафаксина неоднократно доказана в ходе исследований, включавших пациентов с ДПН [17, 18], при этом у него отсутствуют постсинаптические эффекты, свойственные для ТЦА (действие на М-холинорецепторы, альфа-адренергические и гистаминовые рецепторы). Это делает препарат более безопасным, чем ТЦА. Наступление противоболевого эффекта отмечено уже на второй неделе терапии [19].
Таким образом, венлафаксин является эффективным, безопасным, хорошо переносимым лекарственным средством при лечении ДПН. В трех мультицентровых рандомизированных двойных слепых плацебо-контролируемых исследованиях длительностью от 12 до 13 недель показана эффективность применения дулоксетина в дозе от 60 до 120 мг/сут у больных с болевой ДПН. В результате исследований обнаружено 50% снижение интенсивности боли при лечении дулоксетином (вне зависимости от применяемой дозы) у 41% больных, по сравнению с 24% пациентов, принимавших плацебо [20].
Селективные ингибиторы обратного захвата серотонина (СИОЗС) (флуоксетин, пароксетин, сертралин, циталопрам, эсциталопрам) вызывают меньше побочных действий, но оказывают менее отчетливый противоболевой эффект, что, возможно, объясняется отсутствием прямого влияния на норадренергическую передачу. Они показаны, главным образом, в тех случаях, когда боль связана с депрессией, а больной плохо переносит другие антидепрессанты [16].
Поскольку НБ часто сопровождается депрессией, актуальным является выбор препарата, эффективно воздействующего на это психопатологическое состояние и обладающего хорошим профилем безопасности. Одним из таких препаратов является пипофезин (Азафен) [21]. Механизм антидепрессивного действия основан на неизбирательном ингибировании обратного захвата серотонина и норадреналина, что приводит к увеличению их концентрации в ЦНС. Препарат не обладает кардиотоксическими свойствами. В связи с отсутствием холинолитического действия Азафен можно назначать больным глаукомой и другими заболеваниями, при которых противопоказано применение препаратов, обладающих холинолитической активностью, в том числе имипрамина и амитриптилина. Отсутствие выраженных побочных явлений позволяет назначать препарат больным с соматическими заболеваниями и лицам пожилого возраста, прежде всего, в амбулаторной практике.
Среди антиконвульсантов, применяемых при лечении болевой ДПН, наиболее эффективными являются габапентин (Нейронтин) и прегабалин (Лирика) [22, 23]. Механизм действия габапентина и прегабалина, по-видимому, основан на способности связываться с альфа-2-дельта-субъединицами потенциалзависимых кальциевых каналов периферических сенсорных нейронов. Это приводит к снижению входа кальция в пресинаптический нейрон, в результате чего уменьшается высвобождение главных медиаторов боли (глутамата, норадреналина и субстанции Р) перевозбужденными нейронами, что сопровождается редукцией болевого синдрома. Оба препарата обладают хорошей переносимостью и высокой эффективностью, наблюдаемой уже на 1-й неделе лечения. Наиболее частыми побочными эффектами являются головокружение и сонливость. Начальная доза габапентина — 100–300 мг на ночь. Затем суточную дозу постепенно увеличивают каждые 3–5 дней на 100–300 мг, переходя на трехкратный прием.
Средняя эффективная доза составляет 1800 мг/сут (600 мг 3 раза в день), максимальная — 3600 мг/сут. На титрование дозы габапентина может уйти от 2 до 8 недель. Прежде чем делать вывод о неэффективности препарата, его максимально переносимую дозу следует принимать 1–2 недели. По показателям эффективности и безопасности прегабалин примерно соответствует габапентину, но в отличие от габапентина обладает линейной фармакокинетикой, что обеспечивает предсказуемость изменений концентрации препарата в плазме крови при изменении дозы. Диапазон суточных доз преагабалина — 150–600 мг/сут в 2 приема.
При лечении болевой ДПН стартовая доза может составлять 150 мг/сут. В зависимости от эффекта и переносимости дозу можно увеличить до 300 мг/сут через 3–7 дней. При необходимости можно увеличить дозу до максимальной (600 мг/сут) через 7-дневный интервал. В соответствии с опытом применения препарата, при необходимости прекращения приема рекомендуется постепенно снижать дозу в течение недели. Прегабалин быстрее всасывается в кровь и обладает более высокой биодоступностью (90%) по сравнению с габапентином (33–66%). Вследствие этого препарат эффективен в меньших дозах и обладает меньшей частотой и выраженностью побочных эффектов, в особенности седации [22, 23].
Использование опиоидов для лечения болевых синдромов возможно только при отсутствии эффекта от других препаратов. Среди опиоидов наиболее эффективными при лечении болевой ДПН оказались оксикодон в дозе 37–60 мг/сут [24] и трамадол (препарат, обладающий низкой аффинностью к опиоидным μ-рецепторам и одновременно являющийся ингибитором обратного захвата серотонина и норадреналина). Лечение трамадолом начинают с дозы 50 мг на ночь (или 25 мг 2 раза в день), спустя 5–7 дней дозу увеличивают до 100 мг/сут. При необходимости дозу повышают до 100 мг 2–4 раза в день. Пробное лечение трамадолом должно продолжаться не менее 4 недель [25]. Опиоиды ценятся за их болеутоляющие свойства, но препараты этого класса вызывают в организме и чрезвычайно выраженные и опасные побочные эффекты.
Комбинация трамадола с парацетамолом (Залдиар) позволяет снизить дозу трамадола и тем самым риск побочного действия, не жертвуя анальгетическим эффектом [26]. При комбинации двух указанных препаратов, обладающих разным механизмом действия (механизм анальгетического эффекта парацетамола может быть связан с ингибирующим эффектом на центральный синтез простагландинов, возможно, за счет торможения ЦОГ-3), возникает эффект синергизма. Адекватное обезболивание при приеме комплекса препаратов наблюдается в 1,5–3 раза чаще, чем при применении каждого из соединений в соответствующих дозах.
Кроме того, для парацетамола и трамадола характерен взаимодополняющий фармакокинетический профиль, благодаря которому препарат быстро начинает действие — уже через 15–20 минут (за счет парацетамола) и длительное время поддерживает анальгетический эффект (за счет трамадола) [26]. В состав Залдиара входит низкая доза трамадола (в одной таблетке содержится 37,5 мг трамадола и 325 мг парацетамола), поэтому побочные эффекты при его применении возникают реже, чем при применении трамадола. Назначение препарата не требует длительного титрования дозы, лечение может быть начато с дозы 1–2 таблетки в день, в последующем доза может быть повышена до 4 таблеток в сутки.
Пероральный антиаритмический препарат мексилетин также относится к анестетикам. Считается, что мексилетин блокирует натриевые каналы, таким образом стабилизируя мембрану нейронов и блокируя передачу болевых импульсов. Испытания по применению мексилетина при НБ дают противоречивые результаты. В ряде случаев мексилетин значительно уменьшает боль, особенно при его применении в высоких дозах. Однако при этом чаще возникают побочные эффекты, в частности со стороны ЖКТ. Препарат следует применять с осторожностью при наличии в анамнезе сердечной патологии или выявлении нарушений при ЭКГ-исследовании [27].
В ряде исследований было показано, что применение местных анестетиков (кремов, гелей и пластыря (Версатис) с 5-процентным содержанием лидокаина или препаратов на основе экстрактов жгучего перца — капсаицина) было эффективным при лечении болевой формы ДПН [27, 28]. Эффект лидокаина основан на блокировании транспорта ионов натрия через мембрану периферических нейронов, в результате чего происходит стабилизация клеточной мембраны, замедляется распространение потенциала действия, а следовательно, уменьшается боль. Из побочных эффектов может наблюдаться местное раздражение кожи в области нанесения, которое чаще всего незначительно и быстро проходит. Действие препаратов капсаицина основано на истощении запасов субстанции Р в терминалях сенсорных волокон. Жжение, покраснение и зуд в месте нанесения являются наиболее частыми побочными эффектами, часто отмечается усиление боли при первом нанесении препарата.
Тем не менее ни одно лекарственное средство нельзя рассматривать в качестве единственного препарата для лечения боли при ДПН [29]. Нередки случаи, когда применение любого из перечисленных выше средств оказывается недостаточно эффективным и возникает потребность в комбинации препаратов. Поэтому хотя число одновременно принимаемых пациентом лекарственных средств по общему правилу следует стараться ограничивать, но в большинстве случаев НБ при ДПН удается адекватно контролировать лишь с помощью комбинации двух и более препаратов. Нерационально сразу же назначать комбинацию нескольких средств: первоначально следует испробовать один препарат, и лишь убедившись, что в переносимых данным пациентом дозах он оказывает лишь частичный эффект, к нему следует присоединить следующее средство, которое, как правило, обладает иным механизмом действия.
В клинической практике часто комбинируют антидепрессант с антиконвульсантом, антиконвульсант с трамадолом или Залдиаром. Рекомендуется избегать сочетания трамадола (особенно больших доз) с ИМАО, СИОЗС и СИОЗСН, так как подобная комбинация может спровоцировать серотониновый синдром. С осторожностью трамадол следует назначать в комбинации с трициклическими антидепрессантами (учитывая риск серотонинового синдрома) [30].
Нефармакологические методы лечения ДПН включают в себя психотерапию, бальнеотерапию, гипербарическую оксигенацию (1,2–2 атм.), фототерапию, магнитотерапию, электрофорез, диадинамические токи, электростимуляцию паретичных мышц, чрескожную электронейростимуляцию, иглорефлексотерапию. Противопоказанием к их применению является тяжелое состояние больного, обусловленное соматической патологией и/или тяжелая декомпенсация метаболизма. Рядом авторов показана высокая эффективность электростимуляции спинного мозга, используемой для лечения болевой диабетической нейропатии [31]. Как правило, имплантацию стимуляторов производят у пациентов с рефрактерными к фармакотерапии болевыми синдромами.
В заключение следует заметить, что лечение каждого пациента должно быть индивидуальным с учетом клинических особенностей, а также наличия коморбидных заболеваний (тревоги, депрессии, заболеваний внутренних органов и т. д.). При выборе лекарственных препаратов, помимо непосредственного анальгетического эффекта, должны быть учтены другие положительные эффекты выбранного препарата (уменьшение уровней тревоги, депрессии, улучшение сна и настроения), а также его переносимость и возможность развития серьезных осложнений.
Ряд авторов в качестве препаратов первого ряда при лечении болевых форм полинейропатий рекомендуют ТЦА и габапентин или прегабалин. К препаратам второго ряда относят СИОЗСН — венлафаксин и дулоксетин. Они обладают меньшей эффективностью, но более безопасны, имеют меньше противопоказаний по сравнению с ТЦА, и им должно быть отдано предпочтение при лечении больных с сердечно-сосудистыми факторами риска. Препараты третьей линии включают в себя опиоиды. К препаратам с более слабым эффектом относятся капсаицин, мексилетин, окскарбазепин, СИОЗС, топиромат, мемантин, миансерин [32].
Литература
*Первый МГМУ им. И. М. Сеченова, **МОНИКИ им. М. Ф. Владимирского, Москва