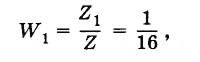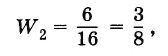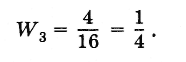какое состояние газа является наиболее вероятным и соответствует равновесному состоянию
§ 81. Второй закон термодинамики
Вспомните формулировку первого закона термодинамики.
Допускает ли первый закон термодинамики самопроизвольный переход тепла от менее нагретого тела к более нагретому?
Наблюдаются ли такие процессы в природе?
Мы уже отмечали, что первый закон термодинамики — это частный случай закона сохранения энергии.
Закон сохранения энергии утверждает, что количество энергии при любых её превращениях остаётся неизменным. Между тем многие процессы, вполне допустимые с точки зрения закона сохранения энергии, никогда не протекают в действительности. Например, с точки зрения первого закона термодинамики в изолированной системе возможен переход тепла от менее нагретого тела к более нагретому, если количество теплоты, полученной горячим телом, точно равно количеству теплоты, отданной холодным телом. В то же время наш опыт подсказывает, что это невозможно.
Важно
Первый закон термодинамики не указывает направление процессов.
Второй закон термюдинамики. Второй закон термодинамики указывает направление возможных энергетических превращений, т. е. направление процессов, и тем самым выражает необратимость процессов в природе. Этот закон был установлен путём непосредственного обобщения опытных фактов.
Есть несколько формулировок второго закона, которые, несмотря на внешнее различие, выражают, в сущности, одно и то же и поэтому равноценны.
Немецкий учёный Р. Клаузиус (1822—1888) сформулировал этот закон так:
Второй закон термодинамики
Невозможно перевести тепло от более холодной системы к более горячей при отсутствии других одновременных изменений в обеих системах или в окружающих телах.
Здесь констатируется опытный факт определённой направленности теплопередачи: тепло само собой переходит всегда от горячих тел к холодным. Правда, в холодильных установках осуществляется теплопередача от холодного тела к более тёплому, но эта передача связана с другими изменениями в окружающих телах: охлаждение достигается за счёт работы.
Важность этого закона в том, что из него можно вывести заключение о необратимости не только процесса теплопередачи, но и других процессов в природе.

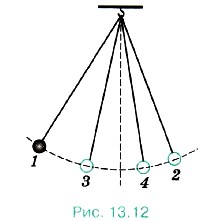
Рассмотрим пример. Колебания маятника, выведенного из положения равновесия, затухают (рис. 13.12) 1, 2, 3, 4 — последовательные положения маятника при максимальных отклонениях от положения равновесия). За счёт работы сил трения механическая энергия маятника убывает, а температура маятника и окружающего воздуха (а значит, и их внутренняя энергия) слегка повышается.
Можно вновь увеличить размах колебаний маятника, подтолкнув его рукой. Но это увеличение возникает не само собой, а становится возможным в результате более сложного процесса, включающего движение руки.
Важно
Механическая энергия самопроизвольно переходит во внутреннюю, но не наоборот. При этом энергия упорядоченного движения тела как целого превращается в энергию неупорядоченного теплового движения составляющих его молекул.

Ещё один пример — процесс диффузии. Открыв пузырёк с духами, мы быстро почувствуем запах духов. Молекулы ароматического вещества благодаря тепловому движению проникают в пространство между молекулами воздуха. Трудно представить, чтобы все они вновь собрались в пузырьке.
Число подобных примеров можно увеличивать практически неограниченно. Все они говорят о том, что процессы в природе имеют определённую направленность, никак не отражённую в первом законе термодинамики.
Важно
Все макроскопические процессы в природе протекают только в одном определенном направлении.
В обратном направлении они самопроизвольно протекать не могут. Все процессы в природе необратимы.
Раньше при рассмотрении процессов мы предполагали, что они являются обратимыми.
Запомни
Обратимый процесс — это процесс, который можно провести в прямом и обратном направлениях через одни и те же промежуточные состояния без изменений в окружающих телах.
Обратимый процесс должен протекать очень медленно, чтобы каждое промежуточное состояние было равновесным.
Запомни
Равновесное состояние — это состояние, при котором температура и давление во всех точках системы одинаковы.
Следовательно, чтобы система пришла в равновесное состояние, необходимо время.

При изучении изопроцессов мы предполагали, что переход из начального состояния в конечное проходит через равновесные состояния, и считали изотермический, изобарный и изохорный процессы обратимыми.
Идеальных обратимых процессов в природе не существует, однако реальные процессы можно с определённой степенью точности рассматривать как обратимые, что является очень важным для теории.

Статистический характер второго закона термодинамики. Второй закон термодинамики определяет направление процессов в изолированной системе, однако этот закон носит статистический (вероятностный) характер.
Любое макросостояние системы, характеризующееся некоторыми макропараметрами, определяется его микросостояниями. Например, для газа давление и температура определяются числом молекул, их скоростью, распределением молекул по объёму сосуда. Если система предоставлена самой себе и она изолирована, то, как мы знаем, постепенно достигается равновесное состояние, при котором давление и температура во всех точках одинаковы. Процесс перехода системы из неравновесного состояния в равновесное — необратимый процесс.
Равновесное состояние соответствует хаотичному движению молекул, т. е. система с точки зрения микросостояний приходит к полному хаосу. Хаотичное движение предполагает непрерывное перемещение молекул газа по объёму, обмен скоростями. Естественно, если мы сможем проследить за отдельными молекулами, то они в разные моменты времени оказываются в разных частях сосуда. Число молекул, находящихся в выделенном объёме, также может быть различным и т. д. В то же время макропараметры газа не меняются.
Движение молекул — это механическое движение, которое является обратимым. В то же время все необратимые процессы, такие, как теплообмен, происходят вследствие механического движения атомов и молекул, так как столкновения молекул обеспечивают передачу энергии. Итак, необратимые процессы являются следствием обратимого механического движения.
Чтобы соединить эти два неоспоримых факта, Л. Больцман использовал понятие вероятности. Так, состояние газа, при котором молекулы движутся хаотично, является наиболее вероятным, наиболее вероятным является и равномерное распределение молекул по объёму сосуда.
Однако возможно, что благодаря случайным перемещениям молекул все они окажутся в какой-то части сосуда, но вероятность такого состояния чрезвычайно мала.
Соответственно не противоречит законам природы даже такой процесс, в результате которого при случайном движении молекул воздуха все они соберутся в одной половине класса, а учащиеся в другой половине класса задохнутся. Но реально это событие никогда не происходило в прошлом и не произойдёт в будущем. Слишком мала вероятность подобного события, чтобы оно когда-либо случилось за всё время существования Вселенной в современном её состоянии — около нескольких миллиардов лет.
По приблизительным оценкам, эта вероятность примерно такого же порядка, как и вероятность того, что 20 000 обезьян, хаотично ударяя по клавишам пишущих машинок, напечатают без единой ошибки «Войну и мир» Л. Н. Толстого. В принципе это возможно, но реально никогда не произойдёт.
Границы применимости второго закона термодинамики. Вероятность обратных процессов перехода от равновесных состояний к неравновесным для макроскопических систем в целом очень мала. Но для малых объёмов, содержащих небольшое число молекул, вероятность отклонения от равновесия становится заметной.
Запомни
Такие случайные отклонения системы от равновесия называются флуктуациями.
Именно флуктуациями плотности газа в областях порядка длины световой волны объясняются рассеяние света в атмосфере Земли и голубой цвет неба. Флуктуации давления в малых объёмах объясняют броуновское движение.
Наблюдение флуктуации служит важнейшим доказательством правильности созданной Больцманом статистической теории необратимости макропроцессов. Второй закон термодинамики выполняется только для систем с огромным числом частиц. В малых объёмах уже становятся существенными отклонения от этого закона.
Ключевые слова для поиска информации по теме параграфа.
Второй закон термодинамики. Обратимость процессов
Вопросы к параграфу
1. Какие процессы называются необратимыми? Назовите наиболее типичные необратимые процессы.
2. Как формулируется второй закон термодинамики?
3. Какое состояние газа является наиболее вероятным и соответствует равновесному состоянию?
§ 81. Второй закон термодинамики (окончание)
Статистический характер второго закона термодинамики
Второй закон термодинамики определяет направление процессов в изолированной системе, однако этот закон носит статистический (вероятностный) характер.
Любое макросостояние системы, характеризующееся некоторыми макропараметрами, определяется его микросостояниями. Например, для газа давление и температура определяются числом молекул, их скоростью, распределением молекул по объёму сосуда. Если система предоставлена самой себе и она изолирована, то, как мы знаем, постепенно достигается равновесное состояние, при котором давление и температура во всех точках одинаковы. Процесс перехода системы из неравновесного состояния в равновесное — необратимый процесс.
Равновесное состояние соответствует хаотичному движению молекул, т. е. система с точки зрения микросостояний приходит к полному хаосу. Хаотичное движение предполагает непрерывное перемещение молекул газа по объёму, обмен скоростями. Естественно, если мы сможем проследить за отдельными молекулами, то они в разные моменты времени оказываются в разных частях сосуда. Число молекул, находящихся в выделенном объёме, также может быть различным и т. д. В то же время макропараметры газа не меняются.
Движение молекул — это механическое движение, которое является обратимым. В то же время все необратимые процессы, такие, как теплообмен, происходят вследствие механического движения атомов и молекул, так как столкновения молекул обеспечивают передачу энергии. Итак, необратимые процессы являются следствием обратимого механического движения.
Чтобы соединить эти два неоспоримых факта, Л. Больцман использовал понятие вероятности. Так, состояние газа, при котором молекулы движутся хаотично, является наиболее вероятным, наиболее вероятным является и равномерное распределение молекул по объёму сосуда.
Однако возможно, что благодаря случайным перемещениям молекул все они окажутся в какой-то части сосуда, но вероятность такого состояния чрезвычайно мала.
Соответственно не противоречит законам природы даже такой процесс, в результате которого при случайном движении молекул воздуха все они соберутся в одной половине класса, а учащиеся в другой половине класса задохнутся. Но реально это событие никогда не происходило в прошлом и не произойдёт в будущем. Слишком мала вероятность подобного события, чтобы оно когда-либо случилось за всё время существования Вселенной в современном её состоянии — около нескольких миллиардов лет.
По приблизительным оценкам, эта вероятность примерно такого же порядка, как и вероятность того, что 20 000 обезьян, хаотично ударяя по клавишам пишущих машинок, напечатают без единой ошибки «Войну и мир» Л. Н. Толстого. В принципе это возможно, но реально никогда не произойдёт.
Границы применимости второго закона термодинамики
Вероятность обратных процессов перехода от равновесных состояний к неравновесным для макроскопических систем в целом очень мала. Но для малых объёмов, содержащих небольшое число молекул, вероятность отклонения от равновесия становится заметной.
Запомни
Такие случайные отклонения системы от равновесия называются флуктуациями.
Именно флуктуациями плотности газа в областях порядка длины световой волны объясняются рассеяние света в атмосфере Земли и голубой цвет неба. Флуктуации давления в малых объёмах объясняют броуновское движение.
Наблюдение флуктуации служит важнейшим доказательством правильности созданной Больцманом статистической теории необратимости макропроцессов. Второй закон термодинамики выполняется только для систем с огромным числом частиц. В малых объёмах уже становятся существенными отклонения от этого закона.
Ключевые слова для поиска информации по теме параграфа.
Второй закон термодинамики. Обратимость процессов
Вопросы к параграфу
1. Какие процессы называются необратимыми? Назовите наиболее типичные необратимые процессы.
2. Как формулируется второй закон термодинамики?
3. Какое состояние газа является наиболее вероятным и соответствует равновесному состоянию?
Вероятность состояния
С течением времени микросостояния непрерывно сменяют друг друга. Время пребывания системы в определенном макроскопическом состоянии пропорционально, очевидно, числу микросостояний Z1, которые реализуют данное состояние. Если через Z обозначить полное число микросостояний системы, то вероятность состояния W определится так:
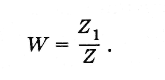
Вероятность макроскопического состояния равна отношению числа микросостояний, реализующих макросостояние, к полному числу возможных микросостояний.
Переход системы к наиболее вероятному состоянию
Чем больше Z1, тем больше вероятность данного макросостояния и тем большее время система будет находиться в этом состоянии. Таким образом, эволюция системы происходит в направлении перехода от маловероятных состояний к состояниям более вероятным. Именно с этим связана необратимость течения макроскопических процессов, несмотря на обратимость законов, управляющих движением отдельных частиц. Обратный процесс не является невозможным, он просто маловероятен. Так как все микросостояния равновероятны, то в принципе может возникнуть макросостояние, реализуемое малым числом микросостояний, но это чрезвычайно редкое событие. Мы не должны удивляться, если никогда не увидим их. Наиболее вероятно состояние теплового равновесия. Ему отвечает наибольшее число микросостояний.
Легко понять, почему механическая энергия самопроизвольно переходит во внутреннюю. Механическое движение тела (или системы) — это упорядоченное движение, когда все части тела перемещаются идентично или сходным образом. Упорядоченному движению отвечает небольшое число микросостояний по сравнению с беспорядочным тепловым движением. Поэтому маловероятное состояние упорядоченного механического движения само собой превращается в беспорядочное тепловое движение, реализуемое гораздо большим числом микросостояний.
Менее нагляден процесс перехода теплоты от горячего тела к холодному. Но и здесь сущность необратимости та же.
В начале теплообмена есть две группы молекул: молекулы с более высокой средней кинетической энергией у горячего тела и молекулы с низкой средней кинетической энергией у холодного. При установлении теплового равновесия в конце процесса все молекулы окажутся принадлежащими к одной группе молекул с одной и той же средней кинетической энергией. Более упорядоченное состояние с разделением молекул на две группы перестает существовать.
Итак, необратимость процессов связана с тем, что неравновесные макроскопические состояния маловероятны. Эти состояния возникают либо естественным путем в результате эволюции Вселенной, либо же создаются искусственно человеком. Например, мы получаем сильно неравновесные состояния, нагревая рабочее тело теплового двигателя до температур, на сотни градусов превышающих температуру окружающей среды.
Расширение «газа» из четырех молекул
Рассмотрим простой пример, позволяющий вычислить вероятности различных состояний и наглядно показывающий, как увеличение числа частиц в системе приводит к тому, что процессы становятся необратимыми, несмотря на обратимость законов движения микрочастиц.
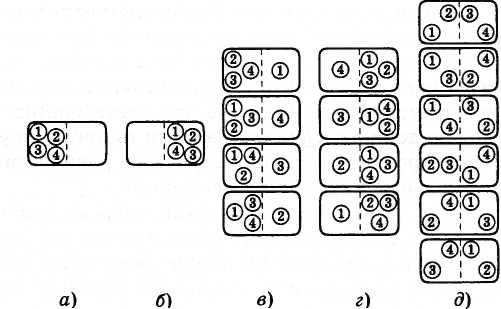
Пусть у нас имеется «газ» в сосуде, состоящий всего лишь из четырех молекул. Вначале все молекулы находятся в левой половине сосуда, отделенной перегородкой от правой половины (рис. 5.12, а). Уберем перегородку, и «газ» начнет расширяться, занимая весь сосуд. Посмотрим, какова вероятность того, что «газ» опять сожмется, т. е. молекулы снова соберутся в одной половине сосуда.
В нашем примере макросостояние будет характеризоваться указанием числа молекул в одной половине сосуда безотносительно к тому, какие именно молекулы здесь находятся. Микросостояния задаются распределением молекул по половинам сосуда с указанием того, какие именно молекулы занимают данную половину сосуда. Пронумеруем молекулы цифрами 1, 2, 3, 4. Возможны 16 различных микросостояний, все они изображены на рисунке 5.12, а — д.
Вероятность того, что все молекулы соберутся в одной половине (например, левой) сосуда, равна:
так как данному макросостоянию соответствует одно микросостояние (см. рис. 5.12, а, б).
Вероятность же того, что молекулы распределятся поровну, будет в б раз больше:
так как данному макросостоянию соответствует шесть микросостояний (см. рис. 5.12, д).
Вероятность того, что в одной половине сосуда (например, левой) будет три молекулы (а в другой соответственно одна молекула), равна (см. рис. 5.12, в, г):
Большую часть времени молекулы будут распределены по половинам сосуда поровну: это наиболее вероятное состояние.
Но примерно 
Тут вы можете оставить комментарий к выбранному абзацу или сообщить об ошибке.
Основные агрегатные состояния вещества
Агрегатные состояния вещества
Чтобы разобраться с тем, какими бывают агрегатные состояния, предлагаю по ходу чтения статьи заполнять таблицу.
Агрегатные состояния
Свойства
Расположение молекул
Расстояние между молекулами
Движение молекулы
Лед, вода и водяной пар — это все три агрегатных состояния одного вещества. Лед — твердое состояние, вода — жидкая, пар — газообразное. Для каждого вещества существует три состояния.
Твердое состояние
Его очень легко представить — это любой предмет, который мы встречаем в жизни. В этом состоянии тело сохраняет форму и объем. Расстояние между молекулами, приблизительно равно размеру самих молекул, которые, в свою очередь, расположены очень структурированно.
Такая структура называется кристаллической решеткой — из-за четкой структуры молекулам сложно двигаться, и они просто колеблются около своих положений.
Заполняем нашу табличку
Агрегатные состояния
Свойства
Расположение молекул
Расстояние между молекулами
Движение молекулы
сохраняет форму и объем
в кристаллической решетке
соотносится с размером молекул
колеблется около своего положения в кристаллической решетке
Жидкое состояние
В этом состоянии сохраняется объем, но не сохраняется форма. Например, если перелить молоко из кувшина в стакан, то молоко, имевшее форму кувшина, примет форму стакана. Кстати, в корове у молока тоже была другая форма.
Расстояние между молекулами в жидком состоянии чуть больше, чем в твердом, но все равно невелико. При этом частицы не собраны в кристаллическую решетку, а расположены хаотично. Молекулы почти не двигаются, но при нагревании жидкости делают это более охотно.
Вспомните, что происходит, если залить чайный пакетик холодной водой — он почти не заваривается. А вот если налить кипяточку — чай точно будет готов.
Агрегатные состояния
Свойства
Расположение молекул
Расстояние между молекулами
Движение молекулы
сохраняет форму и объем
в кристаллической решетке
соотносится с размером молекул
колеблется около своего положения в кристаллической решетке
близко друг к другу
малоподвижны, при нагревании скорость движения молекул увеличивается
Газообразное состояние
В жизни мы встречаем газообразное состояние вещества, когда чувствуем запахи. Запах очень легко распространяется, потому что газ не имеет ни формы, ни объема (он занимает весь предоставленный ему объем), состоит из хаотично движущихся молекул, расстояние между которыми больше, чем размеры молекул.
Агрегатные состояния
Свойства
Расположение молекул
Расстояние между молекулами
Движение молекулы
сохраняет форму и объем
в кристаллической решетке
соотносится с размером молекул
колеблется около своего положения в кристаллической решетке
близко друг к другу
малоподвижны, при нагревании скорость движения молекул увеличивается
занимают предоставленный объем
больше размеров молекул
хаотичное и непрерывное
С агрегатными состояниями разобрались, ура! Но до сих пор неясно, каким образом у каждого вещества их целых три, и как одно переходит в другое. Для этого узнаем, что такое фазовые переходы.
Фазовые переходы: изменение агрегатных состояний вещества
При изменении внешних условий (например, если внутренняя энергия тела увеличивается или уменьшается в результате нагревания или охлаждения) могут происходить фазовые переходы — изменения агрегатных состояний вещества.
Фазовые переходы интересны тем, что все живое не Земле существует лишь благодаря тому, что вода умеет превращаться в лед или пар. С кристаллизацией, плавлением, парообразованием и конденсацией связаны многие процессы металлургии и микроэлектроники.
На схеме — названия всех фазовых переходов:
Переход из твердого состояния в жидкое — плавление;
Переход из жидкого состояния в твердое — кристаллизация;
Переход из газообразного состояния в жидкое — конденсация;
Переход из жидкого состояния в газообразное — парообразование;
Переход из твердого состояния в газообразное, минуя жидкое — сублимация;
Переход из газообразного состояния в твердое, минуя жидкое — десублимация.
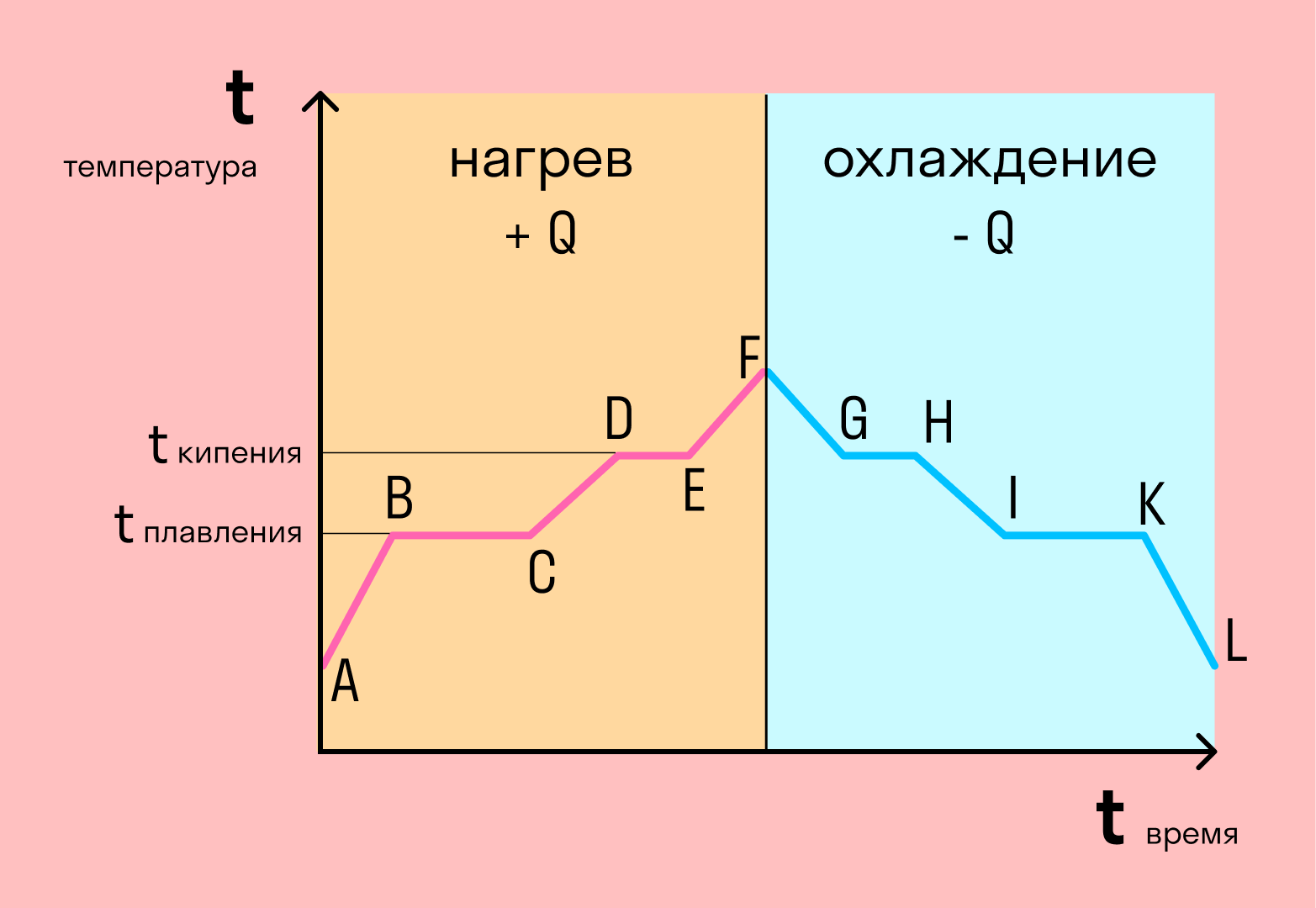
График фазовых переходов
Если взять процесс превращения льда в воду, воды — в пар, и обратные действия, то мы получим очень информативный график.
Разбираемся по шагам. Сначала взяли лед, конечно, при отрицательной температуре, потому что при нуле лед начинает плавиться. Нагрели лед до температуры плавления (до 0 градусов).
После того, как лед нагрелся до температуры плавления, он начинает плавиться. Плавление происходит при постоянной температуре тем дольше длится, чем больше масса плавящегося вещества. Еще этот процесс зависит от свойств самого вещества, но об этом немного позже.
Расправившись вещество уже в жидком состоянии снова начинает нагреваться, и температура увеличивается, пока не достигает температуры кипения. В данном случае нагревается вода — это значит, что ее температура кипения равна 100 градусам Цельсия.
При 100 градусах вода кипит, пока не выкипит целиком. В данном случае процесс аналогично плавлению происходит при постоянной температуре. Данный процесс нельзя путать с испарением, потому что парообразование происходит при конкретной температуре, а испарение — при любой.
Далее полученный пар нагревается, но путем нагревания невозможно дойти до другого фазового перехода — можно пойти только обратно.
Первый шаг в обратную сторону — охлаждение до температуры кипения.
Дойдя до температуры кипения (в данном случае 100 градусов), пар начинает переходить в жидкое состояние. Этот процесс также происходит при постоянной температуре.
Сконденсировавшись, вода охлаждается, пока не начнет замерзать.
Кристаллизуется (замерзает) вода при той же температуре, что и плавится лед — 0 градусов. Кристаллизация также происходит при постоянной температуре.
После кристаллизации лед охлаждается.
С нагреванием и охлаждением все совсем просто — мы либо передаем теплоту телу (веществу), и оно идет на увеличение температуры, либо тело отдает тепло и охлаждается.
В остальных процессах температура не меняется. Это связано с тем, что количество теплоты не всегда зависит от температуры. Формулы для всех процессов выглядят так:
Нагревание
Охлаждение
Q — количество теплоты [Дж]
c — удельная теплоемкость вещества [Дж/кг*˚C]
m — масса [кг]
tконечная — конечная температура [˚C]
tначальная — начальная температура [˚C]
Плавление
Кристаллизация
Q — количество теплоты [Дж]
λ — удельная теплота плавления вещества [Дж/кг]
m — масса [кг]
Парообразование
Конденсация
Q — количество теплоты [Дж]
L — удельная теплота парообразования вещества [Дж/кг]
m — масса [кг]
Решение задач по фазовым переходам
С теорией разобрались — а теперь давайте практиковаться!
Задачка раз. Температура медного образца массой 100 г повысилась с 20 °С до 60 °С. Какое количество теплоты получил образец? Удельную теплоёмкость меди считать равной 380 Дж/(кг умножить на °С)
Q = 380 * 0,1*(60-20) = 1520 Дж
Ответ: образец получил 1520 Дж
Задачка два. Какое количество теплоты необходимо для плавления 2,5 т стали, взятой при температуре плавления? Удельная теплота плавления стали λ=80кДж/кг. Теплопотерями пренебречь.
80 кДж/кг = 80000 Дж/кг
Q = 80000*2500 = 200 000 000 Дж = 200 МДж
Ответ: для плавления 2,5 т стали необходимо 200 МДж теплоты.
Сублимация и десублимация
Мы уже рассказали про такие процессы, как сублимация и десублимация.
Примерчики из жизни🤓
Про принтеры. Цветные принтеры (только не лазерные) печатают путем сублимации. Вот как это работает: частицы краски быстро переходят из твердого состояния в газообразное и оседают на бумаге — так получается цветная картинка.
Рисуночки на окнах. Если вы решите проехаться на автобусе в холодную погоду — увидете на стеклах чудесные узоры. Из-за огромной разницы температур между улицей и автобусом, мы можем наблюдать процесс десублимации в виде красивых рисунков на стеклах. Иней образуется похожим способом — резкое похолодание приводит к десублимации воздуха.
Влажность воздуха: испарение и конденсация
Такие процессы, как испарение и конденсация, становятся более логичными и простыми, если их рассмотреть на примере влажности воздуха.
Влажность воздуха говорит нам о том, сколько в воздухе содержится водяного пара. Любое количество пара в воздух не запихнешь, поэтому, во-первых, его там очень мало, а во-вторых, при избыточном количестве водяного пара происходит конденсация — это когда образуется роса.
Как влажность влияет на человека
Для человека влажность очень важна, потому что мы состоим из воды на 90%. Если окружающей среде нечего испарять, она будет испарять нас. Поэтому при низкой влажности мы чувствуем сухость во рту, а при высокой — волосы впитывают влагу, разбухают и начинают виться. На этом принципе построены некоторые гигрометры — приборы для измерения влажности. Они так и называются — волосяные гигрометры. Только внутри не человеческий волос, а конский, но принцип от этого не меняется.
При высокой влажности холод и тепло воспринимаются более чувствительно. Это связано с потливостью человека при высокой температуре. Такой механизм помогает нам бороться с жарой, но при высокой влажности пот не может испариться. При испарении пота мы теряем избыточное тепло, а в данном случае этого не происходит.
При низкой влажности происходит нечто похожее. Как ни странно, в мороз мы тоже потеем (намного меньше, но все-таки это происходит). Если влажность на улице низкая, то пот испарится из-под куртки и нам будет комфортно, а при высокой влажности — он там задержится и будет проводить тепло наружу, забирая у нас драгоценные Джоули тепла. Поэтому зимой в Петербурге холоднее, чем в Москве.
Влажностью можно управлять. Существуют мешочки с шариками адсорбентами, которые кладут в коробки с обувью, чтобы впитать лишнюю влагу. Чтобы окна не запотевали, можно насыпать в рамы соль, которая также впитает влагу. А если вам наоборот нужно больше влаги — берем увлажнитель воздуха (классная вещь!): он добавляет в воздух водяной пар.