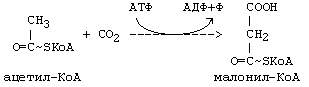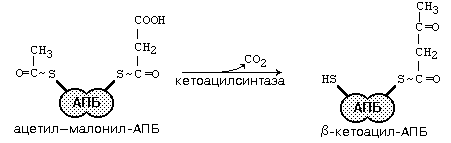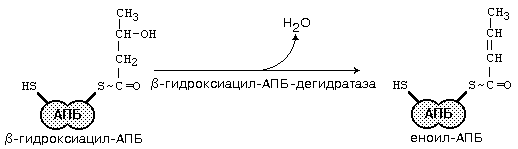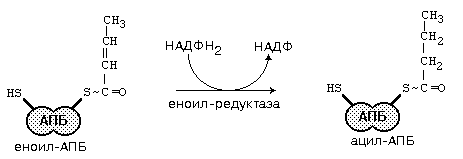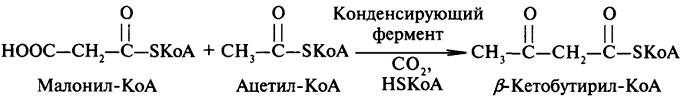СИНТЕЗ ВЫСШИХ ЖИРНЫХ КИСЛОТ
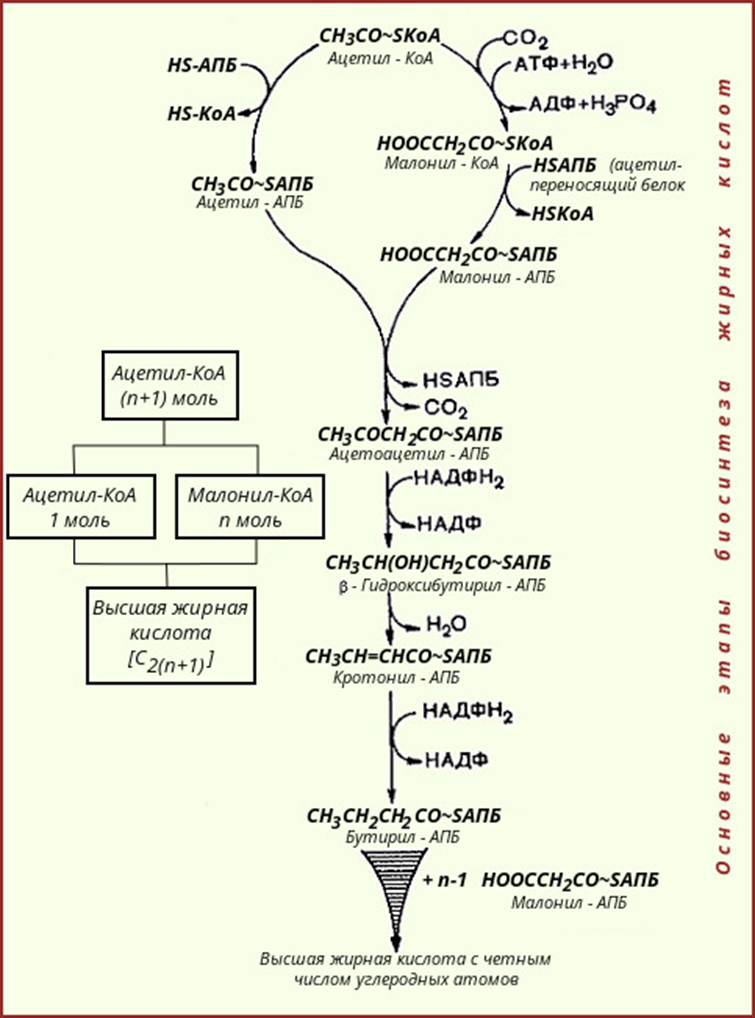
В дальнейшем в ходе синтеза жирных кислот происходит поэтапное удлинение молекулы ацил-КоА на 2 углеродных атома за каждый этап за счет малонил-КоА, который в этом процессе удлинения теряет СО2.
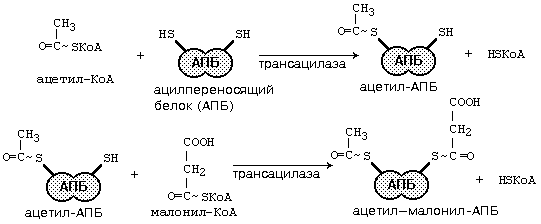
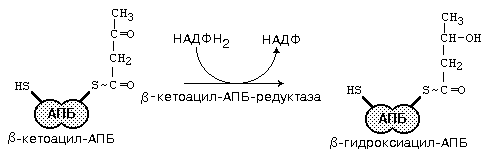
Рис.45. Реакции синтеза высших жирных кислот
После окончания цикла ацил-АПБ вступает в следующий цикл синтеза. К свободной SH-группе ацилпереносящего белка присоединяется новая молекула малонил-КоА. Затем происходит отщепление ацильного остатка, он переносится на малонильный остаток (с одновременным декарбоксилированием) и цикл реакций повторяется.
Таким образом, углеводородная цепочка будущей жирной кислоты постепенно растет (за каждый цикл – на два углеродных атома). Это происходит до момента, пока она не удлинится до 16 углеродных атомов (в случае синтеза пальмитиновой кислоты) или более (синтез других жирных кислот). Вслед за этим происходит тиолиз и образуется в готовом виде активная форма жирной кислоты – ацил-КоА.
Для нормального течения синтеза высших жирных кислот необходимы следующие условия:
1) Поступление углеводов, при окислении которых образуются необходимые субстраты и НАДФН2.
2) Высокий энергетический заряд клетки – высокое содержание АТФ, которое обеспечивает выход цитрата из митохондрий в цитоплазму.
Сравнительная характеристика b-окисления и синтеза высших жирных кислот:
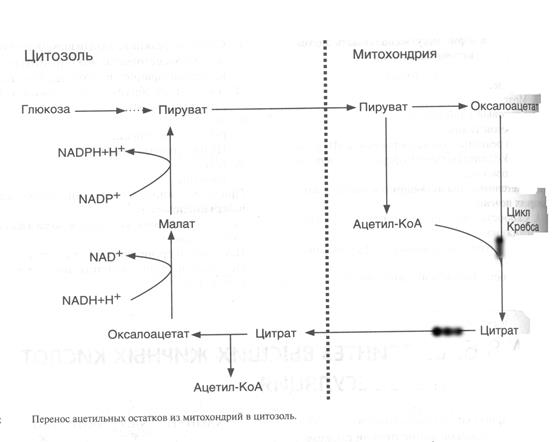
1. b-окисление протекает в митохондриях, а синтез жирных кислот протекает в цитоплазме на мембранах эндоплазматического ретикулума. Однако, образовавшийся в митохондриях ацетил-КоА через мембраны сам проходить не может. Поэтому существуют механизмы транспорта ацетил-КоА из митохондрий в цитоплазму с участием ферментов цикла Кребса (рис.46).
Рис.46. Механизм транспорта ацетил-КоА из митохондрий в цитоплазму.
Таким образом, условием для выхода ацетил-КоА из митохондрии в цитоплазму является хорошее обеспечение клетки АТФ. Если АТФ в клетке мало, то ацетил-КоА расщепляется до СО2 и Н2О.
2. В ходе b-окисления промежуточные продукты связаны с HS-КоА, а при синтезе жирных кислот промежуточные продукты связаны с особым ацил-переносящим белком (АПБ). Это сложный белок. Его небелковая часть похожа по строению на КоА и состоит из тиоэтиламина, пантотеновой кислоты (витамин В3) и фосфата.
В клетке существует 2 основных источника НАДФ*Н2 для синтеза жирных кислот:
а) пентозофосфатный путь распада углеводов;
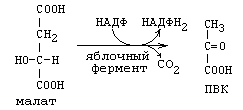
б) в реакции окисления малата:
Эта реакция протекает в цитоплазме и катализируется ферментом малатдегидрогеназой.
Таким образом, обмен углеводов и обмен жиров очень тесно связаны. Углеводы легко могут превращаться в жиры, а вот превращение жиров в углеводы невозможно, так как ацетил-КоА не может превращаться в пируват.
БИОСИНТЕЗ ВЫСШИХ ЖИРНЫХ КИСЛОТ И ЕГО РЕГУЛЯЦИЯ
Образование ацетил-КоА в результате окислительного декарбоксилирования пирувата происходит в матриксе митохондрий, но ацетил-КоА не попадает через мембрану митохондрий в цитоплазму, где идет синтез жирных кислот.Поэтому ацетил-КоА конденсируется с оксалоацетатом с образованием цитрата и цитрат с помощью транслоказы переносится в цитоплазму (рис.12).
В цитоплазме под действием фермента цитратлиазы идет реакция:
Цитрат + HSKoA + АТР ® Ацетил-КоА + ADP + Рi + Оксалоацетат
Пируват переносится обратно в матрикс митохондрий, a NADPH2, восстановленный в результате действия малик-фермента, используется как донор водорода для последующего синтеза жирных кислот. Другой источник NADPH2 — пентозофосфатный путь.
Первая реакция синтеза жирных кислот — это превращение ацетил-КоА в малонил-КоА (рис.13).
Фермент, катализирующий эту реакцию,ацетил-КоА-карбоксилаза, являетсярегуляторным в биосинтезе жирных кислот. Он относится к классу лигаз, кофермент — биотин.
Последующие реакции синтеза жирных кислот происходят на ферменте, который называетсясинтазой жирных кислот или пальмитатсинтазой, так как основной жирной кислотой в липидах человека является пальмитиновая кислота. Некоторые жирные кислоты могут образовываться в организме из пальмитиновой кислоты.
Синтаза жирных кислот (фермент фиксирован на мембранах эндоплазматического ретикулума). Синтаза жирных кислот является полифункциональным ферментом, состоящим из 2 идентичных полипептидных цепей, каждая из которых имеет 7 активных центров и ацилпереносящий белок, который переносит растущую цепь жирной кислоты из одного активного центра в другой. Каждый из белков имеет 2 центра связывания, содержащих SH-группы. Участок, связывающий малонил-КоА, содержит небелковый компонент – витамин B3 (пантотеновую кислоту).
Синтез жирной кислоты начинается с переноса ацетильного остатка, а затем малонильного с помощью ферментов ацетилтрансферазы и малонилтранс-феразы на синтазу жирных кислот. Далее карбоксильная группа малонила выделяется в виде СО2 и по освободившейся валентности присоединяется ацетил с образованием ацетоацетил-Е. Последующие реакции восстановления, дегидратации, восстановления приводят к образованию радикала бутирила, связанного с ферментом. Затем повторяется такой же цикл реакций и образуется радикал жирной кислоты с 6 углеродными атомами. Цикла повторяются вплоть до образования радикала пальмитиновой кислоты. Фермент тиоэстераза отщепляет от фермента жирную кислоту (рис.13).
Биосинтез жирных кислот является процессом, в котором повторяются одни и те же последовательности реакций, поэтому процесс называется циклическим, и в каждом цикле радикал жирной кислоты увеличивается на 2 атома углерода, источником которых являетсямалонил-КоА. В каждом цикле происходят реакции восстановлении с использованием NADPH + Н + одним из источников которого является пентозофосфатный пуп окисления глюкозы, другим — малик-фермент.
Другие жирные кислоты в организме человека синтезируются из пальмитиновой кислоты, при эта происходят реакции удлинения углеродного скелета также с использованием малонил-КоА и реакции дегидрирования.
В организме человекане синтезируются жирные кислоты с двойными связями, расположенными дистальнее С9-го атома углерода, поэтому человек должен получать незаменимые жирные кислоты с пищей.
Синтезированные жирные кислоты не остаются |в свободном виде, а быстро используются для синтеза жиров и в меньшей степени фосфолипидов.
125. Синтез вжк. Основные этапы и значение.
Синтез высших жирных кислот локализован в эндоплазматической сети клетки. Непосредственным источником синтеза является малонил-КоА, образующийся из ацетил-КоА и оксида углерода (IV) при участии АТФ:
Начальным этапом синтеза ВЖК является конденсация малонил-КоА с ацетил-КоА:
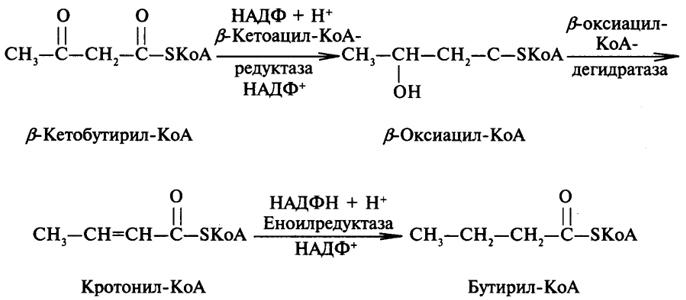
Образовавшийся β-кетобутирил-КоА сначала восстанавливается доβ-оксибутирил-КоА, который далее с участием дегидратазы превращается в кротонил-КоА, содержащий двойную связь. Кротонил-КоА восстанавливается до бутирил-КоА.
Следует подчеркнуть, что ферменты редуктазы в своем составе содержат НАДФ. Работу второго домена синтетазы ВЖК можно представить следующей цепью превращений:
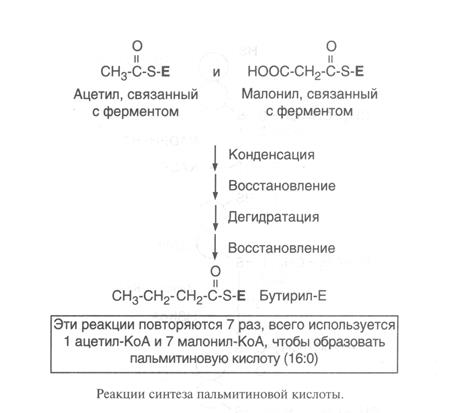
Биосинтез ВЖК носит циклический характер. Синтезированный бутирил-КоА вступает в новый цикл превращений, представленных выше. Для синтеза, например, пальмитиновой кислоты нужно семь таких циклов; в каждом цикле происходит удлинение ацила на два углеродных атома. По достижении ацильным радикалом длины в 16 и более атомов углерода происходит его отщепление от фермента третьим доменом, обладающим тиоэстеразной активностью.
Схема 1. Основные этапы биосинтеза жирных кислот.
134. Превращения аминокислот после всасывания (дезаминирование, переаминирование, декарбоксилирование). Напишите уравнение реакции окислительного дезаминирования аспарагиновой кислоты.
Простые аминокислоты, как и многие другие простые «биологические молекулы», не накапливаются в клетке: как правило, их избыток разрушается при помощи реакций, которые снабжают живую систему энергией. Три основные реакции, катализируемые ферментами, благодаря которым осуществляется превращение аминокислот в клетке, это реакции дезаминирования, переаминирования и декарбоксилирования.
Тут вы можете оставить комментарий к выбранному абзацу или сообщить об ошибке.
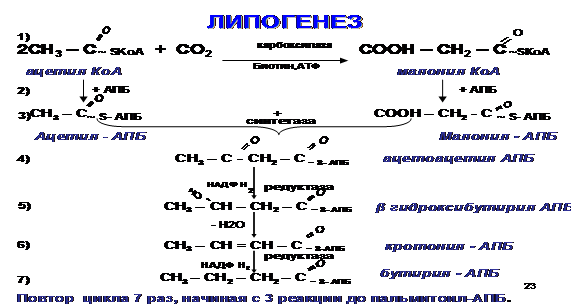
Синтез высших жирных кислот (липогенез). Особенности. Регуляция.
Липогенезнаиболее активно происходит в цитозоле клеток печени, кишечника, жировой ткани, в состоянии покоя или после еды. Особенности:
1) Протекает в цитоплазме.
2) У человека происходит синтез только пальмитиновой кислоты.
3) Принимает участие АПБ (ацилпереносящий белок) – полиферментный комплекс из 6 ферментов.
4) Необходимо участие реакций карбоксилирования, СО2, АТФ, НАДФ∙Н2.
Удлинение пальмитиновой кислоты происходит с участием ацетил-КоА, с образованием стеариновой кислоты. В печени и в тканях мозга из стеариновой кислоты образуются ВЖК с длинной углеродной цепью от С20 до С24, необходимых для образования глико- и сфинголипидов. Из ненасыщенных жирных кислот в организме синтезируется только олеиновая в результате дегидрирования стеариновой кислоты (десатурация) – под влиянием ферментов десатураз, которые могут образовывать двойные связи только у 9 углеродного атома, ω-3 и ω-6 не синтезируются в организме и обязательно должны поступать с пищей.
Гормональная регуляция.Ключевым ферментом синтеза ВЖК явл. карбоксилаза, активность которого регулируется:
1) Глюкагон, адреналин по мембранному механизму вызывают её фосфорилирование, она становится неактивной и липогенез тормозится.
Синтез нейтральных жиров.
Нейтральные жиры – в их состав входит 3хатомный спирт глицерин и ВЖК: олеиновая кислота 55%, пальмитиновая 20%, линолевая 10%.
Ожирение. Первичное и вторичное. Причины.
Ожирение – полигенное заболевание, сопровождающееся накопление ТАГ в адипоцитах, которое явл. фактором риска развития инфаркта миокарда, инсульта, СД, гипертонической и желчнокаменной болезни.
1) Первичное – оно развивается в результате алиментарного дисбаланса – избыточное калорийное питание по сравнению с расходованием энергии. Причины:
Генетические факторы в развитии ожирения. Метаболические различия между тучными и худыми людьми. У людей, склонных к ожирению, вероятно, имеется более прочное сопряжение дыхания и окислительного фосфорилирования, т.е. более эффективный метаболизм. Возможно разное соотношение аэробного и анаэробного гликолиза. Анаэробный гликолиз (как менее эффективный) «сжигает» гораздо больше глюкозы, в результате снижается переработка в жиры.
2) Вторичное ожирение – ожирение в результате основного заболевания, чаще эндокринного.
· Болезнь Иценко-Кушинга – гиперф-я глюкокортикоидов. Гипергликемия, снижение толерантности к глюкозе, обусловленные стимуляцией глюкогеногенезе («стероидный диабет»), усиление катаболизма белков, уменьш. мыш. масса, своеобразное отложение жира (лунообразное лицо, выступающий живот). Гипернатриемия, гипокалиемия, гипертензия, истончение кожи.
· Микседема – гипофун-я щит. железы. Слиз. отёк, пат. ожирение, резкое снижение основного обмена, выпадение волос и зубов, псих. расстройства, сухая кожа, гипергликемия, t снижена, агрессия.
· СД 2—го типа.
· Болезни гипофиза, гипоталамуса.
Дата добавления: 2018-05-30 ; просмотров: 1295 ; Мы поможем в написании вашей работы!
Синтез высших жирных кислот
Синтез высших жирных кислот протекает в цитоплазме клеток, предшественником является ацетил-КоА.
Ацетил-КоА образуется из пирувата при участии ферментовмитохондриального пируватдегидрогеназного комплекса. Внутренняя митохондриальная мембрана непроницаема для ацетил-КоА. В митохондриях фермент цитратсинтаза катализирует реакцию образования цитрата из ацетил-КоА и щавелевоуксусной кислоты (ЩУК). Цитрат выходит из митохондрий в цитоплазму. В цитоплазмефермент цитратлиаза расщепляет цитрат до ацетил-КоА и ЩУК. В цитратлиазной реакции используется 1 молекула АТФ.
Синтаза высших жирных кислот. Комплекс содержит ацилпереносящий белок (АПБ) в качестве своеобразного ядра. Другими ферментами комплекса являются b-кетоацилсинтетаза (КС), малонилтрансфераза (МТ), b-кетоацил-КоА редуктаза (КР), b-гидроксиацилдегидратаза (ГД), еноилредуктаза (ЕР) и ацилтрансацетилаза (АТ).
Ацетил-КоА карбоксилаза катализирует ключевую реакцию в синтезе жирных кислот:
Синтез высших жирных кислот является многостадийным процессом. Количество стадий, или циклов, зависит от длины жирной кислоты. На каждом этапе происходит удлинение синтезирующейся жирной кислоты на два атома углерода. Источником атомов углерода является малонил-КоА.
За 7 таких циклов образуется насыщенная жирная кислота с 16 углеродными атомами (пальмитиновая кислота). В общем виде это выглядит следующим образом:
Ацетил-КоА + 7 Малонил-КоА + 14 НАДФН.Н+ + 14 Н+(r) → Пальмитат + 7 СО2 + 14 НАДФ + 8 КоА-SH + 6 Н2О
Главным источникомвосстановленного НАДФ+ является окислительный этап пентозофосфатного пути обмена глюкозы.
Синтез триацилглицеролов
Клетки большинства тканей, особенно печени и жировой ткани, обладают способностью накапливать ТАГ. Жировая ткань функционально специализируется на хранении и мобилизации ТАГ.
В печени глицерол-3-фосфат может образоваться или в результате фосфорилирования глицерола, или из глюкозы как промежуточный продукт гликолиза. В жировой ткани единственным источником образования глицерол-3-фосфата является гликолиз.
Глицерол + АТФ (r) Глицерол-3-фосфат + АДФ (глицеролкиназа)
Диоксиацетонфосфат + НАДН+Н + (r) Глицерол-3-фосфат + НАД +
Следующим этапом биосинтеза ТАГ является последовательное взаимодействие глицерол-3-фосфата с 2 молекулами ацил-КоА, в результате которого образуется фосфатидная кислота. Реакцию катализирует глицерофосфат-ацилтрансфераза.
Глицерол-3-фосфат + 2 ацил-КоА (r) Фосфатидная кислота + 2 КоА
Далее при участии фосфатидат фосфатазы происходит гидролиз фосфатидной кислоты с образованием 1,2-диацилглицерола (1,2-ДАГ):
На заключительном этапе к 1,2-ДАГ присоединяется третья молекула ацил-КоА с образованием ТАГ. Реакцию катализирует диацилглицерол-ацилтрансфераза:
1,2-ДАГ + ацил-КоА (r) ТАГ + КоАSH
Биосинтез фосфатидилэтаноламинов (кефалинов)
Этаноламин + АТФ (r) Фосфоэтаноламин + АДФ (этаноламинкиназа)
Фосфоэтаноламин + ЦТФ(r) ЦДФ-этаноламин + пирофосфат
ЦДФ-этаноламин + 1,2-ДАГ (r) Фосфатидилэтаноламин (ФЭА) + ЦМФ
Биосинтез фосфатидилхолинов (лецитинов)
ФЭА + 3 S-Аденозилметионин (последовательное присоединение) (r)
(r) Фосфатидилхолин + 3 S-Аденозилгомоцистеин (метилтрансфераза)
Холин + АТФ (r) Фосфохолин + АДФ (холинкиназа)
Фосфохолин + ЦТФ(r) ЦДФ-холин + пирофосфат
ЦДФ-холин + 1,2-ДАГ (r) Фосфатидилхолин + ЦМФ
ФЭА + Серин (r) Фосфатидилсерин + Этаноламин
Фосфатидная кислота + ЦТФ (r) ЦДФ-диацилглицерол + пирофосфат
ЦДФ-ДАГ + Серин (r) Фосфатидилсерин + ЦМФ
Обмен липопротеинов очень низкой плотности (ЛПОНП), липопротеинов промежуточной плотности (ЛППП) и липопротеинов низкой плотности (ЛПНП)Основной функцией этих липопротеинов является транспорт жирных кислот в составе ТАГ из печени к периферическим тканям, особенно в жировую и мышечную. Для синтеза ЛПОНП в гепатоцитах требуется белок апо В-100 и липиды: эфиры холестерола(ЭХС), ТАГ и фосфолипиды (ФЛ).
Триацилглицеролы для ЛПОНП синтезируются путем этерификации жирных кислот. Они поступают в гепатоциты из плазмы крови. Источниками жирных кислот являются жирные кислоты, образовавшиеся в результате гидролиза ТАГ жировой ткани, либо синтезированные в печени жирные кислоты. Образование ЛПОНП регулируется после трансляции за счет контроля синтеза апо В-100.
Обмен ЛПОНП. На эндотелии сосудистой стенки ТАГ в составе ЛПОНП подвергаются действию фермента липопротеинлипазы (ЛПЛ). Необходимым кофактором для проявления активности ЛПЛ является апо С-II. ЛПЛ образуется в клетках многих тканей, среди которых наибольшее значение имеют жировая ткань, скелетная и сердечная мышцы, молочная железа во время лактации. ЛПЛ катализирует гидролиз ТАГ в составе ХМ и ЛПОНП до жирных кислот, моноацилглицеролов (МАГ), в результате ЛПОНП превращаются в кровотоке в ЛППП. Фермент проявляет низкую активность по отношению к МАГи ФЛ.
В жировой ткани синтез ЛПЛ стимулирует инсулин. Тем самым обеспечивается поступление жирных кислот в адипоциты для синтеза и хранения в виде ТАГ. В мышцах ЛПЛ позволяет использовать жирные кислоты для окисления в периоды между приемами пищи, а инсулин подавляет образование этого фермента.
Липопротеины промежуточной плотности (ЛППП). Образование ЛППП происходит из ЛПОНП. Около 75 % ЛППП попадает в печень после связывания апо Е с рецепторами для ЛПНПилирецепторами дляапо В/апо Е.В печени они полностью разрушаются. Около
Липопротеины низкой плотности (ЛПНП). ЛПНП удаляются из кровотока путем взаимодействия с рецепторами для ЛПНП (другое их название апо В/Е рецепторы). Доля этого процесса в удалении всех ЛПНП составляет 75 %. Остальная часть удаляется с помощью «мусорных» рецепторов (скэвенджер (scavenger)-рецепторов), имеющих низкую способность связывания. Этот путь получил образное название «путь уборки мусора».
В отличие от регуляторного действия рецепторов к ЛПНП на обмен холестерола в клетках, скэвенджер-рецепторы продолжают транспортировать ХС в клетку без торможения по принципу обратной связи. Тем самым макрофаги превращаются в пенистые клетки. Их образование рассматривается как начальный этап атеросклероза.
Метаболизм липопротеинов высокой плотности (ЛПВП). ЛПВП синтезируются в клетках печени и кишечника. Сразу после секреции ЛПВП имеют вид плоских дисков, содержащих ФЛ. Белковым компонентом их является апо-А. Из тканей и клеточных мембран на них поступает холестерол. Под действием фермента лецитин-холестерол ацилтрансферазы (ЛХАТ) из неэтерифицированного холестеролаи жирной кислоты фосфатидилхолина образуются ЭХС. В результате частицы ЛПВП созревают, принимая форму глобулы. Затем ЭХС переносятся на ЛППП, ЛПНП, обломки ХМ с помощью липидтранспортирующего белка (ЛПБ) или апо D.