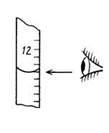
Какое расхождение допускается при титровании параллельных образцов
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
Государственная система обеспечения единства измерений
МЕТОДИКИ ВЫПОЛНЕНИЯ ИЗМЕРЕНИЙ МАССОВОЙ ДОЛИ
ОСНОВНОГО ВЕЩЕСТВА РЕАКТИВОВ И ОСОБО ЧИСТЫХ
ВЕЩЕСТВ ТИТРИМЕТРИЧЕСКИМИ МЕТОДАМИ
State system for ensuring the uniformity of measurements.
Procedures of measurement of mass fraction of the parent substance
of reagents and superpure substances by titrimetric methods.
General requirements
Дата введения 2004-04-01
Сведения о стандарте
1 РАЗРАБОТАН Федеральным государственным унитарным предприятием «Уральский научно-исследовательский институт метрологии» (ФГУП УНИИМ) Госстандарта России
2 ВНЕСЕН Управлением метрологии Госстандарта России
3 ПРИНЯТ И ВВЕДЕН В ДЕЙСТВИЕ Постановлением Госстандарта России от 26 сентября 2003 г. N 273-ст
1 Область применения
2 Нормативные ссылки
В настоящем стандарте использованы ссылки на следующие стандарты:
3 Термины, определения и сокращения
3.1 В настоящем стандарте применен следующий термин с соответствующим определением:
титриметрические методы анализа: Методы количественного химического анализа, основанные на измерениях объема или массы раствора реактива известной концентрации (титранта), расходуемого в процессе стехиометрической реакции с определяемым веществом.
1 В методиках выполнения измерений применяют методы кислотно-основного, окислительно-восстановительного, комплексонометрического и осадительного титрования.
2 В зависимости от способа измерений количества титранта различают гравиметрическое титрование (основано на измерениях массы титранта) и объемное титрование (основано на измерениях объема титранта).
3 Для получения результатов измерений массовой доли основного вещества с наименьшей погрешностью используют гравиметрическое титрование.
4 В зависимости от химического состава и свойств анализируемого реактива при измерениях массовой доли основного вещества реактивов используют методы прямого, обратного, косвенного и реверсивного титрования.
5 Конечную точку титрования находят с помощью соответствующего индикатора или устройства для фиксации.
3.2 В настоящем стандарте применены следующие сокращения:
4 Общие положения
4.1 Разработку, аттестацию и стандартизацию МВИ МДОВ реактива титриметрическим методом проводят в соответствии с требованиями ГОСТ Р 8.563, ГОСТ Р 1.2, ГОСТ Р 1.5 и настоящего стандарта, а также с учетом требований ГОСТ Р ИСО 5725-1-ГОСТ Р ИСО 5725-6.
4.2 Нормативный документ на МВИ МДОВ должен содержать разделы, указанные в приложении В ГОСТ Р 8.563.
4.3 В зависимости от требований к точности измерений МДОВ реактива в качестве титранта используют:
— растворы реактивов, молярная концентрация эквивалента вещества в которых определена с применением ГСО 1-го разряда или ГСО состава.
5 Требования к погрешности измерений и характеристикам составляющих погрешности измерений
Пределы повторяемости и воспроизводимости результатов измерений МВИ определяют экспериментальным путем в соответствии с ГОСТ Р ИСО 5725-2 или [1].
5.2 Характеристику систематической погрешности МВИ, обусловленную несовершенством реализации принятого принципа измерений и погрешностью используемых средств измерений, оценивают с учетом положений ГОСТ Р ИСО 5725-4 и [1]. При определении и расчете систематической погрешности МВИ учитывают неисключенные систематические погрешности, обусловленные погрешностью применяемого ГСО состава; погрешностью реактива, МДОВ которого определена с использованием ГСО 1-го разряда или ГСО состава; погрешностью применяемой мерной лабораторной посуды и весов; погрешностью приготовления индикатора (либо погрешностью устройства фиксации точки конца титрования) и т.д.
5.3 Границы погрешности измерений МВИ устанавливают расчетным путем в соответствии с [1] и ГОСТ 8.207 и указывают для всего диапазона измерений.
ВЫЧИСЛЕНИЯ В ТИТРИМЕТРИЧЕСКОМ АНАЛИЗЕ
При установке титра титранта расчеты производят следующим образом. Если концентрация раствора выражается как молярная концентрация эквивалента (нормальная концентрация), то для расчетов при титровании пользуются формулой:
Где V1, V2 – объемы растворов, мл; N1, N2 – концентрация растворов, н.
Концентрацию подсчитывают с точностью до четвертого десятичного знака.
При выражении точной концентрации титранта часто применяют так называемый поправочный коэффициент К. Это величина, на которую нужно умножить величину предполагаемой концентрации раствора, чтобы получить его точную концентрацию. Например, имеется приблизительно 0,1 н раствор, для которого К=0,945. Следовательно, точное значение концентрации раствора равно 0,1 х 0,0945 н. Величину К находят, разделив определенную титриметрически концентрацию раствора на предполагаемое ее значение:
Где N – определенная концентрация раствора, н; NO – предполагаемая концентрация раствора, н.
Если титрант приготовлен точно заданной концентрации из фиксанала или по точно взятой навеске, К=1.
Пример 2. К приблизительно 0,1 н раствора NaOH, если его определенная титриметрически концентрация 0,0885н., равен:
Концентрация раствора может быть выражена титром, т.е. в граммах вещества на 1 мл раствора:
где Э – эквивалентная масса вещества, г; N – концентрация раствора, н.; g –навеска, г.
В аналитических лабораториях чаще концентрацию титранта выражают через титр по определяемому веществу,т.е. массу (в граммах) определяемого вещества, которой соответствует 1 мл титранта. Для расчета пользуются формулой:
где х – титрант; у – определяемое вещество; Nx— концентрация титранта, н; Эу – эквивалентная масса определяемого вещества, г.
Пример 3. Концентрация раствора АqNO3 равна 0,1020 н., его титр по хлору равен:
Титр рассчитывается до четвертой значащей цифры после запятой.
Пользуясь титром раствора по определяемому веществу, легко вычислить массу определяемого вещества:
Пример 4.Какое количество хлора содержалось в титруемом хлориде, если на титрование затрачено 8,20 мл нитрата серебра?
Для приготовления растворов определенной концентрации навеску рассчитывают по формуле: g = Э x N x V, где
N – требуемая концентрация, н.; Э – эквивалентная масс вещества, г; V – объем приготовляемого раствора, мл.
КОНТРОЛЬНЫЕ ЗАДАНИЯ
1. Что такое титриметрическое определение?
2. Что называется титрованием?
3. Напишите формулу зависимости объемов количественно реагирующих растворов и их концентраций.
4. Перечислите требования, предъявляемые к реакциям, применяемым для титрических определений.
5. Назовите методы титриметрического анализа.
6. Назовите способы титрования.
7. Что такое титрант? Чем измеряют его объем?
8. Что такое установочное вещество? Каковы требования, предъявляемые к установочному веществу?
9. Как приготовить точный раствор по точно взятой навеске?
10. Как приготовить раствор из фиксанала?
11. Что такое точка эквивалентности?
12. Для какой цели при титровании применяются индикаторы?
13. Что такое точка концентитрования?
14. Что такое титрование с применением «свидетеля»?
15. Как подготовить бюретку к титрованию?
16. Какое расхождение допускается при титровании параллельных образцов?
17. Напишите формулу, по которой можно рассчитать титр раствора.
18. Напишите формулу, по которой можно рассчитать титр титранта по определяемому веществу.
19. Напишите формулу для вычисления массы вещества, если известен объем титранта, пошедшего на титрование и, его титр по определяемому веществу.
20. Что такое поправочный коэффициент?
21. На титрование раствора хлорида затрачено 10,53 мл раствора нитрата серебра, ТAqNO3/Cl = 0.003580. Сколько хлора содержалось в растворе?
22. Для определения титра раствора NaOH в качестве установочного вещества взят 0,1 н. Раствор НСl. На титрование 10мл этого раствора пошло 10,55 мл раствора NaOH. Рассчитайте ТNaOH/H2SO4.
23. Приготовлен 0,05 н. Раствор Н2SO4. Точная концентрация этого раствора, определенная объемным путем, 0,0485 н. Рассчитайте К.
24. Чему равна масса железа, если на титрование раствора пошло 10,3 мл раствора KmnO4, a T KmnO4/ Fe = 0.0058 г/мл?
ТЕСТОВЫЙ САМОКОНТРОЛЬ
1. Укажите рабочие раствора (титранты) в методе кислотно-основного титрования: a) NH4OH; b) H2SO4; в) H3BO3; г) NaOH.
3. Укажите, какие массы веществ или объем газа образуют 1 литр 0,1н. раствора:
а) 4,0 г NaOH; б) 2,24 л HCl (н.у.); в) 4,9г H2SO4(fэкв = ½); г)5,6 г КОН?
4. Какие вещества можно определить с помощью кислотно-основного титрования:
5. Какие факторы определяют выбор индикатора при кислотно-основном титровании: а) интервал перехода окраски индикатора; б( зона скачка рН на кривой титрования; в) рН в точке эквивалентности; г). объем титруемого раствора?
6. С какими индикаторами можно титровать раствор аммиака рабочим раствором НNO3: а) бромфеноловый синий (ΔРН = 3,0 – 4,6);б) нейтральный красный (ΔРН =6,8 – 8,0)в) метиловый оранжевый (ΔрН = 3,1 – 4,4);г) фенолфталеин (ΔрН = 8,2 – 10,0)?
7. В водных растворах каких солей лакмус (рТ = 7) окрасится в синий цвет: a) CaCl2; б) Al2(SO4)3; в) NaNO3; г)NaCO3?
8. На титрование 10,0 мл раствора NaOH пошло 12,0 мл 0,1000М раствора НСl. Какие цифры соответствуют составу исследуемого раствора щелочи: а)0,004800 г/мл; б) 7,2 х 10 22 молекул NaOH/k; в) 0,12 моль/л;г) 12 г/л?
9. На титрование 10,0 мл раствора Н3РО4 в присутствии метилоранжа пошло 5,0 мл 0,2М раствора NaOH. Какова масса и количество Н3РО4 в 1 л анализируемого раствора: а) 4,9 г; б) 9,8 г; в) 0,05 моль; г) 0,1 моль?
10. В 1 л воды растворили 22,4 мл газообразного НСl (н.у.). Чему равны рН и рОН полученного раствора: а) рН = 3; б) рН = 1; в) рОН = 11;г) рОН = 13?
К перечню пронумерованных вопросов (фраз) предлагается список ответов, обозначенных буквами. Каждому пронумерованному вопросу соответствует только один ответ. Буквенный ответ может быть использован только один раз, несколько раз или вообще не использован. Необходимо подобрать соответствующие пары «вопрос-ответ».
Чему равен фактор эквивалентности окислителя в превращениях:
Ответы: а) 1|2 ; б) 1/5; в) 1/3; г) 1/6; д)1/4;
Какие исходные вещества используются для стандартизации титрантов:
Какие титранты необходимы для определения следующих веществ методом прямого титрования:
Какие пары титрантов можно использовать для определения следующих веществ методом обратного титрования:
Какой индикатор надо использовать для определения точки эквивалентности при титровании:
18. СР3СООН раствором КОН;
20. Раствора аммиака раствором Н2SO4?
Ответы: a) K2Cr2O7; б) метилоранж (рТ = 4); в) фенолфталеин (рТ = 9); г) крахмал; д) индикатор не нужен.



ГОСУДАРСТВЕННОЕ ПРОФЕССИОНАЛЬНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ТУЛЬСКОЙ ОБЛАСТИ
«ЕФРЕМОВСКИЙ ХИМИКО-ТЕХНОЛОГИЧЕСКИЙ ТЕХНИКУМ»
| Рассмотрено на заседании предметно-цикловой комиссии Протокол №___ от 2020г Председатель ПЦК ____________Л.В.Прасолова | СОГЛАСОВАНО Заместитель директора по УР _______________Е.Е. Саратова «____» _____________ 2020 г. |
ЭКЗАМЕНАЦИОННЫЙ ТЕСТ
ПМ. 01 Подготовка рабочего места, лабораторных условий, средств измерений, испытательного оборудования, проб и растворов к проведению анализа в соответствии с требованиями нормативно-технической документации, требования охраны труда и экологической безопасности
18.01.33 Лаборант по контролю качества сырья, реактивов, промежуточных продуктов, готовой продукции, отходов производства (по отраслям)
Период обучения 2019-2020г.г.
Ефремов 2020 г.
Шкала оценивания вопросов:
1. Что такое титриметрическое определение?
2. Что называется титрованием?
3. Напишите формулу зависимости объемов количественно реагирующих растворов и их нормальных концентраций.
4. Правильное положение глаз при определении объема раствора в бюретке.
1 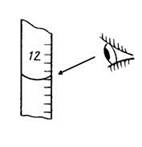
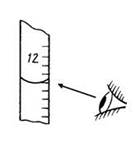
5. Расчеты результатов определений в титриметрии основаны на законе
A. кратных отношений
B. действующих масс
6. Аликвотная часть – это количество.
A. миллилитров добавленного из бюретки раствора
B. капель добавленного из капельницы индикатора
C. миллилитров отобранного пипеткой раствора для анализа
D. миллилитров отобранного мензуркой раствора для анализа
7. Какая мерная посуда применяется при титриметрических определениях?
8. Что такое рабочий раствор?
9. Как выражается концентрация рабочего раствора?
10. Чем измеряют объем рабочего раствора?
11. Как устанавливают точную концентрацию рабочего раствора?
A. вторичный стандарт
C. определяемый раствор
D. первичный стандарт
13. Точка эквивалентности – это…
A. раствор вещества с точно известной концентрацией
B. постепенное смешивание веществ
C. момент, наступающий в ходе титрования, когда реагирующие вещества полностью прореагировали
D. вещество, меняющее окраску в определенных условиях
14. Как приготовить точный раствор по точно взятой навеске?
15. Как приготовить раствор из фиксанала?
16. Что такое точка эквивалентности?
17. Для какой цели при титровании применяются индикаторы?
18. Что такое точка конца титрования?
19. Что такое титрование с применением «свидетеля»?
20. Как подготовить бюретку к титрованию?
21. Расскажите, как выполняется титрование?
22. Что такое поправочный коэффициент?
24. Какое расхождение допускается при титровании параллельных образцов?
25.Формулы, используемые для расчетов в титриметрическом анализе:
26. Напишите формулу, по которой можно рассчитать титр раствора, зная его точную нормальную концентрацию.
27. Напишите формулу, по которой можно рассчитать титр рабочего раствора по определяемому веществу, если известна нормальная концентрация рабочего раствора.
28. Какой формулой рассчитать титр раствора? Что такое титр раствора?
29.Сколько граммов хлорида калия требуется для приготовления раствора массой 600 г с массовой долей 20% КСl?
30.В 500 г воды растворили 20г сульфата калия. Определите массовую долю К2SO4 в растворе.
31.Сколько граммов нитрата натрия потребуется для приготовления 200мл 0,2М раствора?

32. Определите молярность и нормальность серной кислоты в 450 мл которой содержится 10г Н2SO4.
33.Поправочный коэффициент 200мл 0,1 Н раствора натрия гидроксида равен 1,15. Приведите расчет доведения поправочного коэффициента (К) до нормы.
34.2000 мл 0,1 М раствора натрия гидроксида (Mr 40,0) приготовлены из навески массой 8,0 г (m). Поправочный коэффициент полученного раствора равен 0,85 (К). Приведите расчет доведения поправочного коэффициента (К) до нормы.
35.Для приготовления титрованного раствора 0.1 М раствора соляной кислоты в объеме 1000мл взяли кислоту в объеме 9мл. Поправочный коэффициент полученного раствора равен 1,25 (К). Приведите расчет доведения поправочного коэффициента (К) до нормы.
36.Поправочный коэффициент 800мл 0,1 Н раствора натрия гидроксида равен 0,75. Приведите расчет доведения поправочного коэффициента (К) до нормы.
Какое расхождение допускается при титровании параллельных образцов
ГОСТ Р ИСО 5725-2-2002
ГОСУДАРСТВЕННЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
ТОЧНОСТЬ (ПРАВИЛЬНОСТЬ И ПРЕЦИЗИОННОСТЬ) МЕТОДОВ И РЕЗУЛЬТАТОВ ИЗМЕРЕНИЙ
Основной метод определения повторяемости и воспроизводимости стандартного метода измерений
Accuracy (trueness and precision) of measurement methods and results. Part 2. Basic method for the determination of repeatability and reproducibility of a standard measurement method
Дата введения 2002-11-01
Предисловие
1 РАЗРАБОТАН Федеральным государственным унитарным предприятием «Всероссийский научно-исследовательский институт метрологической службы» Госстандарта России (ВНИИМС), Всероссийским научно-исследовательским институтом стандартизации (ВНИИСтандарт), Всероссийским научно-исследовательским институтом классификации, терминологии и информации по стандартизации и качеству (ВНИИКИ) Госстандарта России
ВНЕСЕН Управлением метрологии и Научно-техническим управлением Госстандарта России
3 Настоящий стандарт представляет собой полный аутентичный текст международного стандарта ИСО 5725-1:1994* «Точность (правильность и прецизионность) методов и результатов измерений. Часть 2. Основной метод определения повторяемости и воспроизводимости стандартного метода измерений»
5 ПЕРЕИЗДАНИЕ. Март 2009 г.
* С 1 июля 2007 г. введен в действие ГОСТ Р ИСО/МЭК 17025-2006.
ГОСТ Р ИСО 5725 представляет собой полный аутентичный текст шести частей международного стандарта ИСО 5725, в том числе:
ГОСТ Р ИСО 5725-1-2002 «Точность (правильность и прецизионность) методов и результатов измерений. Часть 1. Основные положения и определения»;
ГОСТ Р ИСО 5725-2-2002 «Точность (правильность и прецизионность) методов и результатов измерений. Часть 2. Основной метод определения повторяемости и воспроизводимости стандартного метода измерений»;
ГОСТ Р ИСО 5725-3-2002 «Точность (правильность и прецизионность) методов и результатов измерений. Часть 3. Промежуточные показатели прецизионности стандартного метода измерений»;
ГОСТ Р ИСО 5725-4-2002 «Точность (правильность и прецизионность) методов и результатов измерений. Часть 4. Основные методы определения правильности стандартного метода измерений»;
ГОСТ Р ИСО 5725-5-2002 «Точность (правильность и прецизионность) методов и результатов измерений. Часть 5. Альтернативные методы определения прецизионности стандартного метода измерений»;
ГОСТ Р ИСО 5725-6-2002 «Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике».
Пользование частями 2-6 ГОСТ Р ИСО 5725 в отдельности возможно только совместно с частью 1 (ГОСТ Р ИСО 5725-1), в которой установлены основные положения и определения, касающиеся всех частей ГОСТ Р ИСО 5725.
В соответствии с основными положениями ИСО 5725-1 (пункт 1.2) настоящий стандарт распространяется на методы измерений непрерывных (в смысле принимаемых значений в измеряемом диапазоне) величин, дающие в качестве результата измерений единственное значение. При этом это единственное значение может быть и результатом расчета, основанного на ряде измерений одной и той же величины.
Применяемый в международных стандартах термин «стандартный метод измерений» адекватен отечественному термину «стандартизованный метод измерений».
В ИСО 5725: 1994-1998 и ИСО/МЭК 17025-99 понятие «метод измерений» («measurement method») включает совокупность операций и правил, выполнение которых обеспечивает получение результатов с известной точностью. Таким образом, понятие «метод измерений» по ИСО 5725 и ИСО/МЭК 17025 адекватно понятию «методика выполнения измерений (МВИ)» по ГОСТ Р 8.563-96 «Государственная система обеспечения единства измерений. Методики выполнения измерений» (пункт 3.1) и соответственно значительно шире по смыслу, чем определение термина «метод измерений» в Рекомендации по межгосударственной стандартизации РМГ 29-99 «Государственная система обеспечения единства измерений. Метрология. Основные термины и определения» (пункт 7.2).
Следует отметить, что в отечественной метрологии точность (accuracy) и погрешность (error) результатов измерений, как правило, определяются сравнением результата измерений с истинным или действительным (условно истинным) значением измеряемой физической величины (являющимися фактически эталонными значениями измеряемых величин, выраженными в узаконенных единицах).
В условиях отсутствия необходимых эталонов, обеспечивающих воспроизведение, хранение и передачу соответствующих значений единиц величин, необходимых для оценки погрешности (точности) результатов измерений, и в отечественной, и в международной практике за действительное значение зачастую принимают общее среднее значение (математическое ожидание) установленной (заданной) совокупности результатов измерений. В ИСО 5725 эта ситуация отражена в термине «принятое опорное значение» (см. пункты 3.5 и 3.6 ГОСТ Р ИСО 5725-1) и рекомендуется ГОСТ Р ИСО 5725-1 для использования в этих случаях и в отечественной практике.
В соответствии с ИСО 5725 цель государственных стандартов ГОСТ Р ИСО 5725 состоит в том, чтобы:
а) изложить основные положения, которые следует иметь в виду при оценке точности (правильности и прецизионности) методов и результатов измерений при их применении, а также при планировании экспериментов по оценке различных показателей точности (ГОСТ Р ИСО 5725-1);
б) регламентировать основной способ экспериментальной оценки повторяемости (сходимости) и воспроизводимости методов и результатов измерений (ГОСТ Р ИСО 5725-2);
в) регламентировать процедуру получения промежуточных показателей прецизионности методов и результатов измерений, изложив условия их применения и методы оценки (ГОСТ Р ИСО 5725-3);
г) регламентировать основные способы определения правильности методов и результатов измерений (ГОСТ Р ИСО 5725-4);
д) регламентировать для применения в определенных обстоятельствах несколько альтернатив основным способам (ГОСТ Р ИСО 5725-2 и ГОСТ Р ИСО 5725-4) определения прецизионности и правильности методов и результатов измерений, приведенных в ГОСТ Р ИСО 5725-5;
е) изложить некоторые практические применения показателей правильности и прецизионности (ГОСТ Р ИСО 5725-6).
Представленные в виде таблицы рекомендации по применению основных положений ГОСТ Р ИСО 5725 в деятельности по метрологии, стандартизации, испытаниям, оценке компетентности испытательных лабораторий со ссылками на нормы государственных стандартов Российской Федерации, содержащих требования к выполнению соответствующих работ, приведены в приложении к предисловию в ГОСТ Р ИСО 5725-1.
Алгоритмы проведения экспериментов по оценке повторяемости, воспроизводимости, промежуточных показателей прецизионности, показателей правильности (характеристик систематической погрешности) методов и результатов измерений рекомендуется внедрять через программы экспериментальных метрологических исследований показателей точности (характеристик погрешности) результатов измерений, выполняемых по разрабатываемой МВИ, и (или) через программы контроля показателей точности применяемых МВИ.
ПРЕДИСЛОВИЕ К МЕЖДУНАРОДНОМУ СТАНДАРТУ ИСО 5725
Международный стандарт ИСО 5725-2 был подготовлен Техническим комитетом ИСО/ТК 69 «Применение статистических методов», Подкомитетом ПК 6 «Методы и результаты измерений».
ИСО 5725 состоит из следующих частей под общим заголовком «Точность (правильность и прецизионность) методов и результатов измерений»:
Часть 1. Основные положения и определения
Часть 2. Основной метод определения повторяемости и воспроизводимости стандартного метода измерений
Часть 3. Промежуточные показатели прецизионности стандартного метода измерений
Часть 4. Основные методы определения правильности стандартного метода измерений
Часть 5. Альтернативные методы определения прецизионности стандартного метода измерений
Часть 6. Использование значений точности на практике
ИСО 5725 (части 1-6) в совокупности аннулирует и заменяет ИСО 5725:1986, область распространения которого была расширена включением правильности (в дополнение к прецизионности) и условий промежуточной прецизионности (в дополнение к условиям повторяемости и воспроизводимости).
ВВЕДЕНИЕ К МЕЖДУНАРОДНОМУ СТАНДАРТУ ИСО 5725
0.2 Общие соображения об этих понятиях представлены в ИСО 5725-1 и поэтому здесь не повторяются. Эта часть ИСО 5725 должна применяться в сочетании с ИСО 5725-1, поскольку в ней даны определения и общие положения.
0.3 Настоящая часть ИСО 5725 касается исключительно оценок, выполняемых с помощью стандартных отклонений повторяемости и воспроизводимости. Несмотря на то, что для оценки прецизионности при определенных обстоятельствах применяют эксперименты и других типов (например, эксперимент с разделенными уровнями), их не рассматривают в настоящей части ИСО 5725, так как они скорее являются предметом ИСО 5725-5. В настоящей части ИСО 5725-2 также не представлены какие-либо другие показатели прецизионности, являющиеся промежуточными между двумя главными показателями: стандартными отклонениями повторяемости и воспроизводимости; промежуточные показатели описаны в ИСО 5725-3.
0.4 При определенных условиях данные, полученные из эксперимента, выполняемого с целью оценки прецизионности, используют также для оценки правильности. Оценку правильности не рассматривают в настоящей части ИСО 5725-2; все аспекты оценки правильности являются предметом ИСО 5725-4.