Сердечно-легочная реанимация (СЛР)
Оказание первой помощи при отсутствии сознания, остановке дыхания и кровообращения
Основные признаки жизни у пострадавшего
К основным признакам жизни относятся наличие сознания, самостоятельное дыхание и кровообращение. Они проверяются в ходе выполнения алгоритма сердечно-легочной реанимации.
Причины нарушения дыхания и кровообращения
Самым распространенным осложнением сердечно-легочной реанимации является перелом костей грудной клетки (преимущественно ребер). Наиболее часто это происходит при избыточной силе давления руками на грудину пострадавшего, неверно определенной точке расположения рук, повышенной хрупкости костей (например, у пострадавших пожилого и старческого возраста).
Избежать или уменьшить частоту этих ошибок и осложнений можно при регулярной и качественной подготовке.
Оцените безопасность для себя, пострадавшего (пострадавших) и окружающих на месте происшествия
На месте происшествия участнику оказания первой помощи следует оценить безопасность для себя, пострадавшего (пострадавших) и окружающих. После этого следует устранить угрожающие факторы или минимизировать риск собственного повреждения, риск для пострадавшего (пострадавших) и окружающих.
Проверьте наличие сознания у пострадавшего
Далее необходимо проверить наличие сознания у пострадавшего. Для проверки сознания необходимо аккуратно потормошить пострадавшего за плечи и громко спросить: «Что с Вами? Нужна ли Вам помощь?». Человек, находящийся в бессознательном состоянии, не сможет отреагировать и ответить на эти вопросы.
Что делать при отсутствии признаков сознания
При отсутствии признаков сознания следует определить наличие дыхания у пострадавшего. Для этого необходимо восстановить проходимость дыхательных путей у пострадавшего: одну руку положить на лоб пострадавшего, двумя пальцами другой взять за подбородок, запрокинуть голову, поднять подбородок и нижнюю челюсть. При подозрении на травму шейного отдела позвоночника запрокидывание следует выполнять максимально аккуратно и щадяще.
Как определить наличие дыхания
Для проверки дыхания следует наклониться щекой и ухом ко рту и носу пострадавшего и в течение 10 сек. попытаться услышать его дыхание, почувствовать выдыхаемый воздух на своей щеке и увидеть движения грудной клетки у пострадавшего. При отсутствии дыхания грудная клетка пострадавшего останется неподвижной, звуков его дыхания не будет слышно, выдыхаемый воздух изо рта и носа не будет ощущаться щекой. Отсутствие дыхания определяет необходимость вызова скорой медицинской помощи и проведения сердечно-легочной реанимации.
Что делать при отсутствии дыхания
При отсутствии дыхания у пострадавшего участнику оказания первой помощи следует организовать вызов скорой медицинской помощи. Для этого надо громко позвать на помощь, обращаясь к конкретному человеку, находящемуся рядом с местом происшествия и дать ему соответствующие указание. Указания следует давать кратко, понятно, информативно: «Человек не дышит. Вызывайте «скорую». Сообщите мне, что вызвали».
Что делать при отсутствии возможности привлечения помощника
При отсутствии возможности привлечения помощника, скорую медицинскую помощь следует вызвать самостоятельно (например, используя функцию громкой связи в телефоне). При вызове необходимо обязательно сообщить диспетчеру следующую информацию: место происшествия, что произошло; число пострадавших и что с ними; какая помощь оказывается. Телефонную трубку положить последним, после ответа диспетчера. Вызов скорой медицинской помощи и других специальных служб производится по телефону 112 (также может осуществляться по телефонам 01, 101; 02, 102; 03, 103 или региональным номерам).
Одновременно с вызовом скорой медицинской помощи необходимо приступить к давлению руками на грудину пострадавшего
Одновременно с вызовом скорой медицинской помощи необходимо приступить к давлению руками на грудину пострадавшего, который должен располагаться лежа на спине на твердой ровной поверхности. При этом основание ладони одной руки участника оказания первой помощи помещается на середину грудной клетки пострадавшего, вторая рука помещается сверху первой, кисти рук берутся в замок, руки выпрямляются в локтевых суставах, плечи участника оказания первой помощи располагаются над пострадавшим так, чтобы давление осуществлялось перпендикулярно плоскости грудины. Давление руками на грудину пострадавшего выполняется весом туловища участника оказания первой помощи на глубину 5-6 см с частотой 100-120 в минуту. После 30 надавливаний руками на грудину пострадавшего необходимо осуществить искусственное дыхание методом «Рот-ко-рту». Для этого следует открыть дыхательные пути пострадавшего (запрокинуть голову, поднять подбородок), зажать его нос двумя пальцами, сделать два вдоха искусственного дыхания.
Вдохи искусственного дыхания выполняются следующим образом:
Необходимо сделать свой нормальный вдох, герметично обхватить своими губами рот пострадавшего и выполнить равномерный выдох в его дыхательные пути в течение 1 секунды, наблюдая за движением его грудной клетки. Ориентиром достаточного объема вдуваемого воздуха и эффективного вдоха искусственного дыхания является начало подъема грудной клетки, определяемое участником оказания первой помощи визуально. После этого, продолжая поддерживать проходимость дыхательных путей, необходимо дать пострадавшему совершить пассивный выдох, после чего повторить вдох искусственного дыхания вышеописанным образом. На 2 вдоха искусственного дыхания должно быть потрачено не более 10 секунд. Не следует делать более двух попыток вдохов искусственного дыхания в перерывах между давлениями руками на грудину пострадавшего. При этом рекомендуется использовать устройство для проведения искусственного дыхания из аптечки или укладки.
Выполнение искусственного дыхания методом «Рот-к-носу»
В случае невозможности выполнения искусственного дыхания методом «Рот-ко-рту» (например, повреждение губ пострадавшего), производится искусственное дыхание методом «Рот-к-носу». При этом техника выполнения отличается тем, что участник оказания первой помощи закрывает рот пострадавшему при запрокидывании головы и обхватывает своими губами нос пострадавшего.
Продолжите реанимационные мероприятия
Далее следует продолжить реанимационные мероприятия, чередуя 30 надавливаний на грудину с 2-мя вдохами искусственного дыхания.
К основным ошибкам при выполнении реанимационных мероприятий относятся:
нарушение последовательности мероприятий сердечно-легочной реанимации; неправильная техника выполнения давления руками на грудину пострадавшего (неправильное расположение рук, недостаточная или избыточная глубина надавливаний, неправильная частота, отсутствие полного поднятия грудной клетки после каждого надавливания); неправильная техника выполнения искусственного дыхания (недостаточное или неправильное открытие дыхательных путей, избыточный или недостаточный объем вдуваемого воздуха); неправильное соотношение надавливаний руками на грудину и вдохов искусственного дыхания; время между надавливаниями руками на грудину пострадавшего превышает 10 сек.
При оказании первой помощи используются простейшие способы проверки наличия или отсутствия признаков жизни:
Показания к прекращению СЛР
Реанимационные мероприятия продолжаются до прибытия скорой медицинской помощи или других специальных служб, сотрудники которых обязаны оказывать первую помощь, и распоряжения сотрудников этих служб о прекращении реанимации, либо до появления явных признаков жизни у пострадавшего (появления самостоятельного дыхания, возникновения кашля, произвольных движений).
В случае длительного проведения реанимационных мероприятий и возникновения физической усталости у участника оказания первой помощи необходимо привлечь помощника к осуществлению этих мероприятий. Большинство современных отечественных и зарубежных рекомендаций по проведению сердечно-легочной реанимации предусматривают смену ее участников примерно каждые 2 минуты, или спустя 5-6 циклов надавливаний и вдохов.
Реанимационные мероприятия могут не осуществляться пострадавшим с явными признаками нежизнеспособности (разложение или травма, несовместимая с жизнью), либо в случаях, когда отсутствие признаков жизни вызвано исходом длительно существующего неизлечимого заболевания (например, онкологического).
Какое оперативное вмешательство приводит к полному прекращению дыхательных движений
12.1. Асфиксия. Определение. Виды
Асфиксия (asphyxia; греческое а- отрицание + phyxis пульс) – это патологическое состояние нарастающего удушья, характеризующееся резким недостатком кислорода и избытком углекислоты в организме.
Асфиксия достаточно часто осложняет различные формы патологии инфекционной и неинфекционной природы. В связи с тем фактом, что запасы кислорода в организме незначительны (2-2,5 литра), этого объема достаточно только для обеспечения жизни человека в течение нескольких минут. В то же время, как известно, за 1 минуту потребляется 6-8 литров воздуха.
В зависимости от причин возникновения и механизмов развития различают внутриутробную, первичную и вторичную асфиксии. К внутриутробным и первичным относятся асфиксии плода и новорожденного. Вторичные асфиксии включают в себя следующие разновидности: механическую асфиксию, асфиксию от недостатка кислорода во вдыхаемом воздухе, асфиксию в результате поражения нервной системы, асфиксию, развивающуюся при длительных спастических состояниях, асфиксию рефлекторной природы, а также вторичную асфиксию новорожденного.
Механическая асфиксия наиболее часто встречается в клинической практике и составляет 28-30% всей насильственной смерти. Ежегодно в России регистрируется 40 000-60 000 случаев смерти от механической асфиксии из них 60% приходится на долю странгуляционной асфиксии и 25% составляет обтурационная асфиксия.
Механическая асфиксия – это вызванное механическими причинами нарушение внешнего дыхания, приводящее к затруднению или полному прекращению поступления в организм кислорода и накоплению в нем углекислоты.
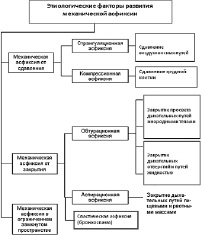
В зависимости от этиологического фактора выделяют следующие виды механической асфиксии (рис. 14):
Рис.14. Инициирующие факторы развития механической асфиксии
Странгуляционная асфиксия, возникает при сдавлении органов дыхания на шее. На фоне нарушения дыхания развивается повышенное внутричерепное давление из-за прекращения оттока крови по сдавленным яремным венам. Хотя сонные артерии также сдавлены, приток крови к головному мозгу осуществляется по позвоночным артериям, идущим через поперечные отростки позвонков. Поэтому цианоз, синюшность лица очень выражены. Следует учитывать, что в ряде случаев сдавления органов дыхания на шее активируются ваго-вагальные рефлексы возникает раздражение верхнее-гортанного и языкоглоточного нервов, а также симпатического ствола, что приводит к рефлекторной остановке сердца и дыхания.
Компрессионная асфиксия, возникающая от сдавления груди и живота. Сильное сдавление легких сопровождается резким ограничением дыхания. Одновременно сдавливается верхняя полая вена, осуществляющая отток крови от головы, шеи, верхних конечностей. Происходит резкое повышение давления и застой крови в венах головы и шеи. При этом возможны разрывы капилляров и мелких вен кожи, что обусловливает появление многочисленных точечных кровоизлияний. Лицо пострадавшего одутловатое, кожа лица и верхних отделов груди багровая, темно-фиолетовая, в тяжелых случаях почти черная (экхимотическая маска). Эта окраска имеет относительно четкую границу в верхней части туловища. В местах плотного прилегания одежды на шее и надключичных областях остаются полосы нормально окрашенной кожи. На коже груди и живота отмечаются полосовидные кровоизлияния в виде рельефа одежды, а также частицы материала, которым было сдавлено туловище.
Обтурационная (аспирационная) асфиксия, возникающая при попадании твердых или жидких веществ в дыхательные пути и их закупоривании. Закрытие просвета дыхательных путей имеет свои особенности, зависящие от свойств, размеров и положения инородного тела. Чаще всего твердые предметы закрывают просвет гортани, голосовую щель. При полном закрытии просвета выявляются признаки типичного развития асфиксии. Если размеры предмета небольшие, то нет полного перекрытия просвета дыхательных путей. При этом развивается быстрый отек слизистой гортани, являющийся вторичной причиной закрытия дыхательных путей. В ряде случаев небольшие предметы, раздражая слизистую гортани и трахеи, могут вызвать отек слизистой, рефлекторный спазм голосовой щели или рефлекторную остановку сердца. В последнем случае асфиксия не успевает полностью развиться, что будет констатироваться отсутствием ряда типичных признаков асфиксии. Таким образом, обнаружение инородного предмета в дыхательных путях является ведущим доказательством причины смерти.
Асфиксия в замкнутом и полузамкнутом пространстве. Этот тот вид механической асфиксии развивается в пространствах с полным или частичным отсутствием вентиляции, где происходит постепенное накопление углекислого газа и уменьшение кислорода. Патогенез данного состояния характеризуется сочетанием гиперкапнии, гипоксии, гипоксемии. Биологическая активность углекислого газа выше, чем кислорода. Повышение концентрации углекислоты до 3–5 % вызывает раздражение слизистых оболочек дыхательных путей и резкое учащение дыхания. Дальнейшее повышение концентрации углекислого газа до 8– 10 % приводит к развитию типичной асфиксии, без развития специфических морфологических изменений.
Независимо от особенностей патогенных факторов, инициирующих механическую асфиксию, различают следующие периоды ее развития.
Предасфиктический – длится до 1 мин, характеризуется наличием тахи- и гиперпноэ, гиперкапнии. В случаях, если препятствие не устранено, развивается следующий период.
Асфиктический – условно делится на несколько стадий, которые могут длиться от 1 до 3–5 мин:
1) стадия инспираторной одышки – характеризуется усиленными, следующими друг за другом вдыхательными движениями, активацией рефлекса Геринга-Брейера за счет возбуждения МАР рецепторов альвеол. В результате легкие сильно расширяются, возможны разрывы легочной ткани. Одновременно усиливается приток крови к легким, переполнение их кровью, образование кровоизлияний. Далее переполняется кровью правый желудочек и правое предсердие сердца, и развивается системная венозная гиперемия. Внешние проявления – синюшность кожи лица, мышечная слабость. Сознание сохраняется только в начале стадии;
2) стадия экспираторной одышки – усиленный выдох при участии рефлекса Геринга-Брейера происходит подавление активности бульбарных инспираторных нейронов и активация экспираторных нейронов, наблюдается уменьшение объема грудной клетки, возбуждение мускулатуры, непроизвольная дефекация, мочеиспускание, семяизвержение, повышение артериального давления, возникновение кровоизлияний. При двигательной активности возможно образование повреждений об окружающие предметы;
3) кратковременная остановка дыхания (обратимое апноэ на фазе экспирации) – отмечается падение артериального и венозного давления, расслабление мускулатуры;
4) терминальная стадия свидетельствует о гибели нейронов дыхательного центра, характеризуется терминальным дыханием Куссмауля, апнейстическим или гаспинг-дыханием.
5) стойкая остановка дыхания наступает вследствие паралича дыхательного центра.
Общая продолжительность асфиксии (от ее начала до наступления смерти) также может колебаться в довольно широких пределах. При внезапном полном прекращении легочной вентиляции длительность асфиксии составляет не более 5—7 минут. В случаях постепенно развивающейся асфиксии (например, при дыхании в замкнутом пространстве или при неврологических заболеваниях) продолжительность асфиксии может быть значительно большей.
Имеются существенные возрастные различия чувствительности к асфиксии. Чем моложе животное, тем оно легче переносит асфиксию. Так, крысенок в возрасте 12 — 15 часов живет без доступа воздуха до 30 минут, шестидневный — около 15 минут, двадцатидневный — около 2 минут; взрослый человек — 3—6 минут, тогда как новорожденный — 10—15 минут.
Клиническая картина асфиксии зависит от степени гипоксии и гиперкапнии. Выделяют легкую, средней тяжести и тяжелую формы.
Асфиксия от недостатка кислорода во вдыхаемом воздухе может наблюдаться при высотной болезни, в специфических производственных условиях, связанных с пребыванием в замкнутых системах с принудительной подачей газовой смеси в тех случаях, когда нарушается подача кислорода и поглощение углекислого газа; асфиксия возникает при пребывании в изолированном замкнутом пространстве, когда происходит постепенное падение содержания кислорода в воздухе и прогрессирующее нарастание концентрации углекислого газа. Характерные для асфиксии расстройства жизнедеятельности развиваются в таких случаях вначале на фоне нормальной или даже увеличенной легочной вентиляции. В дальнейшем деятельность дыхательного центра нарушается, объем вентиляции падает, и асфиксия приобретает обычное течение.
Асфиксия в результате поражения нервной системы обусловлена расстройствами вентиляции при параличах дыхательной мускулатуры. Последние, как известно, могут быть центральными или периферическими, возникать при поражении двигательной зоны КГМ, пирамидных трактов, при параличах дыхательной мускулатуры возникающих в результате нарушений проводимости нервно-мышечных синапсов (отравление курареподобными средствами, действие бактериальных токсинов, отравляющих веществ), множественных невритов, распространенного поражения мотонейронов спинного мозга в шейных и грудных сегментах при травмах, полиомиелите и других инфекционных и неинфекционных заболеваниях.
Одной из частых причин асфиксии являются грубые расстройства деятельности дыхательного центра, возникающие в результате его органических поражений различного характера, а также при интоксикациях, передозировке снотворных и наркотических средств и при гипоксии бульбарных структур, сопровождающейся энергетическим истощением нейронов дыхательного центра и ослаблением или полным прекращением их функции.
Асфиксия как следствие длительных спастических состояний, например при столбняке, отравлении стрихнином и другими ядами, вызывающими, судороги.
Рефлексогенная асфиксия. Наблюдается при раздражении рецепторов трахеи и бронхов различными газо- и парообразными химическими соединениями, дымом, частицами пыли, патологическим процессом (воспаление, опухоль), локализованным в легочной ткани или дыхательных путях. Возникающие при этом рефлекторные влияния на дыхательный центр дезорганизуют акт дыхания.
Асфиксия возникает и в тех случаях, когда дыхательные экскурсии вызывают стойкое болевое ощущение (при переломах ребер, патологических процессах в плевральной полости, межреберной невралгии).
12.2. Асфиксия плода и новорожденного является одной из наиболее распространённых патологий в родах является, которая может быть: внутриутробной (возникает во внутриутробный период); первичной (возникает в момент рождения, у 5-7% новорожденных ); вторичной (развивается в первые сутки жизни младенца).
В основе внутриутробной формы асфиксии лежит кислородное голодание плода. Причинами ее могут быть: нарушения маточно-плацентарного кровообращения (токсикоз беременных, патология плаценты), заболевания матери, сопровождающиеся кислородным голоданием (сердечно-сосудистая и легочная патология, острая кровопотеря, шок), сдавление пуповины, длительный безводный период, затяжные и патологические роды. В результате наступившего кислородного голодания в крови плода накапливается избыточное количество углекислоты. Это приводит к возбуждению дыхательного центра, появлению преждевременных дыхательных движений, аспирации плодом околоплодной жидкости с последующей закупоркой дыхательных путей.
При длительном кислородном голодании в организме плода возникают глубокие метаболические, структурные и функциональные нарушения органов и систем: развивается ацидоз, появляются тяжелые расстройства кровообращения, кровоизлияния в мозг, легкие и другие органы. Первоначальное возбуждение дыхательного центра сменяется его параличом. В центральной нервной системе наступают необратимые изменения.
Нарушение сердечной деятельности плода проявляется в виде тахикардии или брадикардии, аритмии, глухости тонов. Поведение плода становится беспокойным, происходит расслабление сфинктера заднего прохода и околоплодные воды окрашиваются меконием. По мере нарастания асфиксии тоны сердца становятся редкими и глухими. Движения плода замедляются и затем полностью прекращаются. Исходом внутриутробной асфиксии может быть гибель плода до родов, во время родов или рождение ребенка в состоянии асфиксии.
Факторами риска развития первичной асфиксии являются внутриутробная гипоксия (острая или хроническая); внутричерепная родовая травма ребенка; иммунологическая несовместимость матери и плода; полная или частичная закупорка дыхательных путей ребенка околоплодными водами или слизью; экстрагенитальные заболевания матери во время беременности; патологическое течение беременности;аномалии родовой деятельности (патологически узкий таз матери, неправильное врезание головки плода, в некоторых случаях обвитие пуповиной).
Среди причин вторичной асфиксии выделяют: врожденную пневмонию у ребенка; нарушение мозгового кровообращения; попадание в дыхательные пути рвотных масс; нарушение работы центральной нервной системы малыша.
Какое оперативное вмешательство приводит к полному прекращению дыхательных движений
Послеоперационное угнетение дыхания: физиологические механизмы и методы коррекции.
Физиологические механизмы послеоперационного угнетения дыхания
Центральное угнетение дыхания (ЦУД)
В дисфункции дыхательных мышц играют роль не только центральные депрессанты и миорелаксанты, но и некоторые другие вводимые на их фоне препараты (напр. лазикс), физиологическое состояние организма (ацидоз, гипокалиемия), а также направление и длина хирургического разреза.
Независимо от механизма развития, основным физиологическим следствием ЦУД является нарушение адекватной альвеолярной вентиляции, гипоксемия и респираторный ацидоз. Ухудшаются вентиляционно-перфузионные отношения, увеличивается доля мертвого пространства в дыхательном объеме. Все это приводит к нарастанию артериальной гипоксемии и гиперкапнии. Компенсаторные возможности организма в этот период ограничены, поэтому изменения газового состава крови наступают быстро и в скором времени влекут за собой угрожающие расстройства гемодинамики и сердечного ритма.
Следовательно, у всех больных с ЦУД в ближайшем послеоперационном периоде необходимо проведение искусственной или вспомогательной вентиляции легких при тщательном мониторинге показателей вентиляции и гемодинамики в специально оборудованной восстановительной палате в составе операционного блока, если характер операции и состояние больного не требуют более длительного его нахождения в отделении интенсивной терапии. Время, в течение которого у больного происходит восстановление самостоятельного дыхания и сознания, зависит от его исходного состояния, глубины наркоза, фармакокинетики введенных препаратов и их взаимодействия и может занимать от нескольких минут до нескольких часов.
В последнее время в клиническую практику широко входят различные препараты, ослабляющие или полностью блокирующие действие наркотических аналгетиков (налоксон), транквилизаторов (флумазенил) и миорелаксантов (прозерин). Они позволяют в короткие сроки восстановить сознание и дыхание больного и экстубировать его.
Давно известна способность антихолинэстеразных препаратов восстанавливать проводимость в нервно-мышечном синапсе во время пролонгированной миоплегии, обусловленной остаточным действием недеполяризующих миорелаксантов. После их применения на это может понадобиться до 20-30 минут, в зависимости от глубины миоплегии, уровня метаболизма, температуры тела и др. Следует помнить, что антихолинэстеразные препараты способны спровоцировать бронхиолоспазм, вызвать опасные нарушения сердечного ритма, и эти эффекты далеко не всегда поддаются терапии холиноблокаторами.
Для купирования действия наркотических аналгетиков применяются специфические антагонисты опиоидных рецепторов налоксон и налтрексон. Действуя с одинаковой силой на все опиоидные рецепторы, налоксон не только устраняет наркотическую депрессию дыхания, но и полностью купирует аналгезию. Это может повлечь за собой мощную реакцию на болевой синдром, спровоцировать нарушения кровообращения и дыхания, вылечить которые уже гораздо сложнее. Кроме того, из-за относительно непродолжительного действия налоксона возможен эффект ренаркотизации.
Учитывая эти факторы, мы в большинстве случаев являемся сторонниками плавного выхода из наркоза, как наиболее безопасного пути для пациента и лечащего врача.
В последнее время, однако, отмечается неуклонный рост хирургической активности, появление разнообразных эндоскопических операций, а также расширение показаний для диагностических и лечебных манипуляций, выполняемых в стационаре или амбулаторно под наркозом или седатацией. Длительное наблюдение таких больных в послеоперационном периоде при большом их потоке сковывает значительные силы персонала и материальных средств, не только увеличивая стоимость лечения больного, но и повышая вероятность ошибки врачей и сестер. После многих из них быстрое восстановление сознания и дыхания весьма желательно и достаточно безопасно при соблюдении необходимых условий.
Клиническая фармакология флумазенила
Более 10 лет в медицинской практике используется пока единственный в своем роде антагонист бензодиазепиновых рецепторов флумазенил.
Флумазенил был синтезирован в 1979 году. В клинике применяется с 1986 года. В настоящее время выпускается под названиями Anexate, Lanexate, Romazicon. В 1988 году фармацевтическая фирма Hoffmann-LaRoche за внедрение препарата анексат была удостоена престижной международной премии в области фармакологии и биотехнологии Prix Galion.
Флумазенил представляет собой водорастворимое соединение имидазобензодиазепин, которое имеет высокую степень сродства к ГАМКА- эргическим рецепторам головного мозга. Механизм его действия прямо противоположен действию всех известных бензодиазепинов и превосходит их по силе. Флумазенил оказывает тормозящее влияние на проникновение ионов хлора в нейроны и, как следствие, устраняет практически все центральные эффекты бензодиазепинов (диазепам, мидазолам и др.), что, правда, зависит от введенной дозы препарата. Например, для снятия гипнотического эффекта атарактиков требуются меньшие дозы флумазенила (0,25-0,6 мг), чем для полного устранения их анксиолитического, противосудорожного и амнестического действия ( до 15 мг).
При внутривенном введении флумазенила эффект развивается через 1 минуту с пиком действия через 6-10 мин и продолжается в течение 30-40 мин. Период полувыведения из организма составляет около 60 мин. Препарат связывается с белками плазмы на 50%, практически полностью разрушается в печени. Почечный клиренс, а также пол и возраст больного не имеют значения в его метаболизме.
Вводится флумазенил внутривенно, обычно дробно по 0,25-0,3 мг в течение
10-15 сек. Эти дозы повторяют через 30-60 секунд до получения желаемого эффекта. В отдельных случаях флумазенил можно вводить капельно в виде инфузии. Флумазенил мало- или практически нетоксичен, его побочные эффекты главным образом связаны с устранением действия бензодиазепинов. Описанный эффект реседации обычно спустя час после введения флумазенила скорее наблюдается при мощной передозировке бензодиазепинов, что возможно в практике интенсивной терапии (лечение отравлений, длительная седатация больных) и менее вероятно в анестезиологии. Резкое устранение влияния атарактиков может повлечь за собой снятие их анксиолитического действия, усиленный выброс катехоламинов, рост артериального давления и нарушения сердечного ритма.
Флумазенил способен провоцировать судорожные припадки у эпилептиков, получавших диазепам, и вызывать рост внутричерепного давления у больных с патологией ЦНС.
Последние годы ведутся тщательные исследования эффективности этого препарата у больных с различными патологиями. В интенсивной терапии отмечается (правда, далеко не всеми) его положительный эффект у больных в печеночной и алкогольной коме.
Наибольшее распространение флумазенил получил в анестезиологической практике. Продолжается изучение его действия после различных комбинаций с другими препаратами для внутривенной анестезии, у разных категорий больных после больших и малых оперативных и диагностических вмешательств.
В нашем отделении выполнено исследований препарата анексат у больных в возрасте от до после лапароскопической холецистэктомии, проведенной под атарал- или нейролептаналгезией. Отобранные для исследования пациенты не страдали сопутствующей или предшествующей патологией дыхания. Перед операцией у всех больных было получено информированное согласие на введение им анексата в посленаркозном периоде.
Грубая оценка характера дыхательных расстройств при поступлении больного в палату включала наблюдение за дыхательными экскурсиями грудной клетки и живота, аускультацию, оценку уровня сознания и мышечного тонуса. Более точная дифференцировка производилась с помощью измерения нейрореспираторного драйва, показателей механики дыхания и газового состава выдыхаемого воздуха. Регистрировались также частота сердечных сокращений (ЧСС) и артериальное давление (АД).
Исследование функции внешнего дыхания и определение степени и вида посленаркозной депрессии проводились на легочном компьютере UTS фирмы «Jeger» и мониторе Capnomac Ultima фирмы «Datex». Все исследуемые больные в послеоперационном периоде находились на принудительной вентиляции (в случае апноэ) и вспомогательной вентиляции поддержкой давлением (ВПД) (в случае гиповентиляции) с помощью аппарата Puritan-Bennett 7200ае.
ВПД является относительно новым и модным режимом вспомогательной вентиляции. В этом режиме аппарат помогает каждому вдоху пациента, доводя давление в его дыхательных путях до установленного врачом уровня и дополняя дыхательный объем. При этом почти все компоненты дыхательного паттерна и минутная вентиляция остаются под контролем больного, если у последнего сохранен нейрореспираторный драйв, достаточный для включения триггерной системы аппарата ИВЛ.
Мы подбирали давление поддержки в соответствии с дыхательным объемом и частотой дыхания под контролем концентрации углекислого газа в конечной порции выдыхаемого газа. Практически ни в одном случае оно не превышало 15 см Н2О. Чувствительность триггера во всех исследованиях устанавливалась 0,5 см Н2О. Экстубация производилась при поддержке 8-10 см Н2О, если больной был в сознании, его дыхательный объем составлял не менее 5-8 мл/кг, окклюзионное давление в трахее в первые 100 миллисекунд вдоха (Р100 ) было не менее 2,5 см Н2О, сатурация оксигемоглобина (SpO2) не менее 90%, а частота дыханий не меньше 12 и не больше 30 в минуту. В ходе исследования регистрировались также капнографическая кривая, отношение времени вдоха и выдоха (I:E), разница вдыхаемого и выдыхаемого газа по кислороду, аэродинамическое сопротивление дыхательных путей.
У больных с преимущественно центральной депрессией дыхания и низкой минутной вентиляцией нейрореспираторный драйв, частота дыханий и дыхательный объем были снижены или не определялись. Больные с периферическими расстройствами дыхания имели высокую частоту дыханий при малом дыхательном объеме, большое отношение времени вдоха к общей продолжительности дыхательного цикла и значительную разницу по кислороду во вдыхаемой и выдыхаемой смеси. Нейрореспираторный драйв у них был повышен.