Так ли безопасны препараты для лечения доброкачественной гиперплазии предстательной железы?
В декабре 2015 года в Journal of Urology были опубликованы результаты нового исследования, в котором изучалась безопасность новых препаратов для лечения доброкачественной гиперплазии предстательной железы (ДГПЖ): доксазозина, финастерида и их комбинации. Шестью самыми частными побочными эффектами при их применении являлись: головокружение, ортостатическая гипотензия, слабость, импотенция, снижение либидо и нарушение эякуляции.
В исследование были рандомизированы 3047 мужчин с ДГПЖ в возрасте 50 лет и старше, которые получали плацебо, доксазозин (4-8 мг), финастерид (5 мг) или комбинацию доксазозин + финастерид. Период наблюдения за пациентами составил в среднем 4,5 лет. Сравнение частоты развития побочных эффектов проводилось с плацебо.
Анализ первого года терапии показал, что риск развития головокружения был значительно выше на фоне применения доксазозина (в 2,2 раза; p
Всероссийская Образовательная Интернет-Сессия
Информация и материалы, представленные на настоящем сайте, носят научный, справочно-информационный и аналитический характер, предназначены исключительно для специалистов здравоохранения, не направлены на продвижение товаров на рынке и не могут быть использованы в качестве советов или рекомендаций пациенту к применению лекарственных средств и методов лечения без консультации с лечащим врачом.
Лекарственные препараты, информация о которых содержится на настоящем сайте, имеют противопоказания, перед их применением необходимо ознакомиться с инструкцией и проконсультироваться со специалистом.
Мнение Администрации может не совпадать с мнением авторов и лекторов. Администрация не дает каких-либо гарантий в отношении cайта и его cодержимого, в том числе, без ограничения, в отношении научной ценности, актуальности, точности, полноты, достоверности научных данных представляемых лекторами или соответствия содержимого международным стандартам надлежащей клинической практики и/или медицины основанной на доказательствах. Сайт не несет никакой ответственности за любые рекомендации или мнения, которые могут содержаться, ни за применимость материалов сайта к конкретным клиническим ситуациям. Вся научная информация предоставляется в исходном виде, без гарантий полноты или своевременности. Администрация прикладывает все усилия, чтобы обеспечить пользователей точной и достоверной информацией, но в то же время не исключает возможности возникновения ошибок.
Современные возможности медикаментозного лечения доброкачественной гиперплазии ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ
К числу наиболее распространенных урологических заболеваний у пациентов пожилого возраста относится доброкачественная гиперплазия предстательной железы (ДГПЖ) [2].
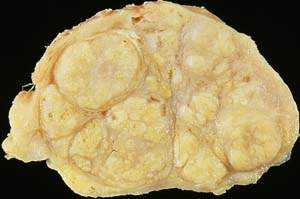 |
| Рисунок 1. Доброкачественная гиперплазия предстательной железы (макропрепарат) |
К числу наиболее распространенных урологических заболеваний у пациентов пожилого возраста относится доброкачественная гиперплазия предстательной железы (ДГПЖ) [2]. Около 80% мужчин старше 80 лет страдают этим заболеванием. Другая статистика свидетельствует, что из всех заболеваний, которым подвержены мужчины старше 50 лет, на долю доброкачественной гиперплазии простаты приходится 36% [1]. Эти сведения настолько общеизвестны, что ухудшение качества мочеиспускания часто рассматривается как естественное явление.
Клинически данное заболевание проявляется различными симптомами, связанными с нарушением пассажа мочи по нижним мочевым путям. При значительно выраженной инфравезикальной обструкции, как правило, прибегают к хирургическому вмешательству. Оперативное лечение по поводу ДГПЖ показано 30% больных в возрасте от 50 до 80 лет [4]. Однако в последние годы все большую популярность завоевывает медикаментозная терапия доброкачественной гиперплазии предстательной железы. Это, с одной стороны, объясняется вполне логичным желанием врача и пациента по возможности избежать операции, с другой — развитием представлений о патогенезе расстройств мочеиспускания при доброкачественной гиперплазии предстательной железы.
До недавнего времени патогенез расстройств мочеиспускания при доброкачественной гиперплазии предстательной железы рассматривали с позиции классических представлений о механической инфравезикальной обструкции и развитии вторичных структурно-функциональных изменений детрузора (компенсация, декомпенсация). За последние два десятилетия получены принципиально новые данные о природе повышенного внутриуретрального сопротивления. Его перестали отождествлять исключительно с механическим сдавлением шейки мочевого пузыря и задней уретры. Обнаружен динамический компонент обструкции, который состоит в повышении тонуса указанных анатомических структур за счет активности a-адренорецепторов. Появились также иные трактовки происхождения ирритативных симптомов. Их считают проявлением первичного нестабильного мочевого пузыря и не связывают напрямую с обструкцией [5].
Результаты нашей работы свидетельствуют, что при ДГПЖ клиническая симптоматика развивается вследствие недостаточности энергетического метаболизма и гипоксии детрузора в условиях повышенного уретрального сопротивления [3]. Об этом свидетельствуют:
Причины нарушений энергетического метаболизма и функций детрузора крайне многообразны. В частности, к таким нарушениям могут привести повышение активности симпатической нервной системы, расстройства органного кровообращения, авитаминоз (группа В), хронические заболевания дыхательной и сердечно-сосудистой систем, влияние приема ряда фармакологических препаратов, угнетающих дыхательную цепь, и, естественно, обструктивные нарушения уродинамики и т. д. Весьма важно, что нарушения гипоксического характера в гладкомышечной ткани могут иметь и первичный митохондриальный генез (первичные нарушения энергетического метаболизма детрузора [3].
Необходимо отметить, что у больных ДГПЖ в нижнем отделе мочевого тракта протекают два параллельных процесса — формирование уретральной обструкции и нарушение энергетического метаболизма детрузора (митохондриальная недостаточность).
Подобное представление патогенеза расстройств мочеиспускания открывает широкие возможности для фармакотерапии. Сокращения и расслабления детрузора можно достичь с помощью средств метаболической терапии, прямого улучшения снабжения детрузора кислородом и т. д. Наиболее значимые расстройства основных функций мочевого пузыря все же опосредованы расстройствами кровообращения. И если процесс обратим, то до или после хирургического вмешательства можно существенно влиять на функциональное состояние мочевого пузыря с помощью вазоактивных препаратов, к которым в первую очередь относятся a1-адреноблокаторы.
При определении критериев отбора пациентов для медикаментозной терапии ДГПЖ мы воспользовались рекомендациями IV Международного консультативного комитета по ДГПЖ.
Основу настоящего исследования составили собственные клинические наблюдения за 1724 пациентами (средний возраст 61,4 года), страдающими ДГПЖ и получавшими различные варианты медикаментозного лечения. Нами применялись препараты всех групп, использующихся в настоящее время для лечения ДГПЖ: a-адреноблокаторы, блокаторы 5-a-редуктазы, препараты растительного происхождения и их комбинации. Схемы проведенного лечения и характеристика групп пациентов приведены в табл. 1.
Из наиболее многочисленной и популярной сегодня группы препаратов для медикаментозного лечения ДГПЖ — селективных a-адреноблокаторов мы использовали альфузозин, теразозин, доксазозин и тамсулозин. Общее число пациентов, получавших a-адреноблокаторы, составило 1408. Финастерид был взят нами как классический представитель блокаторов 5-a-редуктазы. Из препаратов растительного происхождения мы использовали пермиксон и таденан.
В пяти группах общей численностью 1305 человек проводилась терапия селективными a-адреноблокаторами в течение длительного периода времени по стандартным схемам и в стандартных дозах. Результаты лечения приведены в табл. 2.
Улучшение качества мочеиспускания отметили в среднем 86,74% пациентов. Суммарный балл I-PSS сократился на 38,68% к окончанию первого года лечения и на 43,4% к окончанию курса терапии. Балл QOL уменьшился на 29,04% и 35,58% соответственно. Максимальная скорость потока мочи увеличилась на 45,25% к окончанию первого года лечения и стабилизировалась на достигнутом уровне. Количество остаточной мочи сократилось в среднем на 57,6%. Процент пациентов, по тем или иным причинам выбывших из исследования, был тождествен во всех группах и равнялся 14,38%.
Особо следует остановиться на препарате тамсулозин (омник, Yamanouchi) — пока единственном простатселективном a1А-адреноблокаторе на отечественном рынке. Этот препарат обладает рядом свойств, которые позволяют его использовать в различных функциональных тестах. Прежде всего это возможность назначения единой терапевтической дозы (один раз в сутки по 0,4 мг). А отсутствие выраженного влияния на артериальное давление и сердечную деятельность избавляет от необходимости титрования дозы. Мы согласны с рядом авторов, которые считают возможным применение коротких курсов терапии тамсулозином в качестве прогностических тестов эффективности лечения a1-адреноблокаторами, что может иметь решающее значение при выборе того или иного метода медикаментозного лечения ДГПЖ [4].
Части больных (группа А5) проведена проверка возможности разрешения острой задержки мочеиспускания (ОЗМ) приемом альфузозина по 5 мг два раза в сутки. Эта терапия проводилась пациентам с впервые возникшей ОЗМ и отсутствием симптомов нарушения мочеиспускания в анамнезе. Положительный эффект был достигнут у 8 из 14 пациентов (57,1%), которым параллельно приему альфузозина производилось кратковременное (трое суток) дренирование мочевого пузыря катетером. Единовременный прием суточной дозы альфузозина (10 мг) способствовал восстановлению самостоятельного мочеиспускания лишь у одного из четырех пациентов, которым проводилась подобная терапия. Вероятно, это объясняется гипотонией детрузора, усугубляющейся в ситуации длительного перерастяжения мочевого пузыря на фоне задержки мочеиспускания.
Для изучения эффективности и безопасности комбинированной медикаментозной терапии ДГПЖ препаратами разных групп, а также для уточнения целесообразности проведения терапии нами были созданы три группы.
В первой группе (К1) пациенты получали проскар по 5 мг/сут. параллельно с приемом теразозина по 5-10 мг/сут. Обращало на себя внимание значительное повышение показателей максимальной скорости потока мочи (+40%), характерное для группы монотерапии a-адреноблокаторами, и постепенное, на протяжении курса лечения, снижение объема предстательной железы (-20,4%), характерное для группы монотерапии финастеридом. Очевидно, что положительные изменения показателей мочеиспускания в этой группе являются следствием воздействия обоих препаратов. Тем не менее процент выбывших пациентов в этой группе был крайне высоким — 32,3%. Основной причиной прекращения комбинированной терапии ДГПЖ пациенты называли неприемлемо высокую стоимость лечения.
В третьей группе комбинированной терапии (К3) лечение проводилось финастеридом по 5 мг/сут. в сочетании с пермиксоном по 160 мг два раза в сутки. Через два года после начала лечения 50% пациентов покинули группу, приводя причиной отказа от дальнейшей терапии высокую стоимость лечения при отсутствии быстрого улучшения качества мочеиспускания. При сравнении полученных данных с результатами в других группах очевидно, что эффективность лечения в третьей существенно ниже.
Таким образом, эффективность медикаментозной терапии больных ДГПЖ при соблюдении показаний и противопоказаний к ее назначению, правильном выборе препарата и схемы его назначения высока и достигает в среднем 80,2%. При этом эффективность монотерапии a-адреноблокаторами составляет 86,7%, блокаторами 5a-редуктазы — 69,4%, препаратами растительного происхождения — 69,3% и при комбинированной терапии — 95,45%. Комбинированная медикаментозная терапия a-адреноблокаторами в сочетании с блокаторами 5a-редуктазы эффективнее монотерапии этими препаратами. С целью снижения стоимости лечения возможен переход на монотерапию блокаторами 5a-редуктазы после достижения выраженного регресса обструктивной симптоматики. Медикаментозная терапия a-адреноблокаторами является эффективным способом консервативного лечения острой задержки мочеиспускания. Терапия должна проводиться на фоне кратковременного (трое суток) дренирования мочевого пузыря уретральным катетером.
Литература
1. Гориловский Л. М. Эпидемиология и факторы риска развития доброкачественной гиперплазии предстательной железы. В кн.: Доброкачественная гиперплазия предстательной железы / Под ред. Н. А. Лопаткина. М., 1997, с. 10-18.
2. Лопаткин Н. А., Перепанова Т. С. Клинический опыт лечения больных доброкачественной гиперплазией предстательной железы a1-адреноблокатором альфузозином // Урол. и нефрол., 1997, № 5, с. 14-17.
3. Лоран О. Б., Вишневский Е. Л., Вишневский А. Е. Лечение расстройств мочеиспускания у больных доброкачественной гиперплазией простаты a-адреноблокаторами. Монография. М., 1998.
4. Сивков А. В. Медикаментозная терапия доброкачественной гиперплазии предстательной железы. В кн.: Доброкачественная гиперплазия предстательной железы / Под ред. Н. А. Лопаткина. М., 1997, с. 67-83.
5. McConnell J. D. Prostatic growth: new insights into hormonal regulation // Br. J. Urol. 1995. Vol.76.(suppl.1). P. 5-10.
Комбинированная терапия доброкачественной гиперплазии предстательной железы: преимущества и недостатки
Раньше пациенты, не отвечающие на андрогендепривационную терапию (АДТ), считались безнадежными: до 2004 г. онкологи не могли предложить ничего, кроме паллиативной помощи митоксантроном. Сейчас, манипулируя гормонами, можно отсрочить использование цитостатиков даже в отношении мужчин с метастатическим раком предстательной железы (РПЖ), который уже не отвечает на гормо нальную терапию и даже доцетаксел… Противоречие? Нет! Просто изменилось представление о гормональной независимости опухоли, и появились препараты, подавляющие синтез тестостерона даже в клетках самой опухоли.
Рак простаты: истинно гормонозависимая опухоль
 |
| Автор | Дизайн | Число пациентов | Длительность лечения | Контрольная/экспери ментальная группа | Первичные критерии оценки эффективности лечения | Побочные эффекты |
| H. Lepor (VA study), 1996 | RCT | 1007 | 12 мес | теразозин/финастерид/ комбинация/плацебо | AUA-SI, скорость мочеиспускания | Оценивались |
| F. Debruyne (ALFIN), 1998 | RCT | 1051 | 6 мес | альфузозин/финастерид/ комбинация | IPSS, скорость мочеиспускания | Оценивались |
| R. Kirby (PREDICT), 2003 | RCT | 1095 | 12 мес | доксазозин/финастерид/ комбинация/плацебо | IPSS, скорость мочеиспускания | Оценивались |
| J. McConnell (MTOPS), 2003 | RCT | 3047 | 4,5 года | доксазозин/финастерид/ комбинация/плацебо | Прогрессирование заболевания (увеличение баллов AUA-SI, частота развития острой задержки мочеиспускания (ОЗМ), почечной недостаточности, рецидивирующих инфекций мочевыводящих путей, недержания мочи) | Оценивались |
| C. Roehrborn (CombAT), 2008, 2010 | RCT | 4844 | 4 года | тастерид/ тамсулозин/ду комбинация | Через 2 года – снижение суммы баллов IPSS, через 4 года – частота возникновения ОЗМ и оперативного лечения по поводу ДГПЖ | Оценивались |
Анализ клинической эффективности комбинированной терапии доброкачественной гиперплазии предстательной железы
Таблица 2. Изменение суммы баллов индекса IPSS/AUASI к концу лечения
Преимущества и недостатки комбинированной терапии доброкачественной гиперплазии предстательной железы
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Доброкачественная гиперплазия предстательной железы (ДГПЖ) – наиболее распространенное урологическое заболевание мужчин. По данным Н.А. Лопаткина, это заболевание развивается у 10–20% мужчин в возрасте 40–45 лет и у 90% – в возрасте 80 лет. Однако в большинстве случаев у мужчин среднего возраста имеются только морфологические признаки заболевания без клинических проявлений. Характерные симптомы развиваются примерно у 25% из них [1].
В процессе своего увеличения в объеме предстательная железа (ПЖ) создает препятствие для оттока мочи, что приводит к многочисленным жалобам. К их числу относятся затрудненное начало мочеиспускания, прерывистость и слабая струя мочи, чувство неполного опорожнения мочевого пузыря, учащенное мочеиспускание, императивные позывы, особенно в ночное время. Последние 2 симптома особенно негативно влияют на качество жизни пациента и вынуждают его обращаться за урологической помощью. Можно сказать, ДГПЖ на ранних стадиях – заболевание скорее неприятное, чем опасное.
Лечение ДГПЖ долгое время было преимущественно хирургическим, т. к. эффективных лекарственных средств, влияющих на акт мочеиспускания, не существовало. В настоящее время имеются 3 группы лекарственных препаратов, доказавших свою эффективность для лечения ДГПЖ: α1-адреноблокаторы, ингибиторы 5α-редуктазы и некоторые фитопрепараты [2]. Фармакологические аспекты современной фитотерапии достаточно сложны и многогранны. Часть из них все еще является предметом научных исследований и активно обсуждается научным сообществом. В данной публикации они рассматриваться не будут.
Что касается синтетических лекарственных средств, то с начала 1990-х гг. широко применяются α1-адреноблокаторы, ингибиторы 5α-редуктазы. Указанные препараты имеют различные механизмы действия и точки приложения, что подразумевает потенциальную возможность их совместного применения с целью увеличения эффективности лечения. Препараты фармгруппы α1-адреноблокаторов снижают тонус гладкой мускулатуры ПЖ и шейки мочевого пузыря, устраняют динамический компонент обструкции, что приводит к сравнительно быстрому уменьшению выраженности симптомов. Ингибиторы 5α-редуктазы устраняют статический компонент обструкции за счет уменьшения размеров транзиторной зоны ПЖ, тем самым обусловливая долговременный эффект лечения и замедляя прогрессирование заболевания [2, 3]. Можно условно признать, что основное преимущество назначения комбинированной терапии по сравнению с монотерапией α1-адреноблокаторами заключается в предотвращении прогрессирования заболевания.
Исследования эффективности и безопасности комбинированной терапии, включающей α1-адреноблокатор и ингибитор 5α-редуктазы, начались вскоре после выхода указанных препаратов на рынок. Практически сразу было замечено, что подобная комбинация не дает быстрого результата, но приводит к заметному удорожанию стоимости лечения. Именно экономический аспект, который сегодня приобретает существенное, а иногда и решающее значение, во многих случаях являлся поводом для отказа от комбинированной терапии ДГПЖ. Между тем появились работы, свидетельствующие о явных преимуществах комбинации α1-адреноблокатора и ингибитора 5α-редуктазы перед монотерапией каждым из препаратов. Также опубликованы статьи, которые приводят обратные результаты, – комбинированная терапия не имеет преимуществ в отношении клинической эффективности перед монотерапией. В сложившейся противоречивой ситуации практическому врачу бывает сложно принять решение, кому, когда и по каким показаниям назначать комбинированную терапию.
Целями настоящей статьи являются систематизация и анализ результатов исследований эффективности и безопасности одновременного приема α1-адреноблокаторов и ингибиторов 5α-редуктазы у пациентов, страдающих ДГПЖ.
По результатам анализа базы данных PubMed систематических обзоров и метаанализов, посвященных комбинированной терапии ДГПЖ, найдено не было. Из множества проведенных исследований лишь 5 отвечали критериям высокого методологического качества, т. е. были двойными слепыми рандомизированными (табл. 1). Такие исследования соответствуют 2-му уровню достоверности (B), принятому в современной доказательной медицине. На рассмотрении результатов, полученных в этих работах, целесообразно сконцентрировать внимание.
Очень сильно осложняет интерпретацию результатов медикаментозной терапии ДГПЖ отсутствие ярко выраженных «конечных точек»: ремиссии, выздоровления и т. д. Задачей лекарственной терапии ДГПЖ является прежде всего улучшение качества жизни, что, несомненно, очень субъективно оценивается пациентом. Для объективизации нередко применяется такой показатель, как скорость мочеиспускания, рассчитанный при урофлоуметрии. Однако представляется нелепым рассчитывать стоимость терапии, направленной на увеличение скорости мочеиспускания, например, на 1 мл/мин, посредством назначения того или иного препарата. Да и зависимость там, скорее всего, везде нелинейная, так что экстраполяция, по всей видимости, невозможна. (Затраты на повышение скорости мочеиспускания с 3 до 4 мл/с могут существенно отличаться от аналогичных затрат на повышение скорости мочеиспускания с 10 до 11 мл/с.) Вряд ли у урологов встретит поддержку идея оценивать стоимость достижения некоторой скорости мочеиспускания, которая признана приемлемой у таких пациентов, – 12 или 15 мл/с. Вполне очевидно, что на конечный результат терапии оказывает существенное влияние первоначальная скорость мочеиспускания. Тем не менее этот показатель нередко применяется для количественной оценки эффективности проводимой терапии.
Некоторым эквивалентом «конечной точки» может служить предотвращенное оперативное вмешательство или острая задержка мочеиспускания (ОЗМ), хотя вполне очевидно, что больные принимают препараты не ради снижения вероятности оперативного лечения, а с целью нормализации акта мочеиспускания.
Все-таки стоит отметить, что вопросы клинико-экономического анализа мы подняли несколько преждевременно. Начать необходимо с клинических преимуществ и недостатков комбинированной терапии ДГПЖ.
Анализ клинической эффективности комбинированной терапии ДГПЖ
В исследованиях VAStudy [4], ALFIN [5], PREDICT [6] по показателям IPSS (International Prostate Symptom Score) и скорости мочеиспускания комбинированная терапия не продемонстрировала преимуществ перед монотерапией α-адреноблокаторами, в то время как в исследованиях MTOPS [7] и CombAT [8–10] получены диаметрально противоположные результаты, подтверждающие преимущества комбинированной терапии ДГПЖ (табл. 2). Сразу возникает вопрос о причинах таких расхождений в выводах. Чем же принципиально различались эти исследования? Ответ можно выразить одним словом – длительностью. Исследования, подтвердившие преимущества комбинированной терапии, продолжались от 2 до 4 лет, в то время как не подтвердившие ее преимущества – до 1 года. Однако в исследовании дутастерида и тамсулозина (CombAT) [8–10] статистически значимые различия между комбинированной терапией и монотерапией тамсулозином определялись уже с 6 мес. лечения.
Во всех исследованиях оценивались объем ПЖ и уровень простатического специфического антигена (PSA) (табл. 3, 4). Комбинированная терапия нигде не продемонстрировала статистически значимых преимуществ перед монотерапией ингибиторами 5α-редуктазы и, наоборот, везде оказалась эффективнее монотерапии α1-адреноблокаторами. Более того, в большинстве групп пациентов, получавших плацебо или монотерапию α1-адреноблокаторами, объем ПЖ и уровень PSA очень умеренно, но статистически значимо увеличивались к концу лечения. Очевидно, здесь имеет место естественное прогрессирование заболевания, а не негативное влияние препарата. Во всех исследованиях уровень PSA при приеме финастерида или дутастерида в режиме монотерапии или в комбинации с α1-адреноблокаторами снижался примерно на 50% к 6 мес. лечения. Общеизвестно, что ингибиторы 5α-редуктазы статистически значимо уменьшают объем ПЖ и уровень PSA, а α1-адреноблокаторы на эти показатели не влияют. Казалось бы, потратили массу сил и средств на доказательство очевидных фактов. Тем не менее рациональное зерно в этих трудозатратах все же есть. Результаты исследований позволяют сделать вывод, что эффекты изучаемых лекарственных средств при комбинированном применении складываются, но не потенцируются.
В исследовании PREDICT [6] оценивались случаи ОЗМ и выполнения оперативного лечения – трансуретральной резекции ПЖ, частота которых при длительности лечения 1 год в группе плацебо составила 2,6%, в группе финастерида – 1,9%, в группе доксазозина – 0,4%, в группе комбинированной терапии – 0%. В исследовании MTOPS [7] прогрессирование ДГПЖ, под которым подразумевалось увеличение суммы баллов IPSS на 4 и более, ОЗМ, перенесенная трансуретральная резекция ПЖ, недержание мочи и рецидивирующая инфекция мочевыводящих путей (МВП), было зафиксировано у 17% пациентов в группе плацебо, у 10% – в группе доксазозина и финастерида, у 5% – в группе комбинированной терапии, различия статистически достоверны. Снижение относительного риска прогрессирования в группе комбинированной терапии составило 66%. При раздельном анализе влияния различных вариантов терапии на развитие ОЗМ и необходимость хирургического лечения по поводу ДГПЖ отмечено снижение относительного риска по сравнению с плацебо в группе финастерида на 68 и 64%, в группе комбинированной терапии – на 81 и 67% соответственно. Монотерапия доксазозином не оказывала влияния на риск развития ОЗМ и проведения хирургического лечения по поводу ДГПЖ.
В исследовании CombAT [8–10] после 4 лет комбинированной терапии отмечено снижение относительного риска развития ОЗМ и проведения хирургического лечения на 65,8% по сравнению с тамсулозином и на 19,6% по сравнению с дутастеридом. Различия в частоте возникновения ОЗМ и проведения хирургического лечения начали наблюдаться с 8 мес. терапии.
Несколько слов о переносимости комбинированной терапии. При совместном назначении α1-адреноблокаторов и ингибиторов 5α-редуктазы происходит простое суммирование их желательных эффектов. Можно ожидать, что нежелательные, побочные эффекты тоже будут суммироваться. Насколько это существенно для пациентов, является вопросом принципиальной важности. Поэтому в каждом современном исследовании наряду с прямой регистрацией побочных эффектов оценивается и более важный показатель – доля пациентов, выбывших по причине побочных действий. По сути, это – частота нежелательных явлений, по выраженности своей соизмеримых с негативными последствиями самого заболевания или даже превосходящих их. Во всех вышеупомянутых исследованиях в группах больных, получавших комбинированную терапию, процент выбывших был несколько выше, чем в группах, получавших монотерапию или плацебо, однако, несмотря на многотысячные выборки, различия нигде не достигли статистически достоверной величины. Например, исследование VAStudy [4] закончило 82% пациентов, число выбывших из-за развития побочных эффектов составило в группе финастерида 5%, в группе теразозина – 6%, в группе комбинированной терапии – 8%.
В исследовании CombAT [8–10] лечение через 4 года закончили 69% пациентов. Общее число побочных эффектов было достоверно больше в группе комбинированной терапии, однако число выбывших из протокола из-за побочных эффектов в группах достоверно не различалось – 6% при комбинированной терапии и по 4% при монотерапии каждым из препаратов.
Экономическая оценка комбинированной терапии ДГПЖ
Переходим к экономическим аспектам комбинированной терапии ДГПЖ. Для начала необходимо оценить стоимость курса лечения. Как было отмечено в клинических исследованиях, комбинированная терапия начинает демонстрировать преимущества не ранее 6–8 мес. от ее начала, поэтому меньше, чем на 1 год ее назначать нецелесообразно. Из препаратов выберем оригинальные тамсулозин и финастерид. Информацию о ценах на препараты получим на сайте http://aptekamos.ru (предполагается, что пациент будет самостоятельно приобретать лекарственные средства в розничной сети). В столичном регионе 16.03.2015 средняя стоимость оригинального тамсулозина составила 779,5 руб. за упаковку (30 табл.), оригинального финастерида – 665,2 руб. за упаковку (28 табл.). Для расчетов (средняя арифметическая) были использованы 15 новых предложений по продаже каждого из препаратов. Соответственно стоимость 1 дня лечения при использовании среднетерапевтических дозировок оригинального тамсулозина 0,4 мг/сут (1 табл.) и оригинального финастерида 5 мг/сут (1 табл.) составляет 25,98+23,76=49,74 руб. Стоимость годового (365 сут) курса = 18 155,1 руб. (в среднем 1512,93 руб./мес.).
Если использовать оригинальный препарат дутастерид в сочетании с оригинальным тамсулозином (такая комбинация часто назначается в реальной урологической практике), то стоимость 1 дня лечения возрастет до 25,98+50,24=76,22 руб., а годового курса терапии – до 27 820,3 руб. (Средняя цена оригинального дутастерида в аптеках г. Москвы 16.03.2015 составляла 4522,0 руб. за упаковку 90 табл.)
Для сравнительной оценки экономической эффективности комбинированной терапии можно воспользоваться результатами исследования MTOPS, согласно которым за 4,5 года у 9% пациентов, страдавших ДГПЖ и получавших монотерапию тамсулозином, были отмечены признаки прогрессирования заболевания – в частности, увеличение суммы баллов IPSS/AUA-SI (American Urological Association Symptom Index) на 4 и более баллов, а при комбинированной терапии аналогичные явления были отмечены лишь у 5% пациентов. Для анализа использована методика «затраты/эффективность» (табл. 5).
CERincr – это показатель приращения затрат или добавленная стоимость, т. е. сумма, которая требуется для получения одной дополнительной единицы эффекта (например, излечения больного, достижения ремиссии, или, как в данном случае, отсутствия прогрессирования заболевания) при применении более дорогостоящей и более эффективной технологии по сравнению с менее эффективной и менее затратной [11].
В нашем случае на каждый дополнительный случай отсутствия прогрессирования заболевания требуется практически 1 млн руб., не считая трудозатрат, которые необходимы на ведение больного в течение 4,5 года. Вполне очевидно, что эта сумма очень велика.
Отсюда следует вывод, что в предложенном варианте комбинированная терапия ДГПЖ экономически неэффективна.
Примененная методика экономического анализа «затраты/эффективность» предполагает 2 взаимно дополняющих пути выхода из сложившегося положения.
1. Уменьшать CER – стоимость достигнутого эффекта. Существенно изменять схему терапии заведомо бесперспективно, зато можно использовать качественные дженерики. Для пациента они должны обходиться существенно дешевле, чем оригинальные лекарственные средства, иначе сама идея воспроизведенных аналогов потеряет свою экономическую привлекательность. Согласно результатам отечественного исследования дженериков тамсулозина (2009), наибольшее сродство к простатспецифическим α-адренорецепторам, наряду с оригинальным тамсулозином, продемонстрировал Фокусин, выпущенный компанией Zentiva (Чехия) [12]. Также эта компания выпускает дженерик финастерида Пенестер. Препараты поставляются в стандартных дозировках 0,4 и 5 мг соответственно.
В столичном регионе 16.03.2015 средняя стоимость Фокусина составила 1175,1 руб. за упаковку (90 табл.), Пенестера – 543,0 руб. за упаковку (30 табл.). Средняя стоимость курса комбинированной терапии Фокусином и Пенестером на 16.03.2015 составила 11 373 руб./год или 946,78 руб./мес., что в 1,6 раза меньше по сравнению с покупкой оригинальных тамсулозина и финастерида, и в 2,4 раза меньше по сравнению с применением оригинальных тамсулозина и дутастерида (рис. 1).
2. Альтернативный путь – увеличивать ∆CER – разницу в эффективности сравниваемых технологий. То есть каким-либо путем увеличить эффективность более затратного подхода при сохранении эффективности менее затратного. В медицине это обычно достигается более жесткими критериями отбора пациентов. Если среднестатистическому больному с ДГПЖ назначить максимально эффективную терапию – комбинированную, то вероятность прогрессирования составляет 1/20 за 4,5 года, а если его вовсе не лечить, то за аналогичный срок риск прогрессирования повышается менее чем в 3 раза (результаты исследования MTOPS). Вывод: возможно быстрее купируем симптомы заболевания, т. е. повышаем качество жизни пациентов, а тех, у кого будет явная отрицательная динамика, оперируем.
Кому же необходимо назначать высокоэффективную, но дорогостоящую комбинированную терапию? Во-первых, тем пациентам, которых по каким-либо причинам оперировать нельзя, – имеющих тяжелые сопутствующие заболевания, категорически отказавшихся от оперативного лечения по немедицинским причинам.
По статистике НИИ урологии, среди медицинских причин отказа от оперативного вмешательства на ПЖ доминирует ишемическая болезнь сердца (ИБС), осложненная нарушениями ритма и/или недостаточностью кровообращения. Неполная, часто неудовлетворительная обратимость изменений миокарда при поздних стадиях ИБС зачастую препятствует достижению достаточной для безопасного проведения урологического вмешательства компенсации коронарного синдрома и сердечной недостаточности. Вероятно, именно пациенты с коморбидным, сочетанным поражением ПЖ и сердечно-сосудистой системы и составят большинство больных, нуждающихся в комбинированной терапии. Исследования, направленные на оптимизацию оказания урологической помощи пациентам, имеющим сопутствующую ИБС, уже ведутся.
Остальные сопутствующие заболевания, являющиеся препятствием к оперативному лечению аденомы простаты или относительно редки среди пациентов урологического профиля, или под воздействием современной лекарственной терапии сравнительно легко переходят в стадию ремиссии/компенсации. Например, обострение язвенной болезни желудка и двенадцатиперстной кишки является абсолютным противопоказанием к плановой операции на простате, но по завершении 3-недельного курса лечения не менее 80% таких больных могут быть прооперированы [13, 14].
Во-вторых, комбинированную терапию следует назначать обширной группе пациентов с большим объемом ПЖ и/или признаками прогрессирования заболевания без лечения или на фоне монотерапии α1-адреноблокаторами. Именно у них сочетанное назначение α1-адреноблокаторов и ингибиторов 5α-редуктазы должно приводить к существенному (на несколько десятков процентов) росту эффективности медикаментозного лечения по сравнению с монотерапией, не говоря уже о плацебо, что в свою очередь сделает изучаемую методику экономически оправданной. Но для подтверждения этих предположений необходимо проведение специального исследования.
Заключение
Комбинированная терапия ДГПЖ:
– позволяет суммировать эффекты a1-адреноблокаторов и ингибиторов 5a-редуктазы, при этом риск побочных действий существенно не увеличивается;
– демонстрирует преимущества перед монотерапией a1-адреноблокаторами или ингибиторами 5a-редуктазы лишь при длительном (по сути, многолетнем) приеме;
– экономически нецелесообразна при назначении пациентам, имеющим небольшой объем ПЖ, умеренные жалобы, а также незначительный риск прогрессирования заболевания;
– показана при значительном объеме ПЖ, высоком риске или имеющихся признаках прогрессирования заболевания.





