Не нужно бояться хронического аутоимунного тиреоидита
В практике эндокринолога существует 2 страшилки: гормоны и хронический аутоимунный тироидит (ХАИТ). И если гормоны бывают разные, среди них могут попасться те, которых опасаться следует, то опасность ХАИТа явно переоценена.
Что такое ХАИТ? Это выработка организмом антител к своей щитовидной железе. Антитела долгое время атакуют ни в чём неповинный орган и очень часто могут уничтожить его совсем. Страшно.
Первый кошмар, с которым сталкиваются пациенты – повышение антител к тиреопероксидазе (ТПО). Причём, нормальные значения антител очень низкие (обычно до 6 ед), на этом фоне даже 30 ед кажутся кошмаром. Между тем, изолированное повышение антител к ТПО (т.е. если уровень гормонов ТТГ, Т4 свободного и Т3 свободного находятся в пределах нормы), ещё не повод для лечения.
С антителами к тиреоглобулину (ТГ) ситуация ещё интереснее: они к ХАИТу отношения сами по себе не имеют, могут подняться «за компанию». Изолированное повышение антител к тиреоглобулину (когда антитела к ТПО не повышены) диагностически значимо только при полностью удалённой щитовидной железе. В остальных ситуациях это случайная находка, скажем так «личное дело самого организма, не касающееся эндокринолога».
Второй «кошмар» ХАИТа: изменения на УЗИ. Они обычно очень красочно описываются врачами, будя разные ассоциации у пациентов. На самом деле, врачи просто описывают типичную ситуацию, которая происходит со щитовидной железой, если она в беде.
Только по УЗИ диагноз ХАИТа поставить нельзя.
Чем грозят человеку изменения щитовидной железы при ХАИТе? Ничем. В рак это состояние не перерастёт, оперировать его не надо, на другие органы не расползётся.
Когда антитела к ТПО всё-таки имеют значение?
И вот мы плавно подошли к третьему кошмару ХАИТа: пожизненная заместительная гормональная терапия (ЗГТ). Звучит ужасно, но на деле это означает всего одна таблетка с утра. Ограничений и противопоказаний, в принципе, нет никаких.
Четвёртый кошмар ХАИТа – набор веса на ЗГТ. Его не будет. Вы просто заменяете натуральный гормон искусственно произведённым. К счастью, произведённым очень хорошо, поэтому организм разницу не чувствует и живёт себе дальше.
Следует отметить, что ХАИТ был впервые описан японцем Хашимото (поэтому заболевание иногда и называют тироидит Хашимото) в 1912 году, ЗГТ пациенты получают уже не менее 30-ти лет. За это время по препаратам накоплен обширный материал, подтверждающий, что они не влияют ни на продолжительность жизни, ни на её качество.
Наблюдаться с ХАИТом обязательно нужно, но кратность обследований должен определить врач индивидуально. Она зависит от нескольких причин: возраста, уровня ТТГ исходно, назначенной дозы препарата. Скажем сразу, что ежегодное УЗИ в этот список однозначно не войдёт.
Автор: Эндокринолог, кандидат медицинских наук Таныгина Наталья Ивановна.
Причины, симптомы и лечение повышенной васкуляризации щитовидной железы
Щитовидка имеет в своем строении верхнюю и нижнюю артерии – они питают правую и левую доли железы, а так же сам перешеек. Соответственно, при развитии дополнительных сосудов, ставится такой диагноз, как васкуляризация щитовидной железы, о чем и поговорим далее.
Суть патологии и ее механизм
Как отмечалось ранее, васкуляризация щитовидной железы – это патологическое разрастание дополнительных кровеносных сосудов в системе кровотока. В силу того, что железа интенсивно питается, увеличивается кровоток, начинает вырабатываться большее число гормонов. Как отмечают врачи, усиленная васкуляризация щитовидной железы может протекать по причине следующих предрасполагающих к патологии факторов:
Все это может спровоцировать разрастание дополнительных кровеносных сосудов, которые пронизывают ткани щитовидной железы и приводят к ее патологическому росту и увеличению в размере.
Симптоматика патологического процесса
Что представляет собой васкуляризация щитовидной железы – рассмотрели. Но как она показывает себя?
Самый основной признак – увеличение самой щитовидной железы в размере, появление на поверхности органа образования. Могут видоизменяться и контуры железы, но нередко патология протекает без характерных симптомов.
При повышенной васкуляризации щитовидной железы могут проявляться:
Своевременная диагностика – важный этап в будущем лечении, поскольку усиленный рост кровеносной системы часто сопровождается воспалительным процессом. А это уже предпосылки для развития онкологии.
Диагностика патологического процесса

Далее врач направляет пациента на диагностику посредством УЗИ – необходимой процедуры при патологическом изменении щитовидки. Такое предположение может базироваться на самих жалобах пациента, повышении уровня гормонов, на основании итогов пальпации. Параллельно УЗИ позволяет оценить уровень, структуру и эхогенность железы.
При повышенной эхогенности врачи делают заключение о росте новых кровеносных сосудов, соответственно и об избыточном наполнении щитовидки кровью.
Для всесторонней и полной оценки работы щитовидки, специалист направляет пациента на сдачу анализа крови, однако окончательный диагноз, и, соответственно, курс терапии врач назначает по итогам диагностики.
Курс терапии

Когда сама щитовидка увеличена, но при этом серьезных патологических изменений в ней не диагностировано, врач назначает препарат йодида кальция и специальную, богатую на йод диету. При серьезных отклонениях медики назначают такие препараты как Левотироксин и Тиреотом. К данным препаратам добавляются лекарства, которые в своем составе включают искусственные гормоны.
На протяжении всего курса терапии пациент регулярно сдает анализы крови, контролируя тем самым уровень гормонального фона. При отсутствии положительной динамики, врачи направляют пациента на оперативное вмешательство.
Эхографические характеристики поражений щитовидной железы у детей Астраханской области
Педиатры и эндокринологи констатируют, что среди детей, особенно девочек, отмечается увеличение заболеваемости щитовидной железы.
Педиатры и эндокринологи констатируют, что среди детей, особенно девочек, отмечается увеличение заболеваемости щитовидной железы.
Для участковых педиатров актуальными становятся такие вопросы: «С чем мы связываем данную ситуацию? Какое обследование необходимо проводить в амбулаторных условиях? Как трактовать результаты обследования? В каком случае требуется углубленное стационарное обследование и лечение?»
При обследовании пациентов с подозрением на патологию щитовидной железы специалистами широко используется ультразвуковая диагностика, которая позволяет не только оценить размеры щитовидной железы, но и выявить изменения в ее структуре. Не менее важно, что этот метод диагностики из числа неинвазивных, неагрессивных, не несущих психологической нагрузки на растущий организм.
В большей части случаев, несмотря на увеличение щитовидной железы, имеет место эндемический зоб, выявляемый в регионах с йодным дефицитом, при котором не требуется госпитализация ребенка в стационар. Для описания данного заболевания используют термины: юношеский, пубертатный, диффузно-нетоксический, простой, эутиреоидный (то есть без нарушения функции) зоб.
В 2003 г. Министерством здравоохранения Астраханской области, сотрудниками Астраханской государственной медицинской академии, с участием врачей-эндокринологов города и области в рамках мероприятий региональной целевой программы «Профилактика йододефицитных заболеваний» проводилось обследование на «эндемичность» с использованием проекта «Тиромобиль». Частота увеличения щитовидных желез среди учащихся школ города и области в возрасте 8–11 лет варьировала от 17,5% до 30%. Медиана концентрации йода в моче соответствовала средней степени йодной недостаточности — 26 мкг/л. Показатели содержания йода в моче варьировали от 18,8 до 30,4 мкг/л.
Для сравнения: по данным скрининговых исследований, проведенных в 1995–1998 гг. сотрудниками Эндокринологического научного центра, частота увеличения щитовидных желез среди учащихся школ г. Москвы варьировала от 7,3% до 12,5%, достигая в отдельных возрастных категориях 15%, а медиана концентрации йода в моче соответствовала легкой степени йодной недостаточности — 72 мкг/л [2].
В подавляющем большинстве случаев в условиях легкого и умеренного йодного дефицита небольшое увеличение щитовидной железы обнаруживается только при целенаправленном обследовании. Сам по себе факт умеренного увеличения щитовидной железы при нормальной функции последней практически не отражается на работе других органов и систем [3]. Поэтому ребенок чаще всего не предъявляет никаких специфических жалоб и не производит впечатления тяжелобольного. Поэтому о йододефицитном зобе в литературе говорят как о признаке «скрытого голода». Ни о каком явно выраженном и клинически манифестном нарушении функции щитовидной железы речи пока не идет. В принципе, зоб для того и формируется, чтобы предотвратить развитие гипотиреоза.
Для лечения эутиреоидного эндемического зоба, как правило, достаточно назначение препаратов йода (калия йодид) в физиологической дозе, то есть 100–200 мкг в сутки. Эффективность лечения оценивается через 6 месяцев после его начала. В случае тенденции к уменьшению размеров щитовидной железы продолжают терапию в течение 1,5–2 лет. После отмены калия йодида рекомендуют употребление йодированной соли. Если на фоне приема препаратов йода в течение 6 месяцев не произошло нормализации размеров щитовидной железы, то показано применение левотироксина (L-тироксина) внутрь утром за 30 минут до завтрака в дозе 2,6–3 мкг/кг массы тела в сутки в комбинации с 100–200 мкг йода (калия йодида) в день, длительно [2]. Адекватная доза L-тироксина подбирается в соответствии с уровнем тиреотропного гормона в сыворотке крови пациента. После нормализации размеров щитовидной железы по данным ультразвукового исследования, проводимого каждые 6 месяцев, рекомендуется переход на длительный прием профилактических доз йода (рис. 1).
При рассмотрении структуры патологии щитовидной железы у детей Астраханской области в динамике видно, что на долю однородных форм зоба в 1994 г. приходилось 86,4%, а к 1998 г. процент однородных форм зоба уменьшился и составлял уже 34,2%, то есть сократился в 2,5 раза. Неоднородные формы зоба с 1994 г. выросли к 1998 г. по данным динамического осмотра более чем в 5 раз (рис. 1). Скорее всего, данная ситуация была вызвана йодным дефицитом.
.gif) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
.gif) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Размеры узлов | Морфологическое строение узлов | |||||||
|---|---|---|---|---|---|---|---|---|
| Рак | Аденома | Коллоидные узлы | Итого | |||||
| Кол-во | % | Кол-во | % | Кол-во | % | Кол-во | % | |
| До 10 мм | 16 | 28,6 | 5 | 11,1 | 195 | 45,6 | 216 | 40,9 |
| 11-20 мм | 17 | 30,4 | 15 | 33,3 | 102 | 23,9 | 134 | 25,4 |
| 21-30 мм | 13 | 23,2 | 16 | 35,6 | 66 | 15,5 | 95 | 18,0 |
| 31-40 мм | 5 | 8,9 | 5 | 11,1 | 32 | 7,5 | 42 | 8,0 |
| > 40 мм | 5 | 8,9 | 4 | 14,9 | 32 | 7,5 | 41 | 7,8 |
| Всего | 56 | 100,0 | 45 | 100,0 | 427 | 100,0 | 528 | 100,0 |
Таблица 2. Локализация узловых образований щитовидной железы
различной морфологической структуры
| Размеры узлов | Морфологическое строение узлов | |||||||
|---|---|---|---|---|---|---|---|---|
| Рак | Аденома | Коллоидные узлы | Итого | |||||
| Кол-во | % | Кол-во | % | Кол-во | % | Кол-во | % | |
| Верхний полюс | 14 | 25,0 | 2 | 4,4 | 104 | 24,4 | 120 | 22,3 |
| Средняя треть | 24 | 42,9 | 20 | 44,4 | 141 | 33,0 | 185 | 35,0 |
| Нижний полюс | 10 | 17,9 | 20 | 44,4 | 147 | 34,4 | 177 | 34,0 |
| Перешеек | 8 | 14,3 | 3 | 6,8 | 35 | 8,2 | 46 | 8,7 |
| Всего | 56 | 100,0 | 45 | 100,0 | 427 | 100,0 | 528 | 100,0 |
В структуре опухолевых заболеваний ЩЖ обращает внимание присутствие мелких очагов, размерами менее 10 мм (до 28,6% среди раков и до 11,1 % среди аденом) (табл. 1). Это затрудняло их дифференциацию при полинодозном поражении ЩЖ и обнаружение среди мелких пролиферирующих коллоидных узелков и инциденталом. До 17,8% раковых узлов были представлены крупными очаговыми образованиями, размерами более 30 мм в диаметре, что также было характерно и для узлового пролиферирующего зоба. Зависимости частоты встречаемости рака от размеров узла нами не выявлено (χ 2 =3,70, р=0,448).
Малигнизированные узлы чаще локализировались в средней трети доли, тогда как аденомы преимущественно располагались как в нижнем полюсе, так и в средней трети доли (табл. 2). Эхографические характеристики узловых образований различной морфологической структуры отличались большим разнообразием ультразвуковых признаков, что также затрудняло диагностику злокачественной патологии с помощью УЗИ (табл. 3).
Таблица 3. Ультразвуковые признаки узловых образований щитовидной железы
в сопоставлении с результатами морфологического исследования
| Признаки | Морфологическое строение узлов | Статистическая значимость | |||||||
|---|---|---|---|---|---|---|---|---|---|
| Рак | Аденома | Узловой кол. зоб | |||||||
| Кол-во узлов | % | Кол-во узлов | % | Кол-во узлов | % | χ 2 | р | ||
| Эхогенность | Гипоэхогенность | 40 | 71,4 | 18 | 40,0 | 164 | 38,4 | 7,711 | 0,021 |
| Изоэхогенность | 13 | 23,2 | 19 | 42,2 | 172 | 40,3 | 3,116 | 0,211 | |
| Гиперэхогенность | 2 | 3,6 | 2 | 4,4 | 33 | 7,7 | 1,069 | 0,447 | |
| Смешанная | 1 | 1,8 | 6 | 13,3 | 58 | 13,6 | 5,479 | 0,065 | |
| Итого: | 56 | 100 | 45 | 100 | 427 | 100 | |||
| Границы | Ровные | 24 | 42,9 | 42 | 93,3 | 366 | 85,7 | 8,077 | 0,018 |
| Неровные | 32 | 57,1 | 3 | 6,7 | 61 | 14,3 | 35,948 | 0,0001 | |
| Итого: | 56 | 100 | 45 | 100 | 427 | 100 | |||
| Контур | Четкий | 24 | 42,9 | 43 | 95,6 | 394 | 92,3 | 9,677 | 0,008 |
| Нечеткий | 32 | 57,1 | 2 | 4,4 | 33 | 7,7 | 63,644 | 0,0001 | |
| Итого: | 56 | 42,9 | 45 | 100 | 427 | 100 | |||
| Ободок | Ободок Halo | 6 | 10,7 | 14 | 31,1 | 45 | 10,5 | 10,944 | 0,004 |
| Нет | 50 | 89,3 | 31 | 68,9 | 382 | 89,5 | 1,163 | 0,559 | |
| Итого: | 56 | 100 | 45 | 100 | 427 | 100 | |||
| Структура | Однородная | 14 | 25,0 | 10 | 22,2 | 153 | 35,8 | 2,873 | 0,238 |
| Неоднородная | 42 | 75,0 | 35 | 77,8 | 284 | 66,5 | 18,376 | 0,0001 | |
| Итого: | 56 | 100 | 45 | 100 | 427 | 102,3 | |||
| Кальцинаты | Кальцинаты | 23 | 41,1 | 14 | 31,1 | 27 | 6,3 | 48,497 | 0,0001 |
| Нет | 33 | 58,9 | 31 | 68,9 | 400 | 93,7 | 5,297 | 0,071 | |
| Итого: | 56 | 100 | 45 | 100 | 427 | 100 | |||
| Жидкость | Жидкостные участки | 12 | 21,4 | 9 | 20,0 | 123 | 28,8 | 1,59 | 0,451 |
| Нет | 44 | 78,6 | 36 | 80,0 | 304 | 71,2 | 0,41 | 0,815 | |
| Итого: | 56 | 100 | 45 | 100 | 427 | 100 | |||
| Капсула ЩЖ | Нарушение капсулы ЩЖ | 7 | 12,5 | 0 | 0,0 | 0 | 0,0 | 53,14 | 0,0001 |
| Нет | 49 | 87,5 | 45 | 100 | 427 | 100 | 0,21 | 0,9 | |
| Итого: | 56 | 100 | 45 | 100 | 427 | 100 | |||
| I | 2 | 3,6 | 0 | 0,0 | 22 | 7,5 | 4,124 | 0,125 | |
| II | 3 | 5,4 | 2 | 4,4 | 76 | 25,8 | 14,533 | 0,0001 | |
| III с внутриузловой гиперваскуляри-зацией | 12 | 21,4 | 21 | 46,7 | 77 | 26,1 | 4,847 | 0,089 | |
| III с внутриузловой гиповаскуляри-зацией | 32 | 57,1 | 19 | 42,2 | 108 | 36,6 | 3,271 | 0,195 | |
| IV | 7 | 12,5 | 3 | 6,7 | 12 | 4,1 | 5,544 | 0,063 | |
| Итого: | 56 | 100 | 45 | 100 | 295 | 100 | |||
В процессе ультразвукового обследования пациентов с узловыми образованиями ЩЖ решали несколько диагностических задач, которые определяли дальнейшую хирургическую тактику, в том числе выбор объема операции. Главная из них – определение морфологической структуры обнаруженных очагов тиреоидной паренхимы. При обнаружении злокачественной патологии не менее важно было оценить стадийность заболевания, то есть распространение процесса за пределы ЩЖ. И наконец, в-третьих – выявление всех узловых образований в тиреоидной паренхиме, определение их размеров, пространственного расположения, дифференциация участков неизмененной паренхимы, подлежащих сохранению.
При обнаружении узловых образований в тиреоидной паренхиме в первую очередь дифференцировали их злокачественную или доброкачественную природу.
Ретроспективный анализ показал, что в наших наблюдениях рак ЩЖ чаще встречался при множественном узловом поражении ЩЖ (в 62,5% случаев) и присутствовал в одном или нескольких узлах при многоузловом зобе. Одиночные раковые узлы выявлены в 21 случае (37,5%). Вместе с тем частота встречаемости рака ЩЖ в общей структуре моно- и полинодозного поражения ЩЖ практически не различалась и составляла соответственно 28,6%, и 19,9% (различия статистически не значимы, критерий χ 2 =0,912, р=0,340).
Одновременно несколько раковых очагов в одной или обеих долях гистологически верифицированы у 7 (14,3%) пациентов (у 2 в одной доле и у 5 в обеих долях (рис. 3)), причем в 2 случаях в виде микрофокусов до 3-5 мм в диаметре. В этих 2 наблюдениях (4,1% больных) микрофокусы злокачественных новообразований были предположены при УЗИ и определялись в виде гипоэхогенных участков неправильной формы с неровными контурами, размерами 4-5 мм в диаметре, расположенных в непосредственной близости с «основным» раковым узлом (рис. 4). В остальных 5 наблюдениях дополнительные злокачественные новообразования в тиреоидной паренхиме при УЗИ найдены не были.
Рисунок 3. Узлы папиллярного рака (белые стрелки) в правой доле и левой доле ЩЖ.
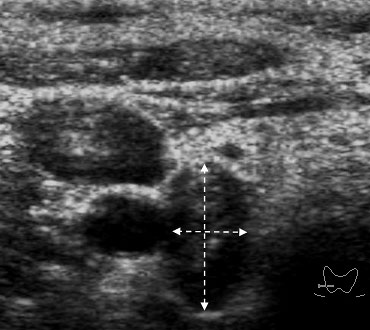
Рисунок 4. Узел папиллярного рака (двусторонняя стрелка)
и микрофокус рака (белая стрелка и пунктирные маркеры).
По морфологическому строению преобладали высокодифференцированные раки: 58,9% узлов соответствовали папиллярной карциноме, 26,8% – фолликулярной карциноме. Солидный (папиллярный и фолликулярный) рак встретился в 7,1% узлов, медуллярный – в 5,4% и недифференцированный – в единичном наблюдении (1,8%). В 10 наблюдениях (20,4%, 10/49) раку ЩЖ сопутствовал аутоиммунный тиреоидит с выраженными диффузно-псевдоузловыми изменениями паренхимы ЩЖ, а у 3 (6,1%, 3/49) больных рак ЩЖ сочетался с фолликулярными аденомами.
Стадия Т1-2 верифицирована у 33 (67,3%) больных, Т3 – у 7 (14,3%), Т4 – у 9 (18,4%). Лимфогенное метастазирование на стороне поражения обнаружено у 10,2% пациентов. Отдаленные метастазы в кости скелета были выявлены у одного больного (2,0%).
Раковые узлы несколько чаще локализовались в средней трети долей (42,9% узлов), реже в верхнем полюсе (25,0%), в нижней трети (17,9%) и в перешейке (14,2%) (критерий χ 2 =8,220, р=0,0540). И, как уже отмечалось, практически 1/3 узлов (28,6%) составили очаги менее 10 мм в диаметре (табл. 1, 2).
По сравнению с доброкачественными образованиями для раковых узлов были характерны следующие эхографические признаки: гипоэхогенность узла (71,4%), неоднородность структуры (75,0%), нечеткие неровные контуры (51,7%), более высокая встречаемость микрокальцинатов (41,1%) (таблица 3, рис. 5) Такие признаки были выявлены у 67,9% злокачественных очагов. При узлах менее 20 мм в диаметре «типичное» ультразвуковое изображение рака ЩЖ встретилось в 78,8% наблюдений, а при более крупных узлах (свыше 20 мм в диаметре) – лишь в 36,4%.
Рисунок 5. Узел папиллярного рака (двусторонняя стрелка).
«Типичное» ультразвуковое изображение злокачественного узла ЩЖ.
В 32,1% случаев определялось иное ультразвуковое изображение ракового узла, больше соответствующее коллоидному зобу (рис. 6) или аденоме (рис. 7). Такое «нетипичное» ультразвуковое изображение рака ЩЖ чаще выявлялось среди узловых образований размерами свыше 20 мм в диаметре (52,4%), а также среди фолликулярных аденокарцином, при солидных раках и в случае низкодифференцированного рака ЩЖ. Установлению правильного диагноза в этих случая на дооперационном этапе особенно помогала тонкоигольная аспирационная биопсия.
Рисунок 6. Узел папиллярного рака ЩЖ (двусторонняя стрелка). «Нетипичное»
ультразвуковое изображение злокачественного узла ЩЖ. Панорамное сканирование.
Рисунок 7. Узел папиллярного рака ЩЖ (двусторонняя стрелка). «Нетипичное»
ультразвуковое изображение злокачественного узла в перешейке ЩЖ.
Изучение сосудистого рисунка узловых образований тиреоидной паренхимы не способствовало значимому повышению результативности УЗИ в дифференциальной диагностике рака среди других узловых образований ЩЖ (табл. 4).
Таблица 4. Сравнение информативности серошкального УЗИ
и УЗИ с использованием цветокодирующих методик
| Показатели | Серошкальное УЗИ | Серошкальное УЗИ + цветокодирующие методики | Значения критерия z |
|---|---|---|---|
| Чувствительность | 62,5% | 64,3% | 0.002, р=0.942 |
| Специфичность | 84,5% | 87,7% | 1.327, р=0.185 |
| Точность | 82,2% | 85,2% | 1.336, p=0.216 |
| Прогностическая ценность положительного результата | 32,4% | 38,3% | 0.817, р=0.414 |
| Прогностическая ценность положительного результата | 95,0% | 95,4% | 0.248, р=0.808 |
Для большинства (78,5%) раковых узлов была характерна смешанная перинодулярная и внутриузловая ангиоархитектоника с преобладанием внутриузловой гиповаскуляризации, что не отличало их от трети коллоидных узлов и половины аденом (табл. 3, рис. 8). Рассчитанный критерий χ 2 для частоты встречаемости III типа сосудистого рисунка среди раков, аденом и узловых коллоидных узлов составил χ 2 =2,790, р=0,248.
Рисунок 8. Узел папиллярного рака ЩЖ (двусторонняя стрелка).
Сосудистый рисунок узла в режиме ЦДК (слева) и ЭД (справа).
Отсутствие васкуляризации в раковых узлах встретилось лишь в 2 наблюдениях (3,6%) при узлах менее 10 мм в диаметре. Невозможность визуализации их ангиоархитектоники объяснялась наличием кальцинатов, которые частично (рис. 9) или практически полностью выполняли очаги.
Рисунок 9. Аваскулярный узел папиллярного рака (стрелка)
с кальцинатами в структуре. Сканирование в режиме ЭД.
Аваскулярные узловые образования нередко встречались среди коллоидных пролиферирующих узлов (в 7,5% случаев), но это, как правило, были мелкие узелки диаметром не более 6-7 мм. Несмотря на отсутствие значимых различий, среди злокачественных новообразований чаще, чем среди коллоидных узлов и аденом, выявлялись очаги с отсутствием перинодулярной васкуляризации (IV тип сосудистого рисунка). В таких узлах в режимах ЦДК (ЭД) регистрировался внутриузловой, как правило, малоинтенсивный кровоток с отдельными внутриузловыми «обрубленными» и хаотично расположенными сосудами (рис. 10). В этих случаях применение 3-мерной реконструкции сосудистого рисунка (режим 3D-ангио) способствовало уточнению ангиоархитектоники узла, наличия, хода, выраженности и взаиморасположения узловых сосудов (рис. 11).
Рисунок 10. Скудная внутриузловая васкуляризация узла папиллярного рака
(двусторонняя стрелка) (IV тип сосудистого рисунка). Сканирование в режиме ЭД.
Рисунок 11. Сосудистый рисунок узла папиллярного рака (двусторонние стрелки)
в режиме ЭД (слева) и в режиме 3D-ангио.
Несмотря на отсутствие значимого повышения информативности УЗИ с использованием доплеровских методик в дифференциальной диагностике узловых образований различного морфологического строения, результаты ЦДК, ЭД, 3-мерной реконструкции сосудистого рисунка (режим 3D-ангио) следует учитывать при интерпретации ультразвукового изображения любого внутрипаренхиматозного очага. В случае выявления узлового образования только с внутриузловой васкуляризацией (IV тип сосудистого рисунка) и хаотичным дезорганизованным ходом сосудов с большой долей вероятности можно предполагать злокачественную природу узла, особенно при наличии «серошкальных ультразвуковых признаков злокачественности». При получении сосудистого рисунка с перинодулярной и внутриузловой васкуляризацией (III тип) дифференцировать рак, аденому и коллоидный узел при сходной серошкальной картине сложно. Вместе с тем, перинодулярная и внутриузловая гиперваскуляризация с правильным равномерным «спицеобразным» ходом сосудов чаще (в наших наблюдениях в половине случаев) соответствует аденоме (рис. 12). Таким образом, несмотря на то, что цветовое картирование существенно не повышает информативности ультразвуковой диагностики узловых образований щитовидной железы, это исследование является, на наш взгляд, необходимым не только для полноты характеристики обнаруженных образований, но и для корректного проведения обязательной пункционной биопсии.
Рисунок 12. Сосудистый рисунок аденомы ЩЖ в режиме 3D-ангио.
Анализируя сосудистый рисунок выявленных узловых образований, мы обратили внимание, что степень васкуляризации узлов в большей степени определялась размером узла, а не его морфологической структурой (табл. 5).
Таблица 5. Зависимость васкуляризации узловых образований от размеров узлов
| Тип сосудистого рисунка | Размеры узловых образований в мм | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ≤ 10 | от 11 до 20 | от 21 до 30 | от 31 до 40 | > 40 | Всего | |||||||
| Кол-во | % | Кол-во | % | Кол-во | % | Кол-во | % | Кол-во | % | Кол-во | % | |
| I | 23 | 18,1 | 1 | 0,9 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 24 | 6,1 |
| II | 48 | 37,8 | 22 | 20,6 | 7 | 8,4 | 2 | 4,9 | 2 | 5,3 | 81 | 20,5 |
| III с внутриузловой гиперваскуляризацией | 15 | 11,8 | 42 | 39,3 | 30 | 36,1 | 12 | 29,3 | 11 | 28,9 | 110 | 27,8 |
| III с внутриузловой гиповаскуляризацией | 31 | 24,4 | 35 | 32,7 | 45 | 54,2 | 25 | 61,0 | 23 | 60,5 | 159 | 40,2 |
| IV | 10 | 7,9 | 7 | 6,5 | 1 | 1,2 | 2 | 4,9 | 2 | 5,3 | 22 | 5,6 |
| Итого | 127 | 100 | 107 | 100 | 83 | 100 | 41 | 100 | 38 | 100 | 396 | 100 |
| значения χ 2 значения р | 28,241 0,0001 | 49,128 0,0001 | 75,567 0,0001 | 39,884 0,0001 | 36,059 0,0001 | |||||||
Так, среди мелких узлов (менее 10 мм в диаметре) преобладали (63,8%) узлы со скудной васкуляризацией (II или IV типа) или аваскулярные очаги. С увеличением размеров узлов уменьшалась частота встречаемости скудно васкуляризированных образований (с 36,2% при размерах менее 10 мм до 9,8% и 10,6% при размерах очагов свыше 30 и 40 мм). Кроме того, среди образований мелкого и среднего калибра (до 20 мм) с III типом сосудистого рисунка в наших наблюдениях встречались преимущественно узлы с внутриузловой гиперваскуляризацией, а среди более крупных (свыше 20 см и особенно свыше 40 мм в диаметре) – с интранодулярной гиповаскуляризацией.
В общей сложности на дооперационном этапе обследования информативность УЗИ в диагностике злокачественных опухолей ЩЖ составила: чувствительность – 63,4%, специфичность – 87,7%, точность – 85,2%, прогностическая ценность положительного результата – 38,3%, прогностическая ценность отрицательного результата – 95,4%. Информативность УЗИ во многом зависела от размеров опухоли, акустической структуры опухолевого узла, распространенности процесса, количества узлов, наличия синхронных поражений ЩЖ. Так, чувствительность УЗИ при выявлении рака при одиночном и многоузловом поражении составляла соответственно 85,7% против 51,4% (различия статистически значимы, z=2,305, р=0,021). Преобладание в наших наблюдениях пациентов с множественными узловыми образованиями ЩЖ (62,5% против 37,5%), высокая встречаемость «нетипичного» ультразвукового изображения ракового узла (32,1%), большое количество (41,0%) крупных узлов диаметром свыше 2 см объясняли недостаточно высокую чувствительность УЗИ в дифференциации злокачественной патологии ЩЖ. Существенному повышению результативности диагностики рака ЩЖ способствовали тонкоигольные аспирационные биопсии (ТАБ) подозрительных узлов с цитологическим исследованием пунктата. При сочетании УЗИ и ТАБ чувствительность метода возросла до 83,9%, специфичность – до 90,9%, точность – до 89,8%, прогностическая ценность положительного результата – до 62,7%, прогностическая ценность отрицательного результата – до 96,9%.
В случае обнаружения подозрительного в плане злокачественности очага в паренхиме ЩЖ возможностями УЗИ определяли распространенность опухолевого процесса, обращая внимание на нарушение целостности капсулы ЩЖ, наличие измененных лимфоузлов. Дополнительно проводили ультразвуковое обследование других органов и систем (печень, почки), учитывая возможность отдаленного метастазирования.
При исследовании всех образований, а особенно с прикапсульной локализацией и подозрительных на малигнизацию, в обязательном порядке изучали целостность капсулы ЩЖ. Среди заподозренных при УЗИ раках ЩЖ нарушения целостности капсулы в виде неровности, «смазанности» и прерывистости ее контура выявлено у 7 больных с раком ЩЖ (рис. 13).
Рисунок 13. Нарушение целостности капсулы ЩЖ (стрелки)
с инвазией опухоли (двусторонняя стрелка) в прилежащие мышцы.
Измененные лимфоузлы в зонах регионарного лимфооттока найдены при УЗИ у 19 пациентов с раковыми узлами в тиреоидной паренхиме. В 3 наблюдениях ультразвуковое изображение пораженных лимфоузлов очень походило на эхографическую картину ракового узла в ЩЖ. Лимфоузлы были гипоэхогенные, с ровным или неровным четким контуром, ближе к округлой форме, с соотношением длины к ширине Вверх