Презентация была опубликована 9 лет назад пользователемwww.bioclass.ru
Похожие презентации
Презентация на тему: » Методы диагностики причин возникновения тромбоцитопении. Российский Кардиологический Научно-производственный Комплекс. Институт экспериментальной кардиологии.» — Транскрипт:
1 Методы диагностики причин возникновения тромбоцитопении. Российский Кардиологический Научно-производственный Комплекс. Институт экспериментальной кардиологии. Московская гимназия на Юго-Западе Даниил Халангот. Научные руководители: Антонова Ольга Александровна Хаспекова Светлана Георгиевна Москва 2012
3 Виды тромбоцитопений. Идиопатическая тромбоцитопеническая пурпура (ИТП) Неонатальная аллоиммунная ТП Неонатальная трансиммунная ТП Псевдотромбоцитопения. Гаптеновые ТП Лекарственные ТП Тромбоцитопении, ассоциированные с вирусной инфекцией Рефрактерность к переливанию тромбоцитов
4 Гликокалицин Гликокалицин (ГК) представляет собой крупный (молекулярная масса 125 кД) внеклеточный протеолитический фрагмент одного из главных мембранных белков тромбоцитов гликопротеина lb.
5 Задачи и цели. 1. Освоить метод лабораторной диагностики, позволяющий определить концентрацию растворимого гликокалицина, как метода определения пролиферативной функции мегакариоцитов. 2. Освоить метод лабораторной диагностики, позволяющий определить уровень тромбоцитассоциированных антител. 3. Освоить метод лабораторной диагностики, позволяющий определить уровень аллоиммунных антител против антигенов на поверхности тромбоцитов. 4. Сравнить полученные результаты анализа крови пациентов с тромбоцитопенией разного генеза и у здоровых доноров. 5. Охарактеризовать практическое значение методов для современной клинической диагностики.
6 Материалы и методы. В работе были исследованы следующие методы: Радиоиммунный метод (РИА) для определения тромбоцит-ассоциированных антител (ТААТ). Иммуноферметный анализ (ИФА) для определения сывороточных антител (сАТ) Сэндвич – ИФА для определения гликокалицина
7 Сэндвич ИФА для определиния гликокалицина
8 Определение ТААТ IgG с помощью прямого РИА.
9 Определение сывороточных антитромбоцитарных антител с помошью непрямого ИФА 1. Прикрепление тромбоцитов отца/матери к пластику 2. Инкубация тромбоцитов отца/матери с исследуемой сывороткой 3. Добавление Рох-АТ 4. Добавление хромогенного субстрата.
10 Результаты. Был проведен «сэндвич» ИФА для определения концентрации гликокалицина, чтобы убедиться в иммунном генезе тромбоцитопении. РИА, чтобы выяснить количество ТААТ. ИФА на адсорбированных тромбоцитах для определения аллоиммунной тромбоцитопении.
13 Результаты пациента 10 Время после забора крови (ч) ЭДТАцитрат Na WBC (тыс.)Plt (тыс.)MPV (у.е)WBC (тыс.)Plt (тыс.)MPV (у.е) цитрат Na ЭДТА 0ч ЭДТА 2ч ЭДТА 4ч
14 Выводы. Представленные в работе методы позволяют диагностировать пациентов без болезненного вмешательства, например, пункций костного мозга.
15 Сниженное концентрация гликокалицина в крови указывает на недостаточную пролиферацию тромбоцитов в костном мозге. Повышенное количество ТААТ является признаком иммунного происхождения тромбоцитопении. При неонатальной аллоиммунной ТП антитела матери действуют против тромбоцитов в плазме отца (которые идентичны тромбоцитам детей). Измерения лучше всего проводить сразу после забора крови, чтобы избежать образования агрегатов в ЭДТА.
16 Благодарю: Ольгу Александровну Антонову и Светлану Георгиевну Хаспекову за активную помощь в проведении работы. Парнеса Евгения Яковлевича за рецензию на данную работу. Глаголева Сергея Менделевича за предоставленную возможность провести научную работу.
Антитела к тромбоцитам
Определение в крови антител к антигенам тромбоцитов, используемое для дифференциальной диагностики геморрагического синдрома и тромбоцитопении.
Антитела к гликопротеинам тромбоцитов, антитела при идиопатической тромбоцитопенической пурпуре.
Синонимы английские
Anti-platelet antibodies, Platelet Abs.
Непрямая реакция иммунофлюоресценции.
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Антитела к тромбоцитам могут быть обнаружены при многих заболеваниях, в том числе при идиопатической тромбоцитопенической пурпуре, аллоиммунной тромбоцитопении новорождённых, системной красной волчанке (СКВ), бактериальных и вирусных инфекциях (ВИЧ, инфекционный мононуклеоз, сепсис), а также при приеме некоторых лекарственных средств. В настоящий момент описано несколько антигенов-мишеней для этих антител, в том числе гликопротеины GPIIb/IIIa, GPIb/IX, GP5 и рецептор тромбопоэтина.
Наличие антител к тромбоцитам связано как с количественными, так и с качественными изменениями тромбоцитов. С одной стороны, взаимодействие антител с антигенами приводит к разрушению тромбоцитов клетками ретикулоэндотелиальной системы в селезенке (и в меньшей степени в печени) и возникновению тромбоцитопении. С другой стороны, антитела, блокирующие гликопротеины тромбоцитов, нарушают процесс дегрануляции и адгезии тромбоцитов, в результате чего развивается тромбоцитопатия. Клиническим проявлением тромбоцитопении и тромбоцитопатии является повышенная кровоточивость разной степени выраженности – от незначительной петехиальной сыпи до обширного внутримозгового кровоизлияния.
Ведущее значение в диагностике заболеваний, протекающих с геморрагическим синдромом, принадлежит лабораторным методам. Антитела к тромбоцитам – один из тестов, входящих в алгоритм дифференциальной диагностики геморрагического синдрома. Этот тест имеет особое значение в следующих клинических ситуациях:
Следует отметить, что исследование на антитела к тромбоцитам не является рутинным тестом при подозрении на идиопатическую тромбоцитопеническую пурпуру, что связано в основном с его недостаточной специфичностью в отношении этого заболевания.
В настоящее время исследование на антитела к тромбоцитам – это дополнительный метод диагностики геморрагического синдрома и тромбоцитопении. Результат анализа оценивают с учетом данных других лабораторных исследований, в первую очередь коагулограммы.
Для чего используется исследование?
Когда назначается исследование?
Что означают результаты?
Титр: Положительный результат:
Что может влиять на результат?
Кто назначает исследование?
Гематолог, терапевт, врач общей практики.
Литература
Подписка на новости
Оставьте ваш E-mail и получайте новости, а также эксклюзивные предложения от лаборатории KDLmed
Тромбоцит: и друг, и враг
Молекулы клеточной адгезии
Тромбоциты образуются в костном мозгу в результате фрагментации мегакариоцитов, и после выхода в сосудистое русло примерно 2/3 этих кровяных пластинок циркулирует в кровотоке в течение 7-10 дней. Примерно треть из них не примет участия в процессах остановки кровотечения или внутрисосудистого тромбообразования и будет выведена из кровотока путем естественного фагоцитоза макрофагами селезенки и печени. Циркулирующие тромбоциты в нормальных условиях не взаимодействуют с внутренней поверхностью сосуда, покрытой атромбогенным слоем эндотелиальных клеток. При повреждении сосудистой стенки обнажаются компоненты, расположенные под эндотелием, способные вызвать активацию тромбоцитов и их прилипание к образовавшемуся просвету. Вследствие этого кровяные пластинки быстро прикрепляются к поврежденному участку. Основными субстратами, к которым прикрепляются тромбоциты, являются волокна коллагена, входящие в состав сосудистой стенки, и фактор Виллебранда, сорбирующийся из крови к поврежденной поверхности. Одновременно с прикреплением тромбоцитов происходит их активация и затем склеивание друг с другом, то есть агрегация. Именно такие агрегаты и составляют основу тромбоцитарного тромба, который впоследствии закрепляется и стабилизируется нитями фибрина.
Процессы прикрепления клеток друг к другу и к компонентам соединительнотканного матрикса принято объединять общим термином «клеточная адгезия». Она обеспечивается специальными клеточными рецепторами, получившими название молекул клеточной адгезии. Эти молекулы по своей структуре являются мембранными гликопротеидами, расположены они на поверхности клеток и обладают способностью к избирательному взаимодействию с белками (лигандами или контррецепторами) на поверхности других клеток или адгезивными («липкими») белками соединительной ткани и плазмы крови. Молекулы клеточной адгезии тромбоцитов обеспечивают протекание начальных стадий процесса тромбообразования.
Большинство исследований проводится с применением иммунохимических методов, для разработки которых были использованы полученные в нашей лаборатории моноклональные антитела против мембранных белков тромбоцитов. Обратной, патологической стороной защитной реакции гемостаза является внутрисосудистое тромбообразование. В этом случае накопление тромбоцитов и фибрина происходит в зоне патологического повреждения сосудистой стенки, чаще всего в результате образования атеросклеротической бляшки, без нарушения целостности сосуда, то есть в отсутствие кровотечения. Образование такого внутрисосудистого тромба может приводить к окклюзии сосуда и в зависимости от локализации тромба клинически выражаться в развитии таких опасных заболеваний, как инфаркт миокарда, инсульт, тромбоз сосудов ног и другие. Наследственные патологии тромбоцитов, связанные с нарушением реакций адгезии и агрегации, составляют до 30 проц. от числа всех наследственных заболеваний гемостаза. Таким образом, общее число больных с наследственными тромбоцитопатиями превышает число пациентов с такими известными наследственными нарушениями гемостаза, как гемофилия и болезнь Виллебранда.
Трудности в диагностике
Однако диагностика многих патологий тромбоцитов может вызывать затруднения даже у опытных врачей. Больным с наследственными тромбоцитопатиями часто неверно выставляют диагноз аутоиммунной тромбоцитопении. Такие ошибки обусловлены сходством клиники геморрагического синдрома и тем, что в ряде случаев наследственные патологии тромбоцитов сопровождаются умеренной тромбоцитопенией или изменениями размеров и морфологии тромбоцитов, затрудняющими их подсчет. В результате больные могут необоснованно получать лечение глюкокортикоидными гормонами, а иногда проводится спленэктомия, которая в связи с нарушениями функциональной активности тромбоцитов осложняется тяжелыми кровотечениями.
Наличие у пациентов умеренной тромбоцитопении в сочетании с выраженным геморрагическим синдромом должно настораживать врачей и заставлять проводить дифференциальную диагностику между иммунной тромбоцитопенией и наследственными тромбоцитопатиями. Чаще всего для постановки правильного диагноза бывает достаточно определить агрегационную способность тромбоцитов при действии различных индукторов и провести исследования тромбоцитов с помощью световой микроскопии для оценки размера и морфологических особенностей. С клинической точки зрения важным является подробный анамнез заболевания, в частности такие факты, как проявление геморрагического синдрома с детского возраста, повышенная кровоточивость у родителей и других родственников, что может указывать на наследственный характер патологии. Для подтверждения диагноза иммунной тромбоцитопении важно провести определение антитромбоцитарных антител и проконтролировать ответ больных на действие кортикостероидов.
Ключевая роль в процессе агрегации тромбоцитов принадлежит комплексу гликопротеидов IIb-IIIa мембраны тромбоцитов. Этот белок относится к семейству интегринов и является рецептором фибриногена. Уникальной особенностью этого рецептора является то, что он приобретает способность к связыванию фибриногена только при активации тромбоцитов в зоне повреждения сосуда. Молекула фибриногена имеет симметричную структуру и, взаимодействуя одновременно с двумя молекулами гликопротеида IIb-IIIa, может образовывать молекулярные «мостики» между активированными тромбоцитами, обеспечивая, таким образом, прикрепление тромбоцитов друг к другу и их агрегацию.
На сегодняшний день наиболее эффективный способ ингибирования агрегации связан именно с блокированием рецепторной функции гликопротеида IIb-IIIa. В связи с тем, что взаимодействие фибриногена с этим белком является конечной стадией любого пути активации тромбоцитов, блокаторы гликопротеидов IIb-IIIa ингибируют агрегацию, запускаемую любыми появляющимися в кровотоке активаторами тромбоцитов.
Антитела к тромбоцитам, метод нРИФ в Москве
Тест предназначен для исследования уровня тромбоцитов и геморрагического синдрома. Проводится методом непрямой иммунофлюоресценции (нРИФ).
Приём и исследование биоматериала
Когда нужно сдавать анализ Антитела к тромбоцитам, метод нРИФ?
Дифференциальная диагностика тромбоцитопении
Подробное описание исследования
Тромбоциты (или кровяные пластинки) представляют собой мелкие диски диаметром от 1 до 4 мкм. Они образуются в красном костном мозге из мегакариоцитов—крупных клеток, которые фрагментируются на мелкие пластинки в костном мозге. Тромбоциты служат для нормального свертывания крови и предупреждения кровопотери.
Антитела(АТ) к тромбоцитамили аутоантитела – это специфические молекулы – иммуноглобулины (Ig), большая часть которых относится к классу IgG, меньшая часть – к IgМ и IgА. Они связываются с другими соединениями (антигенами) на поверхности тромбоцитов и приводят к их разрушению. Это объясняет снижение числа данных клеток в крови у пациентов c такими заболеваниями, как, например, идиопатическая тромбоцитопеническая пурпура и аллоиммунная тромбоцитопения плода и новорожденного.
Существует более 20 тромбоцит-специфичных молекул, т.е. молекул, которые можно обнаружить только в составе тромбоцитов. При аутоиммунных заболеваниях они могут быть мишенью для атаки иммунной системы, то есть антигенами, поэтому снижается число тромбоцитов, возникает тромбоцитопения и множество нарушений в организме.
Тромбоцитопенией называют состояния, при которых количество тромбоцитов в крови составляет менее 150 × 109/л. Люди с тромбоцитопенией склонны к кровоточивости, в результате которой во всех тканях тела появляются мелкие точечные кровоизлияния. На коже такого больного видны многочисленные мелкие пурпурные точки, в связи с чем болезнь называют тромбоцитопенической пурпурой.
Тромбоцитопатия–это нарушение свертывания крови из-за дефекта строения тромбоцитов. Даже если их численность остается нормальной, это приводит к нарушению функции этих клеток. Заболевание может быть врожденными или приобретенными, протекать в легкой форме или же стать причиной жизнеугрожающих состояний. Симптомы патологии могут варьироваться от степени её тяжести, но к основным проявлениям относят кровотечения (например, из носа или межменструальные), а также подкожные кровоизлияния. Они могут быть в виде экхимозов («синяков») и петехий (точечных кровоизлияний менее 3-х мм).
Поводом для назначения данного анализа может быть лекарственная тромбоцитопения. Однако она бывает иммунно- и неиммуноопосредованной. В случае аутоиммунной тромбоцитопении, связанной с приемом лекарств, выделяются специфические антитела, направленные против комплексов, образованных некоторыми препаратами (гепарин, хинин, абциксимаб, эптифипатид и др.) и тромбоцитарными белками.
Дифференциальная диагностика геморрагического синдрома и определение АТ к тромбоцитам.
Дифференциальная диагностика необходима для того, чтобы различить причины кровотечений и кровоизлияний. Анализ на АТ к тромбоцитам помогает выявить/исключить аутоиммунную тромбоцитопению в качестве такой причины. Лабораторная диагностика имеет важное значение в установлении правильного диагноза.
Тест на наличие антител к тромбоцитам входят в алгоритмы по дифференциальной диагностике тромбоцитопений. Метод непрямой иммунофлюоресценции (нРИФ) для определения данных антител является наиболее эффективным.
Уровень растворимого гликокалицина что это значит
Ye.V. Blokhina, M.Yu. Lebedeva, N.V. Nudnov, V.V. Samoylenko, O.P. Skamorina, A.V. Filatov
FSBI «Central Clinical Military Hospital» of FSS of the Russian Federation, Moscow
Общая вариабельная иммунная недостаточность (ОВИН) представляет собой наиболее распространенную клинически значимую форму первичного иммунодефицита, частота встречаемости которой колеблется в пределах от 2 до 4 случаев на 100 тыс. населения. Основным патогенетическим звеном развития клинических проявлений ОВИН является значительное снижение или полной отсутствие продукции иммуноглобулинов G (IgG), IgA и/или IgM, сопровождающееся дефектом образования антител. В отличие от многих генетически обусловленных первичных иммунодефицитов пик заболеваемости приходится на молодой трудоспособный возраст (20–40 лет). Актуальность проблемы ОВИН определяется поздней диагностикой (как правило, через 6–8 лет после манифестации первых клинических проявлений), высокой частотой развития различных осложнений, госпитализаций и необходимостью пожизненной дорогостоящей заместительной терапии препаратами иммуноглобулина человека [1]. К сожалению, заместительная терапия позволяет лишь снизить риск развития острых бактериальных инфекций, в то время как лечение других многообразных клинических проявлений ОВИН, определяющих качество жизни и прогноз пациентов, до настоящего времени не разработано. Легочные проявления ОВИН включают рецидивирующие инфекции дыхательных путей и развитие хронического гранулематозного/лимфоидного инфильтративного поражения паренхимы легких. Нередко именно легочные проявления являются первой манифестацией клинической картины ОВИН, задолго предшествующей установлению диагноза [2].
Клинический случай
Пациентка К. 33 лет обратилась в госпиталь с жалобами на слабость, одышку при ходьбе на расстоянии до 200 м, при подъеме на 2-й этаж.
Из анамнеза известно, что впервые возникновение вышеописанных жалоб пациентка относит к 2007 г. В том же году был установлен диагноз саркоидоза легких, внутригрудных лимфатических узлов на основании гистологического исследования биопсированного лимфатического узла. На компьютерной томографии (КТ) органов грудной клетки отмечены увеличенные лимфатические узлы средостения, множественные очаги в обоих легких. От терапии системными глюкокортикостероидами пациентка отказалась, принимала хлорохин и пентоксифиллин курсами по 2 месяца, затем самостоятельно терапию отменяла. При ухудшении состояния указанное лечение возобновлялось вновь с незначительной динамикой со стороны легких по данным КТ.
В январе 2009 г. на коже больной появились неиндуцированные геморрагии, отмечены возникновение кашля, заложенности в грудной клетки. На КТ органов грудной клетки отрицательная динамика.
В анализе периферической крови выявлена тромбоцитопения до 20000 кл/мкл. Миелограмма – пунктат клеточный; состав миелограммы в пределах нормы. Количество мегакариоцитов достаточное, определяются преимущественно неактивные формы. Трепанобиопсия – в трепанобиоптате признаков специфического поражения костного мозга при каком-либо заболевании системы крови не обнаружены. Изменения имеют реактивный генез, могут наблюдаться при аутоиммунных процессах. Выявлены тромбоцитассоциированные антитела – 0,34 нг × 10 9 клеток, 340 % от контроля (норма – до 200 %). Уровень растворимого гликокалицина – 1,1 мкг/мл (норма – 1–4 мкг/мл), 55 % (норма – 50–200 %). Вторичный характер иммунной тромбоцитопении был исключен: антинуклеарный фактор, анти-ДНК, ревматоидный фактор – отрицательные, циркулирующие иммунные комплексы, рANCA, cANCA – в пределах нормы. Таким образом, на основании цитологического и гистологического исследований костного мозга данных за какую-либо форму гемобластоза не получено, характер имеющихся изменений не противоречил диагнозу иммунной тромбоцитопении.
Проведено лечение преднизолоном по 90 мг/сут. На фоне терапии отмечено развитие выраженного ятрогенного синдрома Иценко–Кушинга. На момент выписки в гемограмме тромбоциты 139 тыс. кл/мкл.
С середины июля 2009 г. больная отметила ухудшение самочувствия, появилась лихорадка до 38 °C, усилилась одышка. Была госпитализирована с прежним диагнозом – генерализованный саркоидоз. На КТ органов грудной клетки дальнейшая отрицательная динамика. С учетом нетипичной картины прогрессирования саркоидоза и отсутствия верификации морфологических изменений в легких пациентке была выполнена диагностическая краевая резекция 4-го сегмента левого легкого с удалением лимфоузлов 4-й и 5-й групп. Патогистологическое заключение: признаков туберкулезного воспаления не обнаружено. Картина соответствует лимфопролиферативному заболеванию легких и лимфатических узлов. С учетом этого патогистологические препараты были пересмотрены в ГНЦ РАМН, затем в патологоанатомическом бюро Санкт-Петербурга.
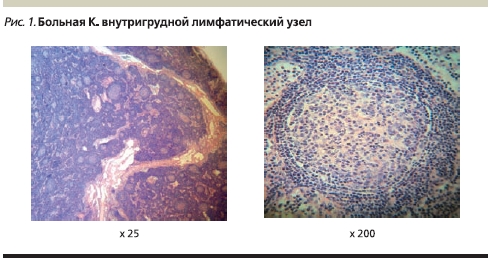
Патогистологическое исследование биоптата внутригрудного лимфатического узла: рисунок строения лимфатического узла сохранен, краевой и промежуточный синусы различимы. Фолликулы с крупными и мелкими светлыми центрами располагаются во всех анатомических зонах. Фолликулы окружены отчетливой зоной мантии. В некоторых местах вокруг фолликулов и перитрабекулярно обнаруживаются незначительные по объему зоны пролиферации моноцитоидных клеток. Межфолликулярные пространства несколько расширены и содержат полиморфную клеточную смесь из мелких и средних лимфоидных клеток, среди них встречаются малочисленные крупные активированные клетки и одиночные мелкие группы гистиоцитов. Гистологическое строение исследованного лимфатического узла соответствует реактивной лимфоаденопатии смешанного типа. Гистологических признаков опухолевого роста в объеме исследованного материала не обнаружено (рис. 1).
При поступлении в госпиталь состояние больной было удовлетворительным. Одышки в покое не отмечено. Аускультативная картина в легких без особенностей, дыхание везикулярное. Среди показателей функции внешнего дыхания отмечено умеренно выраженное снижение проходимости на уровне дистальных отделов бронхов при нормальных показателях объема форсированного выдоха за 1 секунду. Лабораторное обследование, включая показатели полимеразной цепной реакции и иммуноферментного анализа возможных респираторных инфекций, не выявило значимых отклонений от нормы.
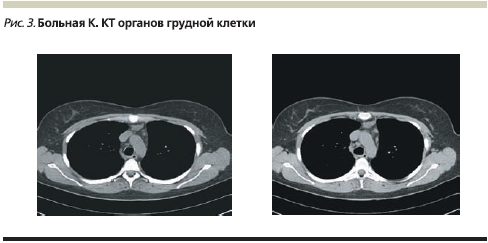
Пациентке выполнена КТ органов грудной клетки: на фоне обогащенного интерстициального компонента по всем легочным полям определяется множество очагов, различных форм и размеров, местами сливающихся между собой. Отмечаются увеличенные лимфатические узлы ретростернальной, паратрахеальной групп (рис. 3).
По данным КТ брюшной полости видимых органических изменений в абдоминальных органах не выявлено.
При бронхоскопии в просвете бронхов определено скудное количество слизистой мокроты. Слизистая оболочка бронхов бледная, с очагами гиперемии и смазанным сосудистым рисунком. Цитология бронхоальвеолярного лаважа (БАЛ): клетки цилиндрического эпителия, альвеолярные макрофаги, элементы воспаления. Посев БАЛ: выявлены Pseudomonasputida10² KOE/мл, Staphylococcusaureus10² KOE/мл, Streptococcusviridans10² KOE/мл. Роста дрожжевых и мицелиальных грибов не получено, Pneumocystis сarinii не обнаружены.
При иммунохимическом исследовании белков сыворотки крови патологических градиентов не выявлено, в т. ч. в иммунофиксации; определен полный дефицит IgA (менее 5 МЕ/мл) и частичный дефицит IgG (52 МЕ/мл).
Таким образом, на основании жалоб, данных анамнеза, объективных данных, результатов лабораторно-инструментального обследования и гистологического заключения установлен клинический диагноз «общая вариабельная иммунная недостаточность: агаммаглобулинемия – полный дефицит IgA, частичный дефицит IgG. Фолликулярный бронхиолит».
Больной проведена заместительная терапия препаратом иммуноглобулинов Интраглобин 25 мл внутривенно капельно. При контрольном иммунохимическом исследовании отмечен подъем уровня IgG до 99 МЕ/мл (в 2 раза от исходного), IgA до 16 МЕ/мл (в 3 раза от исходного).
С учетом необратимости иммунологического процесса, часто рецидивирующих инфекций в дальнейшем рекомендована ежемесячная заместительная терапия препаратами иммуноглобулинов для внутривенного введения по 25 мл на курс.
Обсуждение
Данный клинический случай в очередной раз демонстрирует трудности диагностики диффузных заболеваний легких. Несмотря на то что разработаны различные диагностические алгоритмы, основанные на особенностях клинической картины и определенных рентгенологических паттернах, выявляемых при КТ высокого разрешения и позволяющие существенно сужать спектр диагностического поиска, данная группа поражений легочной ткани, объединенных в первую очередь по принципу сходных рентгенологических изменений и являющихся следствием ряда различных по этиологии патологических процессов, продолжает оставаться серьезной диагностической проблемой [3, 4].
Взаимосвязь между наличием дисгаммаглобулинемии и развитием интерстициальных поражений легких была описана еще в 1973 г. A.A. Liebow и C.B. Carrington [5]. Причины, лежащие в основе поражения легких при ОВИН, до конца не изучены. Предполагается участие в патогенетических механизмах персистирующей вирусной или бактериальной респираторной инфекции, вируса герпеса человека 8-го типа, вируса Эбштейна–Барр, аутоиммунных процессов, изменений активности цитокинов и функции лимфоцитов [1]. Локализованные или диффузные гранулематозные поражения легочной ткани, нередко первоначально ошибочно принимаемые за саркоидоз, наблюдаются среди 8–22 % пациентов с ОВИН. Средний возраст больных составляет 26 (2–59) лет, преобладают женщины. К сожалению, на этом этапе диагностический поиск нередко завершается, диагноз “саркоидоз” считают установленным, и пациенты в течение длительного времени получают специфическую терапию. Нередко помимо легких изменения выявляются также в лимфатических узлах и селезенке. По неустановленной причине у пациентов с гранулематозными поражениями отмечено значительное увеличение риска развития различных аутоиммунных заболеваний (почти во всех случаях аутоиммунной тромбоцитопении или анемии) [1]. Вероятно, это связано с дефектом В-клеточного пула “клеток памяти”, при наличии которого выраженность системных проявлений ОВИН, особенно легочных, существенно увеличивается [6]. У этих пациентов наблюдается развитие интенсивной лимфоидной инфильтрации легочной ткани, сочетающейся с гранулематозными изменениями, что обозначается термином “гранулематозная лимфоцитарная интерстициальная болезнь легких”. При развитии данного типа поражения наблюдается ухудшение прогноза, медиана выживаемости составляет 13,7 года по сравнению с 28,8 года для пациентов без поражения легких [1].
Значительно реже у пациентов с ОВИН наблюдаются лимфопролиферативные изменения в легочной ткани без образования гранулем, связанные с гиперплазией бронхоассоциированной лимфоидной ткани и включающие фолликулярный бронхиолит, диффузную лимфоидную гиперплазию и лимфоцитарную интерстициальную пневмонию. Следует отметить весьма условную доброкачественность течения данных заболеваний, т. к. при прогрессирующем повреждении альвеол они неминуемо приводят к дыхательной недостаточности и необходимости кислородотерапии.
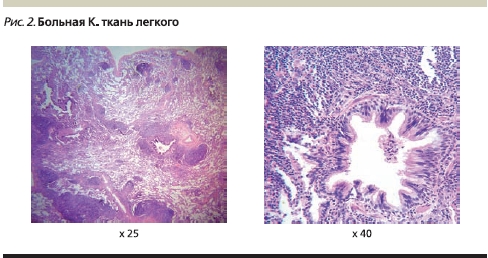
Фолликулярный бронхиолит характеризуется наличием множественных реактивных лимфоидных фолликулов в перибронхиальной или перибронхиолярной зоне, лимфоциты которых несут на себе маркеры В-клеток (CD20, CD79a) [7, 8]. Термин “фолликулярный бронхиолит” был впервые использован в оригинальной работе G.R. Epler и соавт. при описании изменений легких у пациентов с ревматоидным артритом [9]. Надо отметить, что фолликулярный бронхиолит является крайне редким заболеванием. В литературе имеются всего 3 серии наблюдений, включающих 37 пациентов, и серия наблюдений за 5 педиатрическими больными [10], т. е. в совокупности с единичными клиническими наблюдениями к настоящему времени описано не более 50 случаев данного заболевания [11–13], при этом у пациентов с ОВИН описано всего 4 случая [1, 14].
К настоящему времени лечение фолликулярного бронхиолита не разработано. Системная терапия кортикостероидами, как правило, не эффективна. В имеющихся единичных сообщениях имеются данные об умеренной эффективности азатиоприна, циклоспорина и азитромицина [1, 14].
Таким образом, нами представлено первое в России описание случая фолликулярного бронхиолита на фоне ОВИН. Мы полагаем, что у пациентов с наличием ретикулонодулярного рентгенологического паттерна изменений легочной ткани, гранулематозных и лимфоидных изменений, по данным морфологической картины, целесообразно проведение скрининга на наличие иммунодефицита.
Благодарность
Авторы выражают благодарность профессору Ю. Криволапову из Санкт-Петербургского патологоанатомического бюро за неоценимую помощь в установлении морфологического диагноза.