«Золгенсма» поможет не всем?
Почему из-за веса или возраста ребенка могут отказать в введении «Золгенсмы»? Разбираемся в противопоказаниях самого дорогого в мире лекарства
В декабре 2021 года в России был зарегистрирован препарат «Золгенсма» – самое дорогое лекарство в мире, им лечат спинальную мышечную атрофию (СМА).
Теперь российские врачи смогут официально назначать его пациентам, а фонду «Круг добра», созданному государством специально для оплаты редкого и дорогого лечения, будет проще закупать его.
Однако во введении «Золгенсмы» маленькому пациенту могут все равно отказать. Обычно ссылаются на то, что возраст или вес ребенка превышает некие рекомендованные показатели, есть и другие противопоказания. При этом в русскоязычной инструкции к этому препарату, которая уже появилась в сети, среди строгих противопоказаний значится лишь «гиперчувствительность к онасемноген абепарвовеку (действующее вещество. – Ред.) или к любому из вспомогательных веществ». Родители, собиравшие средства в соцсетях и по фондам, не верят, что отказы обоснованы.
Онасемноген абепарвовек (так называется действующее вещество, торговое наименование – «Золгенсма») – первый лекарственный препарат для генной терапии спинальной мышечной атрофии, который выпускает компания Novartis. Известно как самое дорогое лекарство в мире – цена для одного пациента составляет 2,1 млн долларов.
Принцип действия – функциональная копия гена SMN для остановки прогрессирования заболевания. Функциональная копия гена вводится с помощью аденоассоциированного вирус-вектора. Препарат вводится один раз, внутривенно, в течение 60 минут.
Создатели «Золгенсмы» работали над ней 23 года. В 2019 году были представлены результаты клинических исследований с участием 36 пациентов в возрасте от 0,5 до 7,2 месяцев со СМА-1. 33 из них вводили высокую дозу препарата, а троим – низкую. В результате почти все, кто получил высокую дозу «Золгенсмы», в дальнейшем не нуждались в постоянной вентиляции легких, более половины пациентов были способны сидеть без поддержки. Считается, что если бы эти пациенты остались без терапии, выжить смогли бы лишь 8-9 человек. Компания Novartis также вела исследования на пациентах, у которых была диагностирована СМА, но не были выражены симптомы: получив терапию вскоре после рождения, дети научились ходить.
В ходе клинических испытаний умерли два пациента, но установить точную связь их гибели с «Золгенсмой» не удалось.
В 2019-2020 годах препарат был последовательно одобрен к использованию в США, Израиле, Катаре, Японии, Европейском союзе, Бразилии, Канаде, Австралии. В декабре 2021 года состоялась регистрация «Золгенсмы» в России.
Для стран, в которых препарат пока не одобрен или не покрывается за счет той или иной программы государственной поддержки пациентов со СМА, компания Novartis реализует так называемую «программу управляемого доступа». Ежегодно в формате лотереи, посредством случайного выбора 100 бесплатных доз «Золгенсмы» получают пациенты со всего мира. В остальных случаях речь, как правило, идет о благотворительных сборах на лечение «Золгенсмой».
Ограничения по весу ребенка: откуда они взялись и почему рекомендованный вес вырос?
Ограничения по весу разные у разных регистрирующих органов.
Европейская инструкция шире – здесь расчет дозы сделан до 21 килограмма (это вес 5-6 летнего ребенка).
Разница почти в два раза!
Показатель «до 21 кг» содержится и в новой русскоязычной инструкции к «Золгенсме». Такой же показатель был прописан в российском документе «Консенсус в отношении генозаместительной терапии для лечения спинальной мышечной атрофии». Эта научная статья коллектива авторов, среди которых видные неврологи, была опубликована в начале 2021 года, и на нее, в частности, до недавнего времени опирался благотворительный фонд «Круг добра» при анализе обращений пациентов со СМА. Надо отметить, что «Консенсус» устанавливал более узкие рамки, чем новая русскоязычная инструкция. После регистрации «Золгенсмы» в России «Круг добра» пересмотрел свои критерии, они расширились.
Тут надо понимать, что в клинических исследованиях, которые компания Novartis опубликовала в 2019 году (до того, как препарат был одобрен контролирующими органами разных стран) принимали участие всего 36 пациентов, весом до 8,6 кг. Уже после регистрации лекарства в США появился и опыт применения лекарства у детей весом более 13 кг. А в марте 2021 года Novartis объявила, что терапию «Золгенсмой» прошло более тысячи детей. Можно ожидать, что, опираясь на эти данные, критерии веса в ближайшее время могут пересмотреть.
В российской инструкции отмечено, что отсутствуют данные по эффективности и безопасности препарата у пациентов старше 2 лет и весом более 13,5 кг.
Значит, вся проблема в том, что пока просто не набран достаточный материал для исследований?
Глава фонда «Семьи СМА» Ольга Германенко подчеркивает, что критерий веса никак не может быть главным и единственным для лечения СМА у конкретного пациента. «Нельзя рассуждать в духе «Этот ребенок весит 12 килограммов, значит «Золгенсма» ему подходит. Состояние пациента всегда важно оценить в комплексе, ориентироваться на целый комплекс факторов. Ведь специалист лечит живого человека, а не цифры на бумажке».
Возраст: об эффективности «Золгенсмы» для детей постарше нет данных
Критерий возраста присутствует в американских рекомендациях: младше двух лет. В инструктивном описании «Золгенсмы», одобренном FDA (Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США), лекарство называется педиатрическим. «Золгенсма – это генная терапия на основе вектора аденоассоциированного вируса, предназначенная для лечения пациентов младше 2 лет со спинальной мышечной атрофией», – написано в инструкции. Однако в описании препарата нет фразы: «запрещен после такого-то возраста», как это бывает с другими лекарствами.
При этом страховые компании США устанавливали еще более жесткие требования, отказываясь оплачивать лечение «Золгенсмой» для больных старше шести месяцев, часто мотивируя это тем, что по более старшим детям пока нет данных об эффективности.
Получается, что критерий – не противопоказания, а целесообразность расходов (немалых).
В случае отказов «по возрасту» родители пытаются сами собрать на лечение, и иногда это удается. Так, например, юной американке Элиане Леви провели лечение уже после двухлетнего возраста. Диагноз Элиане был поставлен слишком поздно, возраст приближался к критическому, страховые компании семье отказали, зато помог благотворительный фонд «Хесед» – краудфандинговая платформа для ортодоксальной еврейской общины. Два миллиона долларов – такова цена «Золгенсмы» – были собраны за рекордные пять дней. Лечение прошло в 2019 году, однако узнать что-либо о его результатах не представляется возможным: после завершения сбора семья удалила все профили в социальных сетях.
Европейский подход исключает возрастной ценз, здесь важнее вес пациента и другие факторы. Профессор педиатрии Оксфордского университета Лоран Сервэ, который считается одним из ведущих в мире специалистов по СМА, обосновывает важность возрастного критерия также отсутствием данных об эффективности для более старших детей. «Для пациентов старше полугода данных об эффективности препарата нет», – говорил Сервэ в интервью 2020 года и уточнял, что, по его данным, у пациентов, которым вводили «Золгенсму» в возрасте семи месяцев, не происходило развития моторных навыков.
В России же до сих пор отбор по возрасту был еще строже. Для оплаты препарата через фонд «Круг добра» пациенту со СМА-1 должно быть не больше шести месяцев, со СМА-2 – 12 месяцев, и лишь пациентами со СМА-3 не ставили ограничений по возрасту.
Критерий возраста был отменен в России 9 декабря 2021 года. В материалах, которые экспертный совет фонда «Круг добра» опубликовал на своем сайте, указано, что ограничением для применения «Золгенсмы» теперь может быть вес выше 21 килограмма, нахождение пациента на ИВЛ более 16 часов в день в течение более чем 14 дней, наличие гастростростомы или назогастрального зонда или нарушенного глотания, а также наличие у пациента антител к адевирусу, который содержится в «Золгеснме». Возраст среди ограничений вообще не упоминается.
Отметим, что случаи введения препарата «возрастным пациентам» – так принято называть детей со СМА, которые превышают установленные возрастные критерии – известны и изучаются. Правда, речь идет о самостоятельном сборе денежных средств.
Недоношенность, парагрипп, проблемы с печенью: отказ из соображений безопасности
Существуют также относительные противопоказания к генной терапии «Золгенсмой». Это означает, что некоторые из этих факторов могут быть со временем устранены, и препятствие к введению препарата исчезнет.
Одно из таких противопоказаний – недоношенность пациента, в этом случае требуется дождаться, когда ребенок достигнет своего гестационного возраста. Например, если он был рожден на два месяца раньше срока, вводить препарат можно будет лишь после даты, в которую ребенок в норме должен был появиться на свет. Применение «Золгенсмы» у недоношенных детей сразу после рождения может быть небезопасно. Во-первых, о такой терапии нет данных. Кроме того, у рожденных раньше срока чаще и дольше, чем у других малышей, сохраняется повышенный биллирубин (так называемая «желтуха новорожденных»), а значит, страдает печень, нагрузка на которую после введения «Золгенсмы» увеличится.
Еще одним серьезным препятствием может быть наличие у пациента респираторно-синцитиального вируса (РСВ) или парагриппа. Часто такие заболевания свойственны именно новорожденным и в комбинации с «Золгенсмой» могут иметь фатальные последствия: так, во время клинических испытаний препарата один ребенок с диагностированным РСВ умер после введения препарата.
Есть ситуации, когда надо взвесить баланс между потенциальной пользой от терапии и вредом, который «Золгенсма» может нанести детскому организму. Среди побочных эффектов, которые проявляются уже после лечения, могут быть различные реакции печени, а также случаи развития тромботической микроангиопатии (ТМА) – острого и угрожающего жизни состояния, которое характеризуется тромбоцитопенией, гемолитической анемией и остро возникшим поражением почек. В связи с этим пациентам нужно до введения «Золгенсмы» сдать целый ряд анализов на различные показатели крови и ферменты печени. Если состояние ребенка по этим пунктам будет признано неудовлетворительным, в терапии может быть отказано из соображений безопасности.
В «Золгенсме» есть аденовирус. Что делать, если у ребенка сформировался к нему иммунитет?
Действительно, перед тем, как производить лечение препаратом генной терапии, требуется сдать кровь на антитела к аденовирусу AAV9, который служит вектором, проникающим в клетки и доставляющим замену отсутствующего или дефектного гена SMN1 на его функциональную копию. В случае, если в крови пациента обнаружатся антитела к данному аденовирусу, лечение может быть отложено, или последует отказ. Наличие антител говорит об иммунитете к вектору, а значит, дорогостоящее лечение может быть бесполезно.
«Такие случаи редко, но бывают, – комментирует глава фонда «Семьи СМА» Ольга Германенко. – Как правило у пациентов более старшего возраста выше риск обнаружить антитела к аденовирусу, но и у самых маленьких пациентов иногда находят антитела. У нас в России были случаи, когда антитела выявлены, но они были не собственные, а материнские. На фоне прекращения кормления грудью эти антитела через какое-то время пропадают. Одного такого пациента из-за наличия антител сначала не включили в клиническое исследование, но затем мама завершила грудное вскармливание, и ситуация разрешилась благополучно».
Если слишком много нейронов погибло, «Золгенсма» не подействует. Кажется, это и есть самое важное ограничение
Вопреки репутации, которая уже успела сформироваться вокруг самого дорогого лекарства в мире, оно далеко не всегда способно совершить чудо. Пациентам, у которых симптомы СМА уже выражены, откат велик, «Золгенсма» не поможет вернуть утраченные навыки.
Именно поэтому критериями, по которым в России могут отказать пациентам в применении «Золгенсмы», являются потребность в вентиляции легких более 16 часов в сутки в течение 14 суток и долее, постановка гастростомы и отсутствие функции глотания, паралич большей части тела. Такие требования были сформулированы в «Консенсусе в отношении генно-заместительной терапии для лечения спинальной мышечной атрофии», и они, в отличие от критериев веса и возраста, вряд ли будут пересмотрены в ближайшее время.
По словам главного внештатного детский специалиста по медицинской генетике Минздрава РФ Сергея Куцева, ни один генно-заместительный препарат, и «Золгенсма» тоже, не достигает 100% клеток (в случае со СМА – мотонейронов, которые отвечают за движение). Однократная инъекция позволяет генной конструкции попасть примерно в 50% клеток, которые сейчас живы. Оставшиеся не получат поддержки и погибнут.
Например, у ребенка на ранней стадии СМА живы 600 миллионов нейронов. После использования «Золгенсмы» половина из них останутся живы, но этого будет достаточно для сохранения двигательных навыков у ребенка. А если заболевание зашло далеко, то живыми могут остаться только 10 миллионов клеток. При использовании «Золгенсмы» в этом случае удастся сохранить лишь 5 миллионов ценных клеток, восстановить функции это не поможет.
«Вот почему «Золгенсму» очень важно и эффективно применять только на ранних стадиях. На поздних, к сожалению, это уже не дает такой мощный эффект, и лучше использовать препараты многократного применения», – объясняет Куцев.
В этом случае более эффективной считается терапия «Спинразой» и «Рисдипламом». Их необходимо принимать пожизненно, зато, за счет многократного введения они способны «дотянуться» до гораздо большего числа еще живых клеток и сохранить их.
Почему «Золгенсму» трудно совмещать с другой терапией?
Страховые компании в США, оплачивающие лечение СМА, среди ограничений указывают: пациент, получающий «Золгенсму», не должен до нее принимать иную терапию, например, «Спинразу» или «Рисдиплам», а также комбинацию этих лекарственных средств.
Российский фонд «Круг добра» в своих новых критериях упоминает, что пациент может получать «иные методы патогенетического лечения», но только до того, как пройдет лечение «Золгенсмой». После этого законные представители ребенка должны быть готовы отказаться от «Спинразы» и «Рисдиплама».
«На сегодня действительно нет опубликованных достаточных данных о последовательном или комбинированном применении и безопасности или повышении эффективности при таком подходе, это затрудняет принятие практических решений и врачами и в системами здравоохранения», – объясняет глава фонда «Семьи СМА» Ольга Германенко. По ее словам, практика совмещения препаратов существует, но на усмотрение врачей, которые в некоторых случаях идут на риск.
«Бытует такое мнение, что дети на «Спинразе» и «Рисдипламе» погибают, а на «Золгенсме» не умер никто. К сожалению, и это не так. К большому сожалению, в этом году погиб один из малышей через несколько месяцев после введения «Золгенсмы». Как и в случае со «Спинразой» или «Рисдипламом», мы не можем связывать печальный исход напрямую с действием препарата. К сожалению, иногда болезнь оказывается сильнее самых передовых лекарств», – говорит Ольга Германенко.
В России известно как минимум о трех пациентах, получающих комбинированную терапию в разных вариантах. Есть такие случаи и в мире, часть из этого опыта даже публикуется на ресурсе Pubmed (вот пример такой публикации), но данные, представленные зарубежными учеными, пока малы – в каждой работе исследуется не более 10, а чаще – 5 пациентов, и делать выводы довольно трудно.
«В реальной практике таких пациентов, конечно, больше. Но не все врачи делают публикации и делятся своим опытом. К этому медицинское сообщество пока не готово. У российских врачей в федеральных центрах накоплен какой-то опыт, около 10-15 пациентов, в том числе в области применения «Золгенсмы» после «Рисдиплама» и «Спинразы» и несколько пациентов с применением других препаратов после лечения «Золгенсмой». Но это всегда очень трудный выбор и огромная ответственность. Очень важно, чтобы такие данные собирались, анализировались и публиковались», – говорит Ольга Германенко.
По словам главы фонда «Семьи СМА», принять решение о том, какой именно препарат показан тому или иному ребенку, бывает непросто. У родителей есть свои ожидания, в том числе и обещание чуда, которое закрепилось за «Золгенсмой». Врачи в свою очередь должны взвесить все за и против и понять, какое из трех возможных лекарств будет наиболее эффективным.
Мешает и финансовый момент.
«Мы не уникальны, похожим образом обстоит дело в Европе, во многих других странах. И это сложно, потому что если врач и пациент ошиблись в выборе терапии, и вдруг «Золгенсма» не показала того эффекта, на который рассчитывали, то большой вопрос, кто впоследствии будет оплачивать другой препарат», – объясняет Ольга Германенко.
Кто в России принимает окончательное решение об использовании «Золгенсмы»? Что делать, если отказали?
Самостоятельно назначить своему ребенку «Золгенсму» невозможно: это рецептурный препарат, и решение о необходимости такого лечения принимает врачебная комиссия – региональная (после того, как препарат был зарегистрирован в России, этого должно быть достаточно) или федеральная. Федеральный консилиум может понадобиться в случае, если в регионах недостаточно специалистов, способных на экспертизу по редким заболеваниям, к которым в том числе относится спинально-мышечная атрофия.
На основе заключения врачебной комиссии через региональный Минздрав направляется заявка в фонд «Круг добра», который и закупает «Золгенсму». Препарат при этом поступает не в руки родителям больного ребенка, а в медицинский центр, который готов обеспечить введение «Золгенсмы» и контроль за состоянием здоровья пациента. Без этого звена лечение в России также невозможно.
Если «Круг добра» отказывает в применении «Золгенсмы», родители детей со СМА часто начинают самостоятельный сбор средств, и могут преуспеть в этом. Важно понимать, что и в этом случае будет необходимо заручиться поддержкой медиков, готовых провести инфузию лекарственного препарата и затем наблюдать ребенка. Если в России от этого откажутся все специалисты, придется ехать за границу. Причем не исключено, что медцентр, который поддержит спорное решение родителей, может быть аналогичным тем, кого в онкологии называют «торговцами последней надеждой».
«Мы видим очень хорошие результаты у детей получивших генную терапию. И очень хочется, чтобы больше пациентов имели доступ к этой технологии, – говорит Ольга Германенко. – Но есть и обратные случаи. Недавний случай введения препарата ребенку со значительной тяжестью прогрессирования заболевания, которому несколько месяцев отказывали во вливании препарата в разных центрах, чуть не привел к гибели ребенка. После длительной госпитализации в реанимацию и восстановления хотя бы до прежнего состояния ребенок потихоньку восстанавливает силы. Дай Бог, чтобы все у него было хорошо в дальнейшем. При принятии решения о генной терапии должен стоять вопрос не только о потенциально возможном эффекте, но и о возможных рисках в каждом конкретном случае. Сам факт лечения «Золгенсмой» не может рассматриваться как гарантия только выздоровления или значительных улучшений. Ожидания от любого вида терапии должны быть реалистичными и соразмерны реальным возможностям лекарственного препарата».
Мы просим подписаться на небольшой, но регулярный платеж в пользу нашего сайта. Милосердие.ru работает благодаря добровольным пожертвованиям наших читателей. На командировки, съемки, зарплаты редакторов, журналистов и техническую поддержку сайта нужны средства.
Самое дорогостоящее лекарство в мире
Автор
Редакторы
Статья на конкурс «био/мол/текст»: Не так давно, в мае 2019 года, произошло знаковое событие в сфере лечения генетических заболеваний: Управление по санитарному надзору за качеством продуктов и медикаментов США (FDA) одобрило препарат Zolgensma («Золгенсма», или онасемноген абепарвовек). Это лекарственное средство предназначено для генотерапевтического лечения спинально-мышечной атрофии (СМА). Сегодня «Золгенсма» является самым дорогим лекарственным препаратом в мире.
Конкурс «био/мол/текст»-2019
Эта работа опубликована в номинации «Свободная тема» конкурса «био/мол/текст»-2019.

Генеральный спонсор конкурса и партнер номинации «Сколтех» — Центр наук о жизни Сколтеха.
Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.

Спонсором приза зрительских симпатий выступила компания BioVitrum.
Что такое СМА?
Спинально-мышечной атрофией, или СМА, называют смертельно опасное нейродегенеративное заболевание, в процессе развития которого у пациента происходит постепенная атрофия скелетной мускулатуры. В результате человек теряет или так и не приобретает способности ходить, самостоятельно стоять, сидеть без поддержки. Со временем возникает сколиоз и другие ортопедические проблемы. Также СМА-пациенты, если они не получают должного ухода и лечения, постепенно утрачивают способность самостоятельно дышать, глотать, кашлять. Пациенты с первым, самым тяжелым, типом СМА еще несколько лет назад, как правило, не доживали и до двух лет [1].
СМА возникает из-за потери участка хромосомы или точечной мутации гена SMN1, расположенного в пятой хромосоме. В результате этого нарушается синтез SMN-белка, недостаток которого приводит к гибели моторных нейронов и атрофии скелетной мускулатуры [2].
Для того чтобы болезнь проявилась, носителем рецессивной мутации в гене SMN1 должны быть оба родителя. Примерно каждый 40-й житель Земли является таким носителем.
Подробнее о причинах возникновения, диагностике, течении спинально-мышечной атрофии читайте в статье «Надежда для СМАйликов» [3].
Терапия спинально-мышечной атрофии до появления «Золгенсмы»
До недавнего времени методы лечения СМА сводились к поддерживающей терапии. Больным рекомендовали специальное питание, витамины, умеренные физические нагрузки, при необходимости — хирургическое вмешательство, искусственная вентиляция легких. К сожалению, до сих пор значительная часть СМА-пациентов получает лишь такое лечение.
Рисунок 1. «Спинраза» — первый препарат, одобренный для лечения СМА
С 2016 года сначала в США, а затем и в Европе для лечения спинально-мышечной атрофии стали применять препарат «Спинраза» (нусинерсен) [4]. Он позволяет существенно увеличить продукцию полноценного SMN-белка, что ведет к сглаживанию симптомов заболевания. Терапия тем эффективнее, чем меньше возраст пациента.
Стоимость препарата составляет несколько сот тысяч долларов в год, поэтому его закупка осуществляется не за счет пациента. Одна за другой страны разных континентов одобрили препарат и стали применять для спасения жизней своих сограждан. В некоторых государствах этот процесс сильно затянулся из-за бюрократических проволочек и нехватки финансирования.
В РФ «Спинразу» Минздрав одобрил в начале 2019. В свою очередь компания «Биоген», производитель «Спинразы», в апреле 2019 г. объявила об открытии в России «Программы расширенного доступа» для лечения СМА нусинерсеном. Благодаря этой программе доступ к препарату получили 40 детей из России, страдающих СМА I типа [5].
В августе «Спинраза» была включена в Государственный реестр лекарственных средств РФ. Однако охват больных все еще слишком мал. В Российской Федерации зарегистрировано около 800 СМА-пациентов, и далеко не все они получают инъекции «Спинразы».
Отличия «Золгенсмы» от «Спинразы»
После появления на фармацевтическом рынке «Спинразы» все ждали выхода принципиально нового препарата для лечения СМА, основанного на генотерапевтическом подходе. Лидером в данной разработке оказалась компания «Новартис» (Novartis), которая в 2018 году купила компанию «Авексис» (AveXis) за 8,7 млрд долларов, а в 2019 вышла на рынок c препаратом «Золгенсма» (Zolgensma, он же AVXS-101, или онасемноген абепарвовек) [6].
Рисунок 2. Логотип препарата «Золгенсма»
Чем же «Золгенсма» принципиально отличается от препарата «Спинраза»? Самое важное различие заключается в механизме действия: «Спинраза» исправляет дефект сплайсинга матричной РНК гена SMN2, но она никак не затрагивает ген SMN1, мутации в котором и являются основной причиной развития спинально-мышечной атрофии.
Действие же препарата «Золгенсма» направлено именно на ген SMN1. Благодаря использованию этого лекарственного средства, мутировавший или отсутствующий ген SMN1 замещается функционально полноценным геном [1].
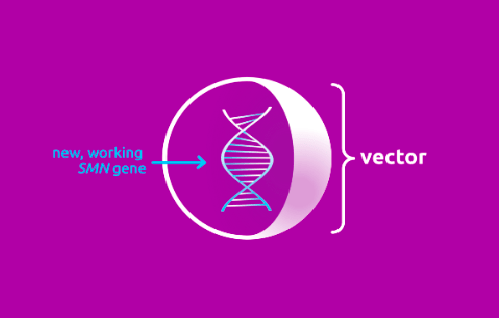
Происходит это следующим образом: препарат содержит функционально полноценный ген SMN1, который находится внутри вектора. Задача вектора — быстро доставить его в мотонейроны тела (рис. 3).
Рисунок 3. Условное изображение вектора, входящего в состав «Золгенсмы»
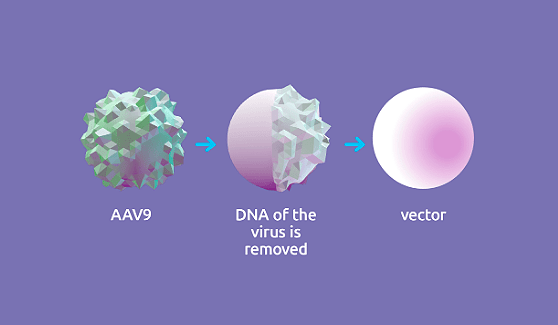
Для создания вектора использовали аденоассоциированный вирус (adeno-associative virus 9, или AAV9). Это представитель семейства парвовирусов, который способен инфицировать клетки человека и других приматов, но при этом не является патогенным. Все это делает AAV9 отличным генетическим вектором. Собственный генетический материал вируса удалили и вместо него поместили функционально полноценный ген SMN1 (рис. 4).
Рисунок 4. Условная схема механизма создания вектора
После того, как ген прибывает в нужную локацию, вектор разрушается и выводится из организма.
СМА-пациенту необходима всего одна инфузия препарата «Золгенсма» в течение жизни, в то время как лечение «Спинразой» требует нескольких доз в год. Отсюда и стоимость «Золгенсмы»: 2 125 000 долл. США. Такая ценовая политика компании-производителя делает данный препарат самым дорогим лекарственным средством на сегодняшний день. Для сравнения, стоимость все той же «Спинразы» составляет 125 тыс. долларов за одну дозу. При этом в первый год лечения нужно шесть инфузий, в последующие периоды — три инфузии ежегодно.
Насколько оправдана такая цена препарата и какова же его себестоимость? «Новартис» не афиширует информацию относительно себестоимости «Золгенсмы», поэтому эксперты оценивают стоимость препарата по двум показателям: качество жизни пациента с учетом прожитых лет (QALY) и добавленные годы жизни (LYG). По данным Института клинико-экономической экспертизы (Institute for Clinical and Economic Review, ICER), исходя из показателя QALY стоимость «Золгенсмы» должна быть в пределах 1,1–1,9 миллионов долл. США; исходя из показателя LYG — 1,2–2,1 миллиона долл. США. Таким образом, можно сказать, что стоимость «Золгенсмы» завышена по отношению к оценкам экспертов [7].
При формировании своей ценовой политики компания «Новартис» отталкивалась от стоимости препарата «Спинраза». По задумке производителя в течение десяти лет на лечение СМА-пациента «Спинразой» необходимо будет потратить более 4 млн долларов, в то время как одна инфузия «Золгенсмы» стоит 2 млн 125 тысяч. Таким образом, в долгосрочной перспективе второй вариант более выгоден [8], [9].
Компания «Новартис» ожидала, что «Золгенсма» станет «блокбастером», то есть принесет более 1 млрд долларов за первый год продаж. Однако скандал, который возник вокруг «Золгенсмы», может не дать осуществиться этим планам. Летом 2019 г. компания «Новартис» сама сообщила FDA о манипуляции с данными при проведении тестирования препарата на животных. Если бы эти данные были известны FDA в мае, то разрешение на использование препарата «Золгенсма» «Новартис» получила бы позже, но сейчас принято решение не отзывать препарат [10].
Сумму в два с лишним миллиона долларов не в состоянии заплатить большинство СМА-семей, поэтому предполагается, что пациенты будут обеспечиваться жизненно важным лечением благодаря государственной поддержке или за счет страховых компаний. Кроме того, производитель «Золгенсмы» предоставляет пятилетнюю рассрочку на оплату генной терапии и дает возможность пациенту не выплачивать оставшуюся сумму, если препарат перестанет действовать [8]. Сегодня препарат «Золгенсма» доступен только для жителей США, так как FDA — это единственная организация, которая его одобрила. Также есть ограничения по возрасту и тяжести заболевания: пока препарат применяется только для пациентов до двух лет с первым типом СМА. В дальнейшем производитель планирует использовать препарат и для других групп людей, страдающих спинально-мышечной атрофией.
Важно также отметить, что «Золгенсма» вводится внутривенно. «Спинраза» же должна попасть в спинномозговую жидкость пациента, что создает ряд дополнительных проблем и рисков.
Побочные эффекты «Золгенсмы»
Кроме высокой стоимости, у «Золгенсмы» есть и другие серьезные недостатки. Возможными побочными эффектами препарата являются:
Не рекомендуется использование «Золгенсмы» у недоношенных детей до достижения ими полного гестационного возраста.
По данным компании-производителя на момент регистрации «Золгенсма» в рамках клинических исследований была применена для терапии 44 детей в возрасте от 0,3 до 7,9 месяцев с массой тела от 3 до 8,4 кг. Такая небольшая выборка объясняется тем, что СМА является редким заболеванием, поэтому набрать большое количество пациентов за короткий период времени — не такая уж и простая задача.
С другой стороны, небольшая выборка означает, что количество побочных эффектов препарата может быть значительно выше, чем известно на данный момент. Так, производитель уведомляет, что один из СМА-пациентов, который участвовал в клинических исследованиях за пределами США, через 12 дней после инфузии препарата начал страдать от дыхательной недостаточности. Также у него были зафиксированы лейкоэнцефалопатия, приступы гипотензии и судорог примерно через месяц после начала лечения. Через 52 дня наступил летальный исход. Но пока сложно сказать, является ли подобное развитие событий реакцией на введение препарата или же эти симптомы появились бы у СМА-пациента и без использования «Золгенсмы».
Важно также отметить, что долгосрочное влияние препарата на организм человека пока неизвестно. Прежде всего, не ясно, будет ли экспрессия гена SMN1 в организме пациента поддерживаться постоянно или постепенно сойдет на нет. Чтобы ответить на этот вопрос, «Новартис» обязана постоянно собирать данные долговременного наблюдения. В разрезе стоимости это является ключевым риском для плательщиков. Компания-производитель пытается снизить эти риски, предлагая рассрочку на пять лет пациентам, с правом приостановить выплаты, если препарат не будет проявлять своего терапевтического действия. Однако если экспрессия гена прекратится после истечения пятилетнего срока, то никакой финансовой компенсации за это не предусмотрено.
Следующий шаг
Компания-производитель «Золгенсмы» планирует в будущем применять препарат для пациентов разных возрастов со СМА II и III типов. Также «Новартис» работает над регистрацией препарата за пределами США.
Рисунок 5. Рисдиплам — препарат для лечения спинально-мышечной атрофии, который находится на стадии клинических испытаний на людях
Появление «Золгенсмы» на фармакологическом рынке повлияло на продажи «Спинразы», поэтому компания «Биоген» уже проводит клинические исследования, направленные на усиление терапевтической активности «Спинразы» путем увеличения ее дозы [11].
Но «Спинраза» и «Золгенсма», возможно, недолго будут единственными препаратами для лечения спинально-мышечной атрофии. Компания «Рош» (Roche) уже достаточно давно ведет клинические испытания своего лекарственного средства (рисдиплама) и, по всей видимости, в ближайшие пару лет данный препарат также выйдет на фармацевтический рынок (рис. 5).
Рисдиплам, как и нусинерсен («Спинраза»), не влияет на ген SMN1, а модифицирует сплайсинг мРНК гена SMN2. Однако у рисдиплама есть существенное отличие: препарат принимается перорально и не требует введения в спинно-мозговую жидкость. Кроме того, рисдиплам подходит для всех типов СМА и в клинических испытаниях показывает более высокую эффективность, чем нусинерсен [12].
По прогнозам экспертов, цена препарата будет значительно ниже, чем «Спинразы» и «Золгенсмы», поэтому новое средство сможет составить серьезную конкуренцию уже существующим лекарствам [8].
Уже в конце 2019 года компания Roche планирует подать документы на одобрение препарата в FDA и EMA (Европейское медицинское агентство) [13].
Сегодня «Золгенсма» является одним из немногих одобренных генотерапевтических препаратов, и единственный — для лечения СМА. Данная технология является чрезвычайно перспективной и теоретически может подарить шанс СМА-пациентам на продолжительную жизнь высокого качества. Однако возможные побочные эффекты и высокая стоимость препарата пока не позволяют делать поспешных радужных выводов.