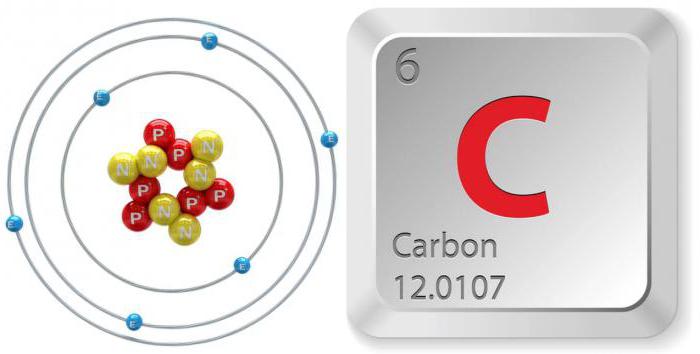
УГЛЕРОД
В этой книге слово «углерод» встречается довольно часто: в рассказах о зелёном листе и о железе, о пластмассах и кристаллах и ещё во многих других. Углерод — «рождающий уголь» — один из удивительнейших химических элементов. Его история — это история возникновения и развития жизни на Земле, потому что он входит в состав всего живого Земли.
А как выглядит углерод?
Сделаем несколько опытов. Возьмём сахар и нагреем его без доступа воздуха. Он сначала расплавится, станет коричневым, а потом почернеет и превратится в уголь, выделив воду. Если теперь нагреть этот уголь в присутствии КИСЛОРОДА, он сгорит без остатка и превратится в УГЛЕКИСЛЫЙ ГАЗ. Стало быть, сахар состоял из угля и воды (сахар, кстати, и называют углеводом), а «сахарный» уголь — это, видимо, и есть чистый углерод, потому что углекислый газ — это соединение углерода с кислородом. Значит, углерод — чёрный, мягкий порошок.
Возьмём серый мягкий камень графит, хорошо тебе знакомый благодаря карандашам. Если его нагреть в кислороде, он тоже сгорит без остатка, хотя и немного медленней, чем уголь, а в приборе, где он горел, останется углекислый газ. Значит, графит тоже чистый углерод? Конечно, но и это ещё не всё.
Если в том же приборе в кислороде накалить алмаз, прозрачный сверкающий драгоценный камень, самый твердый из всех минералов, он тоже сгорит, превратившись в углекислый газ. Если же нагревать алмаз без доступа кислорода, он превратится в графит, а при очень высоких давлениях и температурах можно из графита получить алмаз.
Итак, уголь, графит и алмаз — это различные формы существования одного и того же элемента — углерода.
Ещё более удивительна способность углерода «принимать участие» в огромном количестве разнообразных соединений (поэтому-то слово «углерод» так часто встречается в этой книге).
104 элемента периодической системы образуют более сорока тысяч изученных соединений. А соединений, основу которых составляет углерод, уже известно свыше миллиона!
Причина такого разнообразия заключается в том, что атомы углерода могут соединяться между собой и с другими атомами прочной связью, образуя сложные МОЛЕКУЛЫ в виде цепей, колец и других фигур. Ни один элемент в таблице МЕНДЕЛЕЕВА, кроме углерода, не способен на это.
Углерод: физические и химические свойства
Содержание:
Углерод – важнейший химический элемент периодической таблицы Менделеева. Без него, как и без кислорода и водорода немыслимой была бы сама Жизнь. Можно без преувеличения сказать, что жизнь всех живых существ от амебы до человека построена именно из соединений углерода. Углерод – биогенный элемент составляющий основу жизни на нашей планете. Будучи структурной единицей огромного числа различных органических соединений, он участвует и в построении живых организмов и в обеспечении их жизнедеятельности. Даже возникновение самой Жизни рассматривается учеными как сложный процесс эволюции углеродных соединений. А какие химические и физические свойства этого чудесного элемента, история его открытие и современное применение в химии, читайте об этом далее.
История открытия
На самом деле углерод был известен человеку еще с глубокой древности в виде своих аллотропных модификаций: алмаза и графита. Помимо этого углерод в виде древесного угля активно применялся при выплавке металлов. От угля происходит и само название углерода, как химического элемента.
Но в те далекие времена люди пользовались углеродом в виде угля, или любовались им же, в виде алмазов, неосознанно, без понимания того, какой важный химический элемент стоит за всем этим.
Научное открытие углерода произошло в 1791 году, когда английский химик Теннант впервые получил свободный углерод. Для получения углерода он пропускал пары фосфора над прокаленным мелом. В результате этой химической реакции образовались фосфат кальция и чистый углерод. Впрочем, этому опыту предшествовали и другие искания, например выдающийся французский химик Лавуазье поставил опыт по сжиганию алмаза при помощи большой зажигательной машины. Драгоценный алмаз сгорел без остатка, после чего ученый пришел к выводу, что алмаз представляет собой ничто иное как кристаллический углерод.
Интересно, что в этих опытах совместно с алмазом пробовали сжигать и другие драгоценные камни, к примеру, рубин. Но другие камни выдерживали высокую температуру, только алмаз сгорал без остатка, что и обратило внимание на его отличную химическую природу.
Место в таблице Менделеева
В основе расположения химических элементов в периодической системе Менделеева лежит их атомный вес, рассчитанный относительно атомного веса водорода. Атомная масса углерода составляет 12,011, согласно ней он занимает почетное 6-е место в таблице Менделеева и обозначается латинской литерой С.
Помимо этого следует обратить внимание на следующие характеристики углерода:
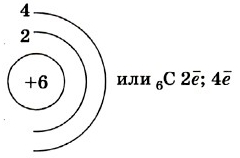
Строение атома
Так на картинке изображена схема электронного строения атома углерода.
Физические свойства
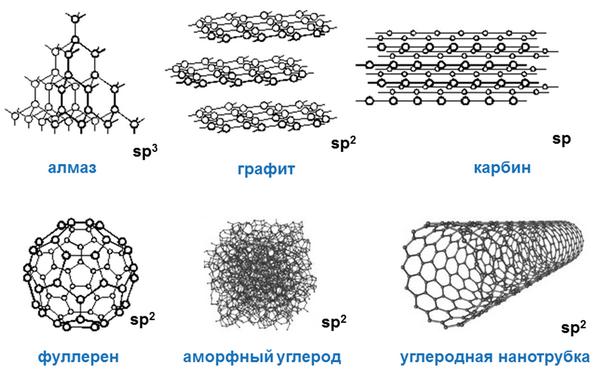
Своими физическими свойствами углерод типичный неметалл. При этом он образует множество аллотропных модификаций («аллотропные» означает существование двух и более разных веществ из одного химического элемента): наиболее популярными из них являются алмаз, графит, уголь, сажа. При этом алмаз – одно из самых твердых веществ, представляющих углерод.
Разумеется, разные аллотропные модификации углерода имеют и разные физические свойства. Если алмаз типичное твердое тело, то, к примеру, жидкий углерод, который можно получить только при определенном внешнем давлении, обладает совершенно иными физическими свойствами, нежели алмаз или графит.
Химические свойства
В обычных условиях углерод, как правило, химически инертен, но при высоких температурах он может вступать в химические взаимодействия со многими другими элементами, обычно проявляя сильные восстановительные свойства. Приведем примеры химических реакций углерода как восстановителя с:
— с кислородом
C 0 + O2 – t° = CO2 углекислый газ
при недостатке кислорода — неполное сгорание:
2C 0 + O2 – t° = 2C +2 O угарный газ
— с водяным паром
C 0 + H2O – 1200° = С +2 O + H2 водяной газ
— с оксидами металлов. Таким образом, выплавляют металл из руды.
C 0 + 2CuO – t° = 2Cu + C +4 O2
— с серой образует сероуглерод:
С + 2S2 = СS2.
Порой углерод может выступать и как окислитель, образуя карбиды при вступлении в химические реакции с некоторыми металлами:
Вступая в реакцию с водородом, углерод образует метан:
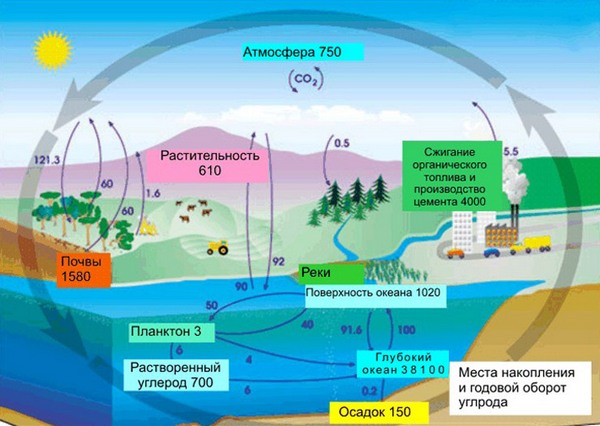
Роль в природе
В земной коре содержание углерода составляет всего лишь 0,15%. Несмотря на эту кажущуюся маленькой цифру, стоит заметить, что углерод непрерывно участвует в природном круговороте из земной коры через биосферу в атмосферу и наоборот. Также именно из углерода состоят такие ценные ресурсы как нефть, уголь, торф, известняки и природный газ. И как мы писали в начале нашей статьи, углерод – основа жизни. Скажем, в теле взрослого человека с весом в 70 кг имеется около 13 кг углерода. Это только в одном человека, примерно в таких же пропорциях углерод содержится в телах всех других живых существ, растений и животных.
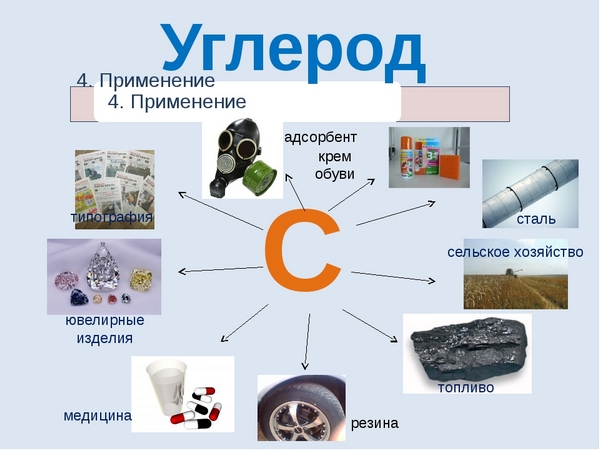
Применение
Можно сказать, что углерод неразрывно связан с самим развитием человеческой цивилизации. Именно из соединений с участием углерода образованы основные топлива, благодаря которым ездят машины, летают самолеты, вы можете приготовить себе еду и обогреть свой дом в холодную пору – это нефть и газ. Помимо этого соединения углерода активно используются в химической и металлургической промышленности, в фармацевтике и строительстве. Алмазы, будучи аллотропной модификацией углерода используются в ювелирном деле и ракетостроении. В целом промышленность современности не может обойтись без углерода, он необходим практически везде.
Рекомендованная литература и полезные ссылки
Видео
И в завершение образовательное видео по теме нашей статьи.
Что такое углерод? Описание, свойства и формула углерода
Кратко рассказать о том, что такое углерод, невозможно. Ведь он – основа жизни. Данный элемент имеется во всех органических соединениях, и только он может формировать молекулы ДНК из миллионов атомов. Его свойства многочисленны, так что о нем стоит рассказать поподробней.
Формула, обозначения, особенности
Следует отметить, что определенная масса углерода содержится в земной коре. 0,023%, если быть точнее. Главным образом он накапливается в верхней части, в биосфере. Большая часть массы углерода литосферы накапливается в доломитах и известняках, в виде карбонатов.
Физические характеристики
Итак, что такое углерод? Это вещество, которое существует в огромном множестве аллотропных модификаций, и их физические свойства перечислять можно долго. А разнообразие веществ обуславливается способностью углерода к образованию химических связей отличающихся типов.
Что касательно свойств углерода, как простого вещества? Их можно обобщить следующим образом:
Также стоит перечислить углеродные модификации.
Из кристаллических веществ самыми известными являются: алмаз, карбин, графит, наноалмаз, фуллерит, лонсдейлит, фуллерен, а также углеродные волокна.
К аморфным образованиям относится: древесный, ископаемый и активированный уголь, антрацит, кокс, стеклоуглерод, сажа, техуглерод и нанопена.
Но ничто из перечисленного не является чистой аллотропной формой обсуждаемого вещества. Это лишь химические соединения, в которых углерод содержится в высокой концентрации.
Структура
Интересно, что электронные орбитали атома углерода не одинаковы. Они имеют разную геометрию. Все зависит от степени гибридизации. Есть три наиболее часто встречающиеся геометрии:
Не так давно, в 2010 году, ученые из университета, который находится в Ноттингеме, открыли соединение, в котором сразу четыре атома оказались в одной плоскости. Его название – мономерный дилитио метандий.
Молекулы
О них стоит сказать в отдельности. Атомы обсуждаемого вещества могут соединяться, вследствие чего образуются сложные молекулы углерода. От насыщенных Na, С2 и Н2, между которыми слишком слабое притяжение, их отличает склонность конденсироваться в твердое состояние. Молекулы углерода могут оставаться в газообразном состоянии, только если поддерживать высокую температуру. Иначе вещество мгновенно затвердеет.
Некоторое время тому назад в США, в Берклеевской национальной лаборатории, была синтезирована новая форма твердого углерода. Это – С36. И его молекулу образует 36 углеродных атомов. Вещество образуется вместе с фуллеренами С60. Происходит это между двумя электродами графита, в условиях пламени дугового разряда. Ученые предполагают, что молекулы нового вещества обладают интересными химико-электрическими свойствами, которые пока не изучены.
Графит
Теперь можно более подробно рассказать о самых известных модификациях такого вещества, как углерод.
Графит – это самородный минерал со слоистой структурой. Вот его особенности:
Если говорить о химических свойствах, то стоит отметить, что с солями и щелочными металлами это вещество образует так называемые соединения включения. Еще графит при высокой температуре реагирует с кислородом, сгорая до углекислого газа. Но вот контакт с неокисляющими кислотами никакого результата за собой не влечет – это вещество в них просто не растворяется.
Применяют графит в самых разных сферах. Его используют при изготовлении футеровочных плит и плавильных тиглей, в производстве нагревательных элементов и электродов. Без участия графита невозможно получить синтетические алмазы. Также он играет роль замедлителя нейтронов в ядерных реакторах. И, конечно же, из него делают стержни для карандашей, мешая с каолином. И это лишь часть сфер, где он используется.
Алмаз
Это метастабильный минерал, который может существовать неограниченное количество времени, что в некоторой степени обусловлено прочностью и плотностью углерода. Алмаз является самым твердым веществом по шкале Мооса, он легко разрезает стекло.
У него высокая теплопроводность, дисперсия, показатель преломления. Он износостойкий, а чтобы заставить его плавиться, нужна температура в 4000 °C и давление около 11 ГПа. Его особенность – люминесценция, способность светиться разными цветами.
Это редкое, хоть и распространенное вещество. Возраст минералов, согласно данным определенных исследований, может колебаться от 100 миллионов до 2,5 миллиарда лет. Обнаружены алмазы внеземного происхождения, возможно, даже досолнечного.
Этот минерал нашел свое применение в ювелирном деле. Ограненный алмаз, именуемый бриллиантом, стоит дорого, но статус драгоценности и красота сделали его еще более популярным. Кстати, также это вещество используют при изготовлении резцов, сверл, ножей и т. д. Благодаря своей исключительной твердости, минерал применяют во многих производствах.
Карбин
В продолжение темы о том, что такое углерод, нужно пару слов сказать и о такой его модификации, как карбин. Он выглядит как черный мелкокристаллический порошок, обладает полупроводниковыми свойствами. Получен искусственным образом в начале 60-х годов советскими учеными.
Особенность данного вещества заключается в увеличивающейся под световым воздействием проводимости. Именно поэтому его стали применять в фотоэлементах.
Графен
Это первый в мире двумерный кристалл. У данной модификации большая механическая жесткость, чем у графита, и рекордно высокая теплопроводность, составляющая
5•10 3 Вт•м −1 •К−. У носителей заряда графена высокая подвижность, именно поэтому вещество имеет перспективы в плане его использования в разных приложениях. Считается, что он может стать будущей основой наноэлектроники и даже заменить кремний в интегральных микросхемах.
Графен получают искусственно, в научных лабораториях. Для этого приходится прибегать к механическому отщеплению графитовых слоев от высокоориентированного вещества. Так получают образцы высокого качества с необходимой подвижностью носителей.
Его свойства изучены не полностью, но кое-что интересное ученые уже успели отметить. Например, в графене нет вингеровской кристаллизации. А в двойном слое вещества поведение электронов напоминает то, которое свойственно жидким кристаллам. Если соблюсти параметры скалывания на кристалле, удастся получить графеновую коробчатую наноструктуру.
Токсичность
Эту тему стоит отметить в заключение рассказа о том, что такое углерод. Дело в том, что это вещество выделяется в атмосферу вместе с выхлопными газами автомобилей. А еще при сжигании угля, подземной газификации и во многих других процессах.
Повышенное содержание этого вещества в воздухе приводит к увеличению численности заболеваний. В частности, это касается легких и верхних дыхательных путей. А токсическое действие обусловлено взаимодействием радиационного характера с β-частицами, которое ведет к тому, что химический состав молекулы меняется и свойства вещества – тоже.
углерод
Полезное
Смотреть что такое «углерод» в других словарях:
Углерод-14 — Таблица нуклидов Общие сведения Название, символ Углерод 14, 14C Альтернативные названия радиоуглерод, радиокарбон Нейтронов 8 Протонов 6 Свойства нуклида Атомная масса … Википедия
Углерод-12 — Таблица нуклидов Общие сведения Название, символ Углерод 12, 12C Нейтронов 6 Протонов 6 Свойства нуклида Атомная масса 12,0000000(0) … Википедия
Углерод-13 — Таблица нуклидов Общие сведения Название, символ Углерод 13, 13C Нейтронов 7 Протонов 6 Свойства нуклида Атомная масса 13,0033548378(10) … Википедия
УГЛЕРОД — (лат. Carboneum) С, химический. элемент IV группы периодической системы Менделеева, атомный номер 6, атомная масса 12,011. Основные кристаллические модификации алмаз и графит. При обычных условиях углерод химически инертен; при высоких… … Большой Энциклопедический словарь
УГЛЕРОД — (Carboneum), C, химический элемент IV группы периодической системы, атомный номер 6, атомная масса 12,011; неметалл. Содержание в земной коре 2,3?10 2% по массе. Основные кристаллические формы углерода алмаз и графит. Углерод главный компонент… … Современная энциклопедия
Углерод — (Carboneum), C, химический элемент IV группы периодической системы, атомный номер 6, атомная масса 12,011; неметалл. Содержание в земной коре 2,3´10 2% по массе. Основные кристаллические формы углерода алмаз и графит. Углерод главный компонент… … Иллюстрированный энциклопедический словарь
УГЛЕРОД — (1) хим. элемент, символ С (лат. Carboneum), ат. и. 6, ат. м. 12,011. Существует в нескольких аллотропных модификациях (формах) (алмаз, графит и редко карбин, чаоит и лонсдейлит в метеоритных кратерах). С 1961 г. / массы атома изотопа 12С принята … Большая политехническая энциклопедия
УГЛЕРОД — (символ С), широко распространенный неметаллический элемент четвертой группы периодической таблицы. Углерод образует огромное количество соединений, которые вместе с углеводородами и другими неметаллическими веществами составляют основу… … Научно-технический энциклопедический словарь
Углерод — C (a. carbon; н. Kohlenstoff; ф. carbone; и. carbono), хим. элемент IV группы периодич. системы Mенделеева, ат.н. 6, ат. м. 12,041. Природный У. состоит из смеси 2 стабильных изотопов: 12C (98,892%) и 13C (1,108%). Известно также 6… … Геологическая энциклопедия
Углерод — химический элемент, важнейшая составляющая органических веществ. По английски: Carbon Синонимы английские: C См. также: Органические вещества Топливо Финансовый словарь Финам … Финансовый словарь
УГЛЕРОД — 14С, радиоактивный изотоп углерода, имеющий массу ядра, равную 14. Изотоп образуется в углекислом газе под воздействием солнечной радиации в предельно малых, но постоянных количествах. После смерти организма углерод 14 разрушается с постоянной… … Экологический словарь
Углерод
Углерод встречается как:
История
Углеро́д в виде древесного угля применялся в глубокой древности для выплавки металлов. Издавна известны алмаз и графит. Элементарная природа углерода установлена А. Лавуазье в конце 1780-х годов.
Происхождение названия
Международное название происходит от латинского carbo — уголь, связанного с древним корнем kar — огонь. Этот же корень в латинском cremare — гореть, а возможно, и в русском « гарь », «жар», «угореть» (в древнерусском «угорати» — обжигать, опалять). Отсюда — и «уголь».
Содержание
Физические свойства
Углерод существует во множестве аллотропных модификаций с очень разнообразными физическими и химическими свойствами. Разнообразие модификаций обусловлено способностью углерода образовывать химические связи разного типа. Основные физические свойства собственно углерода смотри в таблице.
Изотопы углерода
Аллотропные модификации углерода
Упрощенная фазовая диаграмма углерода, заштрихованы области где аллотропные модификации могут быть метастабильны. (diamond — алмаз, graphite — графит, liquid — жидкость, vapor — газ)

Электронное строение атома углерода
Графит и алмаз
Элементарная ячейка (углерода) алмаза
При давлении свыше 60 Г Па предполагают образование весьма плотной модификации С III (плотность на 15—20 % выше плотности алмаза), имеющей металлическую проводимость. При высоких давлениях и относительно низких температурах (ок. 1 200 K) из высокоориентированного графита образуется гексагональная модификация углерода с кристаллической решеткой типа вюрцита — лонсдейлит (а = 0,252 нм, с = 0,412 нм, пространственная группа Р63/ттс), плотность 3,51 г/см³, т. е. такая же, как у алмаза. Лонсдейлит найден также в метеоритах.
Ультрадисперсные алмазы (наноалмазы)
Карбин
Фуллерены и углеродные нанотрубки
Углерод известен также в виде кластерных частиц С60, С70 и подобных (фуллерены), а также графенов и нанотрубок.
Аморфный углерод
Нахождение в природе
Содержание углерода в земной коре 0,1 % по массе. Свободный углерод находится в природе в виде алмаза и графита. Основная масса углерода в виде природных карбонатов (известняки и доломиты), горючих ископаемых — антрацит (94—97 % С), бурые угли (64—80 % С), каменные угли (76—95 % С), горючие сланцы (56—78 % С), нефть (82—87 % С), горючих природных газов (до 99 % метана), торф (53—56 % С), а также битумы и др. В атмосфере и гидросфере находится в виде диоксида углерода СО2, в воздухе 0,046 % СО2 по массе, в водах рек, морей и океанов в
60 раз больше. Углерод входит в состав растений и животных (
В парообразном состоянии и в виде соединений с азотом и водородом углерод обнаружен в атмосфере Солнца, планет, он найден в каменных и железных метеоритах.
Большинство соединений углерода, и прежде всего углеводороды, обладают ярко выраженным характером ковалентных соединений. Прочность простых, двойных и тройных связей атомов С между собой, способность образовывать устойчивые цепи и циклы из атомов С обусловливают существования огромного числа углеродсодержащих соединений, изучаемых органической химией.
Химические свойства
При обычных температурах углерод химически инертен, при достаточно высоких соединяется со многими элементами, проявляет сильные восстановительные свойства. Химическая активность разных форм углерода убывает в ряду: аморфный углерод, графит, алмаз, на воздухе они воспламеняются при температурах соответственно выше 300—500 °C, 600—700 °C и 850—1000 °C.
Степени окисления +4, −4, редко +2 (СО, карбиды металлов), +3 (C2N2, галогенцианы); сродство к электрону 1,27 эВ; энергия ионизации при последовательном переходе от С 0 к С 4+ соответственно 11,2604, 24,383, 47,871 и 64,19 эВ.
Неорганические соединения
Углерод реагирует со многими элементами с образованием карбидов.
Органические соединения
Благодаря способности углерода образовывать полимерные цепочки, существует огромный класс соединений на основе углерода, которых значительно больше, чем неорганических, и изучением которых занимается органическая химия. Среди них наиболее обширные группы: углеводороды, белки, жиры и др.
Применение
Феррит ( твердый раствор внедрения C в α-железе с объемно-центрированной кубической решеткой)
Аустенит ( твердый раствор внедрения C в γ-железе с гранецентрированной кубической решеткой)
Цементит (карбид железа; Fe3C метастабильная высокоуглеродистая фаза)
Графит стабильная высокоуглеродистая фаза
Ледебурит ( эвтектическая смесь кристаллов цементита и аустенита, превращающегося при охлаждении в перлит)
Мартенсит (сильно пересыщенный твердый раствор углерода в α-железе с объемно-центрированной терагональной решеткой)
Перлит ( эвтектоидная смесь, состоящая из тонких чередующихся пластинок феррита и цементита)
Сорбит (дисперсный перлит)
Троостит (высокодисперсный перлит)
Бейнит (устар: игольчатый троостит) — ультрадисперсная смесь кристаллов низкоуглеродистого мартенсита и карбидов железа
Конструкционная сталь (до 0,8 % C)
Инструментальная сталь (до
2 % C)
Нержавеющая сталь ( легированная хромом)
Жаростойкая сталь
Жаропрочная сталь
Высокопрочная сталь
Белый чугун (хрупкий, содержит ледебурит и не содержит графит)
Серый чугун (графит в форме пластин)
Ковкий чугун (графит в хлопьях)
Высокопрочный чугун (графит в форме сфероидов)
Половинчатый чугун (содержит и графит, и ледебурит)
Углерод играет огромную роль в жизни человека. Его применения столь же разнообразны, как сам этот многоликий элемент.
Углерод является основой всех органических веществ. Любой живой организм состоит в значительной степени из углерода. Углерод — основа жизни. Источником углерода для живых организмов обычно является СО2 из атмосферы или воды. В результате фотосинтеза он попадает в биологические пищевые цепи, в которых живые существа пожирают друг друга или останки друг друга и тем самым добывают углерод для строительства собственного тела. Биологический цикл углерода заканчивается либо окислением и возврашением в атмосферу, либо захоронением в виде угля или нефти.
Углерод в виде ископаемого топлива: угля и углеводородов (нефть, природный газ) — один из важнейших источников энергии для человечества.
Углерод в сталелитейной промышленности один из важнеших компонентов сплавов железо-углерод (производсво чугуна и стали).
Графит используется в карандашной промышленности. Также его используют в качестве смазки при особо высоких или низких температурах.
Токсическое действие
Токсическое действие 14 С, вошедшего в состав молекул белков (особенно в ДНК и РНК), определяется радиационным воздействием бета частиц и ядер отдачи азота ( 14 С (β) → 14 N) и трансмутационным эффектом — изменением химического состава молекулы в результате превращения атома С в атом N. Допустимая концентрация 14 С в воздухе рабочей зоны ДКА 1,3 Бк/л, в атмосферном воздухе ДКБ 4,4 Бк/л, в воде 3,0•10 4 Бк/л, предельно допустимое поступление через органы дыхания 3,2•10 8 Бк/год.