Удалили сальник в брюшной полости что это такое
Резекция большого сальника (лапароскопия/лапаротомия)
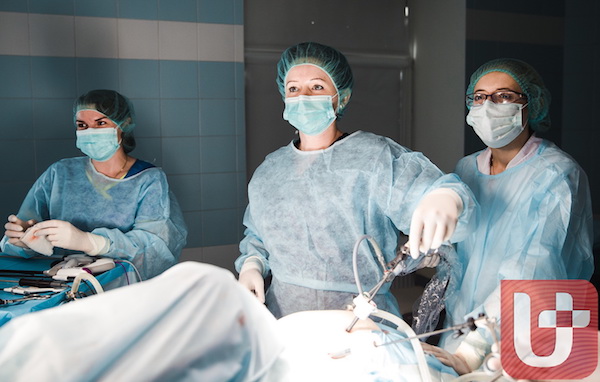
Резекция большого сальника — операция, при которой иссекается и ушивается складка брюшины, покрывающая полость брюшины от области желудка до тонкого кишечника. Данное хирургическое вмешательство, как правило, не является самостоятельной операцией, и чаще выполняется при злокачественном процессе в органах брюшины и малого таза. Как показывает практика, при поражении матки и придатков своевременная выполненная резекция увеличивает выживаемость пациенток. Объясняется это тем, что в ткани сальника легко метастазируют злокачественные клетки. Незамеченные при операции, они будут причиной новых очагов, поэтому удаленная ткань сальника в обязательном порядке должна направляться на гистологический анализ. В ходе хирургического вмешательства по поводу злокачественного процесса удалению также подлежат затронутые раком структуры: лимфатические узлы, кишечник.
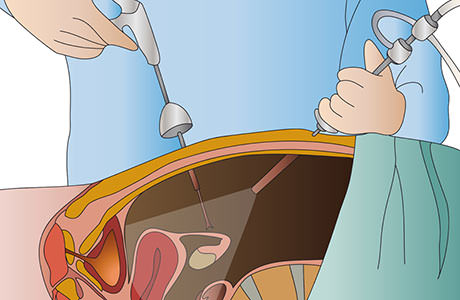
Резекция большого сальника может быть проведена с использованием лапароскопического или лапаротомического доступа. В ходе лапаротомии выполняется разрез передней брюшной стенки, открытый метод целесообразен, если необходим обзор пораженных участков. Продолжительность госпитализации в этом случае составляет около 10 дней, восстановление займет около 1-1,5 месяца. В отличие от лапаротомии, при лапароскопическом доступе манипуляции выполняются через несколько небольших разрезов на животе с использованием видеоэндоскопического оборудования. Все действия хирурга отражаются на мониторе с качественным разрешением, визуальный контроль современной аппаратуры обеспечивает высокую точность манипуляций. После лапароскопии длительность пребывания в клинике составляет не более трех дней, период восстановления занимает не более 4 недель.
Показания и противопоказания
Преимущества резекции большого сальника
Комментарий врача

Руководитель хирургической службы SwissClinic Пучков Константин Викторович
Почему резекцию большого сальника лучше сделать в Швейцарской Университетской клинике?
Часто задаваемые вопросы
В чем заключается подготовка к резекции большого сальника?
Перед операцией необходимо тщательно очистить кишечник. Также за несколько дней до вмешательства нужно исключить из рациона продукты, способные вызвать повышенное газообразование. Операция проводится строго натощак, последний прием пищи, как минимум, за 8 ч до ее начала. При необходимости приема каких-либо медикаментов необходимо предупредить лечащего врача, возможно, некоторые препараты нужно будет исключить на несколько дней.
Возможны ли осложнения при резекции большого сальника?
Как при любом оперативном вмешательстве, при резекции также есть риск развития осложнений, теоретически нельзя исключить кровотечения или повреждения близлежащих органов в ходе вмешательства, инфицирование в ранний послеоперационный период. Поэтому наши пациенты проходят тщательное предоперационное обследование, чтобы исключить факторы, увеличивающие риск развития осложнений. Визуальный контроль процесса и использование при проведении операции оборудования и инструментария последнего поколения сводит к минимуму риск негативных последствий.
Реабилитация после резекции большого сальника
На продолжительность восстановления влияет, прежде всего, метод проведения операции. Но, независимо от используемого доступа, через несколько часов женщина может ходить, ей разрешается принимать жидкую легкую пищу. При лапаротомическом доступе длительность госпитализации составляет около 7-10 дней, восстановление занимает 4-6 недель. После лапароскопии период реабилитации значительно короче, женщина, как правило, выписывается на 3 сутки, полное восстановление занимает 2-4 недели. В послеоперационный период могут быть назначены антибактериальные и обезболивающие препараты. На протяжении месяца следует отказаться от интенсивных физических нагрузок и половых контактов, лучше исключить посещение бассейна или сауны.
Используется ли анестезия при резекции большого сальника?
В ходе оперативного вмешательства какие-либо болезненные ощущения полностью исключены, операция может быть проведена под общим наркозом, эпидуральной или спинальной анестезией. Какому способу отдать предпочтение, решает врач в каждом случае индивидуально.
Заболевания
Рак шейки матки
Рак шейки матки — онкологическое заболевание, при котором эпителий нижнего отдела матки трансформируется в злокачественные клетки. В зависимости от типа эпителия различают плоскоклеточный рак — он диагностируется у 85-95% больных, и аденокарциному — появляющуюся в 5-15%.
Рак эндометрия
Рак эндометрия — онкологическое заболевание, при котором злокачественный процесс развивается во внутреннем слое матки. Среди онкологических патологий женской половой сферы эта болезнь по частоте возникновения занимает лидирующее место. Согласно статистике, на 100 тысяч женщин приходится около 13 пациенток с диагностированным заболеванием. Около 75% заболевших приходится на женщин после 50 лет — предменопаузального и постменопаузального возраста, однако в последние годы все чаще пациентками онколога становятся женщины помоложе.
Рак яичников
Рак яичников — одно из распространенных онкологических заболеваний в гинекологии, по частоте развития уступает первенство лишь злокачественным опухолям матки. Поражение яичника может быть первичным — патологический очаг находится в самом яичнике, и вторичным, называемым метастатическим — очаг патологии расположен в любом другом органе. Злокачественные клетки в тканях яичника могут появляться при опухолях в молочной железе, матке, кишечнике, желудке.
Записывайтесь на консультацию: +7 (495) 782-50-10
Перитонеальный канцероматоз
Перитонеальный канцероматоз
Вам поставили диагноз: перитонеальный канцероматоз (опухоль брюшины)
Предлагаем Вашему вниманию краткий, но очень подробный обзор перитонеального канцероматоза.
Филиалы и отделения, где лечат перитонеальный канцероматоз
МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
Национальный центр лечения больных канцероматозом
МНИОИ имени П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России
Руководитель Центра к.м.н. Владимир Михайлович Хомяков – 8 495 150 11 22
Введение
Причины возникновения перитонеального канцероматоза
Развитие перитонеального канцероматоза является поэтапным процессом. Первый этап – распространение опухолевых клеток из первичного очага поражения. Это связано с нарушением межклеточного взаимодействия и приобретением клетками опухоли подвижности. При этом эпителиальные клетки меняют фенотип на мезенхимальный, происходит деградация межклеточного матрикса. Распространение опухолевых клеток может происходить в ходе оперативного вмешательства. Их механическое отделение возможно при повреждении лимфатических или кровеносных сосудов. Попавшие в брюшную полость клетки опухоли мигрируют под действием силы тяжести, сокращений внутренних органов, имплантируются в местах повышенной резорбции: большом сальнике, в области слепой кишки, дугласовых карманах.
На втором этапе опухолевые клетки взаимодействуют с мезотелием брюшины. Механизмы адгезии определяются природой клеток, особенностями морфологии брюшины, а также наличием участков ее повреждения. Далее клетки закрепляются в мезотелии, происходит их горизонтальное распространение по поверхности перитонеума, а затем инвазивный рост – прорастание в базальную мембрану, соединительную ткань. Следующим этапом является стимуляция неоангиогенеза – обязательного фактора развития опухоли. Морфопатогенетические механизмы формирования канцероматоза брюшины еще недостаточно изучены, в связи с чем отсутствуют радикальные методы лечения.
Частота развития канцероматоза брюшины зависит не только от первичной локализации опухоли, но и от ее размеров, глубины инвазии, гистотипа, степени дифференцировки (недифференцированный рак желудка осложняется поражением брюшины в 60% случаев, ограниченный – в 15%).
Классификация перитонельного канцероматоза
Единая классификация данного заболевания отсутствует, поскольку характеристики первичных опухолей, приводящих к поражению брюшины, весьма разнообразны. Наиболее распространена классификация перитонеального канцероматоза брюшины в зависимости от числа, локализации метастазов, которая предусматривает три степени:
Р1 – локальное поражение брюшины
Р2 – несколько областей канцероматоза, разделенных здоровыми участками брюшины
Р3 – многочисленные очаги поражения
Также используется метод определения индекса канцероматоза брюшины: суммируются баллы измерения максимальных очагов поражения (0-3 балла) в каждой из 13 наиболее вероятных областей поражения брюшины.
Симптомы перитонеального канцероматоза
Перитонеальный канцероматоз брюшины является вторичным поражением, поэтому его клиническая картина во многом определяется проявлениями первичной опухоли. Характерным признаком является обильный выпот в брюшную полость – формирование асцита. Зачастую асцитический синдром, развивающийся вследствие обструкции лимфатического дренажа, является единственным признаком заболевания, и пациенты могут поступать в отделение гастроэнтерологии или терапии для диагностики причин асцита. Состояние больных тяжелое, характерна значительная потеря веса. Неспецифическими признаками являются тошнота, рвота, выраженная слабость, утомляемость. При наличии крупных метастазов возможно их прощупывание через брюшную стенку.
Диагностика перитонеального канцероматоза
Перитонельный канцероматоз имеет неспецифическую клиническую картину, однако консультация гастроэнтеролога или онколога позволяет предположить данное заболевание на основании симптомов и физикальных данных. Лабораторные анализы не выявляют специфических изменений: определяется лейкоцитоз, ускорение СОЭ. Диагностическая программа обязательно должна включать УЗИ органов брюшной полости и малого таза, позволяющее обнаружить распространенное поражение, а также МСКТ брюшной полости с контрастированием. Обязательно проводится цитологическое исследование асцитической жидкости, полученной при лапароцентезе, которое дает возможность впервые установить или подтвердить диагноз, а также определить гистогенез клеток опухоли.
Информативным методом диагностики перитонеального канцероматоза является лапароскопия с осмотром перитонеума, дугласова пространства, диафрагмы, сопровождающаяся биопсией. Высокой специфичностью обладает обратнотранскриптазная полимеразная цепная реакция (ОТ-ПЦР), которая позволяет определить источник диссеминации даже при малом количестве опухолевых клеток.
Сложности диагностики возникают при наличии перитонеального канцероматоза без выявленного первичного очага. Данная форма заболевания, встречающаяся в 3-5 % случаев, проявляется клинически только при уже сформировавшемся поражении брюшины. При этом первичный очаг может иметь настолько малые размеры, что его прижизненное обнаружение невозможно.
В качестве дополнительных методов может использоваться определение онкомаркеров (кислой фосфатазы, раково-эмбрионального антигена, альфа-фетопротеина, бета-субъединицы ХГЧ). Такая диагностика не обладает высокой специфичностью, но применяется для оценки прогноза, раннего выявления диссеминации, рецидивов, а также для контроля эффективности лечения.
Лечение перитонеального канцероматоза
Хирургическое лечение канцероматоза включает удаление первичной опухоли с регионарными метастазами и отсевами по брюшине. Циторедуктивная операция выполняется в объеме перитонэктомии, может сочетаться с удалением матки и придатков, сигмовидной кишки, желчного пузыря. После проведения операции оценивается индекс полноты циторедукции: СС-0: после проведения хирургического лечения очаги поражения визуально не определяются; СС-1: имеются неудаленные очаги диаметром до 2,5 мм; СС-2: очаги диаметром 2,5 мм – 2,5 см; СС-3: очаги поражения более 2,5 см в диаметре. Однако даже при определении индекса СС-0 нельзя полностью исключить возможность диссеминации, поэтому обязательно проводится химиотерапия.
Эффективные подходы к лечению, как правило, подразумевают проведение комбинированной терапии, например, сочетания хирургического вмешательства и системной химиотерапии. Одним из наиболее эффективных методов является локальная химиотерапия. Идея локальной химиотерапии состоит в том, чтобы обеспечить доставку лекарственного препарата непосредственно к опухолевым клеткам, находящимся на внутренней выстилке анатомической полости. Из-за крайне низкой проницаемости этой области для лекарственных препаратов, например, при внутривенном их введении или приеме в виде таблеток, доставка препаратов в виде аэрозоля под давлением углекислого газа даёт накопление препарата в опухоли в значительно больших концентрациях.
Методы лечения перитонеального канцероматоза
Длительное время канцероматоз брюшины и плевры считали терминальной стадией болезни, не подлежащей специальному лечению. Разработка методик непосредственного воздействия на брюшину и плевру позволила улучшить прогноз при этом состоянии. МНИОИ им. П.А. Герцена обладает уникальными возможностями лечения больных с канцероматозом, имея в арсенале весь комплекс новейших методов терапии.
Гипертермическая интраоперационная внутрибрюшная (внутриплевральная) химиотерапия (HITEC).
Это методика, при которой во время операции в брюшную или плевральную полость вводится подогретый до 42,5С, высококонцентрированный раствор химиотерапевтических препаратов, что обеспечивает их воздействие непосредственно на раковые клетки в брюшной (плевральной) полости при минимальном воздействии на другие органы. Сеанс проводится в течение часа, что позволяет разрушить опухолевые клетки, оставшиеся после так называемой циторедуктивной операции.
Внутрибрюшная (внутриплевральная) аэрозольная химиотерапия под давлением (PIРAC)
Это новейший инновационный метод лечения перитонеального канцероматоза, который обеспечивает доставку лекарственного препарата непосредственно к опухолевым клеткам, находящимся на внутренней выстилке анатомической полости. Метод совсем недавно появился в России. Процедуру проводят посредством лапароскопии (торакоскопии). В брюшной или плевральной полости под давлением углекислого газа распыляют аэрозоль химиопрепаратов и оставляют в течение 30 мин. При таком способе введения химиопрепаратов их воздействие на опухоль многократно возрастает при полном отсутствии системной токсичности. Ноу-хау МНИОИ имени П.А. Герцена в этом методе лечения стала разработка собственной специальной форсунки, которая формирует поток мелкодисперсного аэрозоля с размером капель от 1 до 40 мкм. Изделие выполнено из специализированных материалов и не уступает по качеству импортному аналогу, а по ряду технических характеристик его превосходит.
Преимущества лечения перитонеального канцероматоза в МНИОИ имени П.А. Герцена – филиале ФГБУ «НМИЦ радиологии» Минздрава России
Расширенная экстирпация матки с оментэктомией (удаление матки с придатками и резекция большого сальника)
На сегодняшний день в комплексную терапию рака яичников входят хирургическое лечение, традиционная химиотерапия, иммунотерапия, гормональная и таргетная терапия, лучевая терапия. Несмотря на значительное количество лечебных методов, наиболее эффективным считается проведение оперативного удаления новообразования на ранних стадиях заболевания.
К хирургическому лечению злокачественного процесса в яичниках относится расширенная экстирпация матки (удаление матки с придатками) в комплексе с оментэктомией. Оментэктомия — это частичная или полная резекция большого сальника, в ходе которой сальник отделяется от желудка и поперечного участка ободочной кишки. Уже на начальных стадиях онкозаболеваний яичников подобная операция входит в число обязательных компонентов хирургического этапа лечения [1].
У многих пациентов удаление сальника не планируется как самостоятельная операция. Проведение этой процедуры назначается при онкозаболеваниях брюшных и мочеполовых органов, особенно часто при раке яичников [2]. Поскольку отмечается высокая вероятность вовлечения в злокачественный процесс желудка и женских репродуктивных органов, оментэктомия проводится как у пациентов с диагностированным метастазированием, так и при отсутствии метастазов.
В клинике «Добрый прогноз» оментэктомия выполняется как лапаротомным, так и лапароскопическим способом, в зависимости от локализации новообразования и степени распространенности патологического процесса.
В Украине разрешено применение протоколов лечения, утвержденных Европейской ассоциацией онкологов (ESMO [3]) и Американской национальной онкологической сетью (NCCN).
Стандартной схемы лечения, эффективной для каждого пациента с этим диагнозом, не существует. Методы и режим проведения терапии, длительность лечения подбираются индивидуально, в зависимости от стадии заболевания, возраста и общего состояния пациента, наличия у него противопоказаний. Разобраться в ситуации и составить индивидуальный план обследований и лечения сможет только квалифицированный врач-онколог.
Используемые источники литературы
Отзывы пациентов
Отзывы не редактируются, но проходят проверку модератором для защиты от недобросовестной рекламы.
Спасибо за понимание!
Просьба указывать реальный почтовый ящик, если хотите, чтобы мы Вам ответили (жалоба, вопрос, предложение и т.д.). Ваши персональные данные не передаются третьим лицам и не используются в рекламных рассылках.



 Пучков К.В., Баков В.С., Иванов В.В. Симультанные лапароскопические оперативные вмешательства в хирургии и гинекологии: Монография.- М.: ИД МЕДПРАКТИКА – М.- 2005.- 168 с.
Пучков К.В., Баков В.С., Иванов В.В. Симультанные лапароскопические оперативные вмешательства в хирургии и гинекологии: Монография.- М.: ИД МЕДПРАКТИКА – М.- 2005.- 168 с.  Пучков К.В., Иванов В.В.. Технология дозированного лигирующего электротермического воздействия на этапах лапароскопических операций: монография.- М.: ИД МЕДПРАКТИКА, 2005.- 176 с.
Пучков К.В., Иванов В.В.. Технология дозированного лигирующего электротермического воздействия на этапах лапароскопических операций: монография.- М.: ИД МЕДПРАКТИКА, 2005.- 176 с.