Что лучше: Серетид или Сальмекорт
Серетид
Сальмекорт
Исходя из данных исследований, Сальмекорт лучше, чем Серетид. Поэтому мы советуем выбрать его.
Активные вещества одинаковые. Поэтому выбирайте исходя из цены
Сравнение эффективности Серетида и Сальмекорта
Эффективность у Серетида достотаточно схожа с Сальмекортом – это означает, что способность лекарственного вещества оказывать максимально возможное действие схоже.
Например, если терапевтический эффект у Серетида более выраженный, то при применении Сальмекорта даже в больших дозах не получится добиться данного эффекта.
Также скорость терапии – показатель быстроты терапевтического действия у Серетида и Сальмекорта примерно одинаковы. А биодоступность, то есть количество лекарственного вещества, доходящее до места его действия в организме, схожа. Чем выше биодоступность, тем меньше его потерь будет при усвоении и использовании организмом.
Сравнение безопасности Серетида и Сальмекорта
Безопасность препарата включает множество факторов.
При этом у Серетида она достаточно схожа с Сальмекортом. Важно, где метаболизируется препарат: лекарственные вещества выделяются из организма либо в неизмененном виде, либо в виде продуктов их биохимических превращений. Метаболизм протекает спонтанно, но чаще всего задействует основные органы, такие как печень, почки, лёгкие, кожу, мозг и другие. При оценивании метаболизма у Серетида, также как и у Сальмекорта мы смотрим, какой орган является метаболизирующим и наколько критично действие на него.
Соотношение риска к пользе – это когда назначение лекарственного препарата нежелательно, но оправдано при определенных условиях и обстоятельствах, с обязательным соблюдением осторожности применения. При этом у Серетида нет никаих рисков при применении, также как и у Сальмекорта.
Также при рассчете безопасности учитывается проявляются ли только аллергические реакции или же возможная дисфункция основных органов. В прочем как и обратимость последствий от использования Серетида и Сальмекорта.
Сравнение противопоказаний Серетида и Сальмекорта
Исходя из инструкции. Количество противопоказаний у Серетида достаточно схоже с Сальмекортом и составляет удовлетворительное количество. Это и перечень симптомов с синдромами, и заболевания, различные внешних и внутренние условия, при которых применение Серетида и Сальмекорта может быть нежелательным или недопустимым.
Сравнение привыкания у Серетида и Сальмекорта
Как и безопасность, привыкание тоже включает множество факторов, которые необходимо учитывать при оценивании препарат.
Так совокупность значения таких параметров, как «cиндром отмены» и «развитие резистентности», у Серетида достаточно схоже со аналогичными значения у Сальмекорта. Синдром отмены – это патологическое состояние, возникающее после прекращения поступления в организм веществ, вызывающих привыкание или зависимость. А под резистентностью понимают изначальную невосприимчивость к препарату, этим она отличается от привыкания, когда невосприимчивость к препарату развивается в течение определенного периода времени. Наличие резистентности можно констатировать лишь в том случае, если была сделана попытка увеличить дозу препарата до максимально возможной. При этом у Серетида значения «синдрома отмены» и «резистентности» достотачно малое, впрочем также как и у Сальмекорта.
Сравнение побочек Серетида и Сальмекорта
Побочки или нежелательные явления – это любое неблагоприятное с медицинской точки зрения событие, возникшее у субъекта, после введения препарата.
У Серетида состояния нежелательных явлений почти такое же, как и у Сальмекорта. У них у обоих количество побочных эффектов малое. Это подразумевает, что частота их проявления низкая, то есть показатель сколько случаев проявления нежелательного эффекта от лечения возможно и зарегистрировано – низкий. Нежелательное влияние на организм, сила влияния и токсическое действие у Серетида схоже с Сальмекортом: как быстро организм восстановиться после приема и восстановиться ли вообще.
Сравнение удобства применения Серетида и Сальмекорта
Это и подбор дозы с учетом различных условий, и кратность приемов. При этом важно не забывать и про форму выпуска препарата, ее тоже важно учитывать при составлении оценки.
Удобство применения у Серетида примерно одинаковое с Сальмекортом. При этом они не являются достаточно удобными для применения.
Рейтинг препаратов составлен опытными фармацевтами, изучающий международные исследования. Отчет сгенерирован автоматически.
Дата последнего обновления: 2020-12-13 10:32:58
Современная терапия бронхиальной астмы
Бронхиальная астма — заболевание, с которым все чаще сталкиваются врачи в последнее время. Это неудивительно, ибо, по данным международных исследований, в развитых странах мира около 5% взрослого населения и почти 10% детей страдают этим недугом.
Бронхиальная астма — заболевание, с которым все чаще сталкиваются врачи в последнее время. Это неудивительно, ибо, по данным международных исследований, в развитых странах мира около 5% взрослого населения и почти 10% детей страдают этим недугом. Кроме того, в последние десятилетия прослеживается четкая тенденция роста заболеваемости аллергическими болезнями, в том числе бронхиальной астмой.
Именно этим обстоятельством обусловлено появление в последние годы ряда программных документов, руководств, посвященных диагностике и лечению бронхиальной астмы. Такими основополагающими документами являются Совместный доклад ВОЗ и Национального института сердца, легких, крови (США) «Бронхиальная астма. Глобальная стратегия (GINA)», 1996 [1] и «Бронхиальная астма (Формулярная система). Руководство для врачей России», 1999 [2]. Эти руководства предназначены для практических врачей и служат одной цели — формированию единой концепции бронхиальной астмы, ее диагностики и лечения.
В свою очередь, современная терапия бронхиальной астмы базируется на вышеупомянутой концепции, на основании которой определяются форма и степень тяжести заболевания.
Согласно современным представлениям, бронхиальная астма независимо от тяжести ее течения является хроническим воспалительным заболеванием дыхательных путей, в формировании которого участвуют многие клетки: тучные клетки, эозинофилы и Т-лимфоциты. При наличии предрасположенности это воспаление приводит к повторяющимся эпизодам хрипов, одышки, тяжести в грудной клетке и кашлю, особенно ночью и/или ранним утром. Эти симптомы обычно сопровождаются распространенной, но вариабельной обструкцией бронхов, которая по крайней мере частично обратима спонтанно или под влиянием лечения. Воспаление приводит к формированию повышенной чувствительности дыхательных путей к самым различным стимулам, которые у здоровых лиц никакой реакции не вызывают. Это состояние — бронхиальная гиперреактивность, которая может быть специфической и неспецифической. Специфическая гиперреактивность представляет собой повышенную чувствительность бронхов к определенным, специфическим аллергенам, вызвавшим развитие астмы. Под неспецифической гиперреактивностью понимают повышенную чувствительность к разнообразным неспецифическим стимулам неаллергенной природы: холодному воздуху, физической нагрузке, резким запахам, стрессам и пр. Одним из важных признаков гиперреактивности, используемых для оценки степени тяжести бронхиальной астмы, является суточная вариабельность пиковой скорости выдоха (ПСВ), составляющая 20% и более.
Аллергические механизмы становятся причиной развития астмы у 80% детей и приблизительно у 40-50% взрослых, поэтому Европейская Академия Аллергологии и Клинической Иммунологии (EAACI) предлагает использовать термин «аллергическая астма» как основное определение астмы, обусловленной иммунологическим механизмом, причем в тех случаях, когда доказано участие в этом механизме антител класса иммуноглобулинов Е, отсюда и термин «IgE-обусловленная астма» [4]. В нашей стране для обозначения этого варианта применяется термин «атопическая астма». Определение полностью отражает суть процесса, в котором принимают участие IgE-антитела. Другие неиммунологические типы астмы ЕААСI предлагается называть неаллергической астмой [4]. По-видимому, к этой форме может быть отнесена астма, развивающаяся из-за нарушения метаболизма арахидоновой кислоты, эндокринных и нервно-психических расстройств, нарушения рецепторного и электролитного балансов дыхательных путей, воздействия неаллергенных аэрополлютантов и профессиональных факторов.
Установление формы бронхиальной астмы имеет принципиальное значение для ее терапии, ибо лечение любого аллергического заболевания начинается с мероприятий по элиминации аллергена (или аллергенов), виновного в развитии болезни. Можно полностью удалить аллерген, если речь идет о домашнем животном, пищевом продукте или лекарственном препарате, и уже только благодаря этому добиться ремиссии бронхиальной астмы. Но чаще развитие астмы провоцирует клещ домашней пыли, которого не удается удалить полностью. Однако количество пылевых клещей можно существенно сократить, используя специальные безаллергенные постельные принадлежности и акарицидные средства, проводя регулярную влажную уборку с помощью пылесоса с глубокой степенью очистки. Все эти мероприятия, равно как и меры по сокращению содержания пыльцы в воздухе жилых помещений в сезон цветения и меры, позволяющие минимизировать контакт со спорами внедомашних и внутридомашних непатогенных плесневых грибов, приводят к значительному ослаблению симптомов бронхиальной астмы у чувствительных к этим аллергенам пациентов.
Фармакотерапия — неотъемлемая и важнейшая составляющая комплексной лечебной программы бронхиальной астмы. Существует несколько ключевых положений в терапии бронхиальной астмы:
Итак, все препараты, которые используются для лечения бронхиальной астмы, принято делить на две группы: базисные или лечебные, то есть обладающие противовоспалительным эффектом, и симптоматические, обладающие преимущественно быстрой бронхолитической активностью. Однако за последние годы на фармакологическом рынке появилась новая группа противоастматических препаратов, которые представляют собой комбинацию противовоспалительных и бронхолитических средств.
К базисным противовоспалительным препаратам относятся глюкокортикостероиды, стабилизаторы тучных клеток — кромоны и ингибиторы лейкотриенов.
Ингаляционные глюкокортикостероиды (беклометазон дипропионат, флютиказон пропионат, будесонид, флунизолид) в настоящее время являются препаратами выбора для лечения среднетяжелой и тяжелой астмы. Более того, согласно международным рекомендциям, ингаляционные глюкокортикостероиды (ИГКС) показаны всем больным с персистирующей астмой, в том числе и с легким течением, ибо даже при этой форме астмы в слизистой дыхательных путей присутствуют все элементы хронического аллергического воспаления. В отличие от системных стероидов, которые, в свою очередь, являются средством выбора при острой тяжелой астме, ИГКС не имеют тяжелых системных побочных эффектов, представляющих угрозу для больного. Лишь в высоких суточных дозах (выше 1000 мкг) они могут угнетать функцию коры надпочечников. Многофакторное противовоспалительное действие ингаляционных глюкокортикостероидов проявляется в их способности снижать или даже вовсе устранять бронхиальную гиперреактивность, восстанавливать и повышать чувствительность β2-адренорецепторов к катехоламинам, в том числе к препаратам β2-агонистам. Доказано, что противовоспалительная эффективность ИГКС зависит от дозы, поэтому целесообразно начинать лечение со средних и высоких доз (в зависимости от тяжести астмы). При достижении стабильного состояния больных (но не ранее чем через 1-3 месяца от начала терапии ИГКС) и улучшении показателей ФВД дозу ИГКС можно снизить, но не отменять! В случае ухудшения течения астмы и снижения функциональных легочных показателей доза ИГКС должна быть повышена. Возникновения таких неопасных, но нежелательных побочных эффектов ИГКС, как кандидоз ротовой полости, дисфония, раздражающий кашель, можно избежать благодаря применению спейсеров, а также полосканию ротовой полости и горла слабым раствором соды или просто теплой водой после каждой ингаляции препарата.
Кромогликат натрия и недокромил натрия (кромоны) подавляют выделение медиаторов из тучной клетки путем стабилизации ее мембраны. Эти препараты, назначенные до начала воздействия аллергена, способны угнетать раннюю и позднюю аллергические реакции. Их противовоспалительный эффект значительно уступает таковому у ИГКС. Снижение бронхиальной гиперреактивности происходит лишь после длительного (не менее 12 недель) лечения кромонами. Однако преимущество кромонов — в их безопасности. Эти препараты практически не дают побочных эффектов и поэтому с успехом применяются для лечения детской астмы и астмы у подростков. Атопическая астма легкого течения у взрослых иногда также хорошо контролируется кромогликатом или недокромилом натрия.
Антилейкотриеновые препараты, включающие в себя антагонисты цистеиниловых (лейкотриеновых) рецепторов и ингибиторы синтеза лейкотриенов, представляют собой относительно новую группу противовоспалительных препаратов, используемых для лечения астмы. В России в настоящее время зарегистрированы и разрешены к использованию препараты зафирлукаст (аколат) и монтелукаст (сингуляр) — блокаторы лейкотриеновых рецепторов, представленные в форме для орального применения. Противовоспалительный эффект этих препаратов заключается в блокаде действия лейкотриенов — жирных кислот, продуктов распада арахидоновой кислоты, участвующих в формировании бронхиальной обструкции. В последние годы появилось много работ, посвященных изучению клинической эффективности антилейкотриеновых препаратов при различных формах и различной степени тяжести бронхиальной астмы. Эти препараты эффективны в лечении больных с аспириновой формой бронхиальной астмы, при которой лейкотриены являются основными медиаторами воспаления и формирования бронхиальной обструкции. Они эффективно контролируют астму физических нагрузок и ночную астму, а также интермиттирующую астму, вызванную воздействием аллергена. Особое внимание уделяется изучению антилейкотриеновых препаратов, применяемых в терапии детской астмы, так как они удобны в использовании и вызывают относительно низкий по сравнению с ИГКС риск возникновения серьезных побочных эффектов. В последних американских руководствах по диагностике и терапии астмы препараты — антагонисты лейкотриеновых рецепторов рассматриваются как альтернатива ИГКС для контроля легкой, персистирующей астмы у детей 6 лет и старше, а также у взрослых. Однако в настоящее время проводится достаточно много исследований, демонстрирующих эффективность этих препаратов у лиц, страдающих среднетяжелой и тяжелой астмой, которым антагонисты лейкотриеновых рецепторов назначаются как дополнение к ИГКС. Такое сочетание препаратов, потенциирующих действие друг друга, усиливает противоастматическую терапию и позволяет избежать повышения дозы ИГКС у некоторых пациентов, а иногда даже снизить ее.
Таким образом, новые противоастматические препараты — антагонисты лейкотриеновых рецепторов могут использоваться для противовоспалительной (базисной) терапии астмы в следующих ситуациях [5]:
Препараты бронхолитического действия применяются как для купирования острого приступа астмы при хроническом ее течении, так и для профилактики астмы физических нагрузок, острой астмы, индуцированной аллергеном, а также для снятия тяжелого бронхоспазма при обострении бронхиальной астмы.
Ключевые положения в бронхолитической терапии бронхиальной астмы:
Селективные β2-агонисты первой генерации [3]: албутерол (сальбутамол, вентолин), тербуталин (бриканил), фенотерол (беротек) и другие — представляют собой наиболее эффективные бронхолитики. Они способны быстро (в течение 3-5 мин) и на довольно долгий срок (до 4-5 ч) оказывать бронхолитическое действие после ингаляции в виде дозированного аэрозоля при легких и среднетяжелых приступах астмы, а при использовании растворов этих препаратов через небулайзер — и при тяжелых приступах в случае обострения астмы. Однако β2-агонисты короткого действия следует применять только для купирования приступа удушья. Они не рекомендуются для постоянной, базисной терапии, так как не способны уменьшать воспаление дыхательных путей и бронхиальную гиперреактивность. Более того, при постоянном и длительном их приеме степень бронхиальной гиперреактивности может возрастать, а показатели функции внешнего дыхания — ухудшаться [3]. Этих недостатков лишены β2-агонисты второй генерации, или β2-агонисты длительного действия: сальметерол и формотерол. В силу липофильности своих молекул эти препараты очень близки β2-адренорецепторам, чем прежде всего и определяется длительность их бронхолитического действия — до 12 ч после ингаляции 50 мкг или 100 мкг сальметерола и 6 мкг, 12 мкг или 24 мкг формотерола. При этом формотерол кроме длительного действия одновременно оказывает и быстрое бронхорасширяющее действие, сопоставимое со временем начала действия сальбутамола. Все препараты β2-адреномиметики обладают способностью ингибировать высвобождение медиаторов аллергического воспаления, таких, как гистамин, простагландины и лейкотриены, из тучных клеток, эозинофилов, причем максимально это свойство проявляется у β2-агонистов длительного действия. Кроме того, последние обладают способностью уменьшать проницаемость капилляров слизистой бронхиального дерева. Все это позволяет говорить о противовоспалительном эффекте β2-агонистов длительного действия. Они способны подавлять как раннюю, так и позднюю астматические реакции, возникающие после ингаляции аллергена, и снижать бронхиальную реактивность. Эти препараты являются средством выбора при легкой и среднетяжелой астме, а также у пациентов с ночными симптомами астмы; их можно использовать также для профилактики астмы физических нагрузок [1]. У пациентов со среднетяжелой и тяжелой астмой их целесообразно сочетать с ИГКС.
Теофиллины — основной вид метилксантинов, используемых в лечении астмы. Теофиллины обладают бронхолитическим и противовоспалительным действием. Блокируя фермент фосфодиэстеразу, теофиллин стабилизирует цАМФ и снижает концентрацию внутриклеточного кальция в клетках гладкой мускулатуры бронхов (и других внутренних органов), тучных клетках, Т-лимфоцитах, эозинофилах, нейтрофилах, макрофагах, эндотелиальных клетках. В результате происходят расслабление гладкой мускулатуры бронхов, подавление высвобождения медиаторов из клеток воспаления и снижение повышенной сосудистой проницаемости. Теофиллин в значительной степени подавляет как раннюю, так и позднюю фазы астматической реакции. Пролонгированные теофиллины успешно применяются для контроля ночных астматических проявлений. Однако эффективность теофиллина при острых приступах астмы уступает (как по скорости наступления эффекта, так и по его выраженности) β2-агонистам, применяемым ингаляционно, особенно через небулайзер. Поэтому внутривенное введение эуфиллина должно рассматриваться как резервное мероприятие для тех пациентов с острой тяжелой астмой, для которых прием β2-агонистов через небулайзер оказывается недостаточно эффективным [1]. Это ограничение обусловлено еще и высоким риском возникновения побочных реакций на теофиллин (сердечно-сосудистые и желудочно-кишечные расстройства, возбуждение ЦНС), развивающихся, как правило, при превышении концентрации 15 мкг/мл в периферической крови. Поэтому длительное применение теофиллина требует мониторинга его концентрации в крови.
Антихолинергические препараты (ипратропиум бромид и окситропиум бромид) обладают бронхолитическим действием за счет блокады М-холинорецепторов и снижения тонуса блуждающего нерва. В России давно зарегистрирован и успешно применяется один из этих препаратов — ипратропиум бромид (атровент). По силе и скорости наступления эффекта антихолинергические препараты уступают β2-агонистам, их бронхолитическое действие развивается через 30-40 мин после ингаляции. Однако совместное их использование с β2-агонистами, взаимно усиливающее действие этих препаратов, оказывает выраженный бронхолитический эффект, особенно при среднетяжелой и тяжелой астме, а также у пациентов с астмой и сопутствующим хроническим обструктивным бронхитом. Такими комбинированными препаратами, содержащими ипратропиум бромид и β2-агонист короткого действия, являются беродуал (содержит фенотерол) и комбивент (содержит сальбутамол).
Принципиально новым шагом в современной фармакотерапии бронхиальной астмы является создание комбинированных препаратов, обладающих выраженным противовоспалительным и длительным бронхолитическим действием. Речь идет о комбинации ингаляционных кортикостероидов и длительно действующих β2-агонистов. Сегодня на фармакологическом рынке Европы, и России в том числе, существуют два таких препарата: серетид, содержащий флютиказон пропионат и сальметерол, и симбикорт, имеющий в своем составе будесонид и формотерол. Оказалось, что в подобных соединениях кортикостероид и пролонгированный β2-агонист обладают комплементарным действием и их клинический эффект существенно превышает таковой в случае монотерапии ИГКС или β2-агонистом длительного действия. Назначение такой комбинации может служить альтернативой повышению дозы ИГКС у пациентов со среднетяжелой и тяжелой астмой. Пролонгированные β2-агонисты и кортикостероиды взаимодействуют на молекулярном уровне. Кортикостероиды увеличивают синтез β2-адренорецепторов в слизистой бронхов, снижают их десенситизацию и, напротив, повышают чувствительность этих рецепторов к действию β2-агонистов. С другой стороны, пролонгированные β2-агонисты стимулируют неактивный глюкокортикоидный рецептор, который в результате становится более чувствительным к действию ингаляционных глюкокортикостероидов [6]. Одновременное применение ИГКС и пролонгированного β2-агониста не только облегчает течение астмы, но и существенно улучшает функциональные показатели, снижает потребность в короткодействующих β2-агонистах, значительно эффективнее предупреждает обострения астмы по сравнению с терапией только ИГКС.
Безусловным преимуществом этих препаратов, особенно привлекающим пациентов-астматиков, является сочетание двух активно действующих субстанций в одном устройстве для ингаляций: дозированном аэрозольном ингаляторе (серетид ДАИ) или порошковом ингаляторе (серетид мультидиск) и турбухалере, содержащем препараты в виде пудры (симбикорт-турбухалер). Препараты имеют удобный двукратный режим дозирования, для симбикорта возможен также однократный прием. Серетид выпускается в формах, содержащих различные дозы ИГКС: 100, 250 или 500 мкг флютиказона пропионата при неизменной дозе сальметерола — 50 мкг. Симбикорт выпускается в дозировке 160 мкг будесонида и 4,5 мкг формотерола. Симбикорт можно назначать от 1 до 4 раз в сутки, что позволяет контролировать вариабельное течение астмы с помощью одного и того же ингалятора, уменьшая дозу препарата при достижении адекватного контроля астмы и увеличивая при ухудшении симптомов. Это обстоятельство позволяет подобрать адекватную терапию с учетом тяжести астмы для каждого конкретного больного. Кроме того, симбикорт за счет быстродействующего формотерола быстро облегчает симптомы астмы. Из этого вытекает повышение приверженности к терапии: видя, что лечение помогает быстро и эффективно, больной более охотно соблюдает предписание врача. Следует помнить, что комбинированные препараты (ИГКС + длительно действующие β2-агонисты) не должны использоваться для купирования острого приступа астмы. Для этой цели пациентам рекомендуются β2-агонисты короткого действия.
Таким образом, применение комбинированных препаратов ИГКС и пролонгированных β2-агонистов целесообразно во всех случаях персистирующей астмы, когда не удается достичь хорошего контроля над заболеванием только назначением ИГКС. Критериями хорошо контролируемой астмы являются отсутствие ночных симптомов, хорошая переносимость физической нагрузки, отсутствие потребности в неотложной помощи, суточная потребность в бронхолитиках менее 2 доз, пиковая скорость выдоха больше 80% и ее суточные колебания менее 20%, отсутствие побочных эффектов от проводимой терапии [7].
Безусловно, целесообразно начинать лечение ИГКС с комбинации их с сальметеролом или формотеролом, что позволит достичь быстрого клинического эффекта и заставит пациентов поверить в успех лечения.
По вопросам литературы обращайтесь в редакцию
Новый препарат Сальмекорт в базисной терапии бронхиальной астмы
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Внастоящее время бронхиальная астма (БА) относится кчислу наиболее распространенных заболеваний. Основной задачей лечения БАявляется достижение контроля над заболеванием, который заключается втом, что упациентов отсутствуют симптомы болезни или они минимально выражены, нет ограничения повседневной деятельности, отсутствует (или минимальна) потребность впрепаратах неотложной помощи, частота обострений крайне низка [1–3]. Проявления заболевания устраняют спомощью адекватной ирациональной медикаментозной терапии. Фармакотерапия БАвключает 2 класса препаратов: быстродействующие, которые устраняют симптомы острой бронхоконстрикции, ибазисные— для длительного контроля заболевания, при регулярном применении улучшающие контроль над БАвцелом. При этом иногда базисные препараты принимают попотребности, аβ короткого действия— регулярно или профилактически [2, 4, 5]. Нодаже при очень хорошем контроле БАнесуществует гарантий полного отсутствия симптомов иобострений. Контакт саллергеном, пребывание внакуренном помещении идругие подобные ситуации могут вызвать затруднение дыхания, появление кашля ивнезапное развитие приступа удушья. Это может случиться влюбом месте ивлюбое время, азначит, необходимо иметь при себе средство для неотложной помощи и, конечно, уметь его применять.
Основными противовоспалительными препаратами для лечения БА являются ингаляционные глюкокортикостероиды (ИГКС). Контролируемые исследования, проведенные с учетом требований доказательной медицины, показали эффективность ИГКС в плане улучшения функции дыхания, уменьшения гиперреактивности дыхательных путей и выраженности симптомов, снижения частоты и тяжести обострений (уровень доказательности, А) [6–8].
В гг. в клиническую практику вошли селективные агонисты β, которые обладали преимущественным действием на гладкую мускулатуру бронхов и клинически незначимой активностью в отношении α- и β. Пациенты, регулярно принимавшие β короткого действия перед приемом ИГКС, демонстрировали большую клиническую эффективность терапии, чем принимавшие указанные препараты только по потребности. Это привело к созданию селективных длительно действующих β (ДДБА). В терапии БА используют ингаляционные сальметерол или формотерол, которые в комбинации с ИГКС являются основой базисной терапии БА. Включение их в схему лечения больных, у которых БА не удается полностью контролировать различными дозами ИГКС, позволяет достичь лучшего контроля над заболеванием, чем просто увеличение дозы ИГКС в 2 раза и более (уровень доказательности, А) [9–11]. ИГКС и ДДБА следует рассматривать как синергисты, что обусловлено их комплементарным воздействием на молекулярном и рецепторном уровнях [12–15]. Высокий противовоспалительный эффект совместного использования ИГКС и ДДБА является аргументом в пользу применения такого терапевтического подхода при БА, которая сопровождается воспалением слизистой бронхов, ее отеком, экссудацией плазмы (повышением сосудистой проницаемости), гипертрофией гладкомышечных клеток и десквамацией эпителия.
В 2005, 2008 и 2010 гг. Управление по контролю за продуктами и лекарствами США (FDA) провело дополнительную оценку безопасности ДДБА при БА. Из представленных данных следует, что повышенный риск отмечается в первую очередь у вполне определенной группы пациентов — темнокожих американцев, не получавших терапии ингаляционными гормональными препаратами до начала лечения ДДБА. Также отмечалось повышение риска тяжелых обострений в тех случаях, когда лечение этой группой препаратов было начато на фоне выраженного ухудшения или уже имевшегося обострения БА [16].
Пролонгированные β могут назначаться только в дополнение к ИГКС. Регулярное применение ДДБА для плановой терапии требует их обязательного сочетания с ИГКС. Врачам следует знать, что использование монотерапии β вызывает развитие феномена β, что может привести к тяжелым последствиям для пациентов вплоть до развития астматических состояний.
Комбинация флутиказона пропионата (ФП) и сальметерола ксинафоата (САЛ). Компоненты, входящие в состав этих препаратов, применяются достаточно давно: ФП — с 1993 г., САЛ — с 1990 г.
ФП — один из самых высокоактивных противовоспалительных препаратов на сегодняшний день. Препарат имеет низкую системную биодоступность (
1%), а абсолютная биодоступность составляет 10–30% в зависимости от типа ингалятора. ФП обладает высоким сродством к глюкокортикоидным рецепторам и имеет длительную связь с рецептором. Для предотвращения осиплости голоса и развития кандидоза при приеме ФП следует соблюдать те же правила, что и при приеме других ИГКС, полоскать рот и горло водой после ингаляции. В связи с высоким противовоспалительным действием ФП также показан больным с тяжелым течением БА и зависимостью от системных стероидов [17].
САЛ относится к ингаляционным ДДБА. Клинические исследования показали, что ДДБА оказывают стабилизирующее влияние на тучные клетки, ингибируют высвобождение ими гистамина, что приводит к уменьшению его системной и местной концентрации [18]. САЛ назначается только в качестве препарата для базисной терапии и не применяется по потребности, при обострении заболевания, астматическом состоянии, а также для купирования приступов затрудненного дыхания. Следует использовать только рекомендованные дозы, а для купирования симптомов использовать β короткого действия. Отметим, что САЛ имеет и ряд неожиданных свойств — в частности, он вызывает снижение патогенности Pseudomonas aeruginosa и обладает протективным эффектом в отношении Haemophilus influenzae в культурах эпителия респираторного тракта [19–21]. САЛ является высокобезопасным препаратом, что доказано многочисленными клиническими исследованиями.
Первым препаратом с фиксированной комбинацией был Серетид®, содержащий ИГКС ФП и САЛ и относящийся к ингаляционным β длительного действия.
Комбинированный препарат ФП и САЛ. В исследовании S. Kirby et al. было показано, что при использовании комбинации САЛ и ФП у здоровых людей не наблюдается системных фармакодинамических или фармакокинетических взаимодействий [22]. Исследование GOAL (Gaining Optimal Asthma control), результаты которого легли в основу стратегии контроля GINA (2006), демонстрируют преимущества комбинированной терапии ИГКС + ДДБА при среднетяжелой и тяжелой БА [23]. Результаты исследования GOAL имеют важное практическое значение, в нем сформулированы критерии эффективности лечения БА. По данным исследования GOAL, около 40% больных БА, получавших фиксированную комбинацию САЛ/ФП, достигли полного контроля над БА по истечении 12 мес. лечения. Не менее важно, что в группе, получавшей в качестве базисной терапии фиксированную комбинацию, пациентов, достигших полного контроля над БА, было достоверно больше, чем в случае монотерапии ФП. Благодаря исследованию GOAL был сделан важный вывод о том, что улучшить результаты лечения можно, выбрав наиболее эффективную базисную терапию.
Исследование, проведенное et al., продемонстрировало, что у пациентов с персистирующей БА стартовая терапия САЛ/ФП по сравнению с ФП обеспечивала в 1,65 раза более вероятное достижение хорошо контролируемой БА у пациентов с признаками плохого контроля БА до лечения и в 2,6 раза более вероятное достижение хорошо контролируемой БА у пациентов с признаками плохого контроля БА до лечения [24].
Оригинальные препараты и дженерики. Оригинальный препарат с фиксированной комбинацией ФП и САЛ Серетид® широко и с успехом применяется для лечения БА и ХОБЛ с помощью метиодозированного (МDI) и порошкового (Diskus) ингаляторов. Применение оригинальных препаратов возможно только при получении достоверно доказанных результатов клинических испытаний по изучению безопасности и эффективности препаратов. Так, на всех стадиях клинических исследований фиксируются все неблагоприятные реакции; это происходит и в течение ряда лет после вывода препаратов на рынок. Эти условия определяют цену оригинальных препаратов. Когда истекает срок действия патента оригинальных препаратов, наиболее успешные медикаменты начинают выпускать в виде дженериков — копий оригинального лекарства. Причем копия должна быть полной, на нее автоматически экстраполируются результаты клинических исследований оригинального препарата. Дженерики всегда дешевле оригинальных препаратов, что расширяет возможности терапии. Требования ВОЗ к дженерикам в отношении фармацевтической и терапевтической эквивалентности довольно жесткие — дженерик должен действовать точно так же, как оригинальный препарат, иметь такие же эффективность и безопасность.
В настоящее время на рынок выведен препарат Сальмекорт, в котором фиксированная комбинация активных компонентов — ФП и САЛ соответствует по дозировке оригинальному препарату, выпускаемому в MDI. В России было проведено открытое рандомизированное многоцентровое исследование по проверке гипотезы о не меньших эффективности и безопасности препарата Сальмекорт (25/250 мкг, в форме аэрозоля для ингаляций дозированного) по сравнению с препаратом Серетид® (25/250 мкг, в форме аэрозоля для ингаляций дозированного) при лечении пациентов с персистирующей БА и нуждающихся в комбинированной терапии высокими дозами ИГКС и β пролонгированного действия.
Задачи данного исследования:
1. Сравнительная оценка уровня контроля БА и его динамики в течение исследования.
2. Сравнительная оценка безопасности и переносимости препаратов Сальмекорт и Серетид®.
В исследовании принимали участие врачи из 5 ведущих медицинских учреждений России. Диагноз БА устанавливался врачом в соответствии с практикой лечебного учреждения. После подписания информированного согласия на участие в исследовании пациентам (113 человек) проводился скрининг, вводный период имел продолжительность в среднем 14 дней. За это время исследователь оценивал соответствие пациента критериям включения/невключения и стабильность заболевания. Затем 107 пациентов, соответствовавших критериям включения/невключения, были рандомизированы на 2 лечебные группы.
Пациентам группы (n=56) был назначен Сальмекорт по 2 ингаляции 2 р./сут, пациентам группы (n=51) — Серетид® по 2 ингаляции 2 р./сут. Первый прием препаратов проводился в центре под наблюдением медицинского персонала после выполнения спирометрии. Исследователь инструктировал пациентов, как правильно вводить препараты.
Пациенты принимали препараты ежедневно в течение 12 нед. У них систематически проводилась спирометрия. Пациенты должны были ежедневно вести дневник — утром и вечером записывать показатели пикфлоуметрии, а также наличие симптомов БА и потребность в бронходилататорах. В период приема исследуемых препаратов было предусмотрено 3 визита пациентов в центр с периодичностью 4 нед. После завершающего визита на день от начала лечения участие пациента в исследовании прекращалось, дальнейшая терапия осуществлялась лечащим врачом.
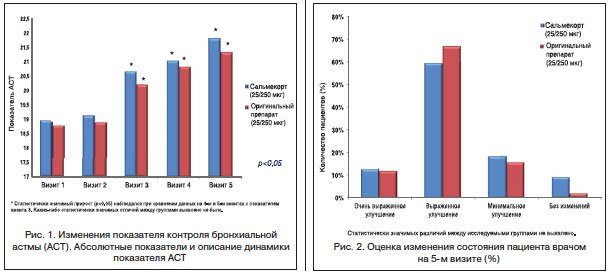
При проведении анализа эффективности было выявлено:
Анализ частоты возникновения нежелательных явлений, проведенный с использованием методики «bootstrap», не выявил статистически значимой разницы между группами терапии по данному параметру.
Ни в одном случае не было отмечено развития кандидозного поражения слизистых ротоглотки на фоне применения исследовавшихся препаратов.
Результаты исследования позволили сделать следующие выводы:
Следует помнить о том, что и Серетид®, и Сальмекорт не назначают для купирования симптомов БА. С этой целью предпочтительно назначать β короткого действия. При необходимости увеличения дозы ИГКС не следует превышать допустимые дозы САЛ. В этом случае следует назначить больному препарат с более высоким содержанием ФП.
Только для зарегистрированных пользователей