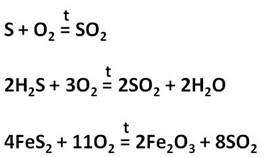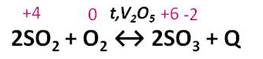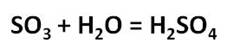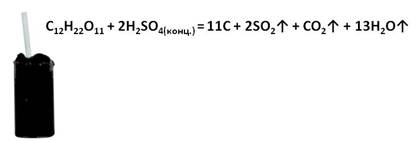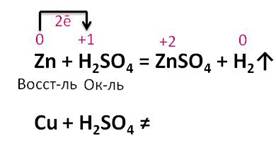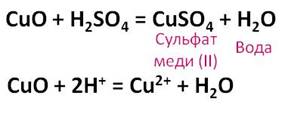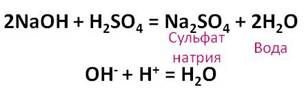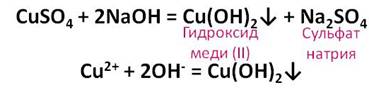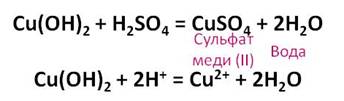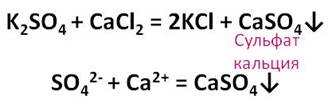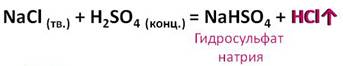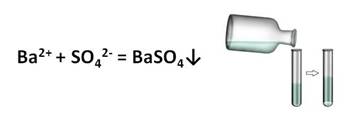с помощью каких реакций можно определить наличие в растворе серной кислоты или ее солей
Серная кислота и её соли
Урок 21. Химия 9 класс ФГОС
В данный момент вы не можете посмотреть или раздать видеоурок ученикам
Чтобы получить доступ к этому и другим видеоурокам комплекта, вам нужно добавить его в личный кабинет, приобрев в каталоге.
Получите невероятные возможности
Конспект урока «Серная кислота и её соли»
Серная кислота и её соли
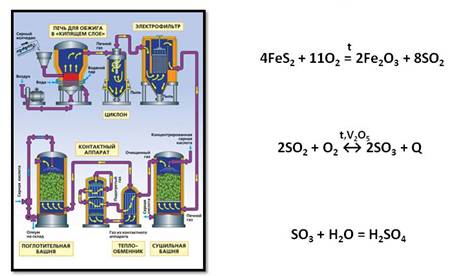
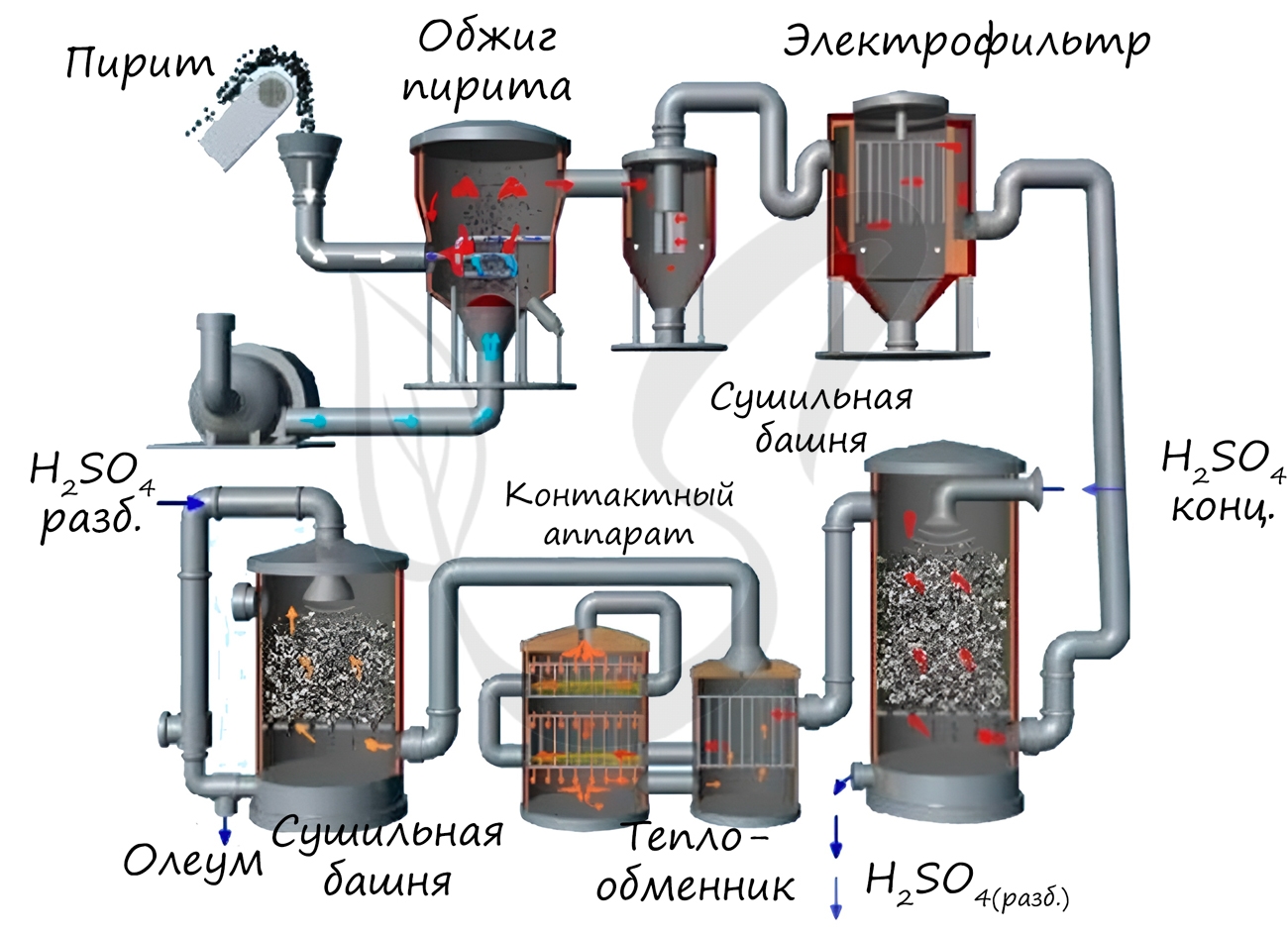
Как получают серную кислоту? Получают серную кислоту в три стадии.
В качестве сырья для получения серной кислоты применяют серу, сероводород или пирит. При обжиге этих соединений образуется сернистый газ.
Затем проводят реакцию окисления оксида серы (IV) до оксида серы (VI). Эта реакция протекает при высокой температуре и в присутствии катализатора – оксида ванадия (V).
Оксид серы (VI) представляет собой летучую бесцветную жидкость с удушливым запахом. Этот оксид при растворении в воде образует серную кислоту.
Однако, при получении серной кислоты оксид серы (VI) растворяют не в воде, а в концентрированной серной кислоте, при этом получается олеум – раствор оксида серы (VI) в безводной серной кислоте.
Поэтому производство серной кислоты идёт в три стадии: на первой стадии из исходного сырья получают оксид серы (IV), на второй стадии из оксида серы (IV) получают оксид серы (VI), а на третьей стадии из оксида серы (VI) получают серную кислоту.
Производство серной кислоты создаёт ряд проблем: выбросы от производств оказывают негативное воздействие на животный и растительный мир, повышается коррозионная стойкость материалов, разрушаются сооружения из мрамора и известняка, а также происходит закисление почв.
Серная кислота – H2SO4 – бесцветная маслянистая и тяжёлая жидкость. Она обладает сильными гигроскопическими, то есть водоотнимающими свойствами, это позволяет использовать её для осушения газов или других веществ.
Концентрированная серная кислота способна отнимать воду у молекул органических веществ, обугливая их. Например, при добавлении к сахару концентрированной серной кислоты сахар чернеет и в виде объёмной массы поднимается вверх.
Помните, при разбавлении концентрированной серной кислоты нельзя приливать воду к кислоте, а следует тоненькой струйкой приливать кислоту в воду, чтобы избежать сильного разогревания раствора.
Химические свойства разбавленной и концентрированной серной кислоты отличаются.
Так разбавленная серная кислота проявляет все характерные свойства кислот. Она изменяет окраску индикаторов: лакмус в растворе кислоты красный, метиловый оранжевый тоже.
Серная кислота вступает во взаимодействие с металлами, стоящими в ряду напряжений металлов до водорода.
Нальём в две пробирки раствора серной кислоты, в первую пробирку поместим гранулу цинка, а во вторую – кусочек меди. Выделение водорода идёт только в первой пробирке, во второй пробирке изменений нет
Цинк, в отличие от меди, стоит в ряду напряжений металлов до водорода, поэтому он вытеснил водород из раствора кислоты. При чем, это окислительно-восстановительная реакция, цинк повышает свою степень окисления с 0 до +2, а водород понижает с +1 до 0. Каждый атом цинка отдаёт по 2 электрона ионам водорода. Поэтому цинк – восстановитель, а водород – окислитель.
Разбавленная серная кислота реагирует с основными и амфотэрными оксидами с образованием соли и воды. Если поместить в пробирку немного чёрного порошка оксида меди (II) и прилить немного раствора серной кислоты, а затем содержимое нагреть на пламени спиртовки, то постепенно чёрный порошок оксида меди (II) начинает растворяться, а раствор меняет свою окраску на голубую.
В результате данной реакции образуется соль – сульфат меди (II) и вода.
Разбавленная серная кислота вступает во взаимодействие с основаниями. Например, к раствору щёлочи добавим несколько капель фенолфталеина, раствор приобретает малиновую окраску. К этому раствору прильём разбавленную серную кислоту до исчезновения окраски. Таким образом, между щёлочью и кислотой прошла реакция нейтрализации, при этом образовалась соль – сульфат натрия и вода.
Разбавленная серная кислота реагирует не только с растворимыми основаниями – щелочами, но и с нерастворимыми. Получим нерастворимое основание – гидроксид меди (II). Для этого, в раствор медного купороса прильём щёлочи – гидроксид натрия, в результате чего образуется гидроксид меди (II) и соль – сульфат натрия.
Теперь, к этому осадку добавим раствор серной кислоты до его исчезновения. В результате данной реакции образуется соль – сульфат меди (II) и вода.
Кроме этого, разбавленная серная кислота реагирует с солями. Прильём к раствору сульфата калия раствор хлорида кальция. В результате образуется малорастворимое вещество белого цвета. Это сульфат кальция.
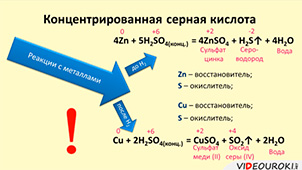
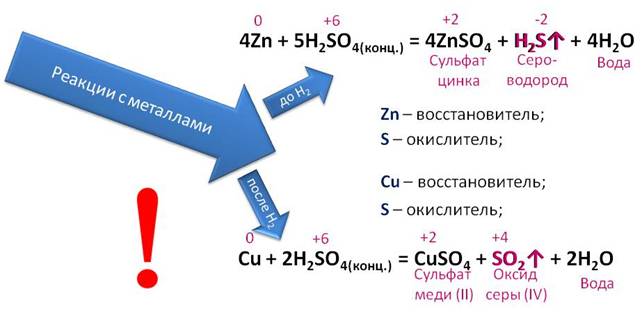
Концентрированная серная кислота также реагирует с металлами. Если металл стоит в ряду напряжений до водорода, то в результате реакции образуется газ сероводород и вода.
В реакции с металлами, стоящими после водорода образуется оксид серы (IV). Например, при взаимодействии меди с концентрированной серной кислотой, образуется соль – сульфат меди (II), оксид серы (IV) и вода. В этой реакции медь повышает свою степень окисления с 0 до +2, а сера понижает с +6 до +4. Поэтому медь восстановитель, а сера – окислитель.
Обратите внимание, что в данных реакциях водород не выделяется, потому что здесь окислителем выступает не водород, а сера.
Железо и алюминий пассивируются концентрированной серной кислотой, потому что покрываются защитной плёнкой, что позволяет перевозить её в стальных и алюминиевых цистернах.
Концентрированная серная кислота вытесняет кислоты из их солей. Например, если к твёрдому хлориду натрия добавить концентрированной серной кислоты, то образуется соль – гидросульфат натрия и хлороводород.
Серная кислота – это двухосновная кислота, поэтому она образует средние и кислые соли. Соли серной кислоты – сульфаты. Например, Na2SO4 – сульфат натрия, NaHSO4 – гидросульфат натрия.
Качественной реакцией на серную кислоту и её соли является ион бария. В результате взаимодействия сульфат-иона и иона бария образуется сульфат бария – осадок белого цвета.
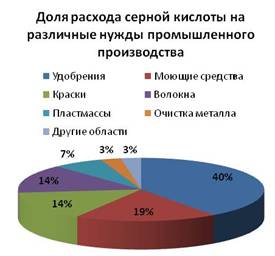
Серная кислота находит широкое применение. Она используется при производстве взрывчатых веществ, минеральных удобрений, электролитической меди, моющих средств, эмалей и красок, искусственного шёлка, лекарств, пластмасс, при очистке нефтепрдуктов, в качестве электролита в аккумуляторах.
Среди солей серной кислоты наиболее распространена глауберова соль – Na2SO4 ∙ 10H2O, гипс – CaSO4 ∙ 2H2O, BaSO4 – сульфат бария и CuSO4 ∙ 5H2O – медный купорос, который используют для борьбы с вредителями и болезнями растений.
Таким образом, серную кислоту получают в три стадии, она представляет собой тяжёлую маслянистую жидкость. При разбавлени концентрированной кислоты следует кислоту приливать к воде, а не наоборот. Свойства разбавленной и концентрированной кислот различаются. Разбавленная серняа кислота реагирует с металлами до водорода, основными и амфотэрными оксидами, с основаниями и солями, а концентрированная серная кислота взаимодействует с металлами и до водорода и после водорода (кроме золота и платины), она пассивирует железо и алюминий, а также реагирует с солями. Серная кислота и её соединения находят широкое применение в промышленности.
С помощью каких реакций можно определить наличие в растворе серной кислоты или ее солей
Физические свойства серной кислоты
Техника безопасности при обращении с концентрированной серной кислотой
Помните! Кислоту вливать малыми порциями в воду, а не наоборот!
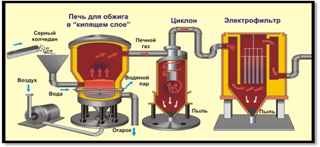
Производство серной кислоты
1-я стадия. Печь для обжига колчедана
1) измельчение железного колчедана (пирита)
2) метод «кипящего слоя»
3) 800°С; отвод лишнего тепла
4) увеличение концентрации кислорода в воздухе
После очистки, осушки и теплообмена сернистый газ поступает в контактный аппарат, где окисляется в серный ангидрид (450°С – 500°С; катализатор V 2 O 5 ):
3-я стадия . Поглотительная башня
Воду использовать нельзя из-за образования тумана. Применяют керамические насадки и принцип противотока.
Химические свойства разбавленной серной кислоты
2) Взаимодействие с металлами:
Разбавленная серная кислота растворяет только металлы, стоящие в ряду напряжений до водорода:
Zn 0 + 2 H + → Zn 2+ + H 2 0 ↑
3) Взаимодействие с основными и амфотерными оксидами :
4) Взаимодействие с основаниями:
H 2 SO 4 + 2 NaOH → Na 2 SO 4 + 2 H 2 O (реакция нейтрализации)
Если кислота в избытке, то образуется кислая соль:
2 H + + Cu ( OH )2 → Cu 2+ + 2 H 2 O
5) Взаимодействие с солями, если в результате реакции образуется осадок или выделяется газообразная летучая кислота:
Качественная реакция на сульфат-ион:
Образование белого осадка BaSO 4 (нерастворимого в кислотах) используется для определения серной кислоты и растворимых сульфатов.
Особые свойства концентрированной серной кислоты
1. Очень гигроскопична, поглощает воду из окружающей среды; органические вещества обугливаются! Опыт «Гигроскопичность серной кислоты»
Взаимодействие серной кислоты с металлами разной активности с образованием соли, воды и продукта восстановления серы (S, H2S, SO2) : ОПЫТ
3. Серная кислота окисляет неметаллы :
С 0 + 2H 2 S +6 O 4 (конц) → C +4 O 2 + 2S +4 O 2 + 2H 2 O
Самый крупный потребитель серной кислоты — производство минеральных удобрений. На 1 т P₂O₅ фосфорных удобрений расходуется 2,2-3,4 т серной кислоты, а на 1 т (NH₄)₂SO₄ — 0,75 т серной кислоты. Поэтому сернокислотные заводы стремятся строить в комплексе с заводами по производству минеральных удобрений.
Применение солей серной кислоты
Железный купорос FеSО4•7Н2O применяли раньше для лечения чесотки, гельминтоза и опухолей желез, в настоящее время используют для борьбы с сельскохозяйственными вредителями.
Медный купорос CuSO4•5Н2O широко используют в сельском хозяйстве для борьбы с вредителями растений.
«Глауберова соль» (мирабилит) Nа2SO4•10Н2O была получена немецким химиком И. Р. Глаубером при действии серной кислоты на хлорид натрия, в медицине ее используют как слабительное средство.
«Бариевая каша» BaSO4 обладает способностью задерживать рентгеновские лучи в значительно большей степени, чем ткани организма. Это позволяет рентгенологам при заполнении «бариевой кашей» полых органов определить в них наличие анатомических изменений.
Гипс СаSO4•2Н2O находит широкое применение в строительном деле, в медицинской практике для накладывания гипсовых повязок, для изготовления гипсовых скульптур.
№1. Осуществите превращения по схеме:
№2. Закончите уравнения практически осуществимых реакций в полном и кратком ионном виде:
№3. Запишите уравнения реакций взаимодействия разбавленной серной кислоты с магнием, гидроксидом железа (III), оксидом алюминия, нитратом бария и сульфитом калия в молекулярном, полном и кратком ионном виде.
Серная кислота
Обладает выраженным дегидратационным (водоотнимающим) действием. При попадании на кожу или слизистые оболочки приводит к тяжелым ожогам.
Получение
Известны несколько способов получения серной кислоты. Применяется промышленный (контактный) способ, основанный на сжигании пирита, окислении образовавшегося SO2 до SO3 и последующим взаимодействием с водой.
Нитрозный способ получения основан на взаимодействии сернистого газа с диоксидом азота IV в присутствии воды. Он состоит из нескольких этапов:
В окислительной башне смешивают оксиды азота (II) и (IV) с воздухом:
Смесь газов подается в башни, орошаемые 75-ной% серной кислотой, здесь смесь оксидов азота поглощается с образованием нитрозилсерной кислоты:
В ходе гидролиза нитрозилсерной кислоты получают азотистую кислоту и серную:
В упрощенном виде нитрозный способ можно записать так:
Химические свойства
В водном растворе диссоциирует ступенчато.
С солями реакция идет, если в результате выпадает осадок, образуется газ или слабый электролит (вода). Серная кислота, как и многие другие кислоты, способна растворять осадки.
Подчеркну, что реакции разбавленной серной кислоты с железом и хромом не сопровождаются переходом этих элементов в максимальную степень окисления. Они окисляются до +2.
Cu + H2SO4(разб.) ⇸ (реакция не идет, медь не может вытеснить водород из кислоты)
Холодная концентрированная серная кислота пассивирует Al, Cr, Fe, Ni, Be, Co. При нагревании или амальгамировании данных металлов реакция идет.
Обратите особое внимание, что при реакции железа, хрома с концентрированной серной кислотой достигается степень окисления +3. В подобных реакциях с разбавленной серной кислотой (написаны выше) достигается степень окисления +2.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
С помощью каких реакций можно определить наличие в растворе серной кислоты или ее солей
Соляную кислоту можно отличить от раствора хлорида натрия с помощью
1) раствора
4) раствора
Соляная кислота имеет кислую реакцию среды, а раствор хлорида натрия — нейтральную. Значит, различить их можно с помощью индикатора, например, лакмуса.
Правильный ответ указан под номером 2.
Установите соответствие между двумя веществами, взятыми в виде водных растворов, и реактивом, с помощью которого можно различить эти два вещества. К каждому элементу первого столбца подберите соответствующий элемент из второго столбца.
| ВЕЩЕСТВА | РЕАКТИВ |
| А) | 1) лакмус |
| Б) | 2) фенолфталеин |
| В) | 3) |
| 4) |
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
1. Медь вытесняет серебро из растворов солей.
Соль серебра можно обнаружить по изменению цвета металла металла и раствора.
С раствором соли натрия медь не реагирует.
2. Серная кислота даёт кислую реакцию среды. Сульфат калия — соль сильного основания и сильной кислоты, даёт нейтральную реакцию среды. Различить растворы можно с помощью лакмуса (появление красной окраски индикатора в случае кислой среды и фиолетовой окраски в случае нейтральной).
3. — выпадение белого творожистого осадка хлорида серебра.
— выпадение жёлтого осадка иодида серебра.
Подтвердить качественный состав карбоната аммония можно с помощью двух растворов, содержащих соответственно ионы
1) и
2) и
3) и
4) и
Карбонат аммония имеет формулу . Чтобы определить его качественный состав, нужно провести качественные реакции на катион и анион. При реакции с кислотой (
) выделится углекислый газ, что говорит нам о наличии карбонат иона, а со щелочью — аммиак, что говорит о наличии катиона аммония.
Правильный ответ указан под номером 4.
С помощью соляной кислоты можно распознать
При реакции соляной кислоты с карбонатом натрия выделится углекислый газ — это качественная реакция на карбонаты.
Правильный ответ указан под номером 1.
Почему 4 не верно?Там тоже должен выделиться газ.
Все продукты растворимы и газ не выделяется, поэтому реакция не идет.
Установите соответствие между двумя веществами и реактивом, с помощью которого можно различить эти вещества.
А) (г) и
(г)
Б) (р-р) и
(р-р)
В) (тв.) и
(тв.)
1) (р-р)
2) (р-р)
4) (р-р)
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
А) (г) и
(г) при пропускании углекислого газа через раствор гидроксида кальция сначала образуется осадок карбоната кальция, который затем растворится перейдя в гидрокарбонат кальция. С кислородом взаимодействия не будет.
Б) (р-р) и
(р-р) в щелочной среде фенолфталеин имеет малиновую окраску.
В) (тв.) и
(тв.) при реакции карбоната бария с раствором азотной кислоты будут выделяться пузырьки углекислого газа, тогда как при реакции оксида бария с кислотой этого наблюдаться не будет.
А если BaCO3 c Ca(OH)2, то получится CaCO3 (осадок). А с BaO реакции вообще не будет. Получается что ответом может быть 232?
Тут может быть 241
Карбонат бария нерастворимая соль, поэтому реакция с сульфатом натрия не пойдет как и для оксида бария.
А взаимодействие кислот, на сколько я знаю, выходит за рамки школьной программы, по крайней мере для 9х классов, хотя соляную кислоту и раствор аммиака действительно можно различить с помощью азотной кислоты.
В пояснении написано, что происходит с фенолфталеином в щелочной среде, однако в задании дана кислота
Раствор аммиака имеет щелочную среду.
Установите соответствие между двумя веществами и реактивом, с помощью которого можно различить эти вещества.
А) (р-р) и
(р-р)
Б) (тв.) и
(тв.)
В) (р-р) и
(р-р)
1)
3) (р-р)
4)
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
А) (р-р) и
(р-р) нитрат бария образует осадок сульфата бария при смешении с раствором сульфата меди(II), а в случае хлорида меди(II) реакции не будет.
Б) (тв.) и
(тв.) сульфат натрия растворим в воде, а сульфат бария — нет.
В) (р-р) и
(р-р) в щелочной среде, которую имеет раствор аммиака, фенолфталеин малиновый.
Установите соответствие между двумя веществами, взятыми в виде водных растворов, и реактивом, с помощью которого можно различить эти два вещества.