Какие группы лекарств эффективны от простатита: полный перечень
Простатит – острый воспалительный процесс в предстательной железе, который устраняется разными группами лекарств. Подбор эффективных препаратов от простатита у мужчин зависит от нескольких факторов – курс лечения подбирает только врач по результатам диагностики.
Группы препаратов от простатита
В зависимости от фазы и стадии заболевания, патогенеза и клинической картины, специалист назначит комплекс лекарств из одной или нескольких групп препаратов:
В дополнение к препаратам назначаются:
Оперативное вмешательство назначается также по показаниям. Подбор препарата, курса лечения и дозировки зависит от причины простатита, степени поражения железы и выраженности симптомов, потому для каждого пациента врач подберет индивидуальную схему.
Антибиотики
Антибактериальные препараты при остром простатите назначаются, когда обнаружена патогенная микрофлора – ее определяют по результатам бакпосева вместе с ее чувствительностью к тем или иным антибиотикам. В числе антибиотиков: Солютаб, Сумамед, Офлоксацин, Ципрофлоксацин, Амоксиклав и др.
Самостоятельный прием антибиотиков угрожает развитием резистентности у бактерий! Принимать антибиотики безопасно только по рекомендации врача, строго в указанной дозировке и не меньше предписанного количества дней.
Адреноблокаторы
Препараты этой группы расслабляют чрезмерно напряженную шейку мочевого пузыря, гладкие мышцы простаты, улучшают дренирование тканей железы. Облегчают симптомы заболевания: задержку мочеиспускания, болезненность при опорожнении мочевого пузыря.
В числе адреноблокаторов: Алфузозин, Артезин, Ницерголин и другие. Форму препарата и его дозировку при необходимости приема определит уролог.
Воспалительный процесс ослабляется негормональными противовоспалительными средствами. Они устраняют болезненные симптомы патологии: отечность, температуру, слабость. Применяются в форме таблеток, свечей, инфузий, инъекций – форму подбирает врач по результатам обследования. К этой группе относятся Диклофенак, Кетопрофен и другие.
Обратите внимание! НПВС способны пагубно влиять на состояние слизистой оболочки желудка и кишечника, имеют ряд побочных эффектов. Не принимайте препараты, если их не назначил врач!
Миорелаксанты
Снимают спазмы мышц, облегчая мочеиспускание и физическую активность. Так как воспаление провоцирует спазмы гладкой мускулатуры близлежащих органов, миорелаксанты используются в рамках симптоматической терапии. К ним относятся Баклофен, Тамсулозин и другие.
Антикоагулянты
Улучают микроциркуляцию крови, предотвращают образование тромбов. Помогают доставлять активные компоненты лекарств к железе за счет улучшенного кровоснабжения. Принимаются строго под наблюдением врача – запишитесь к урологу для получения полной схемы лечения, и только затем приступайте к приему. К группе относятся Кумадин, Синтром, Прадакса и другие.
Растительные препараты при простатите
К недорогим, но эффективным препаратам от простатита относятся растительные биодобавки – они назначаются в рамках комплексной терапии, как вспомогательное средство:
Натуральные препараты содержат антиоксиданты, флаваноиды, которые при неправильном назначении могут ухудшить состояние пациента. Схему лечения назначит уролог после инструментальной и лабораторной диагностики.
Комплексное лечение простатита
Уролог назначает процедуры, медикаменты и физиотерапию по результатам:
Препараты, которые принимают при простатите, действуют комплексно и только в случае, когда назначены в правильной дозировке и длительности приема.
Специалисты клиники Dr. AkNer в Москве более 40 лет занимаются диагностикой и лечением острого, хронического простатита. Обращайтесь, чтоб пройти обследование на современном оборудовании, получить консультацию и лечение от опытных урологов, распрощаться с заболеванием навсегда!
Комбинированная терапия доброкачественной гиперплазии предстательной железы: преимущества и недостатки
Раньше пациенты, не отвечающие на андрогендепривационную терапию (АДТ), считались безнадежными: до 2004 г. онкологи не могли предложить ничего, кроме паллиативной помощи митоксантроном. Сейчас, манипулируя гормонами, можно отсрочить использование цитостатиков даже в отношении мужчин с метастатическим раком предстательной железы (РПЖ), который уже не отвечает на гормо нальную терапию и даже доцетаксел… Противоречие? Нет! Просто изменилось представление о гормональной независимости опухоли, и появились препараты, подавляющие синтез тестостерона даже в клетках самой опухоли.
Рак простаты: истинно гормонозависимая опухоль
 |
| Автор | Дизайн | Число пациентов | Длительность лечения | Контрольная/экспери ментальная группа | Первичные критерии оценки эффективности лечения | Побочные эффекты |
| H. Lepor (VA study), 1996 | RCT | 1007 | 12 мес | теразозин/финастерид/ комбинация/плацебо | AUA-SI, скорость мочеиспускания | Оценивались |
| F. Debruyne (ALFIN), 1998 | RCT | 1051 | 6 мес | альфузозин/финастерид/ комбинация | IPSS, скорость мочеиспускания | Оценивались |
| R. Kirby (PREDICT), 2003 | RCT | 1095 | 12 мес | доксазозин/финастерид/ комбинация/плацебо | IPSS, скорость мочеиспускания | Оценивались |
| J. McConnell (MTOPS), 2003 | RCT | 3047 | 4,5 года | доксазозин/финастерид/ комбинация/плацебо | Прогрессирование заболевания (увеличение баллов AUA-SI, частота развития острой задержки мочеиспускания (ОЗМ), почечной недостаточности, рецидивирующих инфекций мочевыводящих путей, недержания мочи) | Оценивались |
| C. Roehrborn (CombAT), 2008, 2010 | RCT | 4844 | 4 года | тастерид/ тамсулозин/ду комбинация | Через 2 года – снижение суммы баллов IPSS, через 4 года – частота возникновения ОЗМ и оперативного лечения по поводу ДГПЖ | Оценивались |
Анализ клинической эффективности комбинированной терапии доброкачественной гиперплазии предстательной железы
Таблица 2. Изменение суммы баллов индекса IPSS/AUASI к концу лечения
Главное меню
Главное меню
Пермиксон: место препарата в патогенетической терапии ДГПЖ
Проблема лечения больных доброкачественной гиперплазией предстательной железы (ДГПЖ) до сих пор остается актуальной. Согласно литературным данным 15-25% мужчин в возрасте 50-65 лет страдают этим заболеванием, которое приводит к выраженному снижению качества жизни за счет симптомов нарушения функции нижних мочевых путей (СНМП) [1]. В настоящее время считают, что в патогенезе ДГПЖ имеет значение как генетическая предрасположенность, так и дисрегуляция гормонального обмена, которая приводит к активации гиперпластических процессов в предстательной железе (ПЖ), торможению апоптоза, а также – к выделению целого ряда медиаторов, вызывающих хроническое воспаление.
СОВРЕМЕННЫЕ ПРЕДСТАВЛЕНИЯ О ПАТОГЕНЕЗЕ ДГПЖ
Постоянная стимуляция АР необходима, прежде всего, для роста и функции ПЖ. Этот процесс работает путем трансактивации домена закодированного в первом экзоне гена АР (Xq 11-12), которому в норме свойственен полиморфизм CAG, GGN и GGC повторов, кодирующих тракты полиглутамина и полиглицина 3. При исследовании генетического полиморфизма некоторых генов, ответственных за метаболизм стероидов, показана их тесная связь с вероятностью возникновения ДГПЖ. Об этом свидетельствует тот факт, что у родственников – мужчин больных с ранним возникновением ДГПЖ, кумулятивный риск возникновения этого заболевания составляет 66%, тогда как в контрольной группе – лишь 17% (p=0,01) [5,6].
Кроме того, при исследовании полиморфизма генов, кодирующих 5α-R 2 типа (SRD 5A1 и SRD 5 A2), было установлено, что имеется тесная взаимосвязь между выраженностью полиморфизма генов, объемом ДГПЖ, эффективностью проводимой антиандрогенной терапии и концентрацией половых гормонов и их метаболитов [7,8].
Интересна роль α1-адренорецепторов в патогенезе ДГПЖ. Предполагают, что в ПЖ они участвуют в процессе кооперативной регуляции работы внутриклеточных эффекторов, гормонов, факторов роста, которые влияют не только на тонус гладкомышечных элементов ПЖ, но и на их объем [9].
В последнее время появилось большое число исследований, показывающих, что ДГПЖ – это иммуновоспалительное заболевание. При этом, в ткани ПЖ обнаруживают воспалительные инфильтраты, содержащие лимфоциты и макрофаги, количество которых коррелирует с объемом ДГПЖ. Они секретируют факторы роста, включая фактор роста фибробластов (FGF), цитокины: интерлейкин-1 (IL-1), интерлейкин-6 (IL-6), фактор некроза опухоли-α (TNF-α). Также наблюдают повышенную активность Т-клеток и аутоиммунные реакции, которые способствуют пролиферации стромальных и эпителиальных клеток. Было показано, что повышенное содержание в ткани при ДГПЖ провоспалительных цитокинов и цитокинов семейства IL-17 A, E, F и их рецепторов, сопровождает повышение содержания клеток воспаления и сосудов с экспрессией CD 31+, а также провоспалительных хемокинов: MCP-1/CCL2 (фактор хемотаксиса моноцитов), IP-10/CXCL10 (индуцируемый гамма-интерфероном белок), MIF (фактор ингибирующий миграцию макрофагов) [10]. Провоспалительные цитокины повышают активность циклооксигеназы-2 (COX-2) и вызывают образование простагландинов и окиси азота, что стимулирует пролиферативные процессы в ПЖ и вызывает ее отечность. Ряд авторов считают, что активные формы кислорода приводят к повреждению ткани ПЖ, так как после завершения процесса трансляции вызывают модификацию структуры ДНК и ее клеток, что может привести к малигнизации процесса [11,12].
Сахарный диабет и метаболический синдром являются факторами риска образования ДГПЖ. Отмечена взаимосвязь между резистентностью к инсулину, гиперинсулинемией и ДГПЖ. Гиперинсулинемия приводит к образованию в печени инсулиноподобных факторов роста (IGF), которые обладают митогенным и антиапоптическим эффектом. Эти факторы связываются в ПЖ со своими рецепторами и стимулирует увеличение ее объема. Концентрация IGF и белков, связывающих IGF в крови и ПЖ, коррелирует с выраженностью в ней пролиферативных процессов и участвует в регуляции образования андрогенов и гормона роста.
ОБЩИЕ ПОДХОДЫ К ЛЕЧЕНИЮ ДГПЖ
Современное лечение ДГПЖ / СНМП воздействует на различные звенья патогенеза этого заболевания. На первом месте стоят α1А-адреноблокаторы (доксазозин, теразозин, алфузозин, тамзулозин, силодозин): их считают препаратами выбора при ДГПЖ. Затем идут ингибиторы 5α-редуктазы (финастерид, дутастерид), которые при длительной терапии у пациентов с величиной ПЖ более 40 куб. см способны привести к уменьшению объема ДГПЖ. М-холинолитики (толтеродин, троспиума хлорид, солифенацин) и агонист β3-адренорецепторов – мирабегрон чаще используют в комбинации с α1А-адреноблокаторами для купирования проявлений гиперактивного мочевого пузыря при ДГПЖ. Тадалафил (ингибитор фосфодиэстеразы 5 типа) улучшает симптомы ДГПЖ у больных, страдающих эректильной дисфункцией. По показаниям применяют нестероидные противовоспалительные препараты [14,15]. Обсуждают возможность применения антиоксидантов при ДГПЖ [16]. Однако, все эти препараты обладают целым рядом побочных эффектов и воздействуют только на отдельные фазы патогенеза ДГПЖ.
При длительном применении необходимо использовать лекарственные средства, которые оказывают влияние на большинство звеньев патогенеза заболевания, обладают оптимальным терапевтическим действием и отсутствием побочных эффектов. В этом отношении в отдельную группу выделены фитосоединения, в том числе экстракты Serenoa repens (экстракты плодов пальмы ползучей – ЭППП), которые широко используют в Европе и США для лечения ДГПЖ и СНМП 17. Наиболее известным и изученным из них является Пермиксон.
МЕХАНИЗМЫ ДЕЙСТВИЯ ПЕРМИКСОНА
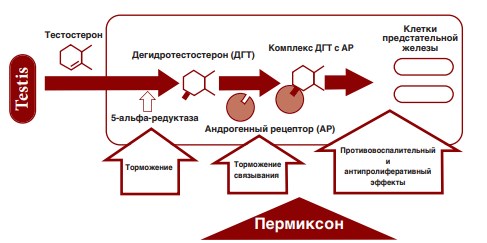
Пермиксон (Permixon) представляет собой комплексную смесь свободных и эстерифицированных жирных кислот, полипренов и фитостеролов, полученных из плодов пальмы ползучей (Serenoa repens или Sabal serrulata). Препарат содержат несколько ингредиентов и поэтому при его применении возможен комплексный фармакологический эффект, действующий на различные звенья патогенеза ДГПЖ (рис. 1).
Рис.1. Патогенез ДГПЖ и механизм действия Пермиксона
Другими словами, эффект этой смеси можно сравнить с комбинированной лекарственной терапией, каждый компонент которой может обладать по отношению к другому аддитивным или синергическим действием.
Влияние Пермиксона на клеточные структуры ПЖ
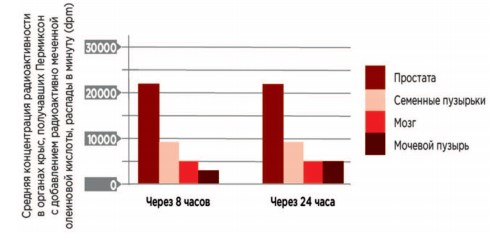
При исследовании любого препарата, как правило, проводят изучение специфичности и селективности его действия. Это касается и Пермиксона. C.W. Bayne и соавт. в культуры тканей из различных органов добавили нарастающие концентрации Пермиксона. При исследовании препаратов этих культур на электронном микроскопе оказалось, что только в клетках ПЖ были отмечены выраженные структурные изменения, которые заключались в накоплении липидных капель в цитоплазме, изменении мембраны ядра, его поляризации, разрушении органелл, конденсации хроматина. Это подтвердило специфичное действие Пермиксона именно на клетки ПЖ [20]. При присоединении радиоактивной метки к входящим в состав Пермиксона свободным жирным кислотам и введении его крысам, оказалось, что в наибольших количествах метка накапливалась в ПЖ (рис. 2), что свидетельствует в пользу селективности действии лекарственного препарата на этот орган [21].
Рис. 2. Простатспецифическое действие препарата Пермиксон [21]
Таким образом, преимущественное накопление компонентов Пермиксона в ПЖ вызывает в ней морфологические изменения, которые могут отразиться на физикохимических характеристиках и повлиять на различные системы регуляции работы органа, как на клеточном, так и молекулярном уровнях.
Влияние Пермиксона на гормональный статус ПЖ
В 1998 году F. Di Silverio с соавт. сообщили, что трехмесячная терапия Пермиксоном приводит к выраженному уменьшению содержания ДГТ в ПЖ [22]. Затем в опытах in vitro на культуре эпителиальных клеток и клеток рака ПЖ было показано, что Пермиксон тормозит активность 5α-R 1 и 2 типов и не вызывает повышения концентрации простатспецифического антигена (ПСА) в культуральной среде. Это, по-видимому, связано с тем, что препарат не влияет на опосредованный АР процесс транскрипции [20,23]. Данный феномен был подтвержден и in vivo [24]. Интересно отметить, что при культивировании клеток других органов не наблюдали торможения активности 5α-R. Тем не менее, до сих пор не удалось объяснить почему Пермиксон тормозит активность 5α-R и рост ПЖ, но не влияет на продукцию эпителиальными клетками ПСА. Возможно это связано тем, что препарат воздействует на клеточную и внутриклеточные мембраны стромальных и эпителиальных клеток ПЖ, приводит к изменению микроокружения 5α-R и, как следствие, торможению ее активности. При этом Пермиксон не влияет на работу генов, от которых зависит действие андрогенов и выработка ПСА [20].
Таким образом, Пермиксон обладает антиандрогенным действием, тормозит активность 5α-R, блокирует АР ПЖ, уменьшает в ней число эстрогенных рецепторов и снижает стимуляцию пролактином гиперпластических процессов. Кроме того, препарат имеет еще одно преимущество перед синтетическими ингибиторами 5α-R, так как не влияет на концентрацию ПСА.
Противовоспалительное действие Пермиксона
Противовоспалительное действие Пермиксона начали исследовать еще в 90-е годы прошлого столетия. В одной из первых работ было изучено его влияние на образование из арахидоновой кислоты полиморфоядерными лейкоцитами крови человека хемоаттрактанта нейтрофилов – лейкотриена (LTB 4) после их стимуляции ионофором А 23127. Было показано, что Пермиксон тормозит продукцию ее метаболитов: 5-HETE, 20-COOH LTB4, LTB4 и 20-OH LTB [28]. Эти результаты были подтверждены дальнейшими иммуногистохимическими исследованиями удаленного гиперплазированного участка ПЖ, которые показали, что трехмесячный прием Пермиксона вызывает резкое снижение количества В-лимфоцитов (но не T-лимфоцитов и макрофагов), TNF-α и IL-1β. При оценке по международной шкале простатических симптомов (IPSS) эти изменения коррелировали с клинически значимым улучшением состояния пациентов, что свидетельствует о противовоспалительном действии препарата [29]. Это затем нашло подтверждение в работах других авторов 31.
Еще одна исследовательская группа провела изучение противовоспалительной активности Пермиксона при ДГПЖ. В опытах in vitro было оценено влияние препарата на пролиферацию и жизнеспособность клеток ПЖ с использованием клеточных линий из тканей здоровой и гиперплазированной железы. В тканях при ДГПЖ были отмечены повышенные индексы пролиферативной активности. Добавление разных концентраций Пермиксона уменьшало клеточную пролиферацию во всех клеточных линиях. Наиболее выраженный эффект отметили в стромальных и эпителиальных клетках при гиперплазии ПЖ. Добавление провоспалительных медиаторов IL-6, IL-17 и FGF в клеточную культуру провоцировало выраженную пролиферацию всех трех типов клеток: стромальных, эпителиальных и здоровых. Последующее добавление Пермиксона уменьшило клеточную пролиферацию, индуцированную FGF-2 в стромальных и здоровых клетках, а IL-6 и IL-17 – в клеточной линии гиперплазированных тканей. Авторы выполнили микроматричный анализ для сравнения экспрессии генов в эпителиальных и стромальных клетках при ДГПЖ после добавления Пермиксона и без него. При добавлении препарата была выявлена, недостаточная экспрессия генов, кодирующих провоспалительные медиаторы (IL-1β, IL-6 и хемокина C-X-C motif). Также отмечено уменьшение экспрессии гена, кодирующего человеческий рецептор эпидермального фактора роста 3 (ERBB3), что привело к избыточной экспрессии человеческого гена блокировки роста (GAS1) [33].
В исследовании de la Taille A. на модели in vivo у самцов крыс линии Спрег-Доули вызвали ДГПЖ путем 14-дневного введения тестостерона пропионата. Животные были рандомизированы на три группы лечения: ЭППП ( Пермиксон), финастерид и контроль (без активного лечения). Проводили количественное определение в ПЖ мРНК для 90 генов. Оказалось, что Пермиксон обеспечил статистически значимое снижение (p 14 мл/сек) наблюдали у 33% и 48% больных, соответственно. Объем остаточной мочи (Vres) снизился, начиная с 16 недели, на 27% и 32% у больных I и II групп, соответственно. При приеме препарата в дозе 320 мг/сут субъективная симптоматика исчезла у 46% больных, 960 мг в день – у 60%. В результате исследования было показано, что оптимальной терапевтической дозой Пермиксона является 320 мг/сут. [40].
Подобные результаты были получены в 1999 году в исследовании В.Н. Степанова и соавт. на 100 амбулаторных больных с ДГПЖ в рандомизированном 3-х месячном исследовании в параллельных группах. Было показано, что к концу первого месяца приема препарата значительно улучшились показатели IPSS, Qmax, Qave, V. К концу третьего месяца лечения все они, за исключением V и Qave продолжали улучшаться. Таким образом, прием Пермиксона в дозе 320 мг/сут улучшает суммарный балл IPSS и все показатели мочеиспускания. Препарат оказывает тот же эффект в дозе 160 мг два раза в день [41].
Исследование Authie D. и Cauquil J. включало 500 пациентов с ДГПЖ (средний возраст 68,2 года). У большинства из них имели место симптомы расстройства мочеиспускания: ноктурия – у 97%; дневная поллакиурия – у 67%; дизурия – у 92% и императивные позывы – у 70%. Все пациенты получали Пермиксон (320 мг/сут) в течение 3 месяцев. Авторами зарегистрирован выраженный симптоматический эффект препарата: к концу лечения средняя частота позывов в ночное время снизилась с 4,0 до 1,8, причем улучшение по данному показателю было отмечено у 82%, а полное исчезновение симптома – у 45% больных. Частота дневных мочеиспусканий сократилась с 6,3 до 4,6 у 2/3 мужчин, а уменьшение дизурии и императивности позывов достигнуто у 75 и 85% пациентов, соответственно [42].
В НИИ урологии в 1999 году проанализированы результаты лечения 48 больных ДГПЖ, которые получали Пермиксон по 160 мг дважды в день в течение 12 месяцев. Было отмечено уменьшение выраженности симптомов по шкале IPSS с 14,35 до 10,61 балла (-26,1%) через 6 месяцев и до 10,42 (27,4%) через 12 месяцев лечения. В те же периоды времени средний показатель Qmax увеличился с 10,62 до 12,60 мл/сек (+18,7%) и до 12,73 мл/сек (+19,9%) соответственно. Индекс качества жизни QOL через 6 месяцев наблюдения снизился с 3,49 до 2,60 баллов (-25,3%), достигнув к концу года 2,49 (-28,7%). Также было зарегистрировано небольшое уменьшение среднего объема предстательной железы: на 11,8% через 6 месяцев и 15,6% через 12 месяцев. Показатель ПСА не изменялся в течение всего периода лечения. Изучение эффективности Пермиксона у больных с различными исходными значениями IPSS и Qmax дало нам возможность сделать заключение о том, что препарат наиболее результативен у пациентов с умеренной выраженностью симптомов ДГПЖ (IPSS 10 мл/сек) [45].
Большое клиническое значение имеют данные уродинамических исследований, характеризующие влияние Пермиксона на состояние мочевого пузыря и степень инфравезикальной обструкции. На основании анализа данных комплексного уродинамического обследования больных ДГПЖ получавших, Пермиксон, был сделан вывод о том, что препарат оказывает позитивное влияние на функциональное состояние мочевого пузыря и уменьшает степень инфравезикальной обструкции. Вместе с тем, ни в одном случае полностью устранить проявления обструкции не удалось [47].
Особый интерес представляют работы, в которых сравнивали эффективность и безопасность Пермиксона с плацебо и другими лекарственными средствами. Результаты 7 плацебо-контролируемых исследований, в которых приняло участие в общей сложности 559 человек, обобщены в 1996 году G. Plosker и R. Brogden [48]. В 3-х наиболее значимых из них, где участвовало 410 больных ДГПЖ, пациенты были разделены на две практически равные группы: принимавшие Пермиксон (320 мг/сут) и плацебо. В этих исследованиях продолжительностью от одного до трех месяцев достоверно продемонстрирована клиническая эффективность препарата по сравнению с плацебо. При этом частота ночных мочеиспусканий уменьшилась на 33-46%, дневная поллакиурия – на 11-20%, a Qmax увеличилась на 29-50%, что было существенно выше, чем в группе плацебо, где аналогичные показатели составили 15-18%, 1-3% и 5-9% соответственно.
В трех других опубликованных исследованиях продолжительностью 1-2 месяца с участием 79 больных, на фоне приема Пермиксона было отмечено уменьшение ноктурии на 50-74%, снижение частоты дневных мочеиспусканий на 29-43% и рост Qmax на 26-43%, тогда как в группе плацебо эти же показатели были равны 13-39%, 8-29% и 2-19%. Лишь в одном из 7 опубликованных исследований авторы не выявили существенных различий между изучаемыми признаками.
В ряде наблюдений Пермиксон выступил в качестве эффективного средства устранения дизурии. В исследовании J. Descotes и соавт., проведенном на 176 больных ДГПЖ, показано, что в течение одного месяца дизурия уменьшилась у 31% из получавших Пермиксон (320 мг/сут) по сравнению с 16% – в группе плацебо (р 10 мл/с), число которых в результате лечения сократилось практически на 80% за счет перехода больных в группы с менее выраженными клиническими проявлениями. В результате применения как Пермиксона, так и финастерида, произошло незначительное, но статистически достоверное (р 19), получавших тамсулозин (n=59) и Пермиксон (n=65). Через 12 месяцев общий показатель IPSS снизился в группе тамсулозина на 5,8, а в группе Пермиксона – на 7,8 баллов, что составило, соответственно, 25% и 35,2% от исходного уровня. Оказалось, что чем выше были исходные показатели IPSS в группе Пермиксона, тем больше они снижались в процессе терапии. В этой группе улучшение наступало через 3 месяца после начала лечения и оставалось на том же уровне весь период наблюдения. В группе тамсулозина Qmax увеличилась на 1,7 мл/сек, а в группе Пермиксона – на 1,2 мл/сек. Объем ПЖ снизился при приеме тамсулозина на 0,9 см3, а при приеме Пермиксона – на 2,2 см3. Таким образом, Пермиксон (320 мг/сут) и тамзулосин (0,4 мг/сут), принимаемые в течение 12 месяцев, вызывают сопоставимое улучшение симптомов и показателей мочеиспускания у пациентов с выраженными СНМП/ДГПЖ [55]. Похожие результаты были получены и в ходе сравнения Пермиксона с празозином [56].
Принципиальные выводы о клинической эффективности Пермиксона были сделаны по итогам метаанализа, представленного P. Boyle и соавт. в 2004 году [57]. В работе были обобщены материалы 12 основных плацебо-контролируемых и сравнительных исследований Пермиксона, включавших результаты лечения 2794 больных ДГПЖ. С высокой степенью статистической достоверности авторам удалось продемонстрировать: лечение Пермиксоном приводит к увеличению Qmax дополнительно на 1,87±0,55 мл/сек по сравнению с плацебо (р 10 мл/с). Им может быть рекомендована длительная (многомесячная) терапия препаратом Пермиксон с целью предотвращения дальнейшего прогрессирования симптомов ДГПЖ, с оценкой результатов лечения через 1012 мес.;
2. Больные с манифестной симптоматикой (IPSS >18) и умеренной выраженностью уродинамических нарушений (Qmax >10 мл/с). Если через 3-6 месяцев лечения препаратом Пермиксон не наступило существенного симптоматического улучшения, необходимо рассмотреть вопрос об изменении проводимой медикаментозной терапии;
3. Больные гиперплазией предстательной железы в сочетании с хроническим простатитом. Терапия препаратом Пермиксон возможна в комплексе с антибактериальными и/или противоспалительными препаратами и физиотерапией. В этом случае Пермиксон назначают с учетом его противовоспалительного и противоотечного действия. После стихания явлений хронического простатита тактику дальнейшего лечения определяют так же, как в группах 1 и 2.
4. Больные относительно молодого возраста с сохранной половой функцией и клиническими признаками хронического простатита. Использование препарата Пермиксон в качестве элемента комбинированной медикаментозной терапии, в первую очередь совместно с α1-адреноблокаторами и антибиотиками, позволяет улучшить результаты лечения.
Показано, что эффективность Пермиксона, возрастает с продолжительностью лечения, которое должно быть рассчитано на многие месяцы (не менее 4-6 мес.), а то и годы. С одной стороны, это необходимо учитывать специалистам, планирующим лечение препаратом Пермиксон, а с другой – на это надо ориентировать и пациентов при обсуждении с ними программы медикаментозной терапии ДГПЖ.
Препарат практически не имеет противопоказаний, не влияет на уровень ПСА и не затрудняет диагностику рака ПЖ. Не описано случаев его взаимодействия с другими лекарственными средствами, что расширяет возможности применения Пермиксона у лиц пожилого возраста с отягощенным соматическим статусом.
ЛИТЕРАТУРА
1. Mobley D, Feibus A, Baum N. Benign prostatic hyperplasia and urinary symptoms: Evaluation and treatment. Postgrad Med 2015; 127: 301307. doi:10.1080/00325481.2015.1018799
2. Konwar R, Chattopadhyay N, Bid HK. Genetic polymorphism and pathogenesis of benign prostatic hyperplasia. BJU Int 2008; 102: 536544. doi:10.1111/j.1464-410X.2008.07667.x
3. Zeegers MP, Kiemeney LA, Nieder AM, Ostrer H. How strong is the association between CAG and GGN repeat length polymorphisms in the androgen receptor gene and prostate cancer risk? Cancer Epidemiol Biomarkers Prev 2004; 13: 1765-1771.
4.Kramer G, Steiner GE, Handisurya A, Stix U, Haitel A, Knerer B, et al. Increased expression of lymphocyte-derived cytokines in benign hyperplastic prostate tissue, identification of the producing cell types, and effect of differentially expressed cytokines on stromal cell proliferation. Prostate 2002;52(1):43-58. DOI:10.1002/pros.10084
5. Park T, Choi JY. Efficacy and safety of dutasteride for the treatment of symptomatic benign prostatic hyperplasia (BPH): a systematic review and meta-analysis. World J Urol 2014; 32: 1093-1105. doi:10.1007/s00345-014-1258-9
6. Bartsch G, Rittmaster RS, Klocker H. Dihydrotestosterone and the concept of 5alpha-reductase inhibition in human benign prostatic hyperplasia. World J Urol 2002;19: 413-425.
7. Gu X, Na R, Huang T, Wang L, Tao S, Tian L, et al. SRD5A1 and SRD5A2 are associated with treatment for benign prostatic hyperplasia with the combination of 5α-reductase inhibitors and α-adrenergic receptor antagonists J Urol 2013;190(2):615-619. doi:10.1016/j.juro.2013.03.024
8. Rył A, Rotter I, Grzywacz A, Małecka I, Skonieczna-Żydecka K, Grzesiak K, et al. Molecular Analysis of the SRD5A1 and SRD5A2 Genes in Patients with Benign Prostatic Hyperplasia with Regard to Metabolic Parameters and Selected Hormone Levels. Int J Environ Res Public Health 2017;14(11): 1318-1322. doi:10.3390/ijerph14111318
9. Hennenberg M1, Stief CG, Gratzke C. Prostatic α1-adrenoceptors: new concepts of function, regulation, and intracellular signaling. Neurourol Urodyn 2014;33(7):1074-1085. doi: 10.1002/nau.22467
10. Latil A, Petrissans MT, Roquet J, Robert G, de la Taille A. Effects of Hexanic extract of Serenoa Repens (Permixon® 160 mg) on Inflammation Biomarkers in The Treatment of Lower Urinary Tract Symptoms Related to benign Prostatic Hyperplasia. Prostate 2015;75:1857-1867. doi: 10.1002/pros.23059
11. Sciarra A, Mariotti G, Salciccia S, Autran Gomez A, Monti S, Toscano V, et al. Prostate growth and inflammation. J Steroid Biochem Mol Biol 2008; 108: 254-260. doi:10.1016/j.jsbmb.2007.09.013
12. Naber KG, Weidner W. Chronic prostatitisan infectious disease? J Antimicrob Chemother 2000; 46:157-161
13. Wang Z, Olumi AF. Diabetes, growth hormone-insulin-like growth factor pathways and asso-ciation to benign prostatic hyperplasia. Differentiation 2011; 82:261-271. doi: 10.1016/j.diff.2011.04.004
14. Van Asseldonk B, Barkin J, Elterman DS. Medical therapy for benign prostatic hyperplasia: a review. Can J Urol 2015;22( Suppl 1):7-17.
16. Minciullo PL, Inferrera A, Navarra M, Calapai G, Magno C, Gangemi S.Oxidative Stress in Benign.Prostatic Hyperplasia:A Systematic Review. Urol Int 2015;94:249–254. doi:10.1159/000366210
17. Cornu JN, Cussenot O, Haab F, Lukacs B. A widespread population study of actual medical management of lower urinary tract symptoms related to benign prostatic hyperplasia across Europe and beyond official clinical guidelines. Eur Urol 2010; 58:450-6. doi:10.1016/ j.eururo.2010.05.045
18. Lukacs B, Cornu JN, Aout M, Tessier N, Hodée C, Haab F, et al. Management of lower urinary tract symptoms related to benign prostatic hyperplasia in real-life practice in France: a comprehensive population study. Eur Uro 2013;64:493-501. doi:10.1016/j.eururo.2013.02.026
19. Scaglione F, Lucini V, Pannacci M, Dugnani S, Leone C. Comparison of the potency of 10 different brands of Serenoa repens extracts. Eur Rev Med Pharmacol Sci 2012;16:569-574.
20. Bayne CW, Donnelly F, Ross M, Habib FK. Serenoa repens (Permixon): a 5alpha-reductase types I and II inhibitor—new evidence in a coculture model of BPH. Prostate 1999;40:232–241.
21. Chevalier G, Benard P, Cousse H, Bengone T. Distribution study of radioactivity in rats after oral administration of the lipido/sterolic extract of Serenoa repens (Permixon) supplemented with [1-14C]-lauric acid, [1-14C]-oleic acid or [4-14C]-beta-sitosterol. Eur J Drug Metab Pharmacokinet 1997;22:73–83.
22. Di Silverio F, Monti S, Sciarra A, Varasano PA, Martini C, Lanzara S, et al. Effects of long-term treatment with Serenoa repens (Permixon) on the concentrations and regional distribution of androgens and epidermal growth factor in benign prostatic hyperplasia 1998; Prostate 37:77–83.
23. Habib FK, Ross M, Ho CK, Lyons V, Chapman K. Serenoa repens (Permixon) inhibits the 5alpha-reductase activity of human prostate cancer cell lines without interfering with PSA expression. Int J Cancer 2005;114:190–194. doi:10.1002/ijc.20701
24. Dreikorn K, Lowe F, Borkowski A. Other medical therapies. In: Chatelain C, Denis L, Foo KT, Khoury S, McConnell J.[Eds.] Benign prostatic hyperplasia. Plymouth, UK: Health Publica-tions; 2001. p. 481–511. 5. Ravenna L, Di Silverio F, Russo MA, Salvatori L, Morgante E, Morrone S, et al. Effects of the lipidosterolic extract of Serenoa repens (Permixon) on human prostatic cell lines. Prostate 1996;29(4):219–30.
26. Van Coppenolle F, Le Bourhis X, Carpentier F, Delaby G, Cousse H, Raynaud JP, et al. Pharmacological effects of the lipidosterolic extract of Serenoa repens (Permixon) on rat prostate hyperplasia induced by hyperprolactinemia: comparison with finasteride. Prostate 2000;43(1):49-58
27. Vacher, P., Prevarskaya, N., Skyrma, R., Audy, M.C.,Vacher, A.M., Odessa, M.F. et al. The lipidosterolic extract from Serenoa repens interferes with prolactin receptor signal transduction. J Biomed Sci 1995;2(4):357-365.
28. Paubert-Braquet M, Mencia Huerta JM, Cousse H, Braquet P. Effect of the lipidic lipidosterolic extract of Serenoa repens (Permixon) on the ionophore A23187-stimulated production of leukotriene B4 (LTB4) from human polymorphonuclear neutrophils. Prostaglandins Leukot Essent Fatty Acids 1997;57:299–304.
29. Vela Navarrete R, Garcia Cardoso JV, Barat A, Manzarbeitia F, Lopez Farre A. BPH and in-flammation: pharmacological effects of Permixon on histological and molecular inflammatory markers.Results of a doubleblind pilot clinical assay. Eur Urol 2003;44:549–55
31. Steiner GE, Newman ME, Paikl D, Stix U, Memaran-Dagda N, Lee C, Marberger MJ. Expression and function of proinflammatory interleukin IL-17 and IL-17 receptor in normal, benign hyperplastic, and malignant prostate. Prostate 2003; 56:171-182. DOI: 10.1002/ pros.10238
33. Sirab N, Robert G, Fasolo V,Descazeaud A, Vacherot F, de la Taille, et al. Lipidosterolic extract of Serenoa repens modulates the expression of inflammation related-genes in benign prostatic hyperplasia epithelial and stromal cells. Int J Mol Sci 2013; 14:14301-14320. doi: 10.3390/ ijms140714301
34. De la Taille A.Therapeutic Approach: The Importance of сontrolling Prostatic Inflammation. Eur Urol Suppl 2013; 12(5): 116-122. doi: http://dx.doi.org/10.1016/j.eursup.2013.08.003
35. Latil A, Pétrissans MT, Rouquet J, de la Taille A. Effects of hexanic extract of Serenoa repens (Permixon® 160 mg) on inflammation biomarkers in the treatment of lower urinary tract symptoms related to benign prostatic hyperplasia. Prostate 2015;75(16):1857-1867. doi: 10.1002/pros.23059
36. Kyprianou N, Tu H, Jacobs SC. Apoptotic versus proliferative activities in human benign prostatic hyperplasia. Hum Pathol 1996;27: 668–675.
37. Bayne CW, Ross M, Donnelly F, Habib FK. The selectivity and specificity of the actions of the lipido-sterolic extract of Serenoa repens (Permixon) on the prostate. J Urol 2000;164:876–881.
38. Vacherot F, Azzouz M, Gil-Diez-De-Medina S, Colombel M, De La Taille A, Lefrère Belda MA, et al. Induction of apoptosis and inhibition of cell proliferation by the lipido-sterolic extract of Serenoa repens (LSESr, Permixon in benign prostatic hyperplasia). Prostate 2000;45:259–266.
39. Vela-Navarrete R, Escribano-Burgos M, Farre AL, Garcia-Cardoso J, Manzarbeitia F, Carras-co C. Serenoa repens treatment modifies bax/ bcl-2 index expression and caspase-3 activity in prostatic tissue from patients with benign prostatic hyperplasia. J Urol 2005;173:507–510. doi: 10.1097/01.ju.0000150533.94952.25
40. Dathe G, Schmid H. Phytotherapie der benignen Prostata hyperplasie (BPH) mit Extractum Serenoa repens (Permixon®). Urologie 1991;31:220-223
41. Stepanov VN, Siniakova LA, Sarrazin B, Raynaud JP. Efficacy and tolerability of the lipidos-terolic extract of Serenoa repens (Permixon®) in benign prostatic hyperplasia: a double-blind com-parative study of two dosage regimens. Adv Ther 1999;16:231-241.
42. Authié, D., Cauquil, J. Appréciation de l’efficacité de Permixon® en pratique quotidienne. C R Ther Pharmacol Clin 1987; 56:4–13.
43. Foroutan F. Wirksamkeit und Vertraglichkeit von Permixon® bei einem grosseren Patienten-kollektiv (592 Patienten) unter Praxisbedingungen. J Urol Urogynakol 1997;2:17–21.
45. Сивков А.В. Пермиксон: механизм действия, клиническая эффективность и место в ле-чении ДГПЖ. В кн.: Доброкачественная гиперплазия предстательной железы. [под ред. Н.А.Лопаткина], М.: 1999, С. 117-133.
46. Аляев Ю.Г., Винаров А.З., Локшин К.Л., Спивак Л.Г. Пятилетний опыт лечения пермиксоном (Serenoa repens, «Pierre Fabre Medicament») больных гиперплазией простаты. Урология 2002;(1):23-25.
47. Винаров А.З. Медикаментозное лечение больных гиперплазией предстательной железы: Aвтореф. дис… докт. мед. наук. М.: 1999. 40 с.
48. Plosker G.L. and Brogden R.N. Serenoa repens (Permixon®). A review of its pharmacology and therapeutic efficacy in benign prostatic hyperplasia. Drugs Aging 1996;9:379-395.
49. Descotes JL, Rambeaud JJ, Deschaseaux P, Faure G. Placebo-controlled evaluation of the effi-cacy and tolerability of Permixon® in benign prostatic hyperperplasia after exclusion of placebo responders. Clin Drug Invest 1995;9:291-297.
51. Champault G, Patel JC, Bonnard AM. A double-blind trial of an extract of the plant Serenoa repens in benign prostatic hyperplasia. Br J Clin Pharmac 1984; 18: 461-462.
52. Carraro JC, Raynaud JP, Koch G, Chisholm GD, Di Silverio F, Teillac P, et al. Comparison of phytotherapy (Permixon®) with finasteride in the treatment of benign prostate hyperplasia: a ran-domized international study of 1,098 patients. Prostate 1996; 29: 231-240.
53. Grasso M, Montesano A, Buonaguidi A, Castelli M, Lania C, Rigatti P, et al, Comparative ef-fects of alfuzosin versus Serenoa repens in the treatment of symptomatic benign prostatic hyper-plasia. Arch Esp de Urol 1995;48:97-103.
54. Debruyne F, Koch G, Boyle P, Da Silva FC, Gillenwater JG, Hamdy FC, et al. Comparison of a phytotherapeutic agent (Permixon) with an alpha-blocker (Tamsulosin) in the treatment of benign prostatic hyperplasia: a 1-year randomized international study. Eur Urol. 2002;41(5):497-506.
55. Debruyne F, Boyle P, Da Silva FC, Gillenwater JG, Hamdy FC, Perrin P, et al. Evaluation of the clinical benefit of Permixon® and Tamsulosin® in severe BPH Patients – PERMAL Study Subset Analysis. Eur Urol 2004; 45:773-780. doi:10.1016/j.eururo.2004.01.015
56. Adriazola Semino M, Lozano Ortega JL, Garcia Cobo E, Tejada Bañez E, Romero Rodriguez F. Symptomatic treatment of benign prostatic hypertrophy. Comparative study of prazosin and Serenoa repens. Arch Esp Urol 1992;45:211-213
57. Boyle P, Robertson C, Lowe F, Roehrborn C. Updated meta-analysis of clinical trials of Serenoa repens extract in the treatment of symptomatic benign prostatic hyperplasia. BJU Int 2004;93:751-756. doi: 10.1111/j.1464-410X.2003.04735.x
58. D’Ottavio G, Lagana A, Zappavigna D. Changes in seminal parameters after long-term treat-ment with Serenoa repens. Urologia 1987;54:616-621.
61. Busetto GM, Giovannone R, Ferro M, Tricarico S, Del Giudice F, Matei DV, et al. Chronic bacterial prostatitis: efficacy of shortlasting antibiotic therapy with prulifloxacin (Unidrox®) in association with saw palmetto extract, lactobacillus sporogens and arbutin (Lactorepens®). BMC Urology 2014;14:53. doi: 10.1186/1471-2490-14-53