Методы лечения флюса на десне
Гнойное образование на десне в народе принято называть флюсом. Очень часто к нему относятся несерьезно, но это не просто небольшая припухлость, которая пройдет сама собой. Флюс – это онтогенный периостит, сложное инфекционное заболевание, поражающее надкостницу и челюстную кость. Встречается периостит достаточно часто, но без адекватного лечения оно чревато серьезными осложнениями, вплоть до заражения крови.
Без помощи стоматолога вылечить флюс практически невозможно. Лечебная программа включает в себя терапевтические, физиотерапевтические, хирургические методы.
Заметили гнойные образования на деснах и припухлость щек? Появилась острая боль в зубе или десне? Приходите на консультацию стоматолога нашей клиники. Вовремя начатое лечение флюса позволяет избавиться от проблемы в течение примерно 7 дней.
Почему образуется флюс
Предшественником флюса всегда являются стоматологические заболевания. Чаще всего к нагноению приводят:
Когда нужна помощь стоматолога
Флюс имеет ярко выраженные симптомы. Основной из них – появление гнойника на десне рядом с больным зубом. Гнойник развивается постепенно. Сначала десна немного припухает, на ней заметна небольшая шишка красного или белесого цвета. Через какое-то время на шишке образуется заметный свищевой ход, из которого вытекает гной. Развитие периостита сопровождают и другие симптомы:
Так как флюс вызывает инфекция, для него характерны симптомы, проявляющиеся при любом инфекционном процессе. Пациент чувствует недомогание, у него повышается температура, болит голова, появляется слабость. На голове и шее увеличиваются лимфоузлы.
Любой из этих симптомов – повод обратиться к врачу. Чем более запущен случай, тем выше риск развития осложнений. Это заболевание нередко сопровождается и другими патологическими процессами. Например, в тканях, пораженных инфекцией, может образоваться киста.
Методы лечения флюса
Начинать лечение нужно как можно раньше. Если абсцесс на десне вскрывается самопроизвольно, есть риск попадания инфекции в кровеносное русло. При таком инфицировании развивается заражение крови, а такое осложнение может привести к серьезным последствиям, вплоть до смерти пациента.
Лечение флюса всегда комплексное. Лечебная программа зависит от степени разрушения зуба и распространения инфекции.
Стоматология для тех,
кто любит улыбаться
Вскрытие гнойника на десне
Гнойник вскрывают всегда. Это позволяет снизить риск самопроизвольного вскрытия, которое может стать причиной развития осложнений. Флюс вскрывают под местной анестезией. Если у пациента есть панический страх или другие показания, врач может выбрать другой способ анестезии.
На обезболенной десне в районе флюса делают небольшой разрез, не больше 2 см в длину. После рассечения врач полностью очищает и стерилизует гнойную полость, обрабатывает ее антисептиками. Нельзя допустить образования корочки в районе разреза, так как она будет препятствовать оттоку сукровицы и гнойного содержимого. Для этого в разрез вставляют дренаж. После того, как полость очищена от гноя, можно приступать к общему лечению, цель которого – устранить причины, вызвавшие периостит.
Общее лечение
Методы зависят от причин, вызвавших флюс. Единственное исключение – периостит, развивающийся на фоне периодонтита. В этом случае сразу после вскрытия абсцесса врач приступает к пародонтологическому лечению. Никаких лечебных манипуляций с зубом проводить не требуется. В остальных случаях болезни зуба нужно лечить:
Физиотерапия
Физиотерапевтические методы используют как дополнительные. Они позволяют быстрее справиться с инфекцией, остановить воспалительный процесс. Хороших результатов позволяют добиться следующие методы:
Медикаментозная терапия
В лечении гнойных процессов обязательно используют антибиотики. Они снижают риск повторного развития инфекции. Обычно врач назначает метронидазол с линкомицином или клиндамицином. Такая комбинация препаратов позволяет воздействовать на граммположительные и анаэробные бактерии.
Метронидазол назначают перорально, линкомицин и клиндамицин – в виде таблеток или внутримышечных инъекций. Линкомицин применяют с осторожностью, так как этот препарат может вызвать аллергию.
Метронидазол назначают перорально, линкомицин и клиндамицин – в виде таблеток или внутримышечных инъекций. Линкомицин применяют с осторожностью, так как этот препарат может вызвать аллергию.
Новейшая технология для протезирования и микропротезирования
Вытягивание гноя из закрытых ран дома
Образование гноя в раневой поверхности говорит о присоединении инфекции. Нагноение — это своеобразная защитная реакция организма. Таким образом, человеческий организм сам пытается избавиться от инородных предметов (древесных частиц, металлической стружки, тканевых волокон и различных микроорганизмов).
Причины нагноения раны
К области, в которой есть повреждение, начинает активно поступать кровь, насыщенная белыми кровяными тельцами — лейкоцитами. Местная иммунная система начинает работать в усиленном режиме, направляя к повреждению макрофаги (иммунные клетки), которые съедают инородные микроорганизмы и тела, специальными ферментами обезвреживают их, но после этого и сами погибают. Именно так происходит нагноение. Если повреждение небольшое, то можно вытянуть гной из раны в домашних условиях, но при обширном гнойном процессе все же не стоит пренебрегать помощью хирурга.
Признаки гнойного воспаления
Визуально иногда сложно увидеть, что в месте повреждения образовался гной, особенно если рана закрытая. Но независимо от места локализации гнойных ран, они имеют определенные местные и общие симптомы. К местным относятся такие проявления гнойного процесса:
болезненные ощущения во время прикосновения к травмированному месту, которые в скором времени становятся постоянными;
повышение температуры в месте раны;
изменение цвета кожи (она становится сине-фиолетовой или бурой);
наличие желтого или белого пятна посредине раны.
К общим признакам нагноения относятся:
присутствие вялости, апатии, упадка сил (это происходит от попадания токсинов в кровоток);
гиперемия (иногда до 39оС);
возникновение головной боли;
появление озноба;
проблемы со сном.
Если присутствуют признаки общей интоксикации организма, это означает, что воспалительный процесс находится в более тяжелой стадии. В такой ситуации лечение должно быть комплексным и включать в себя как препараты для наружного применения, так и для перорального приема.
Что делать при загноившейся ране
Если это позволяет время, то необходимо в первую очередь обратиться к хирургу, обнаружив гнойник. Он сможет определить, действительно ли в ране присутствует гной, сделает надрез, очистит раневой карман, поставит дренаж и перевяжет область повреждения. Под повязку доктор наложит натрий хлорид и мазь для лечения гнойных ран, перед этим обработав поверхность антисептическими растворами.
Для того чтобы удалить отмершие ткани, хирурги пользуются повязками, включающими в себя трипсин. При обширных площадях нагноений, выписываются антибактериальные препараты для перорального приема. Конечно, не желательно самостоятельно вскрывать гнойники и фурункулы ногтями, иглами, маникюрными ножничками и прочими подручными предметами, ведь так можно занести еще больше инфекции в рану. Если нет возможности попасть к хирургу, то для того, чтоб рана скорее открылась сама, нужно знать, как вытянуть гной и какие мази или крема для этого использовать.
Мази для вытягивания гноя
Подкожные гнойные раны появляются на любой части человеческого тела. Нарыв может быть на лице, ноге и даже на пальце. Если антисептиков для того, чтобы убрать рану, недостаточно, в нее попала инфекция, то применяются мази вытягивающие гной из закрытой раны. Независимо от того, от какой причины произошло нагноение, в процессе лечения необходимо удалить его, провести дезинфекцию, применить антибиотики и ранозаживляющие препараты. И если последнее назначает врач, то самостоятельно вытянуть из раны гной можно с помощью одной из следующих мазей:
Левомеколь. Эта мазь имеет комбинированное действие, содержит в себе антибиотик, а также ускоряет регенерацию кожи, убирает воспалительный процесс и вытягивает гнойные скопления. Прежде чем наносить мазь на поврежденный участок, кожа вокруг него должна быть обработана перекисью.
Стрептоцид. Мазь, включающая этот элемент, имеет противомикробное действие и подходит для обработки небольших повреждений (ссадина, царапина), в которых образовался гной. Однако ее нельзя применять во время беременности, а людям, у которых больны почки, следует относиться к этому препарату очень осторожно.
Ихтиоловая мазь. Обладает бактерицидным, обезболивающим, обеззараживающим и вытягивающим гной эффектом. Для того чтоб поучить хороший результат, мазь от гнойных ран нужно выдавить на ватный диск, приложить к повреждению, прикрыть пергаментом и закрепить с помощью пластыря. Менять такую повязку следует четыре раза в день.
Синтомицин в составе мази обладает антибактериальным эффектом. Такая мазь подойдет для нанесения на раны, которые плохо заживают, она предохраняет от появления гнойного процесса. Однако есть у этого препарата один существенный недостаток — она приводит к привыканию. По этой причине пользоваться ею можно только при острой необходимости и в течение короткого периода.
Мазь Вишневского обрела широкую популярность при лечении гнойных ран. Ведь прежде, чем вытащить гной, нужно, чтоб гнойник максимально созрел. С помощью этого препарата стимулируется кровообращение в поврежденной области. Во время применения на уже открытых ранах Вишневского не только убирает гной, но и заживляет кожные покровы. Ее применяют как для компрессов, так и для примочек.
Невозможно точно сказать, какая мазь лучше вытягивает гной из раны, ведь каждый организм индивидуален и заживление повреждений зависит от многих факторов.
Как избавиться от гноя в домашних условиях
Часто бывает так, что человеку в силу тех или иных причин невозможно не только обратиться за врачебной помощью, но и купить необходимую для лечения гнойной раны мазь. В момент нагноения он может находиться на даче или в деревне, где нет аптечного пункта или он работает только в будние дни. Чем вытянуть гной в таких ситуациях, используя то, что обычно есть под рукой? Народная медицина имеет немало проверенных рецептов, решающих эту проблему.
Перед применением любого метода вытягивания гноя, рану нужно обеззаразить. В далеких от аптеки местах это можно сделать с помощью ванночек и примочек из лекарственных растений:
подорожника;
донника;
ромашки;
шалфея;
ольхи;
лопуха;
лука;
свеклы;
моркови;
редьки;
листьев черники и сирени.
После того как с раны смыта грязь, кровь и прочие загрязнения, можно приступать непосредственно к вытягиванию гнойного экссудата с помощью следующих растений, имеющих лечебный эффект:
Алоэ. Это растение широко используется для лечения разных заболеваний, в том числе и гнойных ран. Для того чтоб цветок дал результат, он должен быть не моложе трех лет. Листик следует промыть, осторожно разрезать по длине. Одну половинку следует положить на рану срезом вниз, сверху примотать бинтом. Накладывая такой компресс на ночь, с утра уже можно видеть результат. Все гнойные скопления убираются через три дня;
Мыльно — чесночный компресс. Головка чеснока запекается в духовом шкафу, измельчается, добавляется к натертому хозяйственному мылу. Из полученной массы сформировать лепешку, приложить к гноящемуся месту и перебинтовать. Менять повязку следует каждые четыре часа;
Репчатый лук. В сыром или запеченном виде, этот овощ обладает отличным лечебным действием. Стоит лишь прикладывать его на повреждение перед сном в течение нескольких дней;
Полевой хвощ. Одну ложку сырья следует заварить стаканом вскипяченной воды, выдержать полчаса, процедить и сделать компресс на рану;
Тертая морковь, лист капусты, лист гречихи, болотный аир, сушеная крапива — это все в виде компрессов и примочек помогает гною быстрее выйти на поверхность раны и не дает инфекции распространяться дальше.
При тщательном уходе гнойная рана быстро заживает и не оставляет за собой никаких следов.
Материал предоставлен в информационно-справочных целях, ставить диагноз и назначать лечение должен профессиональный врач.
При любых вопросах, связанных со здоровьем, консультация с лечащим врачом обязательна, не занимайтесь самолечением!
Местное лечение гнойных ран
Местное лечение – один из самых древних способов лечения гнойных ран. В настоящее время основным методом лечения гнойных ран, в т.ч. гнойных ран при сахарном диабете, является радикальная хирургическая обработка с последующим пластическим закрытием раневого дефекта. Однако в ряде случаев при оперативном вмешательстве не всегда удается адекватно удалить все нежизнеспособные ткани. В этой ситуации, для подготовки нагноившейся раны к кожной пластике или её спонтанного заживления, местной терапии отводится важная роль.
Основной принцип при консервативном лечении гнойных ран – направленное применение перевязочных средств с дифференцированным действием на раневой процесс с учетом его фазы и особенностей течения.
Течение первой фазы раневого процесса неоднородно и может проявляться, как ограниченными сухими некрозами, струпом, так и обильно экссудирующей раной. Задачами лечения в первой фазу являются: подавление инфекции в ране, активизация процессов отторжения некротических масс, сорбция и эвакуация раневого отделяемого.
В первую фазу раневого процесса в качестве местного лечения гнойных ран наиболее часто применяются препараты из группы антисептиков (йодофоры, пронтосан, лавасепт) и мазей на гидрофильной основе (левомеколь, диоксиколь). При лечении сильноэкксудирующих гнойных ран целесообразно применение биологически активных перевязочных средств из группы дренирующих сорбентов (диотевин, анилодиотевин). При слабой экксудации раны с формированием сухих некрозов возможно комбинирование дренирующих сорбентов с гидрогелеавыми повязками (Гидросорб, Супрасорб G, АПОЛЛО-ПАК) (рис.1).
Рис.1 Лечение пациента с ожоговой раной голени с помощью гидрогелевых повязок
При наличии в ране участков влажных некрозов в качестве местной терапии используются альгинаты кальция (Сорбалгон, Супрасорб А, Альгисайт) для скорейшего отторжения омертвевших тканей (рис.2).
Рис.2 Местное лечение гнойной раны у больного с диабетической стопой
проводится повязкой «сорбалгон»
После очищения раны от некрозов, появления грануляций, ликвидации перифокального воспаления и инфильтрации тканей необходимо решать следующие задачи: подавление инфекции в гнойной ране, создание оптимальных условий для роста грануляционной ткани и эпителизации, стимулирование репаративных процессов, подготовка к пластическому закрытию раневого дефекта.
Рис. 3 Структура современных раневых покрытий
Во вторую и третью фазы раневого процесса лечение гнойных ран продолжают мазями на водорастворимой и гидрофильно-эмульсионной основе (Винилин, Актовегин, Солкосерил, облепиховое масло), стимулирующими раневыми покрытиями (Коллахит) (рис.4), гидрогелями (Гидросорб, АППОЛО ПАК, Супрасорб G) и гидрокаллоидами (Гидроколл, Супрасорб Н). Его осушествляют до полной эпителизации раны или кожной пластики.
Рис.4. Раневое покрытие «коллахит»
Таким образом, местное лечение гнойных ран с дифференцированным применением современных перевязочных средств с учетом фазы и характера раневого процесса позволяет в скорейшие сроки подготовить рану к кожной пластики, а при невозможности ее выполнения в кротчайшие сроки добиться полной эпителизации раневого дефекта.
Чем вытянуть гной из раны
Гной в ране – не просто больно и неприятно, это опасно. Его появление свидетельствует о присоединении вторичной инфекции. Гнойный экссудат может разнестись по организму и привести к серьезным осложнениям.
Если гноя много и рана долго заживает, рекомендуется обратиться к врачу.
Гной в ране. Когда нужно принять срочные меры?
О начале развития гнойного процесса свидетельствует:
Впоследствии, если не предприняты грамотные меры помощи, к имеющейся симптоматике прибавляются следующие признаки:
Нельзя допускать развития осложнений! На начальном периоде повреждения кожи следует оказать грамотную помощь – провести поэтапную обработку раны, использовать не народные методы, а современные мощные антисептики, а также другие специальные средства для обеззараживания раневой поверхности и быстрейшей регенерации.
Для вытягивания гноя применяются мази – ихтиоловая, Вишневского, стрептоцидовая, синтомициновая эмульсия, Левомеколь и другие средства для наружного применения. С помощью ряда препаратов обеспечивается антибактериальный/анти микробный эффект, стимуляция кровообращения в поврежденных тканях, вытягивание гноя, заживление кожного покрова. Мази используют в качестве компрессов и примочек.
Состояние, когда появляется гной в ране, требует принятия грамотных мер, в противном случае существует высокий риск развития осложнений! Пополните свою домашнюю аптечку средствами оказания первой помощи при ранениях и травмах, а также качественными современными препаратами для их лечения. В социальной сети аптек «Столички» представлен большой выбор самых разнообразных медикаментов по доступным ценам.
ФЛЕГМОНЫ И АБСЦЕССЫ — современные возможности лечения
В чем трудность лечения флегмон и абсцессов? Почему нецелесообразно применять мази на вазелиново-ланолиновой основе? Какие местные препараты соответствуют современным представлениям о лечении флегмон и абсцессов? Несмотря на активное внедрение
В чем трудность лечения флегмон и абсцессов?
Почему нецелесообразно применять мази на вазелиново-ланолиновой основе?
Какие местные препараты соответствуют современным представлениям о лечении флегмон и абсцессов?
Несмотря на активное внедрение в клиническую практику новых групп антибиотиков, проблема профилактики и лечения гнойно-септических осложнений в хирургии по-прежнему актуальна. Так, согласно литературным данным, частота гнойно-воспалительных осложнений после грыжесечений достигает 28,3%, после резекций желудка — 28,4%, холецистэктомий — 32%, аппендэктомий — 40,4%, панкреатитов — 50% (Прискарь В. И., 1999).
Летальность при перитоните колеблется от 16 до 80% (Даценко Б. М. с соавт., 1998, Гельфанд Б. М. с соавт., 1999, Камзакова Н. И., 2000).
В структуре внутрибольничных инфекций послеоперационные инфекции составляют 12,2%, а постинъекционные инфекции — 17%. Необходимо отметить, что процент тяжелых последствий внутрибольничных инфекций практически одинаков для хирургических стационаров и амбулаторно-поликлинических учреждений — 15,2% и 15,6% соответственно.
Особую тревогу вызывают случаи запоздалой диагностики осложненного течения абсцессов или флегмон. Так, например, в зависимости от локализации первичного гнойного процесса могут формироваться тяжелые гнойные артриты (после внутрисуставного введения гормональных, обезболивающих препаратов), тромбофлебиты (после внутрисосудистого введения различных лекарственных средств) с последующей генерализацией инфекционного процесса, с формированием гнойных очагов во внутренних органах (в сердце, легких, почках).
Ретроспективный анализ тяжелых абсцессов и флегмон, осложнившихся сепсисом после длительного консервативного или недостаточно активного хирургического вмешательства, показывает, что одной из основных причин возникновения осложнений можно считать недостаточное внимание к ранней диагностике формирующихся абсцессов и флегмон различной локализации, предполагающей использование современных неинвазивных методов исследования (ультразвука, компьютерной томографии), а также инвазивных диагностических методов, и прежде всего диагностической пункции области инфильтрата. Особую тревогу вызывает так называемая выжидательная тактика, когда, выполнив диагностическую пункцию и удалив некоторое количество гноя, хирурги пытаются дренировать гнойную полость с помощью резиновой трубки и назначают какой-либо антибактериальный препарат.
Радикальные оперативные вмешательства на уже сформированном гнойном очаге выполняются слишком поздно, дренирование послеоперационной раны бывает, как правило, неадекватным.
Кроме того, не уделяется должного внимания проблеме асептики и антисептики при оказании помощи пострадавшим, а также при выполнении различных диагностических и лечебных манипуляций как на амбулаторно-поликлиническом, так и стационарном этапах лечения. Использование традиционных антисептиков в данных ситуациях, к сожалению, не предупреждает развитие инфекционного процесса, так как проблема устойчивости микроорганизмов в равной степени актуальна как для группы антибактериальных препаратов, так и для традиционных антисептиков.
К примеру, чувствительность S.aureus, E.coli, B.fragilis к раствору фурациллина составляет менее 3, 1 и 3% соответственно. Массивность контаминации P.aeruginosa в растворе фурациллина может достигать 106 КОЕ/мл. Частота контаминации раствора фурациллина грибами достигает 58%.
В табл. 1 приводится далеко не полный перечень традиционных препаратов, от которых необходимо отказаться полностью и которые, тем не менее, используются как в домашних условиях, так и в медицинских учреждениях.
В данном сообщении приводится анализ результатов лечения 166 больных с постинъекционными флегмонами и абсцессами в специализированном отделении ран и раневой инфекции Института хирургии им. А. В. Вишневского РАМН. Больных, как правило, переводили из других хирургических стационаров ввиду прогрессирующего нарастания клиники интоксикации, с полиорганной недостаточностью, с сепсисом.
Возраст пациентов колебался от 18 до 84 лет. 124 больных были в возрасте от 30 до 60 лет. Длительность лечения на предыдущем этапе от начала формирования гнойного процесса составляла от 12 суток до 1,5 месяцев.
Сопутствующие заболевания: гипертоническая болезнь — 46 больных, остеохондроз тазобедренных суставов — 31 пациент, пояснично-крестцовый радикулит — 27 больных, почечная колика — 16 и другие заболевания — 46.
Гнойно-воспалительные процессы возникали после введения обезболивающих препаратов (анальгина, баралгина), гипотензивных (папаверина с дибазолом, магнезии), гормональных препаратов, кордиамина, масляных растворов витаминов, кокарбоксилазы и др.
Инфекционный процесс в 139 случаях возникал после инъекций, выполненных медицинскими работниками (бригады «скорой помощи», процедурные и хирургические кабинеты поликлиник, стационары). В остальных 27 случаях препараты вводились в домашних условиях не медицинскими работниками. Локализация абсцессов: в подавляющем большинстве случаев — это места внутримышечных инъекций (ягодичные области, реже — предплечья и места паранефральных, паравертебральных блокад).
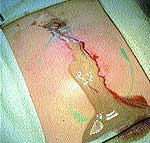 |
| Рис. 1 |
При первичном обращении больного за помощью по месту жительства в случае появления первых признаков формирования воспалительного процесса в качестве препаратов первой помощи использовались 3%-ный раствор йода («йодная сетка»), компрессы со спиртом, мазью Вишневского, ихтиоловой мазью. Консервативное медикаментозное лечение с подключением физиотерапевтических методов иногда продолжалось до 2–3 недель (рис. 1).
В дальнейшем, уже в условиях хирургических стационаров после хирургического вмешательства, послеоперационные раны тампонировались либо марлевыми тампонами, пропитанными 10%-ным раствором хлорида натрия, мазью Вишневского, раствором фурациллина, либо с дренирующей целью в раны устанавливались перчаточные резинки или резиновые трубки.
Такой метод лечения быстро приводил к распространению гнойного процесса за пределы первичной локализации, нарастанию интоксикации, развитию сепсиса.
Ввиду неэффективности лечения после развития септического состояния больные переводились для дальнейшего лечения в специализированное отделение гнойной хирургии им. А. В. Вишневского.
При поступлении практически все больные сразу помещались в блок интенсивной терапии отделения гнойной хирургии, где они получали необходимую пред- и послеоперационную корригирующую медикаментозную терапию.
В Институте хирургии им. А. В. Вишневского РАМН разработан метод активного хирургического лечения гнойных ран, основанный на следующих принципах:
Использование вышеперечисленных дополнительных методов воздействия на раневую поверхность позволяет уменьшить обсемененность раневой поверхности патогенной флорой до уровня ниже «критического» — с 10 7-9 до 10 2-3 микробных тел в 1 г ткани раны.
Клинические примеры закрытия ран с помощью швов, дренирования и окончательный результат приведены на рис. 2, 3, 4.
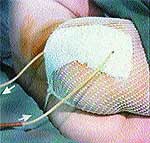 |
| Рис. 3 |
Во время поступления больного в отделение, а также в процессе лечения (во время перевязок, при повторных хирургических обработках ран, перед окончательным закрытием ран) проводятся бактериологические исследования видового состава ран. Результаты представлены в табл. 2.
Как видно из табл. 2, в подавляющем большинстве случаев из ран была выделена грамположительная микрофлора и в единичных случаях — ассоциация грамположительных и грамотрицательных микроорганизмов. Обращает на себя внимание достаточно большое число случаев выявления в ранах неклостридиальной анаэробной инфекции.
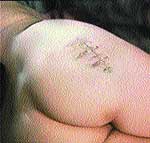 |
| Рис. 4 |
Все штаммы, выделенные из послеоперационных ран больных, ранее прооперированных в других лечебных учреждениях, были полирезистентны к традиционно используемым антибактериальным препаратам, что указывает на госпитальную принадлежность инфекции.
С учетом видового характера выделяемой из ран микрофлоры и чувствительности ее к антибактериальным препаратам назначались общая и местная антибактериальная терапии.
Наиболее часто (38,5%) использовались полусинтетические пенициллины (карбенициллин, ампиокс, диклоксациллин), в 15,7% случаев — аминогликозиды (гентамицин, тобрамицин, сизомицин, нетилмицин), в 12,5% — фторхинолоны (офлоксацин, пефлоксацин, ципрофлоксан), в 10,3% — цефалоспорины (цефотаксим, цефтазидим, цефтриаксон).
При обнаружении гнойно-воспалительного процесса, вызванного неклостридиальной анаэробной инфекцией (27 больных — 16,3%), как правило, назначалась комбинированная антибактериальная терапия — метронидазол с гентамицином или нетилмицином либо клиндамицин с гентамицином или нетилмицином. В последние годы в подобных ситуациях препаратом выбора считается имипенем, позволяющий активно воздействовать как на аэробный, так и анаэробный компонент микрофлоры ран. При локальном гнойном процессе, в случае выявления чувствительности стафилококков к фузидину, назначение этого препарата в комплексном лечении было также оправданно.
Выбор антисептиков, используемых для промывания ран
Как уже было сказано, использование раствора фурациллина в настоящее время нецелесообразно ввиду его крайне низкой антимикробной активности. В настоящее время перспективными можно считать растворы диоксидина, мирамистина, фурагина растворимого.
Прежде всего, очень важно следить за чистотой не только самой раны, но и окружающей рану кожи.
При выборе кожных антисептиков, используемых как с профилактической, так и лечебной целью, предпочтение отдается препаратам с универсальным, широким или умеренным спектром действия, активным против смешанной микрофлоры и обладающим микробоцидным или микробостатическим действием.
1%-ный йодовидон, 1%-ный йодопирон — йодофоры, представляющие собой комплекс поливинилпиролидона с йодом. Различия между этими препаратами связаны со способом их получения, а также разной молекулярной массой поливинилпиролидона. Растворы йодовидона более стабильны при хранении, чем растворы йодопирона, готовящиеся обычно ex tempore. По степени бактерицидного действия эти препараты практически идентичны.
Сульйодопирон представляет собой пенистую жидкость, которая предназначена для мытья грязных инфицированных ран, лечения ран под повязкой, обработки рук хирурга и операционного поля. Сульйодопирон при местном применении оказывает бактерицидное действие.
Бактерицидный эффект при микробной нагрузке 106-107 бактерий на 1 мл среды наступает в течение 1-4 минут, превосходя по этим показателям растворы йодопирона.
1%-ный диоксидин обладает выраженной активностью против большинства аэробных, анаэробных и факультативно анаэробных патогенных бактерий.
К диоксидину чувствительны клинические штаммы бактерий с полирезистентностью к антибиотикам. Препарат используется для промывания и тампонирования гнойных ран, а также может вводиться внутривенно, внутриартериально, интратрахеально через катетер или ингаляционно, внутриплеврально, в брюшную полость через ирригаторы.
Наш 20-летний опыт применения диоксидина в комплексном лечении больных с сепсисом, перитонитом, медиастинитом, с развернутой клиникой интоксикации, прогрессирующей полиорганной недостаточностью не подтверждает мнение некоторых специалистов о высокой токсичности этого препарата. Строгое соблюдение правил введения, разовых, суточных и курсовых доз позволяет избежать таких нежелательных побочных явлений, как тошнота, рвота или судороги.
0,1%-ный фурагин (солафур) — антимикробное средство из группы нитрофуранов. Препарат преимущественно действует на грамположительную микрофлору. Его МПК в 10-20 раз ниже, чем у фурациллина. Используется либо внутривенно при тяжелых формах течения раневой инфекции, при инфекционном процессе в легких, органах мочевыводящих путей, либо местно в виде 0,1%-ного раствора при лечении ран, инфицированных стафилококками, а также для промывания мочевого пузыря.
0,01%-ный мирамистин (миристамидопропилдиметилбензиламмоний хлорид) — новый антисептик из группы катионных ПАВ.
0,01%-ный водный раствор мирамистина с профилактической и лечебной целью используется в хирургии, травматологии и комбустиологии при незначительном количестве гнойного отделяемого в ране. Препаратом орошают поверхность ран и ожогов, рыхло тампонируют раны и свищевые ходы, марлевыми тампонами, смоченными антисептиком, промывают брюшную полость, вводят в плевральную полость и мочевой пузырь.
При обильной гнойной экссудации использование марлевых тампонов с растворами антисептиков для местного лечения ран неоправданно, так как тампоны, помещаемые в рану, быстро высыхают и, следовательно, не обладают необходимой для удаления гноя длительной осмотической активностью. В крайнем случае, рана может заполняться комбинированным тампоном — в центр марлевого тампона помещается силиконовая трубка, через которую 2-3 раза в сутки шприцем в рану вводится антисептик по 10-20 мл. Вместо 10%-ного раствора хлорида натрия для тампонирования послеоперационных ран в настоящее время используются современные мази на водорастворимой основе, высокую клиническую значимость которых можно считать доказанной.
Возможности использования мазей
К сожалению, до сих пор в ряде клиник используются мази на жировой основе с антибиотиками: линимент синтомицина, тетрациклиновая, эритромициновая и др. Однако мази на жировой основе с антибиотиками оказывают только кратковременное действие, поскольку вазелин-ланолиновая основа нарушает отток раневого отделяемого, не обеспечивает достаточного высвобождения активного ингредиента из композиции, не способствует проникновению антибиотика в глубь тканей, где находятся микробы, что приводит к переходу острых воспалительных заболеваний в хронические. Ввиду формирования в стационарах высокорезистентных штаммов микроорганизмов практически полностью утратили свою клиническую значимость и ихтиоловая мазь, и мазь Вишневского.
В последние годы в клиническую практику лечения гнойных ран в первой фазе раневого процесса внедрены новые мази — на полиэтиленоксидной основе (комбинации полиэтиленоксидов с молекулярным весом 400 и 1500).
Полиэтиленоксиды являются производными окиси этилена и обладают низкой токсичностью и выраженными осмотическими свойствами. При создании препаратов для лечения гнойных ран чаще всего используются полиэтиленоксид с молекулярным весом 400 (ПЭО-400) и полиэтиленоксид с молекулярным весом 1500 (ПЭО-1500).
В гнойной ране ПЭГ-1500 активно связывает воспалительный экссудат, отдавая его в повязку, с которой жидкость испаряется, а освободившиеся молекулы ПЭГ-1500 вновь присоединяют к себе экссудат, накапливающийся на дне раны.
Более мелкие молекулы (ПЭГ- 400) способны проникать в глубь тканей. Образуя с антибиотиком комплекс, ПЭГ-400 проводит его в ткани раны, где локализуются микробы. Этим он принципиально отличается от мазей на ланолин-вазелиновой основе, которые способны оказывать антимикробное действие только кратковременно и только на поверхности раны.
В состав современных мазей на полиэтиленоксидной основе введены различные антимикробные препараты:
Кроме того, в состав мазей введены такие препараты, как тримекаин, имеющий обезболивающий эффект, и метилурацил, обладающий анаболической и антикатаболической активностью, в целях стимуляции процессов клеточной регенерации.
Все мази на основе ПЭО отличаются от традиционных препаратов прежде всего многонаправленностью действия — осмотический эффект наблюдается до 18 часов, что позволяет делать перевязки только один раз в сутки, в то время как при использовании 10%-ного хлорида натрия повторные перевязки необходимо выполнять через каждые 3-4 часа, в противном случае повязка, пропитанная раствором и раневым отделяемым, полностью теряет осмотическую способность.
Еще одно преимущество мазей на полиэтиленоксидной основе — это широкий спектр антимикробной активности.
Причем по эффективности воздействия в силу однотипности мазевой основы все мази практически равноценны. При создании новых мазей особое внимание уделялось их антибактериальной активности. А. В. Вишневский по этому поводу писал: «Мы интересуемся силой, степенью бактерицидных свойств мази, ибо снизить, сбить, уничтожить инфекцию в ране всегда является задачей необходимой и благодарной» (Вишневский А. В., 1937).
Антимикробная активность новых мазей в отношении S.aureus находится на уровне 86-97,3%, Е. coil — 71-97%, Р.aeruginosa — 64-90,8%, Proteus spp. — 76-100%.
Для подавления в ранах грамотрицательных бактерий, в частности синегнойной палочки, широко применяется 10%-ная мазь мафенида-ацетата на гидрофильной основе.
Несмотря на интенсивное применение мазей, содержащих левомицетин или диоксидин, их высокая антимикробная активность сохраняется на протяжении более 20 лет, что указывает на слабый процесс нарастания резистентности госпитальных штаммов.
С внедрением полиэтиленгликолевой основы в технологию создания новых лекарственных форм появилась возможность создать мази с нитрофурановыми соединениями. На их основе выпускаются две мази: 0,5%-ная мазь хинифурила, а также фурагель, где в качестве основы использован сополимер акриловой кислоты (СОКАП) и ПЭГ-400.
Новые отечественные мази, содержащие нитрофурановые соединения, показывают высокую клиническую и бактериологическую эффективность. Так, фурагель более активен (94%) при наличии в ране S.aureus и менее активен (79%) при Р.aeruginosa. Maзь хинифурила одинаково высоко активна при наличии в ране грамположительной и грамотрицательной микрофлоры (87-88%). Оба препарата хорошо переносятся даже в случае их длительного использования при лечении трофических язв. Применение сополимера акриловой кислоты с полиэтиленгликолем в различных весовых соотношениях в качестве мазевой основы позволяет регулировать осмотическую активность мази как в сторону ее повышения, так и снижения, что очень важно при переходе раневого процесса во вторую фазу и необходимости продолжения лечения раны под повязкой.
Клиническая эффективность 1%-ной йодопироновой мази и многокомпонентной йодсодержащей мази (йодметриксилена) в качестве лечебного средства составляет 92,6-93,4%. Бактериологическая активность этих двух препаратов была одинаково высокой (91,8-92,6%) в отношении всех основных возбудителей острых гнойных процессов мягких тканей. Побочные эффекты (клинически значимые) наблюдались в 0,7% случаев и клинически незначимые — в 2,3% случаев. Следует особо подчеркнуть высокую эффективность этих препаратов при лечении ран с грибковым поражением, что часто наблюдается у больных ослабленных, с обширными ожоговыми ранами, трофическими язвами, пролежнями.
В настоящее время в клиническую практику внедрены только зарубежные йодсодержащие мази (повидон-йод и бетадин), хотя отечественный аналог был разработан более десяти лет назад.
Установлено, что уровень обсемененности ран аэробной микрофлорой при лечении мазями на ПЭГ-основе опускается «ниже критического» к 3-5-м суткам. Появление грануляций в среднем достигается к 4-м суткам, начало эпителизации — к 5-м.
Широкий спектр антимикробной активности мазей на полиэтиленгликолевой основе, их высокая и длительная осмотическая активность позволяют более чем в 80% случаев в течение 4-5 суток купировать острый гнойный процесс и закончить лечение неосложненных гнойных ран мягких тканей наложением первично-отсроченных швов, тогда как при использовании гипертонического раствора хлорида натрия в 90% случаев только в конце 2-3-й недели лечения под прикрытием системной антибактериальной терапии удается закрыть рану путем наложения вторичных швов.
Для лечения неспорогенной анаэробной инфекции наряду с диоксидином перспективные возможности открылись после изучения препарата нитазола, показавшего высокое антибактериальное действие на стафилококки, стрептококки, кишечную палочку, аэробные спорообразующие бактерии, патогенные анаэробные микроорганизмы как клостридиальные, так и неклостридиальные в виде монокультур и микробных ассоциаций. По спектру антибактериального действия нитазол имеет преимущества перед метронидазолом, к которому нечувствительны стафилококки, кишечная палочка, стрептококки. Нитазол оказывает противовоспалительное действие, являясь нестероидным противовоспалительным средством.
На основе нитазола были созданы пенообразующий аэрозоль «Нитазол» и две многокомпонентные мази «Стрептонитол» и «Нитацид». По антимикробной активности стрептонитол и нитацид значительно превосходят зарубежный препарат «Клион» (Венгрия), в состав которого входит метронидазол. Осмотическая активность стрептонитола гораздо ниже, чем у нитацида, что обусловлено введением в его состав вазелинового масла с водой. И стрептонитол, и нитацид, созданные для лечения ран с неклостридиальной анаэробной инфекцией, обладают равнозначным широким спектром антимикробной активности как в отношении грамположительной, так и грамотрицательной микрофлоры (84,2-88,5%). Обращает на себя внимание высокая активность этих препаратов при наличии в ране Р.aeruginosa (86,3-91,1%). Обе позиции показывают хорошую клиническую эффективность при наличии в ране анаэробной инфекции (88-89%).
Различие в осмотической активности позволяет использовать эти препараты ступенчато — сначала нитацид (с высокой осмотической активностью), затем стрептонитол.
Специалисты, занимающиеся лечением гнойных ран, хорошо знают, что бывают ситуации, когда одного скальпеля для полного удаления некротических тканей недостаточно: необходимы протеолитические препараты.
В настоящее время доказана высокая клиническая эффективность комплексного ферментного препарата «Протогентин», содержащего фермент природного происхождения «протеаза С» с протеолитическим действием, антибиотики (гентамицин и эритромицин), консерванты.
Мазевая основа препарата состоит из полиэтиленоксида с вазелиновым маслом. Умеренная осмотическая активность обеспечивает удаление из раны гноя.
Протогентин, наиболее активный в отношении P.aeruginosa и Е.coli, подавляет рост 83,4-90,4% штаммов.
Антимикробные компоненты мази «Протогентин» хорошо проникают под струп раны, вследствие чего в тканях раны создаются концентрации, намного превышающие МПК.
Достаточная осмотическая активность, широкий спектр антимикробной активности, хорошие фармакокинетические свойства протогентина способствуют сокращению сроков некролизиса. Мазевая основа не повреждает грануляционную ткань, что позволяет использовать этот препарат в течение длительного времени, пока требуется ферментативная очистка раневой поверхности.
После очищения раны от гнойно-некротического содержимого и достижения ее бактериологической санации наступает вторая фаза раневого процесса. Этот период характеризуется появлением в ране островков грануляционной ткани, которая, развиваясь, покрывает раневую поверхность полностью. Здоровая грануляционная ткань всегда яркая, сочная, легко кровоточит. При малейшем ухудшении процессов биосинтеза в ране изменяется внешний вид грануляций: они теряют яркую окраску, становятся мелкими, покрываются слизистым налетом. Одной из причин такого осложнения считается суперинфекция. Всякое замедление развития грануляций ведет к задержке и остановке процесса эпителизации.
Большое значение для скорейшего заживления ран во второй фазе имеет способность препаратов, используемых для местного лечения, оказывать бактерицидное действие в целях предупреждения вторичной инфекции, защитить грануляционную ткань от механических повреждений, а также оказывать умеренное влагопоглощающее действие и стимулировать рост грануляций.
Оптимальный вариант — сочетание этих факторов в одном препарате. К таким препаратам относятся современные комбинированные мази на регулируемой осмотической основе: метилдиоксилин, стрептонитол, а также пенные аэрозоли «Cульйодовизоль», «Гипозоль-АН», раневые покрытия на основе натриево-кальциевой соли альгиновой кислоты, масла, аэрозоли, гидроколлоидные покрытия (табл. 3).
Мазь «Метилдиоксилин» — многокомпонентная мазь, содержит диоксидин, метилурацил и гидрофобную эмульсионную основу с наличием касторового масла. Композиция винилина с эмульгатором и ПЭГ-400 в качестве основы мази позволила снизить осмотическую активность этого препарата до такого уровня, чтобы новая мазь не пересушивала молодую грануляционную ткань.
Мазь «Стрептонитол» содержит антибактериальные вещества стрептоцид и нитазол на гидрофильной эмульсионной основе, которая оказывает слабое осмотическое действие, удаляя избыток влаги, и одновременно защищает грануляционную ткань от механических повреждений. Препарат показан для лечения во второй фазе воспаления ранее инфицированных анаэробной, грамположительной и грамотрицательной микрофлорой ран при наличии ярких сочных грануляций.
Аэрозоли
На переходном этапе первой фазы раневого процесса во вторую высокую клиническую эффективность показывают современные пено- и пленкообразующие аэрозоли. Пенные препараты в аэрозольной упаковке перспективны для профилактики и лечения гнойных осложнений. Это обусловлено тем, что пены создают барьер для инфицирования ран, они не обладают «парниковым эффектом»; небольшим количеством препарата в составе пены можно покрывать большие по площади раневые поверхности и заполнять объемные раневые каналы и «карманы». Преимуществом аэрозольной формы является быстрота обработки, что важно при массовом поступлении пострадавших. Аппликации пен атравматичны.
В настоящее время создан ряд пенных препаратов:
В состав современных пенных препаратов обязательно входит какое-нибудь антимикробное средство, действующее на аэробную или на анаэробную микрофлору, включая неклостридиальную (бактероиды, пептококки, пептострептококки). Чаще всего используются диоксидин, йодовидон, циминаль и нитазол. Исследования антибактериальных свойств этих препаратов на моделях гнойных ран, вызванных анаэробной инфекцией, показывают выраженный терапевтический эффект, заключающийся в снижении высеваемости бактерий из ран к 3-5-му дню лечения до 10 1-2 микробов на 1 г ткани, уменьшении отечности и гиперемии, прекращении гнойной экссудации и в дальнейшем в заживлении ран.
Цимезоль кроме антисептика циминаля содержит анестетик тримекаин и гемостатик — порошок окисленной целлюлозы. Антисептическое действие циминаля усиливается благодаря сочетанию с димексидом и 1,2-пропилен-гликолем, которые обеспечивают проникновение циминаля в зоны некрозов и умеренный осмотический эффект.
Диоксизоль приготовлен на высокоосмотичной основе, а дегидратирующее действие диоксипласта сведено до минимума. Это определяет их применение соответственно в первой и во второй фазах раневого процесса при отсутствии в ранах большого количества гнойного отделяемого. Изучение антимикробной активности нового аэрозоля-диоксизоля показало преимущество этого препарата в случае выявления в ранах грамотрицательной микрофлоры. Диоксизоль подавляет Ps.aeruginosa в 92,5%.
Сульйодовизоль — пенообразующий аэрозольный препарат, расширяет возможности лечения ран йодовидоном в хирургии. Препарат показан для лечения ран во второй фазе раневого процесса, ранее инфицированных грамположительной и грамотрицательной аэробной микрофлорой.
Широкие клинические исследования показали необходимость использования пенообразующих аэрозолей только при отсутствии выраженного гнойно-воспалительного процесса на этапах подготовки раны к ее закрытию швами или методом пластики.
Масла
В настоящее время для лечения ран широко используются различные масла, в том числе и растительного происхождения (масло облепихи, масло шиповника, просяное масло — милиацил). Первые публикации о применении с этой целью различных масел относятся к эпохе Возрождения (Джованни де Виго, 1460-1520, Ambroslse Pare, 1510-1590).
Сравнительные экспериментальные исследования показали, что просяное масло прежде всего обладает более широким антимикробным спектром действия по сравнению с маслом шиповника или облепихи.
Просяное масло (милиацил) имеет высокое кислотное число (151,5-178,3), обусловленное большим содержанием свободных, ненасыщенных жирных кислот (олеиновой, линолевой, линоленовой). Этим объясняются стерильность препарата и его достаточный антимикробный эффект. Кроме того, входящее в состав просяного масла сложное стероидное соединение — пентациклический тритерпеноид — милиацин — обладает анаболическим действием и является стабилизатором мембран. Стабилизируя лизосомальные мембраны, милиацин предохраняет их от действия мембраноповреждающих факторов, например токсинов. В связи с этим уменьшается активность катепсинов, кислых РНК-азы и ДНК-азы, что приводит к уменьшению экссудации ткани, гипоксии, деполяризации РНК и ДНК.
Раневые покрытия
Широкие возможности в местном медикаментозном лечении ран открылись с появлением различных раневых покрытий, обладающих такими ценными качествами, как антимикробная активность, способность надежно предупреждать реинфицирование раневой поверхности, способность обеспечивать локальный гемостаз, ускорять образование грануляций, эпидермиса и активно поглощать раневой экссудат. Кроме того, современные раневые покрытия активно стимулируют образование грануляций и эпидермиса. При смене повязок эти препараты не вызывают болезненных ощущений. При длительном нахождении раневых покрытий на ране не возникает неприятного запаха.
В целях стимуляции процессов регенерации в ране наиболее широко используются перевязочные средства на основе производных белков и полисахаридов. С учетом специфического воздействия коллагеновых соединений на репаративные процессы в ране, а также данных по эффективности полисахаридных соединений с позиций создания оптимальных условий для формирования грануляционной ткани и миграции эпителиальных клеток разработаны раневые покрытия на основе белково-полисахаридных комплексов и их композиций с лекарственными препаратами. В качестве полисахаридных соединений использованы растительный полисахарид (альгинат натрия) и полисахарид животного происхождения (хитозан).
Биологически активные стимулирующие раневые покрытия
Биологически активные стимулирующие раневые покрытия с антимикробным и местно-анестезирующим действием выпускаются в четырех вариантах:
Перечисленные раневые покрытия благотворно влияют на течение регенераторных процессов в ране. Коллаген-альгинатные покрытия стимулируют рост грануляционной ткани, а коллаген-хитозановые — рост эпителиальных клеток.
В последние годы наибольшее распространение получили препараты на основе альгиновой кислоты и коллагена.
На основе смешанного натриево-кальциевой альгиновой кислоты созданы полифункциональные влагопоглощающие препараты для местного лечения ран во второй фазе (альгипор, альгимаф).
Стимулирующие раневые покрытия хорошо моделируются на различных участках тела, обеспечивают нормальный парообмен в ране, сорбируют избыток раневого экссудата, обладают пролонгированным антимикробным и обезболивающим действием, создают влажную среду, оптимальную для миграции эпителиальных клеток. Выход лекарственных средств из стимулирующих раневых покрытий осуществляется в течение 48-72 часов в зависимости от количества раневого экссудата в ране.
Все современные раневые покрытия обладают высокой антимикробной активностью за счет введенных в них противомикробных компонентов (сизомицин — в сипролине, мафенид-ацетат — в альгимафе, фурагин — в альгиколе АКФ и коллахите ФА).
Сравнительная оценка антибактериальной активности этих препаратов показывает, что элиминация S.aureus, Proteus spp. из ран быстрее происходит при использовании альгимафа и сипролина.
Гидроколлоиды
В последние годы за рубежом для лечения больных с длительно незаживающими ранами, трофическими язвами, пролежнями нашли применение гидроколлоидные лекарственные средства, в частности содержащие пектин — дуодерм (США), варигесив (США).
В НПО «Биотехнология» (Россия) совместно с Институтом хирургии им. А. В. Вишневского РАМН разработаны две гидроколлоидные лекарственные формы нового поколения на основе пектина: галактон — жидкий гидроколлоид, предназначенный для лечения длительно незаживающих глубоких ран мягких тканей с умеренным количеством гнойного отделяемого; галагран — сухой гидроколлоид (порошок) для лечения поверхностных ран мягких тканей, пролежней, трофических язв.
За счет введенного в состав диоксидина гидроколлоиды показывают лучшую активность по сравнению с другими препаратами в отношении P.auruginosa.
При сравнении гидроколлоидов (галаграна и галактона) с сорбентами (дежизаном и дебризаном) выявляется более широкий спектр положительных свойств гидроколлоидов. Прежде всего, гидроколлоиды стимулируют процессы регенерации и эпителизации, предупреждают реинфицирование раневой поверхности, поддерживают влажную среду под повязкой. Показатель сорбционной способности галаграна невысок: по воде — 3,56 г/г, по крови — 2,57 г/г; при этом верхний слой галаграна не смачивается модельными жидкостями на протяжении всего срока наблюдения (одни сутки).
Основное поглощение воды идет в течение 5 часов, далее наблюдается снижение количества сорбированной жидкости за счет подсыхания верхнего слоя и образования корочки, затрудняющей процесс дренирования. Частицы галаграна в контактном слое набухают, превращаясь в гелеобразную массу, которая равномерно растекается по ране.
По данным цитологического исследования, в первые трое суток использования галаграна в раневых отпечатках выявляется тенденция интенсивного формирования грануляционной ткани.
Учитывая природу биополимера, гидроколлоиды (галагран и галактон) целесообразно применять на стадии развития в ране репаративных процессов.
Гентацикол
Высокоэффективным препаратом для лечения длительно незаживающих ран, трофических язв, остеомиелита, диабетической стопы является препарат гентацикол — пролонгированная форма гентамицина на биодеградируемой (коллагеновой) основе.
Содержание антибиотика в биоптатах ран, получаемых от больных различных клинических групп, зависит от количества раневого отделяемого и скорости рассасывания коллагеновой основы.
Длительные и высокие концентрации гентамицина обнаруживаются при использовании гентацикола в лечении остеомиелита или в случаях окончательного закрытия швами остеомиелитической полости.
Гентацикол создает высокие концентрации гентамицина в тканях раны на протяжении 2 недель, причем эти концентрации намного превышают МПК основных возбудителей хирургической инфекции.
Биодеградируемая коллагеновая губка с гентамицином способствует купированию инфекционного процесса, активизирует пролиферацию всех клеточных элементов грануляционной ткани, усиливает коллагеногенез. Препарат может использоваться в ургентной хирургии в качестве местного гемостатика. Использование гентацикола в комплексном лечении различных ран позволяет сократить показания к проведению общей антибактериальной терапии с 16,6 до 5,5%; при этом в 98,2% случаев ранние реконструктивно-восстановительные кожно-пластические операции оказываются успешными.












