Фенолы
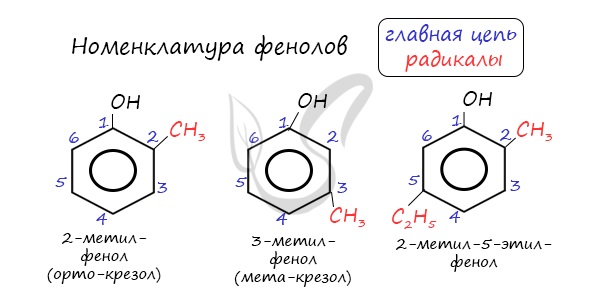
Номенклатура фенолов
Нумерацию атомов углерода в молекуле фенола начинают в такой последовательности, чтобы заместители получили наименьшие номера (идут кратчайшим путем). В основе названия принято сохранять тривиальное название «фенол».
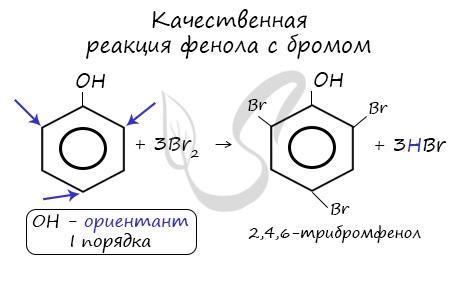
Напомню, что гидроксильная группа является ориентантом I порядка (орто-, пара-ориентант). Поэтому реакции галогенирования, нитрования протекают в орто- и пара-положениях.
Получение фенолов
При гидролизе галогенбензолов происходит обмен: гидроксогруппа встает на место атома галогена.
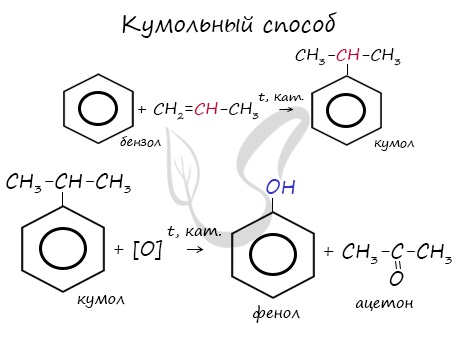
Этим способом получают 95% всего производимого фенола. В ходе этой реакции кумол (изопропилбензол) подвергают окислению, в результате получается фенол и ацетон.
Химические свойства фенолов
При гидрировании разрываются двойные связи бензольного кольца, образуется циклогексанол.
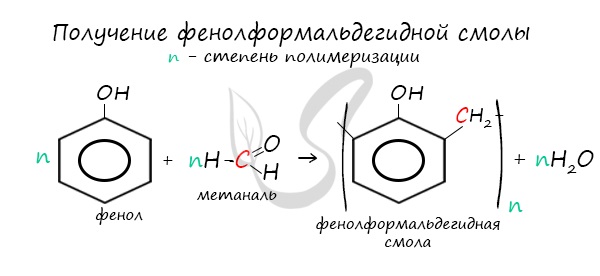
В промышленности получила широкое распространение реакция поликонденсации фенола с формальдегидом, приводящая к образованию смолообразных полимеров (фенолформальдегидные смолы) и воды.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Фенолы
Содержание
Изомерия
Электронное строение
Фенолы представляют собой полярные соединения (диполи). Бензольное кольцо является отрицательным концом диполя, группа — OH — положительным. Дипольный момент направлен в сторону бензольного кольца.
Во-первых, повышается способность к замещению атомов водорода в орто- и пара-положениях бензольного ядра, и в результате реакций замещения обычно образуются тризамещённые производные фенола.
Во-вторых, увеличение полярности связи O-H под действием бензольного ядра и появление достаточно большого положительного заряда на атоме водорода приводит к тому, что молекулы фенола диссоциируют в водных растворах по кислотному типу.
Фенол является слабой кислотой. В этом состоит главное отличие фенолов от спиртов, которые являются неэлектролитами.
Физические свойства
Большинство одноатомных фенолов при нормальных условиях представляют собой бесцветные кристаллические вещества с невысокой температурой плавления и характерным запахом. Фенолы малорастворимы в воде, хорошо растворяются в органических растворителях, токсичны, при хранении на воздухе постепенно темнеют в результате окисления. Фенол C6H5OH (карболовая кислота) — бесцветное кристаллическое вещество на воздухе окисляется и становится розовым, при обычной температуре ограниченно растворим в воде, выше 66 °C смешивается с водой в любых соотношениях. Фенол — токсичное вещество, вызывает ожоги кожи, является антисептиком.
В живых организмах
Химические свойства
1. Реакции с участием гидроксильной группы
При взаимодействии фенолятов с галогенпроизводными образуются простые и сложные эфиры (реакция Фриделя — Крафтса).
2. Реакции с участием бензольного кольца
Качественные реакции на фенолы
В водных растворах одноатомные фенолы взаимодействуют с хлоридом железа (III) с образованием комплексных фенолятов, которые имеют фиолетовую окраску; окраска исчезает после прибавления синильной кислоты
Способы получения
1. Из каменноугольной смолы. Каменноугольную смолу, содержащую в качестве одного из компонентов фенол, обрабатывают вначале раствором щелочи (образуются феноляты), а затем — кислотой. 2. Сплавление аренсульфокислот со щелочью: C6H5-SO3Na + NaOH → C6H5-OH + Na2SO3 3. Взаимодействие галогенпроизводных ароматических УВ со щелочами: C6H5-Cl + NaOH → C6H5-OH + NaCl или с водяным паром: C6H5-Cl + H2O → C6H5-OH + HCl
Применение фенолов
Примечания
Ссылки
Полезное
Смотреть что такое «Фенолы» в других словарях:
ФЕНОЛЫ — ФЕНОЛЫ, группа АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ, в молекулах которых содержится одна или несколько гидроксильных групп ( ОН), присоединенных к бензольному кольцу (см. БЕНЗОЛ). Простейший представитель этого ряда веществ также называется фенолом или… … Научно-технический энциклопедический словарь
ФЕНОЛЫ — Третичные спирты, наиболее известна из них карболовая кислота. Словарь иностранных слов, вошедших в состав русского языка. Чудинов А.Н., 1910. ФЕНОЛЫ третичные спирты известной формулы; наиболее известен из них обыкновенный ф., называемый в… … Словарь иностранных слов русского языка
ФЕНОЛЫ — ФЕНОЛЫ, производные ароматических углеводородов, у к рых один или несколько атомов водорода заменены гидроксилами. По количеству гидроксильных групп различают одноатомные Ф. (С„Нгп 7. ОН), как напр. карболовая кислота (см.), крезолы (см.),… … Большая медицинская энциклопедия
ФЕНОЛЫ — органические соединения ароматического ряда, в молекулах которых гидроксильные группы связаны с атомами углерода ароматического кольца. По числу ОН групп различают фенолы одноатомные (напр., фенол), двухатомные (гидрохинон, пирокатехин, резорцин) … Большой Энциклопедический словарь
Фенолы — одно и двузамещенные гидроксильные производные ароматических углеводов, применяемые в практической медицине и ветеринарии как дезинфектанты и антисептики. Чаще используют карболовую к ту, крезолы, лизол, ксилол, судол, тимол, ментол, карвакрол,… … Словарь микробиологии
ФЕНОЛЫ — ароматические соединения, образованные путем замещения одного или нескольких атомов водорода бензольного кольца гидроксильной группой. Ф. твердые, кристаллические или жидкие вещества с характерным запахом и слабокислотными свойствами. Простейший… … Геологическая энциклопедия
ФЕНОЛЫ — ароматические соединения, имеющие гидроксильные группы, непосредственно связанные с атомами углерода ядра. Применяют в производстве феноло формальдегидных смол, клеев, лаков, фенолятов, термостойких лаков, красителей, пестицидов, ПАВ, лекарств,… … Российская энциклопедия по охране труда
фенолы — органические соединения ароматического ряда, в молекулах которых гидроксильные группы связаны с атомами углерода ароматического кольца. По числу ОН групп различают фенолы одноатомные (например, фенол), двухатомные (гидрохинон, пирокатехин,… … Энциклопедический словарь
ФЕНОЛЫ — ароматич. соед., содержащие в молекуле одну или неск. гидроксильных групп, связанных с атомами углерода ядра. По кол ву ароматич. ядер различают собственно Ф., наф толы (2 конденсированных ядра), антролы (3 ядра), фенант ролы (4), бензотетролы… … Химическая энциклопедия
Фенол
Химическое название
Химические свойства
Что такое Фенол? Гидроксибензол, что это такое? Согласно Википедии – это один из простейших представителей своего класса ароматических соединений. Фенолы – это органические ароматические соединения, в молекулах которых к гидроксильной группе присоединены атомы углерода из ароматического кольца. Общая формула Фенолов: С6Н6n(ОН)n. Согласно стандартной номенклатуре, органические вещества этого ряда различают по числу ароматических ядер и ОН-групп. Различают одноатомные аренолы и гомологи, двухатомные арендиолы, терхатомные арентриолы и многоатомные формулы. Также Фенолам свойственно иметь ряд пространственных изомеров. Например, 1,2-дигидроксибензол (пирокатехин), 1,4-дигидроксибензол (гидрохинон) являются изомерами.
Спирты и Фенолы отличаются друг от друга наличием ароматического кольца. Этанол является гомологом метанола. В отличие от Фенола, метанол взаимодействует с альдегидами и вступает в реакции этерификации. Утверждение, что гомологами являются метанол и Фенол неверно.
Его подробно рассмотреть структурную формулу Фенола, то можно отметить, что молекула представляет собой диполь. При этом бензольное кольцо – отрицательный конец, а группа ОН – положительный. Наличие гидроксильной группы обуславливает повышение электронной плотности в кольце. Неподеленная пара электронов кислорода вступает в сопряжение с пи-системой кольца, а для атома кислорода характерна sp2 гибридизация. Атомы и атомные группы в молекуле обладают сильным взаимным влиянием друг на друга, и это отражается на физических и химических свойствах веществ.
Физические свойства. Химическое соединение имеет вид бесцветных игольчатых кристаллов, которые розовеют на воздухе, так как подвержены окислению. У вещества специфический химический запах, оно умеренно растворимо в воде, спиртах, щелочи, ацетоне и бензоле. Молярная масса = 94,1 грамм на моль. Плотность = 1,07 г на литр. Кристаллы плавятся при 40-41 градусах Цельсия.
С чем взаимодействует Фенол? Химические свойства Фенола. В связи с тем, что молекула соединения содержится, как ароматическое кольцо, так и гидроксильную группу, то оно проявляет некоторые свойства спиртов и ароматических углеводородов.
С чем реагирует группа ОН? Вещество не проявляет сильных кислотных свойств. Но является более активным окислителем, чем спирты, в отличие от этанола взаимодействует с щелочами образуя соли-феноляты. Реакция с гидроксидом натрия: С6Н5ОН + NaOH → C6H5ONa + H2O. Вещество вступает в реакцию с натрием (металлическим): 2C6H5OH + 2Na → 2C6H5ONa + H2.
Фенол не реагирует с карбоновыми кислотами. Эфиры получают при взаимодействии солей фенолятов с галогенангидридами или ангидридами кислот. Для химического соединения не характерны реакции образования простых эфиров. Эфиры образуют феноляты при действии на них галогеналканов или галогенпроизводных аренов. Гидроксибензол реагирует с цинковой пылью, при этом происходит замещение гидроксильной группы на Н, уравнение реакции выглядит следующим образом: C6H5OH + Zn → C6H6 + ZnO.
Химическое взаимодействие по ароматическому кольцу. Для вещества характерны реакции электрофильного замещения, алкилирования, галогенирования, ацилирования, нитрования и сульфирования. Особое значение имеет реакций синтеза салициловой кислоты: C6H5OH + CO2 → C6H4OH(COONa), протекает в присутствии катализатора гидроксида натрия. Затем при воздействии соляной кислоты образуется салициловая к-та.
Реакция взаимодействия с бромной водой является качественной реакцией на Фенол. C6H5OH + 3Br2 → C6H2Br2OH + 3HBr. При бромировании образуется твердое белое вещество — 2,4,6-трибромфенол. Еще одна качественная реакция – с хлоридом железа 3. Уравнение реакции выглядит следующим образом: 6C6H5OH + FeCl3 → (Fe(C6H5OH)6)Cl3.
Реакция нитрования Фенола: C6H5OH + 3HNO3 → C6H2(NO2)3OH + 3 H2O. Для вещества также характерна реакция присоединения (гидрирования) в присутствии металлических катализаторов, платины, оксида алюминия, хрома и так далее. В результате образуются циклогексанол и циклогексанон.
Химическое соединение подвергается окислению. Устойчивость вещества значительно ниже, чем у бензола. В зависимости от условий реакции и природы окислителя образуются разные продукты реакции. Под действием перекиси водорода в присутствии железа образуется двухатомный Фенол; при действии диоксида марганца, хромовой смеси в подкисленной среде – пара-хинон.
Фенол реагирует с кислородом, реакция горения: С6Н5ОН +7О2 → 6СО2 + 3Н2О. Также особое значение для промышленности имеет реакция поликонденсации с формальдегидом (например, метаналем). Вещество вступает в реакцию поликонденсации до тех пор, пока не израсходуется полностью один из реагентов и не образуются огромные макромолекулы. В результате образуются твердые полимеры, фенолформальдегидные или формальдегидные смолы. Фенол не взаимодействует с метаном.
Получение. На данный момент существуют и активно применяются несколько методов синтеза гидроксибензола. Кумольный способ получения Фенола является наиболее распространенным из них. Таким способом синтезируют порядка 95% всего объема производства вещества. При этом некаталитическому окислению воздухом подвергается кумол и образуется гидропероксид кумола. Полученное соединение разлагается под действием серной кислоты на ацетон и Фенол. Дополнительным побочным продуктом реакции является альфа-метилстирол.
Также соединение можно получить при окислении толуола, промежуточным продуктом реакции будет являться бензойная кислота. Таким образом, синтезируют около 5% вещества. Все остальное сырье для различных нужд выделяют из каменноугольной смолы.
Как получить из бензола? Фенол можно получить с помощью реакции прямого окисления бензола NO2 (закись азота) с дальнейшим кислотным разложением гидропероксида втор-бутилбензола. Как из хлорбензола получить Фенол? Существует два варианта получения из хлорбензола данного химического соединения. Первый – реакция взаимодействия со щелочью, например, с гидроксидом натрия. В результате образуется Фенол и поваренная соль. Второй – реакция с водяным паром. Уравнение реакции выглядит следующим образом: C6H5-Cl + H2O → C6H5-OH + HCl.
Получение бензола из Фенола. Для этого сначала требуется обработать бензол хлором (в присутствии катализатора), а затем прибавить к полученному соединению щелочь (например, NaOH). В итоге образуется Фенол и хлорид натрия.
Превращение метан — ацетилен — бензол — хлорбензол можно осуществить следующим образом. Сначала проводится реакция разложения метана при высокой температуре 1500 градусов Цельсия до ацетилена (С2Н2) и водорода. Затем ацетилен при особых условиях и высокой температуре переводят в бензол. К бензолу прибавляют хлор в присутствии катализатора FeCl3, получают хлорбензол и соляную кислоту: C6H6 + Cl2 → C6H5Cl + HCl.
Одним из структурных производных Фенола является аминокислота тирозин, которая имеет важное биологическое значение. Данную аминокислоту можно рассмотреть в виде пара-замещенного Фенола или альфа-замещенного пара-крезола. Крезолы – достаточно распространены в природе на ряду с полифенолами. Также свободную форму вещества можно обнаружить в некоторых микроорганизмах в равновесном состоянии с тирозином.
Фармакологическое действие
Фармакодинамика и фармакокинетика
Средство проявляет бактерицидную активность по отношению в аэробным бактериям, их вегетативным формам и грибам. Практически не оказывает влияния на споры грибов. Вещество вступает во взаимодействие с белковыми молекулами микробов и приводит к их денатурации. Таким образом, нарушается коллоидное состояние клетки, значительно повышается ее проницаемость, нарушаются окислительно-восстановительные реакции.
В водном растворе является отличным дезинфицирующим средством. При использовании 1,25% раствора практически микроорганизмы погибают в течение 5-10 минут. Фенол, в определенной концентрации оказывает прижигающее и раздражающее действие на слизистую оболочку. Бактерицидный эффект от применения средства усиливается с ростом температуры и кислотности.
При попадании на поверхность кожи, даже если она не повреждена, лекарство быстро всасывается, проникает в системный кровоток. При системной абсорбции вещества наблюдается его токсическое действие, преимущественно на центральную нервную систему и дыхательный центр в головном мозге. Порядка 20% от принятой дозы подвергается окислению, вещество и продукты его метаболизма выводятся с помощью почек.
Показания к применению
Противопоказания
Вещество не используют:
Побочные действия
Иногда лекарственное средство может спровоцировать развитие аллергических реакций, зуд, раздражение в месте нанесения и чувство жжения.
Инструкция по применению (Способ и дозировка)
Консервацию лекарственных препаратов, сывороток и вакцин проводят с помощью 0,5% растворов Фенола.
Для наружного применения лекарство используют в виде мази. Препарат наносят тонким слоем на пораженные участки кожи несколько раз в сутки.
При лечении отита вещество используют в форме 5% раствора в глицерине. Препарат подогревают и закапывают по 10 капель в пораженное ухо на 10 минут. Затем необходимо удалить остатки лекарства с помощью ваты. Процедуру повторяют 2 раза в день в течение 4 суток.
Препараты Фенола для лечения ЛОР-заболеваний используют в соответствии с рекомендациями в инструкции. Продолжительность терапии – не более 5 дней.
Для ликвидации остроконечных кондилом их обрабатывают 60% раствором Фенола или 40% раствором трикрезола. Процедуру проводят один раз в 7 дней.
При дезинфекции белья применяют 1-2% растворы на основе мыла. С помощью мыльно-фенольного раствора обрабатывают помещение. При дезинсекции используются фенольно-скипидарные и керосиновые смеси.
Передозировка
При попадании вещества на кожу возникают жжение, покраснение кожи, анестезия пораженного участка. Поверхность обрабатывают растительным маслом или полиэтиленгликолем. Проводят симптоматическую терапию.
Симптомы отравления Фенолом при попадании внутрь. Наблюдаются сильные боли в животе, глотке, в ротовой полости, пострадавшего рвет бурой массой, бледность кожи, общая слабость и головокружение, миоз, коллапс, падение температуры тела, судороги, кома, острая печеночная недостаточность. В качестве терапии желудок промывают растительным маслом с добавлением белков, затем дают пострадавшему 10% раствор глицерола и активированный уголь. Показан прием оксида магния и глюконата кальция, форсированный диурез, тиосульфат натрия капельно внутривенно, витамины группы В. Проводят лечение токсического шока.
Взаимодействие
Лекарственное взаимодействие не происходит.
Особые указания
Фенол обладает способностью адсорбироваться пищевыми продуктами.
Средством нельзя обрабатывать обширные участки кожи.
Перед использованием вещества для дезинфекции предметов быта, их необходимо механически очистить, так как средство абсорбируется органическими соединениями. После обработки вещи могут еще длительное время сохранять специфический запах.
Химическое соединение нельзя использовать для обработки помещений для хранения и готовки пищевой продукции. Оно не влияет на окраску и структуру ткани. Повреждает поверхности, покрытые лаком.
Детям
Средство нельзя использовать в педиатрической практике.
При беременности и лактации
Фенол не назначают во время кормления грудью и при беременности.
Препараты, в которых содержится (Аналоги)
Фенол входит в состав следующих препаратов: Ферезол, Фукорцин, Фенола раствор в глицерине, Орасепт, Фармасептик. В качестве консерванта содержится в препаратах: Экстракт Белладонны, Набор для кожной диагностики медикаментозной аллергии, Постеризан и так далее.
Отзывы
Фенол – хорошее антисептическое средство, которое подходит, как для обработки инструментов и помещений, так и при лечении воспалительных ЛОР-заболеваний. При соблюдении рекомендаций врача и инструкции по применению, необходимых мер безопасности при работе с такого рода веществами, средство хорошо переносится и не вызывает негативного влияния на организм. Отзывы о применении препаратов Фенола, как правило, положительные. Особенно хорошие отзывы при лечении заболеваний горла.
Цена, где купить
Стоимость вещества для технического использования зависит от количества и производителя. Купить спрей для готовой полости Орасепт можно примерно за 400 рублей – флакон.
Образование: Окончила Ровенский государственный базовый медицинский колледж по специальности «Фармация». Окончила Винницкий государственный медицинский университет им. М.И.Пирогова и интернатуру на его базе.
Опыт работы: С 2003 по 2013 г. – работала на должностях провизора и заведующего аптечным киоском. Награждена грамотами и знаками отличия за многолетний и добросовестный труд. Статьи на медицинскую тематику публиковались в местных изданиях (газеты) и на различных Интернет-порталах.
Что такое фенол? Свойства и применение
Фенол – это самое простое соединение из класса фенолов, производное аренов, в молекуле которого непосредственно реализуется связь гидроксильных групп и бензольного кольца. По сути, это слабая кислота, что и есть главным отличием между фенолами и спиртами, являющимися неэлектролитами. Выпускается мировой промышленностью в миллионах тонн ежегодно. По объемах среди всех химических веществ занимает 33 место, среди органических – 17. Характеризуется токсичностью и достаточно большой едкостью, способно обжигать кожу и выступает мощным ирритантом. Может выполнять роль антисептика в виде 5 %-го водного раствора, и не просто может, а выполняет и активно с этой целью используется в медицине.
Названия-синонимы: гидроксибензол, карболовая кислота (устар.).
Свойства
Выглядит это вещество как бесцветная прозрачная твердая масса, сформированная игольчатыми кристаллами. Запах – специфический, у большинства ассоциируется с запахом гуаши, так как в ее составе присутствует фенол.
Растворяется в воде в стандартных условиях ограниченно: в соотношении 6,5 г на 100 мл. При температуре 66 °C и более смешивается с H2O в различных пропорциях. Именно к водным растворам чаще используют наименование «кислота карболовая». Кроме того, растворению поддается в щелочах, спиртах, бензене и диметилкетоне.
Пребывая на воздухе, данное соединение окисляется и приобретает розоватый окрас. Появление цветных компонентов объясняется промежуточным формированием хинонов.
Молярная масса – 94,11 г/моль, плотность – 1,07 г/см³. Термосвойства: t плавления – 40,9 °C, t кипения – 181,84 °C, t вспышки – 79/85 °C (в закрытом и открытом тигле, соответственно). Формула: C6H5OH.
Химическим свойствам гидроксибензола характерна двуплановость. С одной стороны, у них присутствует ароматическое кольцо, с другой – гидроксильная группа. Поэтому фенол обладает свойствами и спиртов, и аренов:
— по гидроксильной группе. Небольшие кислотные качества (сильнее, по сравнению со спиртами). Формирование солей, именуемых фенолятами, в частности натрия фенолята, при воздействии щелочей. В виду очень слабых свойств кислоты, из фенолятов ее может вытеснить даже угольная к-та. А более интенсивное разложение фенолятов характерно при влиянии сильных кислот, к примеру, H2SO4 (сульфатной кислоты).
Кроме того, C6H5OH реагирует с металлическим натрием. Этерификации карбоновыми кислотами не поддается. Для получения эфиров может задействоваться реакция между фенолятами и ангидридами/галогенангидридами кислот.
Этеры появляются тогда, когда на фенол воздействуют алкилгалогениды, либо же на феноляты – галогенпроизводные ароматических углеводородов. Итог первого варианта воздействия – сочетания жирных ароматических простых эфиров, второго – чисто-ароматические эфиры. Для обеспечения реакции необходимо присутствие катализатора, которым выступает медь в форме порошка.
Перегонка совокупности «фенол + цинковая пыль» приводит к тому, что гидроксильную группу замещает водород.
— по ароматическому кольцу. Данному соединению свойственно вступление в реакции электрофильного замещения. Оно легко поддается таким воздействиям, как алкилирование, ацилирование, галогенирование, нитрование и сульфирование.
В этом ракурсе стоит упомянуть также реагирование с водным раствором брома, хлорным железом (качественные реакции на гидроксибензол) и концентрированной HNO3 (нитратной кислотой).
Гидрируя фенол в ходе присоединительной реакции и при условии наличия катализирующих металлических компонентов, создают гексалин и циклогексанон.
Что касается окисления карболовой кислоты, то так как в фенольной молекуле присутствует гидроксильная группа, стойкость к окислению значительно слабее, по сравнению с бензолом. Продукт на выходе зависит от природы окисляющего материала и условий, при которых проводилась реакция.
Получение
На сегодняшний день пром. изготовление фенола происходит 3-мя способами:
— кумол (изопропилбензол) помещают в каскад барботажных колонн и выполняют некаталитическое окисление с помощью воздуха, при этом формируется гидропероксид кумола (2-гидроксипропан-2-илбензол);
— полученный ГПК при воздействии H2SO4 катализируется и разлагается на фенол и диметилкетон.
Кстати, в ходе данного процесса в качестве побочного продукта выделяется еще одно ценное вещество, а именно α-метилстирол (изопренилбензол).
Кстати, сейчас подвергаются испытаниям установки, с помощью которых предполагается синтез фенола в ходе прямого окисления бензола оксид диазотом и кислотного разложения гидропероксида втор-бутилбензола. Кроме того, это вещество может быть получено при восстановлении хинона.
Применение
Рассматриваемый материал имеет очень широкий спектр использования. Без него не обходятся в разноплановых процессах, о которых не помешает знать.
Фенол – это соединение, которое было выведено искусственным путем. Ему характерна низкая t плавления, растворение в средах и органической, и неорганической природы. Оно – ценная основа для создания различных материалов, важных в пром. масштабах. Ввиду антисептических свойств, применяется для дезинфекционных мероприятий, направленных на белье, помещения и т.д. Но если раньше для этих целей вещество использовалось активно, то сегодня его задействование ограничено, из-за высокотоксичности.
Сферы применения фенола:
— изготовление красителей (указанную субстанцию берут для этого направления, поскольку она под влиянием воздуха способна менять свой окрас);
— производство пластических масс, а именно фенолформальдегидных смол и ДФП, используемого, в свою очередь, при создании поликарбонатов и эпоксидных смол;
— переработка нефти (селективное маслоочищение, очистка ортокрезола и создание присадок для масел). Фенол характеризуется значительной эффективностью, если нужно удалить смолистые вещества, серосодержащие соединения и прочее из масел;
— молекулярная биология и генная инженерия (участие в очищении ДНК и в выделении ДНК из клетки совместно с метилтрихлоридом);
— медицина и фармацевтика, а именно создание популярных и востребованных медикаментов, в частности производных фенольной к-ты. Это, прежде всего, аспирин, или ацетилсалициловая кислота – средство для понижения жара. Это также салол – дезинфицирующий препарат, используемый при болезнях кишечника и мочевой системы. Это и ПАСК, показанная при туберкулезе, и хорошо известный пурген (фенолфталеин) – лекарство со слабительным эффектом, и орасепт – препарат для обезболивания и антисептической обработки;
— химия, а если быть точнее, то производство искусственного волокна, в частности капрона и нейлона;
— легкая промышленность (дезинфекционная обработка шкур животных в составе кожно-меховых дубителей);
— производство пластифицирующих составов для полимеров;
— парфюмерная отрасль (изготовление парфюмерии);
— косметология (задействуется как средство для глубокого хим. пилинга);
— аналитическая химия (служит реагентом);
— обработка с/х насаждений (выступает защитным средством для растений, входит в состав пестицидов);
— скотоводство (дезинфекционные мероприятия, направленные на животных).
Раньше фенол активно использовали при изготовлении стройматериалов, товаров бытового назначения, пластика для различных изделий, в том числе игрушек. Сегодня же это либо максимально сокращено, либо вообще запрещено, ввиду опасного воздействия на человеческий организм, в частности на нервную систему, сердце и сосуды, почки и печень, а также на иные внутренние органы. Хотя до сих пор есть производители, которые, не смотря на все запреты и ограничения, используют фенол даже при создании игрушек для детей.
На заметку! Фенол как отдельное соединение используется в разных сферах, но еще в больших объемах в работу берутся его различные производные.
Опасность фенола
Данный реактив токсичен (принадлежит ко 2-му классу опасности хим. продуктов), является одним из пром. загрязнителей, способен наносить вред людям и животным. Кроме того, губительно воздействует на большое число микроорганизмов, как результат – биоочистка промышленных стоков, содержащих много фенола, сопровождается немалыми сложностями.
Контактируя с кожей, не только обжигает (а ожоги после могут еще и трансформироваться в язвы), но и всасывается внутрь, провоцируя отравления и пагубное воздействие на головной мозг. Попадая в организм сквозь органы дыхания, раздражает и опять же обжигает. Если площадь хим. ожога будет составлять 25 % и более, не исключен летальный исход.
Негативное воздействие фенола на организм может заключаться также в следующем: кашле, чихании, мигренях и головокружениях, побледнении, тошноте, потере сил, мышечной атрофии, язве желудка и двенадцатиперстной кишки.
Это не значит, что указанное вещество следует полностью вычеркнуть из жизни. Нужно правильно с ним обращаться, чтобы минимизировать риски, и тогда эффект, который с его помощью можно получить, порадует во всех смыслах. Используйте фенол правильно, соблюдая нормы, правила и технику безопасности, чтобы ни вам, ни другим людям, ни окружающей среде не было нанесено ни малейшего вреда.