Фенилаланин

Но чтобы получить реальную пользу от этой аминокислоты, необходимо присутствие витаминов В3, В6, С, а также меди и железа. В организме фенилаланин трансформируется в другую аминокислоту – тирозин.
Роль в организме
Аминокислоты – это питательные вещества, из которых формируются протеины. Фенилаланин относится к группе данных соединений. Он является основой для инсулина, меланина и папаина.
Существуют три варианта аминокислоты. L-фенилаланин – естественная форма, которая содержится в продуктах. D-фенилаланин – синтетическое зеркальное отражения природной формы или по-научному – изомер. Но поскольку оба варианта имеют собственные уникальные преимущества, была создана третья форма фенилаланина, которая объединила полезные свойства двух предыдущих форм. Ее название – DL-фенилаланин.
Эта аминокислота незаменима для здоровья центральной нервной системы. Она помогает избавить от депрессии и других психических расстройств. Это обусловлено способностью повышать настроение, избавлять от тревоги, концентрировать внимание, а также улучшать мотивацию. Фенилаланин участвует в формировании нейромедиаторов, таких как дофамин, эпинефрин, норэпинефрин, от которых зависит правильное функционирование системы. Аминокислота благотворно влияет на самочувствие людей, страдающих хронической усталостью; восстанавливает бодрость и ясность мышления. Также является важным элементом для укрепления памяти.
Фенилаланин содействует формированию мелатонина, от которого зависит правильное протекание циклов сна. Также он необходим для производства другой аминокислоты – тирозина, эффективной в лечении тревог и депрессий. И помимо этого, фенилаланин регулирует метаболические процессы, тормозя отложение жира.
Исследователям еще до конца неясно, по какому принципу работает в организме фенилаланин, но понятно, что он выполняет свою функцию по передаче сигналов. Известно, что вещество способно проникать в центральную нервную систему, пересекая гематоэнцефалический барьер (эта преграда защищает мозг от попадания в него токсинов, бактерий и вирусов).
И еще один интересный факт. Фенилаланин помогает избавляться от кофейной зависимости и побороть чрезмерный аппетит.
В чем польза для организма

Фенилаланин действует на организм в качестве эффективного обезболивающего. Эта способность аминокислоты особо действенна при мигренях и других видах головных болей. Помогает и при дискомфорте в шее, нижней части спины, при артритах и во время менструаций. Есть свидетельства, что фенилаланин снимает неприятные ноющие ощущения в местах давних травм.
Это происходит за счет влияния аминокислоты на эндогенную систему обезболивания, которая снижает передачу болевых ощущений. Эффективен при лечении артритов, невралгии, судорог.
Фенилаланин способен ослабить проявления депрессии и тревоги. Многие нейромедиаторы, созданные при участии аминокислоты, являются эффективным средством улучшения настроения, дают чувство благополучия, помогают бороться со стрессами, снижают степень беспокойства и тревожности. Потребление продуктов, богатых фенилаланином или биодобавок, содержащих аминокислоту, поможет положительно повлиять на настроение и общее состояние нервной системы, быстрее приведет к эмоциональному равновесию.
Суточная норма
Существует довольно широкий диапазон рекомендуемых доз фенилаланина: от 100 мг до 5 г в сутки. Наиболее распространенная дневная норма вписывается в рамки между 1 и 2 граммами вещества в день.
Кому полезен
Фенилаланин не является средством, часто используемым в лечении. К нему прибегают, в основном, для снятия хронических болей, депрессий, при лечении витилиго (белые пятна на коже). Немного повысить суточную норму аминокислоты полезно детям, а также при дисфункции поджелудочной железы, ПМС и разного рода интоксикациях (в том числе алкогольной).
Побочные эффекты
Биодобавки, в составе которых есть фенилаланин, как правило, считаются безопасными, хотя некоторые побочные эффекты редко, но могут проявляться. Это тошнота, головные боли, неприятные ощущения в сердце.
Людям, принимающим антидепрессанты, или проходящим антипсихотическое лечение, нежелательно употреблять фенилаланин без рекомендаций врача.
Передозировка

Другие симптомы неприятия организмом фенилаланина:
Доза, превышающая 5 г в сутки, может спровоцировать серьезные повреждения нервной системы.
Дефицит фенилаланина
Недостаточное потребление фенилаланина чревато рядом серьезных нарушений в работе организма.
Во-первых, недостаток аминокислоты сказывается на работе мозга – ослабевает память. Во-вторых, возможно обострение депрессий, развитие болезни Паркинсона, а также усиление хронических болей. Дефицит вещества вызывает снижение мышечной массы, похудение, волосы теряют свой натуральный цвет.
Принимать с осторожностью
Существуют обстоятельства, при которых лучше избегать фенилаланина. В частности, это касается людей с болезнью Паркинсона или шизофренией. Также нельзя принимать препараты, содержащие аминокислоту, людям с аллергией на фенилаланин. С осторожностью – гипертоникам, страдающим бессонницей или психическими расстройствами.
Удержаться от приема синтетической формы вещества советуют беременным и кормящим матерям. Гипертоникам, диабетикам, беременным, лицам с сердечной недостаточностью или поражениями центральной нервной системы, пациентам с лучевой болезнью или фенилкетонурией (генетическое заболевание, проявляется нарушением обмена аминокислот) лучше ограничиться минимальным потреблением вещества.
Взаимодействие

Фенилаланин в пище
В пищевой промышленности фенилаланин используют в качестве ингредиента для аспартама – искусственного подсластителя. Поэтому люди, страдающие фенилкетонурией (неспособность организма расщеплять аминокислоту) должны избегать продуктов с аспартамом.
Натуральная форма аминокислоты в высоких дозах содержится в сое, сыре, орехах, семенах, говядине, баранине, курином мясе, свинине, рыбе, яйцах, молочных продуктах, бобах, злаках, грибах, петрушке, инжире, сушеных абрикосах, бананах, топинамбуре.
| Название продукта (100 г) | Содержание фенилаланина (мг) |
|---|---|
| Соевые продукты | 2066 |
| Сыр (твердых сортов) | 1922 |
| Семена, орехи | 1733 |
| Говядина | 1464 |
| Домашняя птица | 1294 |
| Свинина (нежирные куски) | 1288 |
| Тунец | 1101 |
| Яйца | 680 |
| Фасоль | 531 |
| Цельные зерна | 300 |
В категории твердых сыров наивысшая концентрация аминокислоты в пармезане. Немного меньше, но достаточно для удовлетворения суточной нормы, в швейцарском, эдаме, моцарелле, горгонзоле, гауде и твороге. Семена подсолнечника, льна и кунжута, а также арахис, фисташки, миндаль и кешью способны насытить организм фенилаланином. Выбирая среди мясных продуктов, предпочтение лучше отдать индейке, курице, нежирной свинине, постной говядине, а также мясу ягненка.
Ищите хорошие источники аминокислоты в рыбном отделе? Тогда обязательно запасайтесь лососем, скумбрией, треской, палтусом, а также омарами. Среди молочных продуктов, бесспорно, стоит обратить внимание на йогурты и цельное молоко. А в категории бобовых, помимо фасоли, не стоит забывать о не менее полезной чечевице.
Фенилаланин – важный элемент здорового и правильного питания. Его благотворное влияние сказывается на работе почти всех систем в организме и на внешнем виде.
Больше свежей и актуальной информации о здоровье на нашем канале в Telegram. Подписывайтесь: https://t.me/foodandhealthru
Что такое фенилкетонурия? Причины возникновения, диагностику и методы лечения разберем в статье доктора Алексенцева Е. С., врача УЗИ со стажем в 12 лет.
Определение болезни. Причины заболевания
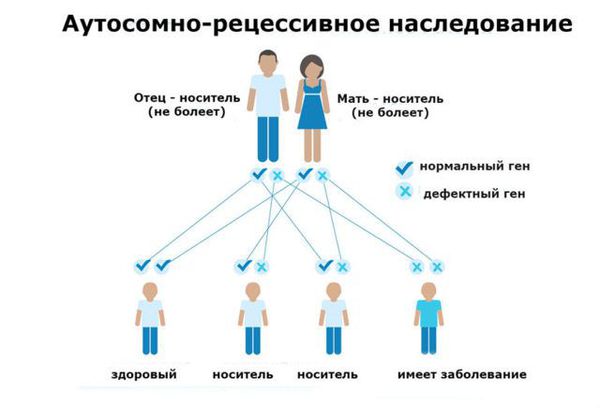
Фенилкетонурия (ФКУ) — генетическое заболевание, в основе которого лежит врождённое нарушение метаболизма аминокислот, характеризующееся повышенным содержанием фенилаланина в крови. Это аутосомно-рецессивная патология, т. е. ребёнок может унаследовать данное заболевание только в том случае, если оба родителя являются носителями дефектной версии гена.
Распространённость фенилкетонурии
Факторы риска фенилкетонурии
Основной фактор риска фенилкетонурии — это наличие у обоих родителей дефекта в гене PAH (Phenylalanine hydroxylase gene). Заболевание развивается, если оба родителя передают ребёнку копию повреждённого гена.
Симптомы фенилкетонурии
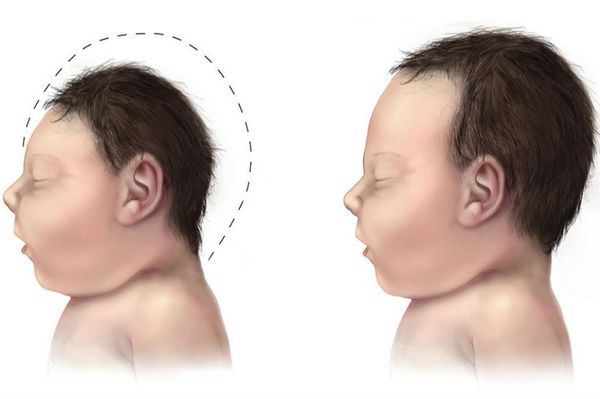
Как проявляется фенилкетонурия у новорождённых
Чем дольше ребёнок с фенилкетонурией не получает специфического лечения, тем быстрее развивается умственная отсталость и необратимые нарушения развития. Кроме того, для детей с фенилкетонурией характерны следующие признаки [4] :
Патогенез фенилкетонурии
Фенилкетонурия как самостоятельное заболевание было открыто норвежским врачом Иваром Асбьёрном Фёллингом ещё в 1934 году. Несмотря на это, вопрос о патогенезе долгое время оставался открытым.
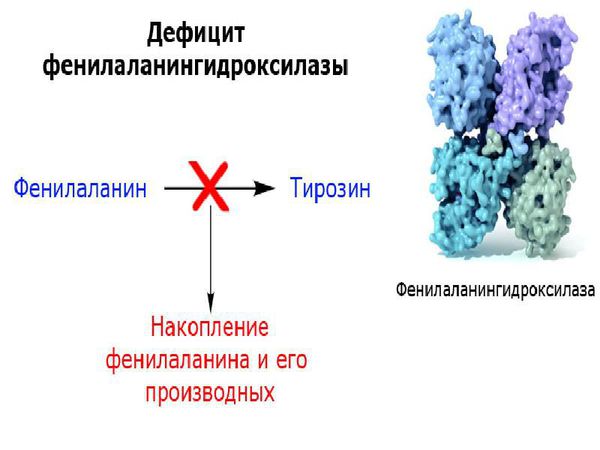
Фенилаланин — это незаменимая аминокислота, которая участвует с синтезе белков. Незаменимая она потому, что организм не может самостоятельно её синтезировать, фенилаланин можно получить исключительно из пищи (мясных и рыбных продуктов, творога, сыра, яйц, орехов, хлебобулочных изделий, круп) или с помощью протеолиза — процесса гидролиза белков с помощью ферментов-протеаз.
У пациентов, страдающих фенилкетонурией, из-за дефекта гена и недостатка фермента фенилаланин-гидроксилазы происходит увеличение в плазме крови концентрации фенилаланина (более 1200 мкмоль/л при норме 0-120 мкмоль/л ) и его метаболитов. Одновременно с этим снижается уровень тирозина и его производных (дофамина, адреналина, норадреналина и меланина). Такое состояние оказывает выраженное нейротоксическое действие на структуры мозга. Если пациент с фенилкетонурией не получает или не соблюдает лечение, то у него отмечаются повреждения мозолистого тела, полосатого тела, изменения коры и гипомиелинизация (снижение содержания миелина, образующего оболочку нервных волокон, в различных структурах оболочек мозга). Эти изменения могут привести к снижению интеллектуального развития и нейродегенерации — прогрессирующей гибели нервных клеток. Поэтому пациенты с фенилкетонурией более восприимчивы к нарушениям, связанным с дефицитом дофамина в головном мозге, таким как паркинсонизм.
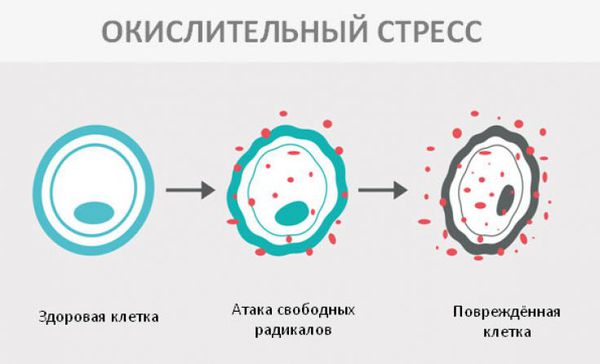
Хотя патофизиологические механизмы повреждения головного мозга у пациентов с фенилкетонурией ещё не совсем понятны, существует множество свидетельств метаболических изменений, которые включают:
Окислительный стресс — это повреждение клеток активными формами кислорода, которые представляют собой молекулы с повышенной реактивностью из-за наличия неспаренного электрона на внешнем электронном уровне. Активные формы кислорода образуются в клетках постоянно, но в норме их уровень настолько низкий, что организм самостоятельно их нейтрализует с помощью антиоксидантной системы. Окислительный стресс происходит в том случае, когда активных форм кислорода образуется слишком много и антиоксиданты не могут полностью их инактивировать. Такой дисбаланс может вызвать окислительное повреждение белков, липидов или ДНК.
Классификация и стадии развития фенилкетонурии
Пожизненная диетотерапия ассоциирована с нарушением роста, снижением минеральной плотностей костей и дефицитом питательных веществ, что требует постоянного контроля у профильных специалистов.
Диагностика фенилкетонурии
Развитие медицины привело к созданию тандемной масс-спектрометрии для быстрого определения концентраций аминокислот в небольших объёмах крови или плазмы. Данный метод даёт более низкую частоту ложноположительных результатов, измеряя уровни фенилаланина и тирозина в исследуемых образцах.
Для неонатального скрининга медицинским персоналом с помощью скарификатора осуществляется забор крови из пятки новорождённого строго через 3 часа после кормления. Полученные образцы крови помещаются на специальные фильтровальные бумажные тест-бланки и отправляются в лабораторию.
Стоит отметить, что у некоторых детей, особенно у рождённых раньше срока, может наблюдаться незрелость ферментных систем, участвующих в метаболизме аминокислот. Это приводит к кратковременному повышению фенилаланина и положительному результату при скрининге [12] Около 2 % всех случаев повышенного уровня фенилаланина в крови, выявленного при скрининге новорождённых, связаны с нарушением метаболизма кофермента BH4, который участвует в преобразовании фенилаланина. Это подчёркивает важность проведения дифференциальной диагностики при всех выявленных уровнях гиперфенилаланинемии. Фенилкеторурию необходимо дифференцировать с такими заболеваниями, как транзиторная гиперфенилаланинемия недоношенных, наследственная доброкачественная гиперфенилаланинемия, тирозинемия, галактоземия.
Лечение фенилкетонурии
Контроль уровня фенилаланина в крови
Мнение медицинского сообщества относительно начала лечения пациентов с концентрациями фенилаланина 360-600 мкмоль/л достаточно противоречивы. Costello и соавторы [18] проводили исследование, в котором пациенты были разделены на три группы:
Общее потребление белка должно обеспечивать безопасные уровни потребностей данного макронутриента с дополнительной дотацией 40 % L-аминокислот (20 % L-аминокислот необходимы для компенсации потребностей в незаменимой аминокислоте и еще 20 % L-аминокислот используются для контроля фенилаланина в крови).
При введении неадекватных дозировок L-аминокислот они ограничивают синтез белка. Белковый обмен, который в норме складывается из процессов анаболизма (синтеза) и катаболизма (распада) белков, смещается в сторону катаболизма. При данном процессе фенилаланин остается неиспользованным для синтеза белка, и его концентрация в крови будет расти.
При фенилкетонурии необходимо избегать продуктов, богатых белком (мясо, рыба, яйца, обычный хлеб, большинство сыров, орехи и семена), а также продуктов, содержащих аспартам (подсластитель, который используется при изготовлении некоторых газированных изделий и конфет). Пища с низким содержанием белка при диетотерапии данного заболевания должна содержать 50 мг или менее фенилаланина на 100 г сухого продукта. Фрукты и овощи, содержащие менее 75 мг фенилаланина на 100 г пищевого продукта, также могут быть включены в рацион. При употреблении таких овощей, как картофель, брокколи, цветная капуста, брюссельская капуста, нужно учитывать, что даже их небольшое количество в рационе обеспечивает организм 50 мг фенилаланина, поэтому их потребление не должно быть бесконтрольным. Для удобства родителей и ребёнка следует пользоваться «пищевым светофором», где все продукты разделены на группы, разрешённые (ограниченно или неограниченно) и запрещённые к употреблению.
Когда ребёнок маленький, соблюдение диеты не является проблемой для семьи, так как родители контролируют потребление продуктов. В младенческом возрасте предлагается использовать специализированные смеси без добавок фенилаланина, которые дополняются либо грудным молоком, либо стандартной семью для перекрытия суточной потребности в фенилаланине.
Дети более старшего возраста продолжают не только пить специальный безфенилаланиновый продукт, который способен обеспечить потребности в белках и калориях, но и получают дополнительное количество разрешённых продуктов (овощи и фрукты, мёд, животные и растительные масла, зефир, пастила, варенье), необходимых для создания пищевого разнообразия.
По мере взросления ребёнка соблюдение диеты становится всё труднее, так как дети с фенилкетонурией, в отличие от своих сверстников, значительно ограничены в выборе продуктов, что часто приводит к скачкам концентрации фенилаланина у подростков [20] [21] Долгосрочное поддержание диеты необходимо, поскольку пациенты после периода нарушений диеты намного труднее возвращаются к прежнему режиму питания.
Прогноз. Профилактика
Если пациенты с фенилкетонурией получают и соблюдают лечение с самого раннего возраста, то их качество и продолжительность жизни ничем не отличается от их здоровых сверстников.
Пациенты, не получающие или не соблюдающие лечение, часто имеют инвалидность и низкий уровень качества жизни. Кроме того, несоблюдение диеты и отсутствие контроля фенилаланина в организме часто приводит к снижению продуктивности и внимания, нарушению поведения (особенно при уровне аминокислоты свыше 360 мкмоль/л).
Адекватное наблюдение за концентрацией фенилаланина в пределах допустимых показателей достаточно эффективно в профилактике большинства нарушений центральной нервной системы. Большинство людей демонстрируют нормальное общее развитие, легко справляются с образовательными стандартами, ведут самостоятельную жизнь и получают работу, будучи взрослыми.
При соблюдении пациентом режимов диеты и дополнительной дотации минеральных веществ не отмечается увеличения риска таких осложнений, как остеопороз или частые переломы при отсутствии других заболеваний костно-мышечной системы и соединительной ткани.
Профилактика фенилкетонурии
Если у будущих родителей или их близких родственников выявлена фенилкетонурия, то при планировании беременности рекомендуется проконсультироваться с генетиком и пройти обследование. Так можно определить риск рождения ребёнка с фенилкетонурией.
Фенилаланин
Фенилаланин принадлежит к группе незаменимых аминокислот. Он является строительным материалом для производства таких белков как инсулин, папаин, а также меланин. Кроме того, он способствует выведению продуктов метаболизма печенью и почками. Также он играет важную роль по улучшению секреторной функции поджелудочной железы.
Продукты богатые фенилаланином:
Общая характеристика фенилаланина
Фенилаланин представляет собой ароматическую аминокислоту, которая входит в состав белков, и кроме того имеется в организме в свободном виде. Из фенилаланина в организме образуется новая очень важная аминокислота тирозин.
Для человека фенилаланин является незаменимой аминокислотой, так как не вырабатывается организмом самостоятельно, а поставляется в организм вместе с пищей. Данная аминокислота имеет 2 основные формы – L и D.
L-форма наиболее распространена. Она входит в состав белков тела человека. D-форма является отличным анальгетиком. Существует еще смешанная LD-форма, обладающая комбинированными свойствами. LD-форма иногда назначается в виде БАДов при ПМС.
Суточная потребность в фенилаланине
Потребность в фенилаланине возрастает:
Потребность в фенилаланине снижается:
Усваиваемость фенилаланина
У здорового человека усваивается фенилаланин хорошо. При употреблении продуктов богатых фенилаланином, следует быть осторожным тем людям, у которых имеется наследственное заболевание нарушения обмена аминокислот, называемое фенилкетонурией.
В результате этого заболевания, фенилаланин не способен преобразовываться в тирозин, что оказывает негативное влияние на всю нервную систему и головной мозг в частности. При этом развивается фенилаланиновое слабоумие, или болезнь Феллинга.
К счастью, фенилкетонурия является наследственным заболеванием, которое можно победить. Достигается это при помощи специальной диеты и специального лечения, назначенного врачом.
Полезные свойства фенилаланина и его влияние на организм:
Попадая в наш организм, фенилаланин способен оказывать помощь не только при производстве белка, но также и при ряде заболеваний. Он хорошо помогает при синдроме хронической усталости. Обеспечивает быстрое восстановление бодрости и ясности мышления, укрепляет память. Действует как естественное болеутоляющее. То есть, при достаточном содержании его в организме, чувствительность к болевым ощущениям значительно снижается.
Способствует восстановлению нормальной пигментации кожи. Применяется при расстройствах внимания, а также при гиперактивности. При определенных условиях преобразовывается в аминокислоту тирозин, которая в свою очередь является основой двух нейромедиаторов: дофамина и норадреналина. Благодаря им улучшается память, усиливается половое влечение, повышается способность к обучению.
Кроме того, фенилаланин является исходным материалом для синтеза фенилэтиламина (вещества, ответственного за чувство влюбленности), а также эпинефрина, улучшающего настроение.
Еще фенилаланин используется для снижения аппетита и уменьшения тяги к кофеину. Применяется при мигрени, судорогах мышц рук и ног, послеоперационных болях, ревматоидном артрите, при невралгиях, болевых синдромах и болезни Паркинсона.
Взаимодействие с другими элементами
Попадая в наш организм, фенилаланин вступает во взаимодействие с такими соединениями, как вода, пищеварительные ферменты и другие аминокислоты. В результате этого, образуются тирозин, норадреналин и фенилэтиламин. Кроме того, фенилаланин способен взаимодействовать с жирами.
Признаки нехватки фенилаланина в организме:
Признаки избытка фенилаланина в организме:
Факторы, влияющие на содержание фенилаланина в организме:
Систематическое употребление продуктов питания, содержащих фенилаланин, и отсутствие наследственной болезни Феллинга – являются двумя основными факторами, играющими главную роль в достаточном обеспечении организма данной аминокислотой.
Фенилаланин для красоты и здоровья
Фенилаланин еще называют аминокислотой хорошего настроения. А человек в хорошем настроении всегда притягивает взгляды окружающих, отличаясь особой привлекательностью. Кроме того, некоторым людям с помощью фенилаланина удается снизить нездоровую тягу к вкусненькому и стать стройнее.
Достаточное содержание фенилаланина в организме придает волосам насыщенный цвет. А отказавшись от регулярного употребления кофе, и заменив его фенилаланино-содержащими продуктами, можно добиться улучшения цвета лица и укрепления своего здоровья.
Внимание! Информация носит ознакомительный характер и не предназначена для постановки диагноза и назначения лечения. Всегда консультируйтесь с профильным врачом!
Фенилаланин что это по простому
Гиперфенилаланинемия (ГФА) представляет собой повышение уровня фенилаланина в крови натощак по сравнению с показателями, выявляемыми у здоровых пациентов идентичного возраста. Гиперфенилаланинемия (ГФА) является группой заболеваний, среди которых наиболее частым является дефицит фенилаланингидроксилазы (ФАГ). Небольшое количество случаев связано с дефектом системы кофактора биоптерина (Burgard et al, 2000).
а) Биохимические и генетические изменения при фенилкетонурии и гиперфенилаланинемии:
1. Дисфункция метаболизма. Для гидроксилирования фенилаланина до образования тирозина необходимо три фермента: ФАГ, карбиноламиндегидротаза (КАД) и дигидропротеинредуктаза (ДПР), и два кофактора: тетрагидробиоптерин (ТГБ) и редуцированный НАД. На основании уровня фенилаланина в плазме и остаточной активности ФАГ в печени выделено три наследственных фенотипа ГФА в связи с дефицитом ФАГ: классическая фенилкетонурия, атипичная фенилкетонурия и нефенилкетонурическая ГФА. Дефекты синтеза и метаболизма 5,6,7,8-тетрагидробиоптерина (ТГБ) являются причиной ГФА и нарушений обмена нейротрансмиттеров.
2. Генетические изменения. ГФА является преобладающим нарушением метаболизма аминокислот среди представителей белой расы, частота заболевания составляет приблизительно 1 на 10000 живых новорожденных. Данное аутосомно-рецессивное заболевание вызвано более чем 500 мутациями локуса ФАГ. Различные группы мутаций преобладают в определенной этнической популяции, что позволяет проводить пренатальную диагностику, выявлять носителей и прогнозировать фенотип фенилкетонурии, связанный с определенным гаплотипом.
Некоторые мутации ФАГ приводят к дефициту ФАГ с остаточной ферментной активностью, которая усиливается под действием ТГБ. В таких случаях фармакологические дозы ТГБ приводят к минимум 30% снижению уровня фенилаланина в крови (Fiori et al., 2005).
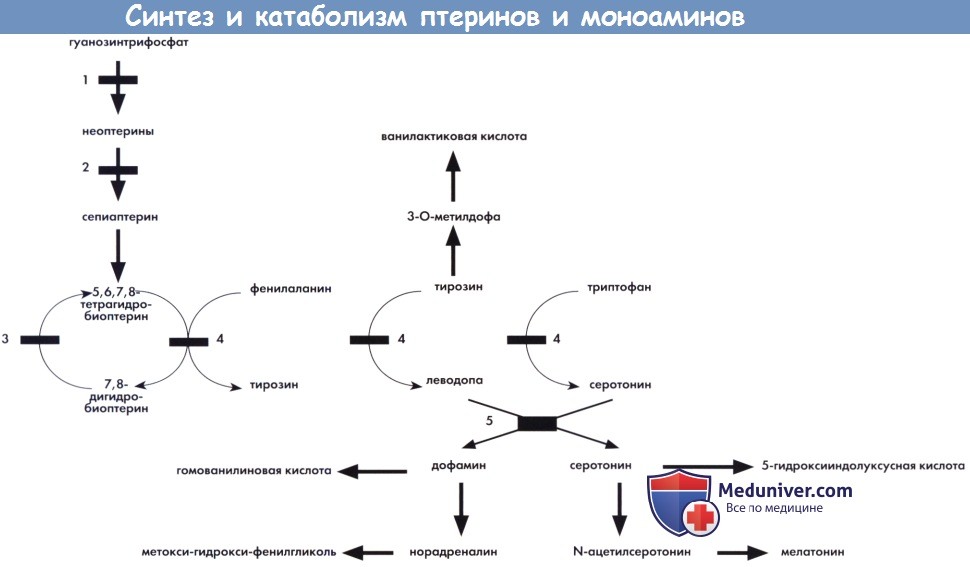
1 — гуанозинтрифосфатциклогидролаза. 2 — биоптеринсинтаза. 3 — дигидроптеридинредуктаза.
4 —фенилаланин-, тирозин-, триптофангидроксилазы.
5 — ароматическая L-декарбоксилаза аминокислот (зависимая от пиридоксальфосфата).
3. Патогенез. Считается, что клинические проявления гиперфенилаланинемии (ГФА) являются результатом накопления фенилаланина и его вторичного воздействия на химические процессы в головном мозге. Фактически, фенилкетонурия чаще всего сопровождается задержкой умственного развития, в то время как при нефенилкетонурической гиперфенилаланинемии умственное развитие не меняется, что предполагает наличие порогового уровня фенилаланина во внеклеточных жидкостях, при превышении которого персистирующая постнатальная (или фетальная) гиперфенилаланинемия приводит к необратимому повреждению головного мозга. В случае если пороговая величина достигается позже, после прекращения соблюдения диеты пациентами, которым ранее проводилось лечение фенилкетонурии, развиваются обратимые химические изменения, способные оказывать воздействие на нейрофизиологические функции.
У пациентов с фенилкетонурией при высоком уровне фенилаланина в плазме отмечается снижение синтеза нейротрансмиттеров. Дефект синтеза нейротрансмиттеров может быть связан с конкурентным ингибированием транспорта крупных аминокислот (тирозина, триптофана и разветвленных цепей аминокислот) в головной мозг через гематоэнцефалический барьер и из спинномозговой жидкости обратно в кровь, что приводит к низкой концентрации тирозина и триптофана в головном мозге пациентов, несмотря на высокое содержание данных веществ в спинномозговой жидкости, а также, возможно, с конкурентным ингибированием гидроксилирования тирозина высоким уровнем фенилаланина.
В головном мозге пациентов старшего возраста, которым не проводилось лечения фенилкетонурии, отмечается аномальная миелинизация, уменьшение массы мозга и снижение содержания миелина. Данное пагубное влияние подтвердилось в ходе исследования на мышах (модель НРН-5). Результаты настоящих или ранее проведенных наблюдений стали основой для гипотезы о снижении количества миелина вследствие ингибирования специфичной для олигодендритных клеток АТФ-сульфурилазы, приводящего к низкому содержанию сульфатидов в миелине, который в свою очередь подвергается протеолитическому распаду. В дальнейшем отмечается потеря нейронов и уменьшение количества межнейронных связей, что было продемонстрировано путем количественной оценки плотности рецепторов нейротрансмиттеров. Если перенести на человека результаты, полученные в ходе исследований на животных, особое поражение гиппокампа и затылочного пространства могут объяснить некоторые нейрофизиологические нарушения у пациентов с фенилкетонурией, которым не проводилось лечения или лечение было недостаточным.
Аномальный синтез белков головного мозга вследствие дезагрегации полисом и снижении скорости удлинения полипептидной цепи могут приводить к снижению массы головного мозга. Дезагрегация полисом отмечается также в сердце и головном мозге плодов крыс, подвергающихся воздействию ГФА беременной самки; данное обстоятельство имеет отношение к фетопатии, связанной с ГФА беременной женщины.
Снижение содержания ДНК и синтеза в нейронах, подвергающихся воздействию фенилаланина в высоких концентрациях, также может объяснять снижение пролиферации нейронов, потерю нейронов и нарушение роста головного мозга.
б) Клинические проявления. Фенилкетонурия при отсутствии лечения Клинические проявления фенилкетонурии, по поводу которой не проводилось лечения, включают задержку умственного развития, неврологические аномалии и вненеврологические симптомы (хотя сроки их возникновения варьируют у различных пациентов). Задержка умственного развития часто сочетается с микроцефалией. Аномалии ЭЭГ встречаются часто (78-95% случаев), но только у 25% пациентов отмечаются припадки, чаще всего генерализованные. Нередко встречается психотическое поведение с гиперактивностью, деструктивным и самодеструктивным поведением, импульсивностью и неконтролируемым поведением с эпизодами эмоционального возбуждения.
У большинства пациентов слабопигментированная кожа с экзематозными проявлениями. Общее физическое развитие обычно хорошее.
Клинический фенотип представляет преимущественно исторический интерес, так как в настоящее время симптомы предотвращаются за счет ранней диагностики и лечения. Тем не менее, до сих пор отмечаются случаи пропущенной ГФА у новорожденных в случае, если тесты не проводились или были получены ложноотрицательные результаты.
в) Фенилкетонурия, по поводу которой проведено раннее лечение. У детей с фенилкетонурией, выявленной при рутинном скрининге новорожденных, по поводу которой вскоре после рождения была начата диетотерапия с ограничением фенилаланина, отмечается нормальный уровень умственного развития (Hanley, 2004). Тем не менее, результаты ретроспективных исследований свидетельствуют о том, что даже при максимально благоприятных условиях лечения у детей отмечается тенденция к более низкому коэффициенту IQ, чем у родственников первой линии, и худшей способности к обучению, чем у сибсов и детей контрольной группы. Часто встречаются субклинические нейрофизиологические (изменения вызванных потенциалов и проводимости нерва) и нейропсихологические нарушения, особенно у пациентов, не строго соблюдающих диету.
Частота аномалий на ЭЭГ увеличивается с возрастом вне зависимости от раннего и строгого соблюдения диеты, а результаты МРТ свидетельствуют о том, что дисмиелинизация является практически универсальным проявлением среди пациентов с классической и атипичными формами фенилкетонурии. Изменения на МРТ затрагивают затылочно-теменные области и в наиболее тяжелых случаях распространяются на лобные и височные доли. Описанные изменения не имеют явной взаимосвязи ни с клиническими или нейропсихологическими проявлениями, ни с контролем потребления фенилаланина в раннем детском возрасте, но коррелируют с уровнем фенилаланина в крови на момент проведения нейровизуализации и частично обратимы при снижении концентрации фенилаланина в крови.
г) Лечение фенилкетонурии и гиперфенилаланинемии (ГФА). У пациентов с классической и атипичной фенилкетонурией для предотвращения необратимых повреждений головного мозга диета с исключением фенилаланина должна быть начата вскоре после рождения. Ежедневное пероральное применение тетрадигидробиопентина может быть альтернативой диете у пациентов с чувствительной к тетрадигидробиопентину формой атипичной фенилкетонурии (Muntau et al., 2002). Для предотвращения интеллектуальной, неврологической и нейрофизиологической деградации после расширения диеты универсальной тактикой является пожизненное лечение. У пациентов с нефенилкетонурической ГФА (уровень фенилаланина в сыворотке
Редактор: Искандер Милевски. Дата публикации: 12.12.2018