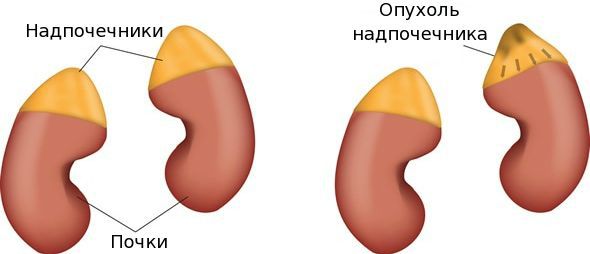
Узелковое заболевание надпочечников
Введение: Что такое узелковое заболевание надпочечников?
Множество узелковых поражений надпочечников представляют хирургический интерес. Некоторые из них, так называемые «функциональные» (например, аденома, карцином, феохромоцитома и т.д.) могут образоваться из-за гормонального синдрома (например, Синдром Кушинга, Синдром Конна, Синдром феохромоцитомы). Другие не выделяют каких-либо гормонов и поэтому называются «нефункциональными» (например, нефункциональные аденомы и карциномы, миелолипомы, кисты и т.д.).
Симптомы: Как узнать имеешь ли ты узловую болезнь надпочечников?
Симптомы и признаки узлового поражения надпочечников многообразны и зависят от: 1) возможной гиперсекреции гормонов и 2) размера и массы. Во многих случаях, она диагностируется случайно при рентгенологических исследованиях, не относящихся к подозрению на заболевания надпочечников (инциденталома). Среди клинических синдромов, связанных с гормональной гиперсекрецией мы включаем:
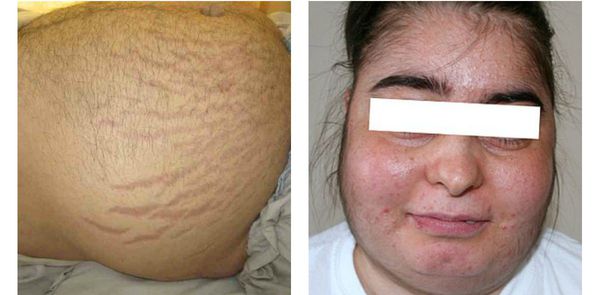
— Синдром Кушинга, обусловлен избыточной секрецией гормонов коры надпочечников, прежде всего глюкокортикоидов. Наиболее ранним признаком болезни является ожирение, с типичным отложением жировой клетчатки в области лица, шеи, груди живота. Лицо при этом выглядит округлым, лунообразным, Другие признаки: на щеках появляется пурпурный румянец, повышение аппетита, изменение обмена веществ, увеличивается уровень глюкозы в крови, усиленное отложение жира, уменьшается масса мышечной ткани конечностей, появляются стрии, на коже появляются угревые высыпания, раны и порезы заживают медленно, нарушения менструального цикла, снижение либидо, импотенция, подавление иммунитета и предрасположенность к инфекции, риск тромбоза. Синдром Кушинга вызывает
аденому, рак или гиперплазию микро / макроузлов одной или обеих сторон,
— Первичный гиперальдостеронизм, в результате гиперсекреции альдостерона при поддержке односторонней аденомы надпочечника (синдром Конна) или узловой гиперплазии односторонней или двусторонней, которые обычно проявляются повышенным кровяным давлением, часто резистентные к лекарственной терапии, и гипокалиемия (которая не является необходимым условием для установления диагноза), что приводит к судорогам, парестезии, мышечной усталости;
— Синдром феохромоцитомы приводит к гиперсекреции катехоламинов, характеризующихся повышенным кровяным давлением, связанным с кризисом с учащенным сердцебиением, головной болью, потливостью, бледностью, тошнотой, беспокойством, тремором, гипергликемией;
— Синдром вирилизации (появление мужских половых признаков у женщин, таких как гирсутизм, акне, гипертрофия мышц, выпадение волос, увеличение клитора) или феминизации (увеличение объема груди (гинекомастия), уменьшение роста бороды и волос на теле у мужчин), из-за наличия нарушений, которые секретируют мужские гормоны (андрогены) или женские (эстрогены).
Эпидемиология: Как часто встречается узловая болезнь надпочечников?
Узелковые образования надпочечников обычно обнаруживаются случайно. По оценкам, 3-5% «здорового» населения является невольным носителем одного или нескольких узелков надпочечника. В подавляющем большинстве случаев эти узелки являются небольшими по размеру, не имеют клинического значения и не требуют удаления. Секретирующие гормоны или злокачественные поражения надпочечников встречаются редко.
Синдром Кушинга имеет 4-5 новых случаев заболеваемости надпочечников на миллион.
Диагноз: Как диагностировать заболевания надпочечников?
Как лечить болезнь надпочечников?
Узелковые заболевания надпочечников с хирургической индикацией в большинстве случаев лечатся при помощи лапароскопической адреналэктомии (рис. 1) односторонние (функциональные аденомы, инциденталомы, феохромоцитомы) или двусторонние (узелковая гиперплазия коры надпочечников, болезнь Кушинга, рецидив после операции гипофиза). Традиционная открытая операция или замораживание (криодеструкция) надпочечников применяются в редких случаях.
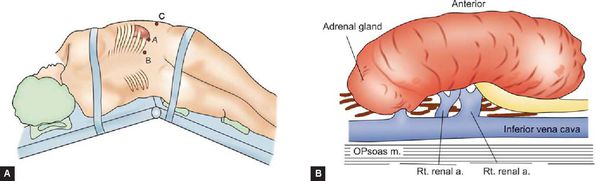
Вовремя лапароскопической адреналэктомии пациент получает общий наркоз и находится в положении на боку (рис.2).
В случае феохромоцитомы, пациент получает вмешательство с альфа-блокаторами (доксазозин, феноксебензомин), также применяются бета-блокаторы, блокаторы кальциевых каналов.
В случае первичного альдостеронизма, контроль давления достигается при введении антагониста альдостерона, это связано с интеграцией калия в случае гипокалиемии.
Перед хирургическим вмешательством помещают катетер в мочевой пузырь, когда пациент находится в состоянии сна. Как правило, делаются от 4 до 5 небольших надрезов, для введения лапароскопических инструментов. Операция может быть выполнена трансперитонеальным или забрюшинным доступом на основе тщательного предоперационного обследования. В отдельных случаях можно прибегнуть к частичному удалению надпочечника. Средняя продолжительность хирургического вмешательства, адреналэктомии, составляет около 2 часов. В конце устанавливается дренаж слева, который, как правило, удаляется на 2-3 послеоперационный день. Средняя послеоперационная продолжительность госпитализации составляет 3-4 дня. Пациент в состоянии ходить, есть в первый день после операции, и в конечном итоге применяется заместительная терапия.
Лапароскопия надпочечников (Рис 1.)
Лапароскопическая адреналэктомия 2.png
Как вести себя после лапароскопической адреналэктомии?
Период после операции при узловой адренокортикальной болезни делится в основном на две категории, основывающиеся на гистологическом исследовании.
В случае доброкачественного заболевания (например, аденомы надпочечника), мониторинг должен выполняться, лабораторные анализы и УЗИ брюшной полости, как правило, через один и три месяца после операции. Также необходимо проходить контроль у эндокринолога, в течение долгого времени.
Наши результаты
В нашей клинике лапароскопическая адреналэктомия является отработанной технологией с 1992 года (первая в Европе), около 400 проведенных вмещательств. Эта тема часто была предметом многочисленных публикаций и презентаций на крупных национальных и международных конференциях по урологии.
Что такое опухоль надпочечника? Причины возникновения, диагностику и методы лечения разберем в статье доктора Хитарьян А. Г., флеболога со стажем в 31 год.
Определение болезни. Причины заболевания
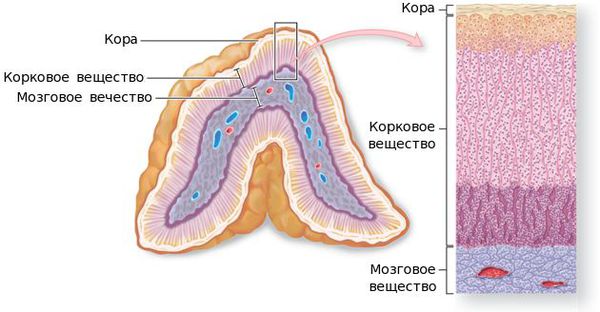
Опухоль надпочечников — это патологический рост ткани надпочечников (коркового или мозгового слоя), в составе которой возникли изменившиеся клетки, ставшие атипичными в плане дифференцировки, характера роста и продукции гормонов. [1]
Распространенность патологии различна, т. к. зависит от вида опухоли. Адренокортикальный рак встречается в 1-2 случаях на один миллион человек. Достоверной статистической информации по распространённости доброкачественных опухолей в настоящее время нет.
Заболеванию подвержены все возрастно-половые группы населения, но пик заболеваемости приходится на 30-40 лет. Имеются лишь небольшие различия в частоте встречаемости андростером: у женщин они возникают в 2-3 раза чаще.
Этиология опухолевого роста изучена не до конца, поэтому единого мнения о причинах его возникновения нет. Однако выделяют несколько теорий возникновения и развития опухоли:
Зная причину появления опухолевых клеток в конкретном случае, можно определиться с тактикой лечения и основами профилактики заболевания.
Симптомы опухоли надпочечника
Доброкачественные новообразования зачастую клинически не вызывают никакой симптоматики, так как они не продуцируют гормонов и имеют малый размер.
Злокачественные опухоли проявляются симптоматикой, характерной для злокачественной опухоли любой другой локализации:
Наибольший интерес представляют гормонально-активные опухоли, так как в клиническом течении, диагностике и тактике лечения они значительно отличаются от злокачественных опухолей, которые в любом случае подлежат хирургическому лечению.
Альдостерома — опухоль, развивающаяся в клубочковом слое коры надпочечников. Её причиной является повышение гормона альдостерона.
В клиническом течении данной опухоли можно выделить три основных синдрома:
Кортикостерома — новообразование, возникающее в мозговом слое надпочечников. При её развитии в крови повышается концентрация стероидных гормонов.
Один из главных признаков человека с такой опухолью — ожирение по центральному типу, округление лица и багровые полосы на животе.
Также заболевание проявляется:
У всех пациентов с кортикостеромой может возникнуть остеопороз.
Андростерома — новообразование надпочечников, которое сопровождается увеличением количества мужского полового гормона андрогена.
При возникновении опухоли в раннем возрасте у мальчиков происходит раннее формирование вторичных половых признаков, увеличение полового члена, мускулатуры, огрубение голоса, но при этом наблюдается атрофия яичек.
Девочки развиваются по мужскому типу: гипертрофия клитора, гирсутизм (избыточный волосяной покров кожи), повышенная мышечная масса.
Независимо от пола возникает угревая сыпь.
При возникновении опухоли у взрослых женщин симптоматика сходна с вышеописанным проявлением заболевания у девочек, а у взрослых мужчин симптомы могут быть неявно выражены.
Феохромоцитома — опухоль, развивающаяся из клеток центральной части надпочечников, которая продуцирует гормоны, приводящие к повышению давления в крови. Она проявляется:
Часто АД нормализуется довольно резко и сопровождается обильным мочеиспусканием.
Инциденталома — гормонально-неактивная опухоль, как правило, небольших размеров. Клинически не проявляется и является случайной находкой при проведении визуализирующих методов исследования по причинам, несвязанным с поражением надпочечников. [4]
Патогенез опухоли надпочечника
Патогенез заболевания довольно сложен. Он зависит от многих причин: морфологической структуры, темпа роста, гистологического строения, и других факторов. Но вне зависимости от природы этиологического фактора в ткани надпочечников появляется атипичная клетка. Она может образоваться там в процессе эмбрионального развития либо трансформироваться из нормальной в опухолевую под воздействием онкогенов (вирусов, радиоактивного излучения, химических канцерогенов и других), тем самым нарушая процессы деления, дифференцировки и роста клетки. Эта атипичная клетка начинает делиться и не подвергается аппоптозу — запрограммированной гибели клеток. Со временем количество атипичных клеток становится настолько большим, что возникает симптоматика того или иного вида опухоли.
При гормонально-активной опухоли происходит гиперпродукция того или иного гормона и, как следствие, увеличивается эффект от воздействия этих гормонов. Такое влияние гормонов на организм вызывает соответствующую клиническую симптоматику. В случае, если опухоль не продуцирует никакого гормона, то патогенез будет связан с избыточным ростом ткани и сдавлением соседних структур надпочечника или других органов. [5]
Понимать патогенез опухолей очень важно, так как зная его можно проводить патогенетическую терапию, которая не так эффективна, как этиологическая, но, в свою очередь, лучше симптоматической и является в настоящее время единственным оптимальным методом консервативного лечения.
Классификация и стадии развития опухоли надпочечника
По локализации новообразования надпочечников делятся на:
Опухоли коры надпочечников встречаются достаточно редко по отношению к опухолям мозгового слоя.
Новообразования надпочечников делятся на:
Также можно разделить опухоли на:
Первичные опухоли делятся на гормонально-неактивные (инциденталомы) и гормонально-активные, т. е. те, которые производят какой-либо гормон. Инциденталомы чаще доброкачественны (липома, фиброма, миома) и одинаково встречаются в любых возрастно-половых группах. Довольно редко они могут быть злокачественными (меланома, тератома, пирогенный рак).
Не стоит забывать и о том, что гормонально-активные опухоли также могут быть злокачественными. Например, феохромоцитома в 10% носит злокачественный характер, андростерома — в половине случаев, альдостерома — до 5% случаев. [7]
Осложнения опухоли надпочечника
Самыми грозными осложнениями доброкачественных гормон-неактивных опухолей является их трансформация в злокачественные. Зачастую это происходит при достаточно позднем обращении и запоздалой диагностике.
В случае поздней диагностики злокачественных опухолей могут возникнуть метастазы, которые усложняют процесс лечения, так как обнаружить все метастазы довольно сложно, а удалить ещё сложнее. Самые частые органы-мишени, куда происходит метастазирование злокачественного новообразования надпочечника — это лёгкие, печень и кости.
Феохромоцитома может осложниться нарушением мозгового кровообращения (инсультом), сердечного кровообращения (инфарктом), аритмией и острой почечной недостаточностью. Поэтому не стоит забывать, что длительное и частое повышение артериального давления влечёт за собой ремоделирование (перестройку) сердца и возникновение кардиологической патологии (например, сердечной недостаточности).
Самым грозным осложнением является катехоламиновый криз, который проявляется внезапным подъёмом артериального давления до 300 мм рт.ст. продолжительностью до 30 минут, головокружением, тремором, потливостью и внезапно оканчивается, после чего происходит обильное мочеиспускание. Его могут вызвать механические факторы (даже пальпация врача при исследовании), стресс, и другие. Купируется криз в/в введением альфа-адреноблокаторов (фентоламина) или нитратами.
гипергликемическая кома. Также из-за постоянного повышения сахара у больных происходят изменения в сосудах и чувствительных нервных волокнах.
Постоянное воздействие повышенного количества гормонов на клетки приводит к их необратимым изменениям. [7] [8] [9]
Диагностика опухоли надпочечника
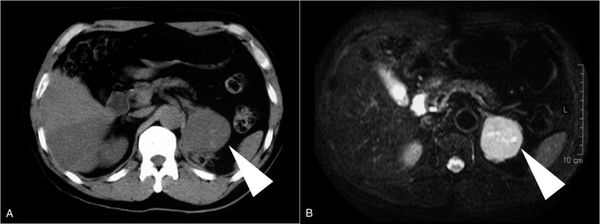
В настоящее время существует множество методов диагностики заболеваний надпочечников, благодаря которым можно определить наличие опухоли. В этом нам помогают магнитно-резонансная и компьютерная томография, ультразвуковое исследование и радионуклеидная сцинтиграфия. [9] Такие визуализирующие методы позволяют понять, где расположена опухоль, определить её размеры и отношение к другим органам. Также МРТ, КТ и УЗИ являются основополагающими методами для определения хирургической тактики лечения, так как врач ещё до начала операции с их помощью уточняется объём вмешательства, операбельность, возможные осложнения и подобирается необходимое оборудование.
При феохромоцитоме определяют содержание продуктов обмена катехоламинов:
Существует множество иных способов диагностики опухоли, таких как катетеризация вен надпочечников, определение уровня гормонов в крови, оттекающей от надпочечника и другие. Но они являются более сложными методами обследования, которые необходимо проводить по строгим показаниям в сложных клинических ситуациях. [10]
К сожалению, несмотря на большое многообразие способов инструментальных и лабораторных методов диагностики, всё же опухоли надпочечника остаются случайной находкой в ходе обследования. Поэтому первостепенную роль в диагностике играют такие рутинные методы, как исследование общего анализа и биохимии крови, общего анализа мочи, а также физикальное обследование. Это связано с тем, что все они позволяют врачу заподозрить какую-либо патологию, а все вышеописанные методы подтверждают наличие заболевания.
Лечение опухоли надпочечника
Подход к лечению опухоли надпочечников является комплексным:
Это позволяет влиять на все звенья патогенеза заболевания.
Стоит отметить, что лучевая и химиотерапия имеют много осложнений, так как действуют не только на опухолевые, но и на здоровые клетки. Однако существует такой современный метод, как адъювантная химиотеапия, которая накапливает химиопрепарат именно в зоне патологического разрастания ткани.
Медикаментозную терапию проводят тогда, когда есть противопоказания к операции. Также этот метод лечения применяется в качестве временной предоперационной терапии для коррекции нарушений гемодинамики и электролитного дисбаланса.
Радикальным является только хирургическое лечение. Оно имеет меньшее число осложнений по сравнению с таргетной и лучевой терапией.
Оперативное лечение при доброкачественных опухолях выполняется в объёме адреналэктомии (удаления надпочечника). [12] При злокачественных опухолях производят адреналэктомию и удаление местных лимфоузлов.
Перед операцией возможно проведение химиотерапии для уменьшения количества атипичных клеток, а значит и размера опухоли.
После удаления новообразования пациент находится под наблюдением у онколога и врача-эндокринолога, так как возможно ему потребуется заместительная терапия. В случае, если удалены оба надпочечника, то заместительная терапия назначается в 100% случаев.
Восстановление пациента после удаления надпочечника по поводу доброкачественных операций происходит в течение 1-2 месяцев. При удалении обоих надпочечников реабилитация длится немного дольше и сопровождается пожизненной заместительной гормонотерапией.
Сроки восстановления после удаления злокачественной опухоли зависят от размеров опухоли, поражения соседних органов, наличия метастазов и сопровождается послеоперационной лучевой и химиотерапией на протяжении не более двух лет.
Отдельные сложности имеются в оперативном лечении феохромоцитомы: манипуляции с надпочечником могут вызвать криз и нарушение гемодинамики во время операции, поэтому такие пациентам проводится тщательная предоперационная подготовка и мониторинг гемодинамики во время операции. В случае возникновения криза его купируют назначением фентоламина и нитратов. [13]
Все обозначенные главные принципы и аспекты лечения опухоли надпочечников не являются универсальными, так как каждый отдельный вид опухоли лечится по своим точным стандартам и клиническим рекомендациям, принятыми ведущими врачами-исследователями и Научно Исследовательскими Институтами. Поэтому следует понимать, что при появлении каких-либо жалоб важно обратиться за медицинской помощью к специалисту, а не заниматься самолечением.
Прогноз. Профилактика
Прогноз при опухолевых поражениях надпочечников зависит от вида опухоли, её стадии и гистологического строения. Он может быть как благоприятным, так и неблагоприятным.
Так, при феохромоцитоме прогноз благоприятный, в 10-15% случаев сохраняется повышенное артериальное давление, учащённое сердцебиение, но всё это довольно легко поддаётся медикаментозной корректировке. Даже при феохромобластоме прогноз относительно благоприятный, если не выявлено отдалённых метастазов.
При удалении альдостеромы в 75-80% случаев так же, как и при феохромоцитоме, симптоматика, связанная с повышением артериального давления, регрессирует, а в тех случаях, если она не проходит, то её коррегируют антигипертензивной терапией.
При удалении кортикостеромы уменьшается и исчезает избыточное оволосенение (гирсутизм), но если опухоль удалена в раннем возрасте, то может возникнуть задержка в развитии.
Прогноз при злокачественных опухолях зависит от величины распространения опухолевой ткани в надпочечнике и метастазирования раковых клеток в организме, так как адреналэктомия технически выполняется, но обнаружить и удалить отдалённые метастазы довольно проблематично. [14]
Нельзя с абсолютной точностью и уверенностью прогнозировать результаты лечения и вероятность осложнений. Это зависит от множества факторов, в том числе и от реакции организма на оперативное лечение, лучевую и химиотерапию.
Так как этиология опухолевого поражения надпочечников неоднозначна, профилактика патологии состоит из соблюдения принципов здорового образа жизни. Главным образом необходимо избегать избыточного воздействия на организм факторов, провоцирующих возникновение опухоли — ионизирующего излучения и химических канцерогенов.
Не стоит забывать, что питание тоже является неотъемлемой частью профилактики, так как именно в еде содержится большое число канцерогенов (например, копчености или большинство консервантов, усилителей вкуса и многое другое, обнаруживаемое на полках в современных магазинах).
Также важно профилактировать вероятное рецидивирование и осложнения после оперативного лечения. Пациентам, перенёсшим удаление надпочечника, необходимо находиться под наблюдением врача-эндокринолога, который в зависимости от того, осталась ли симптоматика или нет, назначает медикаментозную терапию. Осмотры производятся каждые полгода.
Пациентам после удаления надпочечника необходимо:
После адреналэктомии пациентам необходимо более тщательно коррегировать терапию гипертонической болезни в том случае, если она первичная. Также это необходимо выполнять и пациентам с ишемической болезнью сердца. [15]
Образования надпочечников: тактика ведения
Частота выявления новообразований надпочечников постоянно возрастает, их распространенность составляет 1-10%. Хотя в каждом случае необходимо выявить гормональную активность и злокачественный потенциал, большая часть из них представлена гормонально неакти
Abstract. Detection of adrenal neoplasms frequency is increasing constantly, their estimated at 1 to10%. Although in each case it is necessary to identify hormonal activity and malignant potential, most of them are represented by hormone inactive and benign adenomas. Approximately a fifth of the adrenal formations after further verification are hormone-active or carcinomas that require surgical treatment. The main goal of imaging studies in adrenal incidentalomas is the timely detection of malignant tumors; to determine the characteristics of neoplasms, computed tomography, magnetic resonance imaging and, if necessary, a number of radioisotope studies are used. The size of the lesion detected on computed tomograms exceeding 4-6 cm, its uneven edge or heterogeneity of the structure, an attenuation coefficient of 10 Hounsfield units or higher with a non-contrast study, washout of the contrast agent after 10 or 15 minutes by less than 40%, calcification and invasion in the surrounding tissues suggest the malignancy of the adrenal gland lesion, the likelihood of this increases with a combination of these signs. The developed visualization methods and laboratory evaluation allow to assess their morphological structure and functionality with high confidence. The principles of monitoring the growth and hormonal activity of adrenal formations had been currently developed, but the aspects of the long-term dynamic monitoring remain poorly understood. For citation: Morgunov L. Yu. Аdrenal tumors: management tactics // Lechaschy Vrach. 2020; 12 (23): 18-23. DOI: 10.26295/OS.2020.98.90.004
Резюме. Частота выявления новообразований надпочечников постоянно возрастает, их распространенность составляет 1-10%. Хотя в каждом случае необходимо выявить гормональную активность и злокачественный потенциал, большая часть из них представлена гормонально неактивными и доброкачественными аденомами. Примерно пятая часть образований надпочечников после дальнейшей верификации представляет собой гормонально активные или карциномы, требующие оперативного лечения. Основная цель визуализирующих исследований при инциденталомах состоит в своевременном выявлении злокачественных опухолей; для определения характеристик новообразований используют компьютерную томографию, магнитно-резонансную томографию и при необходимости ряд радиоизотопных исследований. Размер выявленного на компьютерных томограммах образования, превышающий 4-6 см, его неровный край или неоднородность структуры, коэффициент ослабления 10 единиц Хаунсфилда или выше при неконтрастном исследовании, вымывание контрастного вещества через 10 или 15 минут менее чем на 40%, кальцификация и инвазия в окружающие ткани предполагают злокачественность поражения надпочечников, вероятность этого повышается при сочетании данных признаков. Разработанные методы визуализации и лабораторная оценка с большой достоверностью позволяют судить об их морфологической структуре и функциональности.
В настоящее время разработаны принципы наблюдения за ростом и гормональной активностью образований надпочечников, однако вопросы длительного динамического наблюдения за ними остаются малоизученными.
Образования надпочечников, случайно обнаруженные при визуальном исследовании, выполненном по причинам, не связанным с их патологией, носят название инциденталом (ИН). Как правило, образования менее 1 см не именуются ИН, и дополнительные диагностические тесты рекомендуются лишь для объемных процессов, превышающих данный размер, при отсутствии клинических симптомов гормональной активности. Быстрое развитие технологий визуализации в последние годы существенно повысило шансы на их обнаружение.
Распространенность ИН составляет от 1% до 8,7% [1] и увеличивается с возрастом, гендерные различия отсутствуют. Например, в стационары Италии ежегодно госпитализируются около 1 450 000 пациентов, у 58 000 из них выявляются ИН [2]. N. Unger (2019) полагает, что распространенность ИН несколько выше – около 3% и увеличивается до 10% у пожилых людей; у 15% пациентов с ИН выявляются признаки их гормональной активности [3]. Хотя данная патология встречается достаточно редко, ее клиническое и экономическое бремя представляется весомым, а вопросы длительного динамического наблюдения пока остаются без ответа.
11-20% выявляемых образований надпочечника являются гормонально активными; с самым высоким риском смертности ассоциированы феохромоцитомы, поэтому их наличие требуется исключить в первую очередь. В 80% случаев в надпочечниках выявляются гормонально неактивные и доброкачественные образования, в то время как распространенность феохромоцитомы составляет от 3,0% до 6,0% адренокортикальной карциномы – от 2,0% до 5,0%. Надпочечник – место метастазирования различных видов рака, встречающихся в 1-2% случаев [4, 5].
Если у пациента ранее выявлялись злокачественные опухоли иной локализации, вероятность того, что ИН окажется метастазом рака, составляет почти 50%. По данным J. T. Lenert с соавт. (2001), адренокортикальная карцинома встречается в 4-5% случаев, но прогноз неблагоприятен из-за частого ее выявления в далеко зашедшей стадии, а ее рецидив является достаточно распространенным явлением. В надпочечник часто метастазирует рак легких, почек, толстой кишки, молочной железы, пищевода, поджелудочной железы, печени или желудка, а сами метастазы нередко бывают двусторонними [6]. Метастатические поражения, как правило, неоднородны по структуре, имеют края неправильной формы и являются двусторонними в 10-15% случаев [7].
Национальное многоцентровое исследование, проведенное по инициативе министерства здравоохранения, труда и социального обеспечения Японии в период с 1999 по 2004 г., включало 3672 случая ИН у 1874 мужчин и 1738 женщин; средний возраст 58,1 ± 13,0 лет. Средний размер ИН составил 3,0 ± 2,0 см; диаметр образований оказался значимо большим у пациентов с верифицированными адренокортикальными карциномами, феохромоцитомами, развернутым синдромом Кушинга, миелолипомами, метастазами рака, кистами и ганглионевромами (p 10 ЕХ) (69%) выполнялась повторная визуализация. 105 врачам первичного звена, чьи пациенты включались в исследование, была разослана стандартизированная анкета, состоящая из 16 вопросов. Большинство специалистов первичного звена полагали, что подавляющей части пациентов с ИН и отсутствием клинической симптоматики не требуется гормональная оценка (71%) или последующее наблюдение (72%). Проведенное исследование демонстрирует необходимость междисциплинарного подхода к наблюдению пациентов с ИН путем взаимодействия между эндокринологами, хирургами и врачами общей практики [38].
Европейское общество эндокринологии (ESE) опубликовало рекомендации по ведению пациентов с ИН (2017), которые полагают возможным воздержаться от повторного гормонального исследования у пациентов с ИН с нормальным уровнем гормонов при первоначальной верификации образования. Рекомендации ESE также полагают нецелесообразным выполнять повторную визуализацию при размерах образования менее 4 см и явных признаках доброкачественности. Однако на сегодняшний день не существует достаточных доказательств, подтверждающих нецелесообразность динамического биохимического и морфологического наблюдения у пациентов с ИН даже при изначально выявленных доброкачественных и гормонально неактивных образованиях надпочечников, поэтому желательно оценивать структурные признаки и уровень гормонов по крайней мере в течение 5 лет [39].
Обобщая рекомендации, предложенные Американской ассоциацией клинических эндокринологов, Американской ассоциацией эндокринных хирургов, Национальным институтом здоровья США, J. M. Lee с соавт. (2017) свидетельствуют о том, что при наличии образования менее 4 см требуется КТ-визуализация через 6 месяцев, не превышающая в дальнейшем 2 лет, а также проведение гормональных тестов – ежегодно в течение 4-5 лет [40].
Клинические рекомендации Российской ассоциации эндокринологов ориентируют на нецелесообразность динамического наблюдения при низкоплотных гормонально неактивных опухолях по данным первичной КТ, в этих случаях также не показан мониторинг гормональной активности. Исключение составляют новые клинические проявления (появление или клиническое прогрессирование артериальной гипертензии, сахарного диабета, ожирения, остеопороза), о чем необходимо предупредить пациента. При неопределенном злокачественном потенциале образования требуется контроль размеров через 3-6 мес, а при увеличении максимального размера опухоли за короткий период на 5 мм или росте объема опухоли на 20% необходимо рассмотреть вопрос об оперативном лечении. При наличии ССК показан ежегодный контроль уровня кортизола и мониторинг коморбидных состояний (артериальной гипертензии, сахарного диабета, ожирения, остеопороза) [41].
Тем не менее круг заболеваний, могущих являться потенциальными предикторами появления гормональной активности ИН, настолько широк, что сводит на нет ограничения к проведению дополнительных визуализирующих и лабораторных исследований в динамике. Так, распространенность артериальной гипертензии среди населения РФ достигает 39,7% [42]. Реальная численность пациентов с СД в РФ составляет не менее 9 млн человек и во всем мире возросла более чем в 2 раза за последние 10 лет [43]. Распространенность ожирения среди россиян с возрастом линейно возрастает у мужчин с 14,3% до 36,3%, а у женщин – с 10,7% до 52,3% [44]. Остеопорозом в России страдают не менее 14 млн человек (10% населения страны), еще у 20 млн граждан России имеет место остеопения [45].
Таким образом, тактика в отношении диагностики, наблюдения и ведения пациентов с новообразованиями надпочечников у разных исследователей практически одинакова. Вопросы лечения пациентов со злокачественными и гормонально активными образованиями решены, но результаты длительного наблюдения за больными с доброкачественными ГНОН пока отсутствуют. Темой для дискуссий остается специальность врача, обеспечивающего дальнейшее наблюдение за пациентом (эндокринолог, врач общей практики, онколог, хирург). Вероятно, создание единого регистра больных с образованиями надпочечников даже в пределах крупного мегаполиса позволит определиться с периодом их наблюдения и тактикой дальнейшего ведения.
Литература/References
Л. Ю. Моргунов, доктор медицинских наук, профессор
ФГАОУ ВО РУДН, Москва, Россия
Образования надпочечников: тактика ведения/ Л. Ю. Моргунов
Для цитирования: Моргунов Л. Ю. Образования надпочечников: тактика ведения // Лечащий Врач. 2020; 12 (23): 18-23. DOI: 10.26295/OS.2020.98.90.004
Теги: новообразования, аденома, карцинома, злокачественная опухоль