Узелковый полиартериит (M30.0)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Эпидемиология
| Заболевание | Распространенность (на 1 000 000 населения) | Средний возраст начала заболевания, годы | Доля мужчин среди заболевших, % | Преобладающая географическая распространенность |
| Узелковый полиартериит | 4,6 (2-18) | 48±1,7 | 60 | Нет |
Клиническая картина
Клинические критерии диагностики
Cимптомы, течение
Диагностика
Лабораторная диагностика
Лабораторная диагностика УП.
При УП ассоциированном с HBV наблюдается повышение активности ЩФ, АСТ, АЛТ, определяется HbsAg, обнаруживают HBV ДНК.
При иммунологическом исследовании сыворотки крови выявляют повышение СРБ, иногда выявляют РФ, криоглобулинемию. АНЦА определяются крайне редко.
Гистологическое исследование при УП.
У пациентов с предполагаемым диагнозом УП желательно проведение гистологического исследования, выявляющего характерную картину фокального некротизирующего артериита с клеточным инфильтратом смешанного характера в сосудистой стенке. Наиболее информативна биопсия скелетной мышцы. При проведении биопсии внутренних органов у больных УП высок риск развития внутреннего кровотечения.
Инструментальные методы исследования при УП.
При ультразвуковой допплерографии у 60% больных выявляют изменения в артериях почек (прежде всего стеноз).
Ангиография позволяет обнаружить множественные микроаневризмы и стенозы отдельных участков артерий среднего калибра преимущественно в артериях почек, брыжейки, печени. Эти изменения могут исчезать на фоне эффективного лечения.
Осложнения
Лечение
Лечение узелкового полиартериита.
(Уровень доказательности А): Для индукции ремиссии УП без HBV инфекции рекомендуется ЦФ в сочетании с ГК.
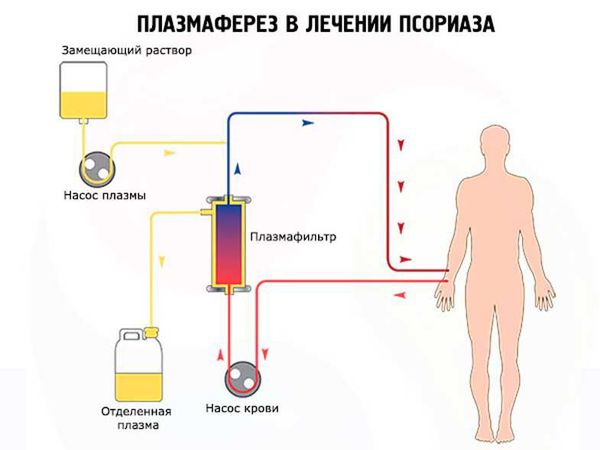
(Уровень доказательности С): При HBV- ассоциированном УП рекомендуется использовать комбинированную терапию, включающую противовирусные препараты, плазмаферез и ГК.
Лечение УП без инфекции вируса гепатита В:
При ограниченном поражении сосудов, отсутствии признаков прогрессирования и невысокой воспалительной активности назначают средние дозы ГК. При тяжелом, быстропрогрессирующем течении целесообразно раннее назначение комбинированной терапии ГК и ЦФ. Развитие почечной недостаточности, периферической гангрены, полинейропатии, поражения ЖКТ является показанием для проведения в/в пульс- терапии МП в сочетании с ЦФ. Цитостатики назначают так же в случае невозможности снижения дозы ГК вследствие частых обострений заболевания.
Быстропрогрессирующее тяжелое течение УП:
ЦФ в/в пульсовые введения 15 мг/кг (не более 1 г) через 2 недели N 1- 3, далее каждые 3 недели.
+
МП в/в 0,5- 1 г/сутки 3 дня подряд с последующим назначением ПЗ внутрь 1 мг/кг/сутки (не более 80 мг) однократно утром до достижения эффекта, как правило, не менее месяца. После достижения эффекта постепенно снижают дозу ПЗ (по 1,25 мг) на 25% в месяц до 20 мг/сутки, затем на 10% каждые 2 недели до 10 мг/сутки. Далее возможно снижение дозы ПЗ на 1,25 мг каждые 4 недели.
или:
ЦФ внутрь 4 мг/кг/сутки в 2- 3 приема, 3 суток, затем ЦФ внутрь 2 мг/кг/сутки (не более 200 мг/сутки) в 2- 3 приема 7 суток, с последующим постепенным снижением дозы на 25- 50 мг/месяц в течение 2- 3 месяцев. При повышении сывороточного креатинина (> 300 ммоль/л) или в пожилом возрасте пациента дозу ЦФ снижают на 25- 50%.
+
ПЗ внутрь 1- 2 мг/кг/сутки (не более 80 мг) однократно утром до достижения эффекта, как правило, не менее месяца, с последующим постепенным снижением дозы.
Плазмаферез 7- 10 процедур в течение 14 суток с удалением 60 мл/кг плазмы и замещением равным объёмом 4,5- 5% альбумина человека.
Нормальный иммуноглобулин человека в/в 0,4- 2 г/кг 1 раз/сутки, 3- 5 суток. Возможно проведение повторных курсов 1 раз в месяц на протяжении 6 месяцев.
Ограниченное поражение сосудов, отсутствие признаков прогрессирования УП:
ПЗ внутрь 1- 2 мг/кг/сутки в 2- 3 приема (после еды) в течение 7- 10 суток,
затем, при положительной динамике клинических и лабораторных показателей:
ПЗ внутрь 1- 2 мг/кг/сутки (не более 80 мг) однократно утром до достижения эффекта, как правило, не менее месяца, с последующим постепенным снижением дозы ПЗ. В процессе снижения дозы ПЗ внимательно наблюдают за динамикой клинических симптомов и контролируют СОЭ каждый мес. в течение первых 2- 3 месяцев, затем каждые 2- 3 мес. течение 12- 18 месяцев.
Обострение УП на фоне снижения дозы ГК:
ЦФ внутрь 1- 2 мг/кг/сутки (не более 200 мг/сутки) в течение 10- 14 суток, скорость последующего снижения дозы определяется клинической картиной и данными лабораторных анализов.
Поддерживающяя терапия :
ПЗ внутрь 5- 10 мг однократно утром + АЗА 2 мг/кг/сутки с возможным снижением дозы до 1,5 мг/кг/сутки через год с длительностью поддерживающей терапии не менее 24 месяцев.
Лечение УП, ассоциированного с вирусом гепатита В.
При обнаружении маркёров активной репликации HBV лечение включает противовирусную терапию в комбинациии со средними дозами ПЗ и повторными сеансами плазмафереза. Применение высоких доз цитостатиков, способствующих усилению репликации вируса гепатита В и потенциально обладающих гепатотоксическим действием, противопоказано при серологических признаках активной репликации HBV или нарушении функций печени.
Показаниями к лечению УП противовирусными препаратами являются:
· наличие очевидных признаков активной вирусной инфекции (у HBeAg- позитивных больных: HBV DNA > 10 5 копий /мл; при отсутствии HBeAg: HBV DNA > 10 4 копий /мл);
· креатинин сыворотки крови 1 этап комбинированной терапии (первые 2 недели) :
ПЗ 1 мг/кг/сутки (не более 80 мг) однократно утром, через неделю быстрое снижение дозы (если возможно до отмены).
или:
МП в/в 15 мг/кг/сутки (не более 1 г) в течение 3 дней с последующим назначением ПЗ внутрь 1 мг/кг/сутки (не более 80 мг) однократно утром с быстрым снижением дозы через неделю (если возможно до отмены).
2 этап комбинированной терапии:
Противовирусные препараты назначают исходя из вирусологических, иммунологических и других объективных параметров в каждом конкретном случае. Арсенал средств лечения хронической инфекции гепатита В постоянно расширяется, перспективно использование комбинированной терапии (2 или 3 противовирусных препарата, включая интерфероны). Использование монотерапии ламивудином (особенно у пациентов с избыточной массой тела и у мужчин) может способствовать появлению новых, устойчивых к ламивудину, штаммов вируса гепатита В, провоцирующих обострение УП. С применением ламивудина может быть связано развитие интерстициального нефрита. Интерферон- a назначают в средних дозах (3 млн ЕД в/м 3 раза в неделю на протяжении 6- 12 месяцев). Следует помнить, что лечение интерфероном α в ряде случаев вызывает обострение васкулита, способствует развитию ряда системных проявлений (лихорадка, диспепсия, алопеция, миалгии/миопатия, тиреоидит, депрессия, цитопения).
+
Плазмаферез повторно в течение первых 3 недель- 3 раза в неделю, затем в течение 2 недель- 2 раза в неделю, далее 1 раз в неделю.
+
Нормальный иммуноглобулин человека в/в 0,4- 2 г/кг 1 раз/сутки, 3- 5 суток. Возможно проведение повторных курсов 1 раз в месяц на протяжении 6 месяцев.
+
ПЗ (низкие дозы) при невозможности его отмены.
Лечение артериальной гипертензии при УП :
При тяжёлом течении требуется одновременное назначение нескольких препаратов: ингибиторов АПФ или блокаторов рецепторов ангиотензина ІІ, блокаторов ß- адренорецепторов, которые более эффективны в комбинации с диуретиками и/или блокаторами медленных кальциевых каналов. Стабилизация артериального давления с помощью антигипертензивных лекарств разных групп, назначаемых в различных комбинациях, позволяет затормозить прогрессирование почечной недостаточности, уменьшить риск развития сосудистых катастроф (инфаркт миокарда, инсульт), недостаточности кровообращения.
Поскольку ингибиторы АПФ или блокаторы рецепторов ангиотензина II могут ухудшать функцию стенозированной почки и способствовать развитию почечной недостаточности, лечение этими препаратами требует мониторирования функции почек и их размеров и проведение при возможности повторной ультразвуковой допплерографии для оценки скорости кровотока в кортикальном слое.
Программный гемодиализ:
Необходимости проведения программного гемодиализа не мешает активной патогенетической терапии. При успешном лечении, впоследствии может исчезнуть потребность в гемодиализе.
Хирургическое лечение:
Неотложная хирургическая помощь необходима при разрыве аневризмы сосудов внутренних органов. Показаниями для ангиопластики или хирургического лечения при стенозе почечной артерии являются:
· рефрактерность гипертензии, несмотря на адекватно выбранный режим лечения;
· невозможность лекарственного лечения из- за опасности побочных эффектов;
· стремление сохранить функцию почки.
Что такое полиартрит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Бабинцевой Марины Юрьевны, эндокринолога со стажем в 27 лет.
Определение болезни. Причины заболевания
Полиартрит (Polyarthritis) — это воспаление нескольких суставов. В отличие от олигоартрита, при котором поражается 2–4 сустава, диагноз полиартрита ставится при воспалении четырёх и более суставов. Они могут воспаляться одновременно или последовательно.
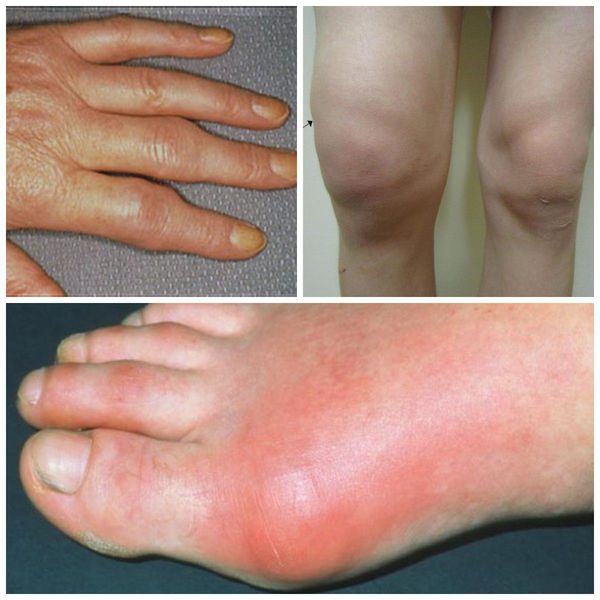
Основными симптомами полиартрита является боль, припухлость и ограничение движений в нескольких суставах. Сначала движения ограничиваются из-за боли. Если болезнь прогрессирует, то суставы постепенно деформируются, возможны их разнонаправленные подвывихи, остеолиз суставной поверхности (рассасывание костной ткани) и костные анкилозы (неподвижность суставов из-за сращения костей).
Хронический артрит вызывает атрофию (уменьшение размеров) мышц в области воспалённого сустава, из-за этого снижается мышечная сила.
Причины полиартрита
Полиартрит — не самостоятельное заболевание. Иногда это проявление болезней суставов, таких как ревматоидный или псориатический артрит. В других случаях полиартрит является одним из симптомов других заболеваний, как ревматических, так и не ревматических [1]
Можно выделить следующие причины полиартрита:
Распространённость
Симптомы полиартрита
Для всех полиартритов характерна триада симптомов: боль, отёчность и ограничение движений в четырёх и более суставах. При длительном течении полиартрита атрофируются мышцы, из-за чего снижается их сила.
В патологический процесс суставы могут вовлекаться постепенно, или воспаление возникает в нескольких суставах одновременно.
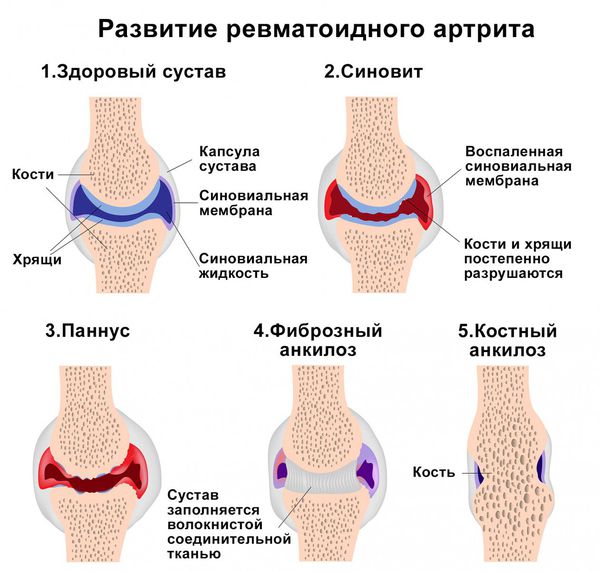
Второй важный признак полиартрита — припухлость суставов. Отёчность связана с воспалительными изменениями синовиальной оболочки и скоплением воспалительной жидкости в полости сустава. Синовиальная оболочка — это внутренняя поверхность суставной полости, которая вырабатывает синовиальную жидкость. При хроническом полиартрите она разрастается и грубая рубцовая ткань проникает в мягкие ткани, окружающие суставы. Из-за этого меняется форма сустава. При дальнейшем прогрессировании артрита суставы деформируются из-за разрушения суставной поверхности костей, костных разрастаний, подвывихов и костных анкилозов (сращений).
Ещё одним симптомом, сопровождающим полиартрит, является ограничение движения в суставах. Этот симптом встречается почти при всех вариантах полиартрита. Исключение составляют некоторые нейропатические артропатии (например, сифилитическая), при которых суставы сохраняют свою подвижность, несмотря на выраженные костные поражения. Это связано с тем, что пациенты с сифилисом не чувствуют боль из-за повреждения болевых рецепторов.
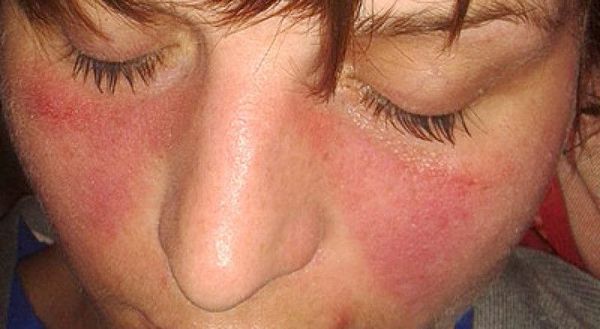
Для ряда заболеваний с полиартритом характерны кожные проявления: симптом «бабочки» при системной красной волчанке, псориатические бляшки и др. Кроме того, полиартриты могут сопровождаться общесоматическими проявлениями: лихорадкой, общей слабостью, симптомами интоксикации (снижением аппетита, лёгкой тошнотой, учащением сердцебиения и дыхания, апатией и др.).
Патогенез полиартрита
В развитии воспаления суставов при полиартрите основную роль играют иммунные механизмы.
Накопление провоспалительных ферментов и продуктов распада фагоцитов приводит к разрушению хрящевой и костной ткани. Из-за этого суставы деформируются и появляется костный анкилоз (сращение).
Классификация и стадии развития полиартрита
Полиартрит — это одна из разновидностей большой группы воспалительных заболеваний суставов — артритов. В эту группу также входит моноартрит (поражение одного сустава) и олигоартрит (поражение 2–4 суставов).
Классификация полиартритов по течению:
Классификация полиартритов по причине развития:
Классификация полиартритов, принятая на первом Всесоюзном съезде ревматологов в 1971 году:
К самостоятельным нозологическим формам полиартритов относятся:
К полиартритам при других заболеваниях относят:
В особую группу выделяют травматические полиартриты в связи с особенностями их возникновения, течения и лечения. Такие полиартриты возникают после травмы. Для их лечения необходимо устранить травматические повреждения, например вправить вывих, ушить связки и т. д., а также исключить травмирующий агент при хронической травме. Если не восстановить целостность сустава после травмы, лечение полиартрита не будет эффетивным.
Осложнения полиартрита
Внутрисуставные осложнения
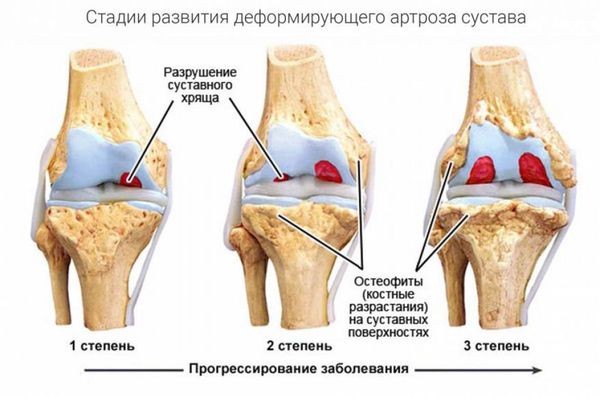
Разрушение суставов — одно из частых осложнений полиартритов. Оно более характерно для таких заболеваний, как ревматоидный и псориатический полиартрит, но в той или иной степени встречается при любом типе артрита. Разрушается суставной хрящ с развитием остеоартроза. При остеоартрозе суставной хрящ постепенно разрушается и истончается, суставная щель сужается, а по краям суставов появляются патологические наросты.
В кости под суставным хрящом могут наблюдаться кистовидные изменения, остеопороз, единичные или множественные эрозии суставных поверхностей, остеонекроз и разрушение эпифизов (концевых отделов) костей. Это приводит к суставным осложнениям полиартритов — подвывихам и вывихам суставов, разнонаправленным костным деформациям, костным сращениям. В результате функциональная способность суставов резко снижается: на 60–90 % уменьшается амплитуда движения в суставах (т. е. их невозможно согнуть или разогнуть), в кистях рук снижается мышечная сила, нарушается их хватательная функция, страдает опорная функция стопы.
Внесуставные проявления
Полиартрит из-за тяжёлого дезадаптирующего характера является значимым психотравмирующим фактором и провоцирует развитие различных психических расстройств, преимущественно депрессивных. Причиной становится длительный хронический стресс. Нарушенный в результате хронического стресса механизм обратной связи между надпочечниками и гипоталамо-гипофизарной системы приводит к хронизации воспаления, возникновению хронической боли, усталости, тревожных и депрессивных расстройств.
Диагностика полиартрита
При подозрении на полиартрит необходимо обратиться к ревматологу или терапевту. Диагностика полиартрита основывается на клинической картине заболевания, данных анамнеза, лабораторных и инструментальных исследованиях.
Жалобы и осмотр
Пациент жалуется на боль, припухлость и ограничение движения в четырёх и более суставах.
Лабораторная диагностика
Методы лабораторной диагностики широко используются как для дифференциального диагноза полиартрита (чтобы отличить его от других болезней), так и для определения степени его активности.
Анализ крови чаще всего используется в клинической практике для диагностики артритов. Существуют специфические маркеры аутоиммунного поражения суставов:
При инфекционных и инфекционно-аллергических полиартритах в анализах крови иногда выявляются антитела к возбудителям инфекции. Для выявления антител выполняется специальный иммунологический анализ крови.
Для определения активности процесса используют показатели скорости оседания эритроцитов (СОЭ) и С-реактивного белка (СРБ). Лейкоцитарная формула необходима как диагностический критерий: лейкопения и тромбоцитопения (снижение количества лейкоцитов и тромбоцитов) наблюдаются при системной красной волчанке, тромбоцитоз и небольшой лейкоцитоз (увеличение количества тромбоцитов и лейкоцитов) — при ревматоидном артрите.
Инструментальная диагностика
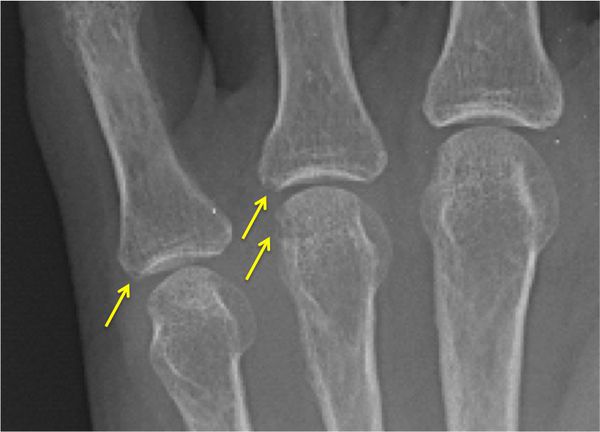
При использовании методов визуализации, таких как ультразвуковое исследование суставов (УЗИ), рентген, компьютерная или магнитно-резонансная томография (КТ или МРТ), могут быть видны признаки дегенерации и разрушения хряща, остеопороза, эрозий суставных поверхностей костей, костных разрастаний, синовитов (воспаления синовиальной оболочки) и поражения сухожильно-связочного аппарата. Для некоторых заболеваний характерна типичная рентгенологическая картина, например изменения по типу «карандаш в стакане» при мутилирующем псориатическом артрите.
Дифференциальная диагностика
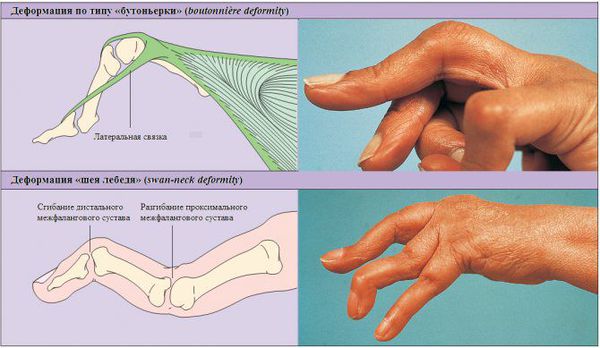
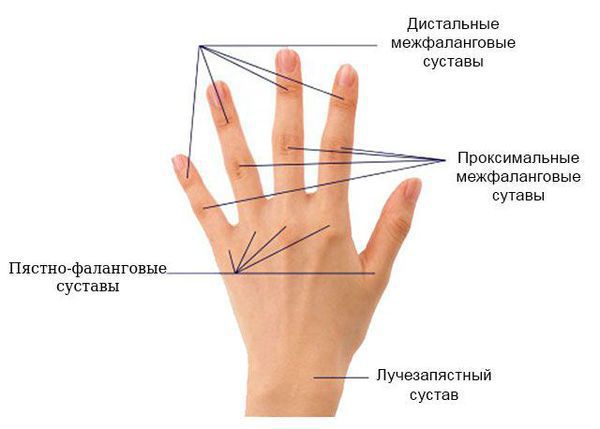
Для дифференциальной диагностики полиартрита важное значение имеет локализация патологического процесса, особенно вначале заболевания. Например, ревматоидный артрит чаще всего начинается с проксимальных межфаланговых и пястно-фаланговых суставов указательного и среднего пальцев кисти и характеризуется их симметричным поражением. Исключение — суставы мизинца: они никогда не поражаются при ревматоидном артрите. При дистальной форме псориатического артрита обычно сначала поражаются дистальные (т. е. самые удалённые) межфаланговые суставы кистей и стоп.
Лечение полиартрита
Большинство полиартритов (ревматоидный, псориатический, полиартриты при системных заболеваниях соединительной ткани и др.) требует многолетней или пожизненной терапии. Лечение полиартритов можно условно разделить на «симптом-модифицирующее» и «болезнь-модифицирующее».
Симптом-модифицирующее лечение
Направлено на уменьшение симптомов (боли и скованности суставов) и улучшение качества жизни пациентов. Оно включает в себя:
2. Глюкокортикоиды (ГК), например Метипред, Преднизолон. Эти сильные противовоспалительные препараты применяются в качестве терапии первого ряда при активных формах системной красной волчанки, ревматоидном артрите с системными проявлениями, системных васкулитах и др. При реактивных артритах назначаются в случае неэффективности НПВП.
Болезнь-модифицирующее лечение
Влияет на механизмы развития болезней, а в ряде случаев (при инфекционных или реактивных полиартритах) — и на причину заболевания.
1. Цитостатики (иммуносупрессоры) являются базисными препаратами при ревматоидном и псориатическом полиартритах. К ним относятся Метотрексат, Азатиоприн, Циклоспорин, Арава (Лефлуномид) и др. Эти препараты избирательно снижают активность некоторых иммунных клеток. Также цитостатики подавляют рост клеток синовиальной оболочки и фибробластов. В результате улучшаются лабораторные показатели, уменьшаются симптомы и задерживается развитие эрозий.
Однако у цитостатиков много побочных эффектов. Очень часто возникает тошнота и рвота, иногда развивается стоматит. Цитостатики могут влиять на кроветворение и приводить к развитию анемии, снижению уровня тромбоцитов и лейкоцитов. Иногда они нарушают работу печени: возможно повышение уровня печёночных трансаминаз (АЛТ и АСТ) более чем в три раза. Это может привести к развитию нефропатии и почечной недостаточности.
Препаратом выбора является Метотрексат из-за менее выраженных побочных действий. Клинически значимый эффект от применения цитостатиков развивается относительно медленно (1 – 3 месяца), поэтому в начале лечения возможно их применение в сочетании с НПВП или глюкортикоидами. Т. е. ГК назначают на 1 – 2 месяца, пока не начнут «работать» болезнь-модифицирующие препараты: Метотрексат, Арава и др.
Методы физического модулирования
Физиотерапевтическое лечение
Физиотерапевтические процедуры могут применяться для уменьшения боли и воспаления. Может использоваться электро- или фонофорез с лекарственными препаратами, воздействие токами различной частоты, магнитами и магнитолазером.
Прогноз. Профилактика
Профилактика полиартритов
Для полиартритов с иммунным механизмом развития (ревматоидного, псориатического и др.) мер первичной профилактики не существует, так как неизвестны их точные причины.
Первичная профилактика возможна для инфекционных и инфекционно-аллергических артритов. Чтобы не допустить их развития, рекомендуется:
Пациентам с избыточным весом, особенно в сочетании с артериальной гипертонией и нарушением углеводного обмена, необходимо проводить первичную профилактику подагрического артрита. Она заключается в нормализации обмена мочевой кислоты за счёт снижения массы тела и низкопуриновой диеты. При необходимости применяются лекарственные средства, которые уменьшают образование мочевой кислоты или увеличивают её выведение с мочой.
Узелковый периартериит
Узелковый периартериит — ведущее к прогрессирующей органной недостаточности воспалительное поражение артериальной стенки сосудов мелкого и среднего калибра с образованием микроаневризм.
Эпидемиология
Из-за редкости заболевания его эпидемиология изучена слабо. Ежегодно регистрируется 0,2-1 случай на 100 000 населения. Средний возраст начала заболевания 48 лет. Мужчины заболевают в 3-5 раз чаще, чем женщины.
Этиология
Однозначной причины заболевания нет. В настоящее время выявлено два основных фактора:
Насчитывается уже около сотни медицинских препаратов, которые удалось связать с возникновением узелкового периартериита.
У 30-40% больных в крови был обнаружен поверхностный антиген гепатита B (HBsAg) или иммунные комплексы включающие его, а также другие антигены гепатита B (HBeAg) и антитела к антигену HBcAg, образующиеся при репликации вируса. Известно, что во Франции частота HBV-ассоциированного узелкового полиартериита снизилась с 36% в начале 1980-х годов до менее 5% в 2000-х годах, что обусловлено массовой вакцинацией против гепатита B.
Также у 5-12% больных обнаруживается вирус гепатита C, однако его роль возникновении заболевания пока не доказана. Рассматриваются и другие вирусы: ВИЧ, цитомегаловирус, вирус Эпштейна-Барр, краснухи, парвовирус В 19, человеческий Т-лимфотропный вирус 1 типа, но их роль пока не доказана.
Также опубликованы отдельные наблюдения о возникновении симптомов узелкового полиартериита после введения вакцины против гепатита B, гриппа.
Ещё один предполагаемый этиологический фактор — наследственная предрасположенность, но установить связь с определённым HLA-антигеном пока не удалось.
Патогенез
Патогенез заключается в гипераллергической реакции организма в ответ на этиологические факторы, аутоиммунной реакции антиген-антитело (в том числе к сосудистой стенке), формировании иммунных комплексов.
Так как клетки эндотелия имеют рецепторы для Fc-фрагмента IgG и первой фракции комплемента Clq, это облегчает взаимодействие иммунных комплексов с сосудистой стенкой. Иммунные комплексы откладываются в сосудистой стенке, что приводит к развитию в ней иммунного воспаления.
Сформировавшиеся иммунные комплексы активируют комплемент, из-за чего происходит повреждение сосудов, а также образование хемотаксических веществ, которые привлекают в очаг поражения нейтрофилы. Они фагоцитируют иммунные комплексы, однако при этом происходит выделение лизосомальных протеолитических ферментов, повреждающих структуры сосудистой стенки. Также нейтрофилы способны прилипать к эндотелию и выделять в присутствии комплемента активированные кислородные радикалы, усугубляющие повреждения сосудов.
Также усиливается выделение эндотелием факторов, способствующих свёртыванию крови и тромбообразованию в воспалённом сосуде.
Клиническая картина
Заболевание обычно начинается с общих синдромов: постоянная лихорадка, прогрессирующее похудение, мышечно-суставные боли.
Лихорадка встречается у 95-100% больных, обычно неправильного типа, не реагирующая на антибиотики, но исчезающая при кортикостероидах. Как правило исчезает в дальнейшем, при появлении органной патологии.
Похудение при узелковом периартериите патогномично. В некоторых случаях масса тела уменьшается на 30-40 кг за несколько месяцев, а степень кахексии выше, чем при онкологических заболеваниях.
Миалгии и, реже, артралгии встречаются в начале заболевания. Проявляются характерными болями в икроножных мышцах и крупных суставах.
При развитии узелкового периартериита наиболее часто встречаются органные патологии пяти типов. Они и определяют специфическую клиническую картину болезни.
В моче наблюдается протеинурия (1—3 г в сутки), микрогематурия, изредка макрогематурия.
У некоторых больных происходит разрыв аневризматически расширенного сосуда с образованием околопочечной гематомы.
Поражение почек при хроническом узелковом периартериите обычно приводит к развитию почечной недостаточности в течение 1-3 лет.
Также характерны диспептические явления: обычно диарея с частотой стула до 6-10 раз в сутки с примесью крови. Встречаются анорексия, тошнота, рвота.
Вследствие перфорации язвы или гангрены кишечника нередко развивается перитонит. Возможны желудочно-кишечные кровотечения.
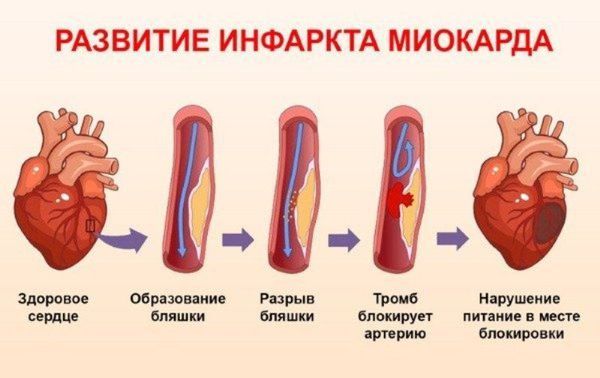
Развиваются инфаркты миокарда, в основном мелкоочаговые. Быстро прогрессирует кардиосклероз, что приводит к нарушениям ритма, проводимости, сердечной недостаточности.
Проявляется бронхоспазмами, гиперэозинофилией, эозинофильными лёгочными инфильтратами.
Типично развитие сосудистой пневмонии, характеризующейся кашлем со скудным количеством мокроты, изредка кровохарканием, нарастающими признаками дыхательной недостаточности.
Рентгенографическое исследование показывает резкое усиление сосудистого рисунка, напоминающее застойное лёгкое, инфильтрацию лёгочной ткани, преимущественно в прикорневых зонах.
Проявляется развитием асимметричного моно- или полиневрита. Наблюдаются резкие боли, парестезии, иногда парезы. В основном поражаются нижние конечности. Иногда развивается картина полимиелорадикулоневрита с парезом кистей и стоп.
У некоторых больных (15-30 %) можно выявить узелковые образования (и давшие название болезни) по ходу сосудистых стволов. Иногда встречаются язвенно-некротические изменения кожи.
Иногда поражение периферических сосудов при узелковом периартериите может привести к некрозу мягких тканей и развитию гангрены.
Диагностика
Диагноз устанавливается на основании анамнеза (лекарственная аллергия, персистирование вируса гепатита B), типичной полисиндромной клинической картины заболевания, результатов лабораторных исследований.
Однако лабораторные исследования при узелковом периартериите неспецифичны. Их диагностическая ценность невелика, показатели отражают главным образом степень активности процесса.
Различаются следующие диагностические критерии узелкового периартериита:
Наличие 3 и более любых критериев позволяет поставить диагноз узелкового периартериита.
Лечение
Основой лечения являются глюкокортикоиды, которые наиболее эффективны при ранних стадиях заболевания. При длительном применении преднизолона наблюдается стабилизация гипертензии, прогрессирование ретинопатии и почечной недостаточности. При остром течении возможно парадоксальное действие кортикостероидов с развитием множественных инфарктов. Также кортикостероиды могут резко ухудшить течение синдромов злокачественной гипертензии. Для снижения осложнений рекомендуется также применять цитотоксические препараты — циклофосфан и азатиоприн.
Прогноз
При отсутствии лечения прогноз крайне неблагоприятен. Болезнь протекает молниеносно, или с периодическими обострениями на фоне неуклонного прогрессирования. Причиной смерти становятся почечная недостаточность, поражения ЖКТ (особенно инфаркт кишечника с перфорацией), сердечно-сосудистые патологии. Часто поражение почек, сердца и ЦНС усугубляется за счёт упорной артериальной гипертонии, с которой связаны поздние осложнения.
Пятилетняя выживаемость без лечения не превышает 13%, при лечении кортикостероидами достигает 40%. Трудовой прогноз сомнителен из-за стойкости осложнений болезни — периферических и центральных параличей, тяжёлой гипертонии, поражения сердца и других.