ЭКГ: описание, норма и признаки патологий
Принцип ЭКГ
Работа аппарата ЭКГ заключается в том, что датчики, размещенные на теле пациента фиксируют вектор и силу электрического заряда, который создает сердце в процессе работы. Изменения вектора электрического заряда записывается на бумажной ленте в виде графика. Анализ этого графика позволяют сделать вывод о правильности работы сердца и возможных заболеваниях.
Регистрация электрокардиограммы осуществляется в:
Регистрация ЭКГ в 3 стандартных отведениях
Регистрация электрокардиограммы в 3 стандартных отведениях называется одноканальной ЭКГ. Она позволяет получить общую картину состояния сердца и используется при кардиологическом обследовании пациента при отсутствии специфических жалоб.
Определяется разность потенциалов между:
Эти отведения образуют равносторонний треугольник Эйнтховена, вершины которого расположены на электродах, размещенных на конечностях. В середине треугольника находится электрический центр сердца. Электрод на правой не используется для отведений, а предназначен для заземления.
Регистрация ЭКГ в 12 отведениях
Регистрация электрокардиограммы в 12 отведениях используется при специфических жалобах пациентов для получения дополнительной информации о работе сердечно-сосудистой системы, небольших изменениях, выявления очага ишемии или некроза, причин нарушения проводимости и ритма.
Помимо 3 стандартных отведений определяется разность потенциалов между:
Кроме этого используются шесть однополюсных грудных отведений, когда 6 электродов устанавливаются непосредственно на грудную клетку:
Регистрация данных с однополюсных грудных отведений позволяет судить о положении сердца в грудной клетке, величине желудочков, определить гипертрофию правых отделов, оценить состояние предсердий и выявить различные патологии.
Регистрация ЭКГ в 12 отведениях позволяет определить даже небольшие изменения в работе сердца, которые не покажет регистрация ЭКГ в 3 стандартных отведениях.
Что показывает ЭКГ
При наличии патологий электрокардиография может выявить:
Нормальная ЭКГ
На нормальной электрокардиограмме последовательно отображаются:
Норма интервалов составляет:
Частота сердечных сокращений рассчитывается как:
Нормой считается 50-90 ударов в минуту.
Например, если расстояние R составило 20 мм, а кардиограмма снята при скорости 25 мм/c:
ЧСС = 60/(20*0,04) = 75 ударов в минуту (в норме).
Сердечный ритм оценивается по степени ритмичности кардиограммы. В норме она должны быть повторяющейся с возможными отклонениями до 10%. Для оценки отклонений сравниваются расстояние между зубцами R-R.
При этом сердечный ритм в норме имеет синусовую природу, на что указывает зубец P, который положителен в 1 и 2 отведении и отрицателен в отведении aVR.
В основном такие показатель говорят о том, что сердце здорово. Но стоит помнить, что расшифровку ЭКГ должен делать врач, только он может поставить правильный диагноз, поэтому не стоит расшифровывать электрокардиограмму самостоятельно.
Патологии в ЭКГ
Электрокардиограмма отличная от нормальной может указывать на различные заболевания и нарушения в работе сердца.
Среди заболеваний могут быть:
Аритмия
Аритмия характеризуется тем, что среди нормальных сокращений сердца есть и сокращения с отклонениями от нормы, сердце бьется реже или чаще, чем нужно, размер зубцов кардиограммы не одинаковый в каждом сердцебиении.
Такие особенности ЭКГ могут говорить об аритмии.
Аритмия может быть опасна и приводить к тромбоэмболии, сердечной недостаточности и даже остановке сердца при отсутствии своевременного лечения и помощи.
Гипертрофия предсердий
При гипертрофии левого предсердия на ЭКГ зубец P в 1 и 2 отведении является двугорбым, а в V1 отрицательным и продолжительными.
Гипертрофия миокарда предсердий — это увеличение толщины миокардиальной стенки сердца, в условиях хронической перегрузки работы сердца объемом и давлением. Гипертрофия может привести к аритмии сердца.
Блокада
При блокаде ножек пучка Гиса на ЭКГ наблюдается уширением интервала QRS, а при полной блокаде сегмент ST и зубец Т становятся отрицательными.
Ишемическая болезнь
При ишемической болезни сердца на ЭКГ сегмент ST слегка опущен, а зубец T имеет неглубокое отрицательное значение.
Ишемическая болезнь представляет собой стеноз коронарных артерий в результате атеросклероза. В результате закупорки артерии может развиться инфаркт миокарда.
Перикардит
При своевременной диагностике и лечении пациент полностью выздоравливает.
Миокардит
При миокардите на ЭКГ чаще наблюдается депрессия сегмента ST и отрицательный зубец Т. Но не всегда, бывают и другие особенности ЭКГ, которые указывают на миокардит, такие как изменение продолжительности интервала PQ, признаки, указывающие на блокады левой или правой ножки ПГ и нарушение ритма сердца.
При обнаружении миокардита положена госпитализация и лечение.
Тромбоэмболия
Тромбоэмболия представляет собой закупорку сосуда тромбом и нарушение кровотока.
При обнаружении тромбоэмболии необходима срочная госпитализация и лечение.
Гипокалиемия
Лечение направлено на восполнения уровня калия в организме.
Тахикардия
Тахикардия характеризуется увеличением частоты сердечных сокращений выше 90 ударов в минуту в покое. При тахикардии на ЭКГ может наблюдаться увеличенный сегмент QRS.
Тахикардия это симптом, который указывает на наличие ряда заболеваний чаще эндокринной и нервной систем.
При выявлении тахикардии требуется дальнейшая диагностика для выявления причины и ее устранения.
Инфаркт миокарда
При инфаркте миокарда на ЭКГ в одном случае может наблюдаться как отсутствие подъема сегмента ST и зубца Q, так и подъем и деформация сегмента ST, большой зубец Q и остроконечный отрицательный зубец T.
Инфаркт миокарда возникает из-за тромбоза коронарной артерии, в результате чего возникает закупорка артерии, частичное или полное прекращение кровоснабжения и начало процесса отмирания тканей.
Как проходит диагностика ЭКГ
Процедура электрокардиографии происходит безболезненно и быстро:
При суточном холтеровском мониторировании врач размещает датчики на теле пациента, которые подключены к небольшому портативному устройству, собирающими данные электрокардиографии непрерывно в течение суток. Датчики и устройство ЭКГ прячутся под одежду и пациент носит их 24 часа. Затем возвращается к врачу, снимает устройство и датчики. Доктор анализирует ЭКГ, делает выводы и ставит диагноз пациенту.
Методы ЭКГ
Расшифровка ЭКГ
Расшифровкой электрокардиограммы занимается врач, только он может выявить заболевания, поставить правильный диагноз и дать дальнейшие направления. Человеку без медицинского образования заниматься расшифровкой ЭКГ не следует.
При расшифровке электрокардиограммы диагност обращает внимание на продолжительность, амплитуду, форму, частоту, повторяемость и прочие параметры следующих элементов кардиограммы:
Когда нужно делать ЭКГ
Электрокардиографию следует делать в следующих случаях:
Стоимость ЭКГ в нашей клинике
Мы оказываем следующие услуги в области кардиологии и ЭКГ диагностики:
Записаться на ЭКГ к врачу можно через онлайн форму на сайте или по телефонам 8 (800) 350-94-58 и +7 (4872) 49-57-57.
Увеличенная ptfv1 экг что это
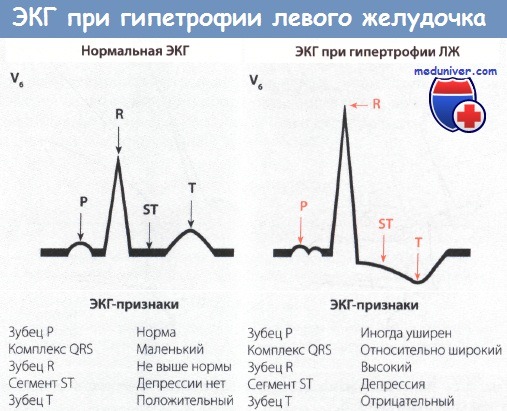
• Как правило, регистрируется ЭКГ левого типа, на которой зубец R в I отведении высокий, а зубец S в III отведении глубокий. Наряду с этими изменениями, которые обычно появляются на ЭКГ левого типа, отмечаются также депрессия сегмента ST и отрицательный зубец Т в I отведении.
• Важные изменения отмечаются в грудных отведениях V5 и V6. В этих отведениях регистрируется высокий зубец R, сегмент ST иногда бывает снижен, зубец Т отрицательный. Это важные признаки гипертрофии ЛЖ.
• В отведениях V1 и V2, наоборот, регистрируется глубокий зубец S.
• Признаки гипертрофии ЛЖ наблюдаются часто при митральной недостаточности, пороках аортального клапана и при артериальной гипертензии (АГ).
В силу физиологических особенностей, толщина миокарда левого желудочка (ЛЖ) в норме больше, чем ПЖ. При гипертрофии ЛЖ главный вектор ЭДС направлен влево и назад и в зависимости от степени гипертрофии более или менее выражен, а иногда бывает обращен вниз. Главный вектор ЭДС увеличивается из-за увеличения мышечной массы желудочка.
Для диагностики гипертрофии левого желудочка (ЛЖ) необходимо сначала просмотреть ЭКГ, зарегистрированную в отведениях от конечностей, и определить ее тип. Затем следует искать отклонения от нормальной формы кривой. Далее рассматривают ЭКГ, снятую в грудных отведениях, и ищут, как в случае анализа ЭКГ в отведениях от конечностей, изменения, указывающие на гипертрофию ЛЖ.
ЭКГ в отведениях от конечностей (во фронтальной плоскости) относится к левому типу, так как главный вектор ЭДС направлен влево. Поэтому в 1 отведении зубец R высокий, а в III отведении глубокий зубец S. Далее обращают внимание на то, что при нормальном левом типе ЭКГ зубец Т в I отведении положительный, в то время как при гипертрофии ЛЖ, наоборот, он отрицательный. Кроме того, отмечается также депрессия сегмента ST.
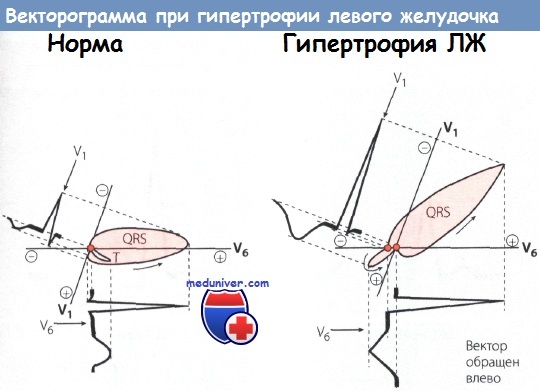
Слева: Нормальная маленькая векторная петля комплекса QRS, направленная влево. Нормальные зубцы R и Т в отведениях V1 и V6.
Справа: Большая векторная петля комплекса QRS направлена влево и назад. Т-петля обращена в противоположную сторону по отношению к петле комплекса QRS и дискордантна ей.
Высокий зубец R и отрицательный зубец Т с депрессией сегмента ST в отведении V6. Глубокий зубец S в отведении V1.
Если в I отведении имеются высокий зубец R, депрессия сегмента ST и отрицательный зубец Т, то можно вполне обоснованно заподозрить гипертрофию левого желудочка (ЛЖ).
При анализе ЭКГ, снятой в отведениях Гольдбергера, нередко в отведении aVL выявляют изменения, аналогичные описанным выше, так как это отведение направлено к левому желудочку (ЛЖ) и отражает его потенциал. Это значит, что в отведении aVL регистрируются высокий зубец R, депрессия сегмента ST и отрицательный зубец Т.
В грудных отведениях отмечается увеличение потенциала в V5 и V6, где регистрируется высокий зубец R, обусловленный увеличением мышечной массы ЛЖ. Вследствие гипертрофии миокарда время распространения возбуждения по желудочкам (ширина комплекса QRS) увеличено и ВВО несколько удлинено (>0,052 с), однако обычно блокады ЛНПГ нет. Чем больше гипертрофия ЛЖ, тем выше зубец R в отведении V5 и V6, т.е. высота зубца R составляет более 2,6 мВ или 26 мм. При тяжелой гипертрофии ЛЖ нарушено также восстановление возбудимости миокарда (реполяризация). Поэтому в отведениях V5 и V6 отмечаются также депрессия сегмента ST и отрицательный зубец Т, особенно при перегрузке давлением (например, при аортальном стенозе).
Поскольку главный вектор сильно отклонен влево, он направлен от ПЖ (т.е. от отведения V1). Поэтому в отведениях V1 и V2 регистрируется отрицательный, т.е. глубокий зубец S.
Если сумма амплитуды зубца R в отведениях V5 или V6 и зубца S в отведениях V1 и V2 превышает 35 мм, то говорят о положительном индексе Соколова-Лайона. Этот показатель позволяет судить, имеется ли у пациента гипертрофия ЛЖ. Однако следует помнить, что у спортсменов, а также иногда и у лиц с практически здоровым сердцем индекс Соколова-Лайона оказывается ложноположительным.
При выраженной гипертрофии левого желудочка (ЛЖ) может произойти вторичное увеличение ЛП. Поэтому у больных с тяжелой гипертрофией левого желудочка (ЛЖ) на ЭКГ может регистрироваться также левопредсердный зубец Р.
Признаки гипертрофии левого желудочка (ЛЖ) обнаруживаются при пороках сердца, в частности митральной и аортальной недостаточности или при АГ и дилатационной кардиомиопатии.
ЭКГ признаки гипетрофии левого желудочка
а) Отведения от конечностей:
• Левый тип ЭКГ
• RI + S III >2,5 мВ,
RI > RII > RIII и
TI 1,1 мВ
• Левопредсердный зубец Р
б) Грудные отведения:
• V1: глубокий S (S >2,4мВ)
• V5 или V6: высокий R (R >2,6мВ)
• SV1 + RV6 или RV6 >3,5 мВ (индекс Соколова-Лайона)
• V5,V6:BBO>0,052c
• BBOV6-V1>0,032c
• RV8, второй МРП>1 мВ
• TV1 >TV6 + RV6>1,7mB
• Нарушение реполяризации в левых отведениях
• Левопредсердный зубец Р
Гипертрофия левого желудочка:
• Левый тип ЭКГ
• Высокий зубец R в V5/V6 (>2,6 мВ)
• Глубокий S в V1 (>2,4 мВ)
• R в V5/V6 + SbV1>3,5mB
• Заболевания: митральная недостаточность, пороки аортального клапана, АГ
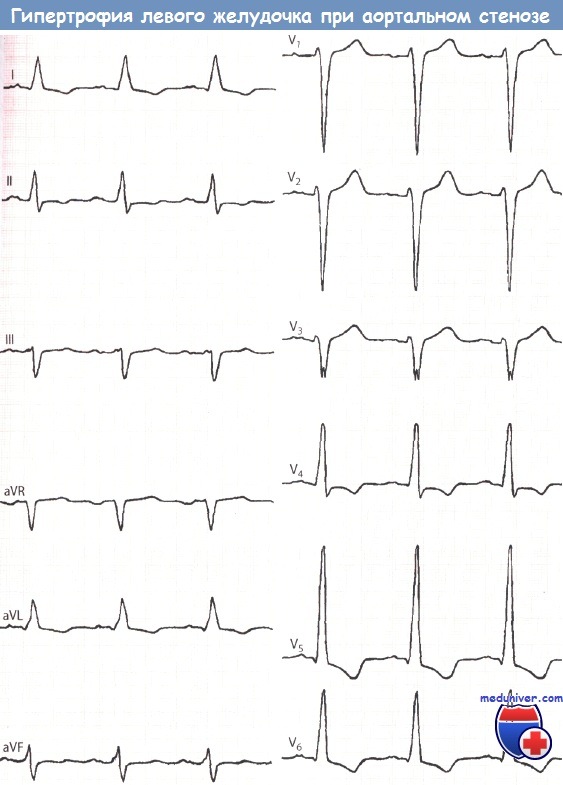
Левый тип. Глубокий зубец S (36 мм, т.е. 3,6 мВ) в отведении V1 и высокий зубец R (42 мм, т.е. 4,2 мВ) в отведении V5, а также депрессия сегмента ST и отрицательный зубец Т в отведениях V5 и V6 указывают на гипертрофию ЛЖ.
Индекс Соколова-Лайона значительно повышен и составил 78 мм (в норме до 35 мм).
Учебное видео оценки ЭКГ при гипертрофии желудочков
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Какие признаки увеличенного сердца и чем это опасно
Кардиомегалия — это состояние, при котором по той или иной причине сердце увеличивается в размерах. Большое сердце может быть вариантом нормы. К примеру, у спортсменов, занятых физическим трудом или беременных сердце перекачивает большие объемы крови. После родов, ухода из большого спорта, смены трудовой деятельности размеры постепенно возвращаются к нормальным показателям. Если этого не происходит, пациенту потребуется консультация кардиолога и, возможно, лечение. Проблема может быть врожденной (чаще обнаруживается у детей) и приобретенной — от такого состояния страдают взрослые.
Почему увеличено сердце?
Увеличение размеров сердца отмечается как на фоне сердечно-сосудистых заболеваний, так и из-за болезней, никак не связанных с кровеносной системой. Причины и последствия увеличенного сердца у взрослого:
Причины увеличения сердца могут быть различны, но такое состояние рано или поздно приводит к сердечной недостаточности, которая достаточно опасна. От сердечно-сосудистых заболеваний гибнет больше людей, чем от других болезней, например, онкологии. Проблемы с кровообращением могут привести к сердечному приступу и инсульту, инвалидизации человека. Еще одна угроза — разрастание соединительной ткани, что ведет к снижению эластичности стенок и атрофии мышцы. В группе риска люди преклонного возраста, но это не означает, что молодежи не нужно проходить периодическое обследование.
Признаки увеличенного сердца
На первых порах кардиомегалия протекает без выраженных клинических проявлений. Человек может долгое время вообще не знать о проблеме, а патологию часто обнаруживают случайно, например, на рентгене или флюорографии. Обследуйтесь, если вы входите в группу риска — опасность гипертрофии сердца в том, что она может долгие годы не давать о себе знать и обнаруживается, когда мышца уже достаточно повреждена.
О заболевании сердечной мышцы могут свидетельствовать следующие симптомы:
Синдром «бычьего сердца» хорошо диагностируется кардиологами, но на выяснение причин, вызвавших патологию, может уйти время. Могут понадобиться обследования других органов — щитовидной железы, почек, печени, легких, иммунной системы.
Диагностика, профилактика, лечение
Хотя осложнения кардиологических патологий весьма опасны, в действительности большинство ССЗ можно предотвратить с помощью профилактики. Даже если человек уже заболел, тяжелых последствий можно избежать. Благодаря современному лечению можно затормозить болезнь на ранней стадии и не допустить необратимых последствий.
Физиологическая гипертрофия — это временное состояние: чаще всего спортсменам или людям физического труда требуется обычное наблюдение. Патологически гипертрофированное сердце нуждается в лечении, которое подбирается в зависимости от причин кардиомегалии. Если проблема в сердечных клапанах, проводят операцию и протезирование. АГ, болезни почек и органов дыхания лечат медикаментами. При риске образования тромбов назначают антитромботические препараты. Таким образом, какой-то единой терапии не существует, ведь причины патологии могут быть совершенно разными.
Заниматься самолечением при кардиомегалии бессмысленно, а порой и вредно. Без специальных обследований установить причину патологии невозможно: человек может думать, что осложнение связано с сердцем, а в действительности корни проблемы могут крыться в почках или другом органе. Но пациент может сделать свою жизнь лучше с помощью мер профилактики: умеренных физических нагрузок, контроля давления, коррекции питания, избавления от вредных привычек. Для постановки диагноза делают:
В Октябрьском сосудистом центре республики Башкортостан можно пройти необходимую диагностику, получить консультацию и лечение у профессионалов. В центре пациентам оказывают всестороннюю помощь и обнаруживают признаки гипертрофии уже на первом осмотре. Врачи назначают только необходимый объем исследований, по результатам которых ставят диагноз и подбирают адекватную терапию.
Гипертрофия левого желудочка неясной этиологии
В статье приведены клинические наблюдения и рассматриваются некоторые причины гипертрофии миокарда неясной этиологии, в том числе гипертрофическая кардиомиопатия (ГКМП), болезнь Фабри, AL и ATTR-амилоидоз. Важность своевременной диагностики трех последних заболеваний связана с тем, что сегодня стало возможным патогенетическое их лечение, позволяющее затормозить прогрессирования поражения сердца. Важное значение в диагностике ГКМП, болезни Фабри, наследственного ATTR-амилоидоза и некоторых других генетических заболеваний имеют изучение семейного анамнеза и молекулярно-генетическое исследование. При обследовании пациентов с необъяснимой гипертрофией левого желудочка необходимо обращать внимание на экстракардиальные проявления, которые могут оказаться ключом к правильному диагнозу, например, полиневропатия и нефротический синдром при системном амилоидозе, ангиокератомы и нейропатическая боль при болезни Фабри, прогрессирующая мышечная слабость и повышение активности креатинфосфокиназы при болезни Помпе, птоз век при митохондриальных заболеваниях и др. Для подтверждения диагноза амилоидоза следует проводить гистологическое исследование биоптата сердца или других органов и тканей.
С.В. Моисеев. Гипертрофия левого желудочка (ГЛЖ) часто встречается в практике кардиолога. Она может быть заподозрена на основании ЭКГ, однако более надежными методами оценки массы миокарда являются эхокардиография и особенно магнитно-резонансная томография (МРТ). При эхокардиографии критерием ГЛЖ считают увеличение индекса массы миокарда левого желудочка, соответственно, >115 г/м2 у мужчин и >95 г/м2 у женщин (с поправкой на площадь поверхности тела) или >50 г/м2,7 у мужчин и >47 г/м2,7 у женщин (с поправкой на рост) [1], а при МРТ – >85 г/м2 у мужчин и >81 г/м2 у женщин [2]. В зависимости от относительной толщины стенки (ОТС) левого желудочка [(2 × толщина задней стенки)/ конечный диастолический размер левого желудочка] выделяют концентрическую (ОТС≥0,43) и эксцентрическую (ОТС Е.В. Привалова. ГКМП – это наследственное заболевание, которое передается по аутосомно-доминантному типу [4]. В соответствии с рекомендациями Евро пейского общества кардиологов 2014 г., ГКМП может быть диагностирована при наличии гипертрофии миокарда ≥15 мм по крайней мере в одном сегменте левого желудочка, которую нельзя объяснить другими причинами, а у родственников пациента с установленным диагнозом – при наличии гипертрофии миокарда ≥13 мм [3]. Гипертрофия миокарда при ГКМП может быть как асимметричной (рис. 1), так и симметричной. У 4060% пациентов с ГКМП определяются мутации генов, кодирующих белки саркомеров сердца, прежде всего тяжелой цепи бета-миозина (MYH7) и миозин-связывающего белка С (MYBPC3). Реже встречаются мутации генов, кодирующих тропонины I и T (TNNI3, TNNT2), α1-цепи тропомиозина (TPM1) и легкой цепи миозина 3 (MYL3). В целом у пациентов с мутациями генов саркомерных белков выше частота семейного анамнеза ГКМП и внезапной смерти и отмечаются более выраженные ГЛЖ и миокардиальный фиброз, чем у пациентов без мутаций [5]. При обследовании пациента важно оценить наличие обструкции выносящего тракта левого желудочка [6]. Критерием ее является градиент давления в выносящем тракте, который измеряют допплеровским методом, ≥30 мм рт. ст. в покое или после провокационных проб (проба Вальсальвы, физическая нагрузка). Гемодинамически значимым считают увеличение этого показателя ≥50 мм рт. ст. [3].

В.Ю. Каплунова. Пациент К., 45 лет, обследован в клинике госпитальной терапии имени А.А. Остроумова в октябре 2018 г. Старший брат пациента внезапно умер в возрасте 54 лет. ГКМП была диагностирована у другого брата, умершего в возрасте 54 лет, и 29-летней дочери пациента. С 18-летнего возраста у больного выслушивался систолический шум по левому краю грудины при отсутствии клинических проявлений и хорошей переносимости физической нагрузки. В возрасте 27 лет появились одышка, сердцебиение, перебои в работе сердца, головокружение и дурнота, дискомфорт в области сердца при умеренной физической нагрузке. В возрасте 33 лет обнаружена асимметричная ГЛЖ (толщина межжелудочковой перегородки – 20 мм, задней стенки – 12 мм) с признаками обструкции выносящего тракта левого желудочка и градиентом давления в покое 45 мм рт. ст. Диагностирована обструктивная форма ГКМП. С 44-летнего возраста отмечает пароксизмы фибрилляции предсердий с последующим переходом аритмии в постоянную форму. При эхокардиографии было выявлено нарастание гипертрофии межжелудочковой перегородки до 31 мм и увеличение градиента давления до 94 мм рт. ст. в покое. В Научном центре сердечно-сосудистой хирургии им. А.Н. Баку ле ва выполнена миэктомия доступом из правого желудочка, которая привела к уменьшению степени обструкции выносящего тракта левого желудочка и диастолической дисфункции. При молекулярно-генетическом исследовании у пробанда и его дочери выявлена миссенс мутация в 22 экзоне гена, кодирующего тяжелую цепь β миозина (MYHT A870C).
Представленное наблюдение иллюстрирует типичные проявления и течение ГКМП: асимметричная гипертрофия межжелудочковой перегородки, которая была выявлена в молодом возрасте, медленно нарастала и длительное время не сопровождалась клиническими симптомами, в частности застойной сердечной недостаточностью, обструкция выносящего тракта левого желудочка с высоким градиентом давления в его полости, семейный анамнез (диагноз ГКМП и/или случаи внезапной сердечной смерти у близких родственников), мутация гена, кодирующего саркомерный белок, которая была обнаружена как у пробанда, так и его дочери. Лечение ГКМП обычно начинают с β-адреноблокаторов, не обладающих вазодилатирующей активностью, которые уменьшают градиент давления в полости левого желудочка и клинические симптомы. При их неэффективности могут быть использованы дизопирамид или верапамил. При выраженной гипертрофии межжелудочковой перегородки и высоком градиенте давления в левом желудочке может быть выполнена миэктомия, которая более чем в 90% случаев позволяет ликвидировать или значительно уменьшить обструкцию выносящего тракта, улучшить переносимость физической нагрузки и выживаемость [7].
Е.В. Привалова. Дифференциальная диагностика ГКМП с другими заболеваниями, сопровождающимися ГЛЖ, может представлять трудности, например, при наличии умеренной гипертрофии миокарда, особенно симметричной, не сопровождающейся обструкцией выносящего тракта левого желудочка, и при отсутствии семейного анамнеза. Мутации генов саркомерных белков определяются не у всех пациентов с ГКМП, а у части больных с необъяснимой ГЛЖ молекулярно-генетическое исследование не проводится по экономическим причинам. Следует учитывать, что асимметричная гипертрофия межжелудочковой перегородки, характерная для ГКМП, встречается и при других заболеваниях, в том числе вторичной гипертрофии миокарда при артериальной гипертонии. Причиной ГЛЖ могут быть не только перегрузка левого желудочка давлением, но и физические тренировки, хотя в крупном исследовании увеличение толщины стенки левого желудочка более 12 мм было выявлено всего у 1,7% из 947 спортсменов, занимающихся различными видами спорта, а толщина стенки не превышала 16 мм. Более частым эхокардиографическим признаком “сердца спортсмена» была дилатация полости левого желудочка, которая определялась в 38% случаев [8]. Важное значение для диагностики некоторых заболеваний, сопровождающихся ГЛЖ, имеет тщательный анализ клинической картины, позволяющий выявить те или иные экстракардиальные проявления болезни, которые отсутствуют при ГКМП. Проведение биопсии миокарда для подтверждения диагноза ГКМП не требуется, однако гистологическое исследование может быть обоснованным для исключения инфильтративных заболеваний, сопровождающихся утолщением стенки левого желудочка.
Е.А. Каровайкина. Болезнь Фабри – это редкое заболевание, которое характеризуется нарушением обмена гликофосфолипидов вследствие недостаточности или отсутствия лизосомного фермента – α-галактозидазы А [9]. Причиной дефицита этого фермента являются мутации гена GLA, расположенного на Х-хромосоме, поэтому типичные клинические проявления болезни Фабри наблюдаются чаще и более выражены у гемизиготных мужчин, однако они нередко встречаются и у гетерозиготных женщин. При классическом фенотипе болезни Фабри первые симптомы, в частности нейропатическая боль (эпизоды жгучей боли в кистях и стопах, возникающей при лихорадке, физической нагрузке, стрессе и быстрых изменениях температуры окружающей среды), ангиокератомы (поверхностные ангиомы, локализующиеся на передней брюшной стенке, в частности внутри или вокруг пупка, в паховой области, на ягодицах, верхних конечностях, губах; рис. 2), снижение или отсутствие потоотделения, желудочно-кишечные нарушения, появляются в детском или подростковом возрасте, а в возрасте 20-40 лет развивается поражение внутренних органов, в том числе сердца, почек (протеинурия и прогрессирующее снижение скорости клубочковой фильтрации) и центральной нервной системы (транзиторные ишемические атаки и инсульт). При атипичном “кардиальном» варианте заболевания ГЛЖ развивается в возрасте 40-50 лет и старше при отсутствии ранних симптомов. Результаты нескольких крупных скрининговых исследований свидетельствуют о том, что патогенные мутации гена GLA, ассоциирующиеся с развитием болезни Фабри, могут быть обнаружены у 0,5-1% пациентов с диагнозом ГКМП [10].

А.С. Моисеев. Иллюстрацией ГЛЖ, обусловленной болезнью Фабри, могут служить следующие два наблюдения. Пациент Л., 48 лет, был обследован в клинике им. Е.М. Тареева в октябре 2016 года. С 19 лет выраженная лимфедема нижних конечностей и снижение потоотделения. В возрасте 47 лет появились редкие боли за грудиной, не связанные с физической нагрузкой, а при эхокардиографии выявлено утолщение межжелудочковой перегородки и стенки левого желудочка до 14 мм при отсутствии дилатации камер сердца и нарушений систолической функции. Наблюдался у кардиолога с диагнозом ГКМП. Через 1 год при скрининге обнаружено снижение активности α-галактозидазы А в высушенных пятнах крови, увеличение уровня глобо триазилсфингозина (Lyso-GL3) до 117 нг/мл (в норме G), которые позволили установить диагноз болезни Фабри. На ЭКГ отмечались признаки ГЛЖ (рис. 3). При МРТ сердца наблюдались увеличение индекса массы миокарда левого желудочка до 123 г/м2 и признаки интрамиокардиального фиброза. Кроме того, имелись симптомы поражения почек – снижение расчетной скорости клубочковой фильтрации до 62 мл/мин/1,73 м2 при отсутствии протеинурии.

Одновременно мы обследовали 67-летнюю мать пациента, у которой за 2 года до госпитализации в клинику также была выявлена необъяснимая ГЛЖ, сопровождавшаяся постоянной формой фибрилляции предсердий, частой желудочковой экстрасистолией и сердечной недостаточностью, в связи с чем принимала β-адреноблокаторы, мочегонные средства, дигоксин, антикоагулянты. При МРТ сердца определялись утолщение межжелудочковой перегородки (19 мм) и задней стенки левого желудочка (12 мм), увеличение индекса массы миокарда левого желудочка до 141 г/м2 и участки интрамиокардиального фиброза. При МРТ головного мозга выявлены многочисленные очаги в белом веществе, а при осмотре окулистом – воронковидная кератопатия, характерная для болезни Фабри, диагноз которой подтверждался результатами молекулярногенетического исследования (мутация с.145C>G), повышением уровня Lyso-GL3 до 23 нг/мл и снижением активности α-галактозидазы А. Пациент и его мать в течение 1,5 лет получают ферментозаместительную терапию.
Представленные наблюдения демонстрируют важность скрининга в диагностике болезни Фабри у пациентов с необъяснимой ГЛЖ, так как клинически заподозрить правильный диагноз было сложно в связи с отсутствием типичных ранних симптомов – нейропатической боли и ангиокератом. С целью диагностики болезни Фабри у мужчин необходимо определять активность α-галактозидазы А и/или уровень Lyso-GL3 в высушенных пятнах крови. У женщин активность фермента нередко остается нормальной или снижается незначительно, поэтому более информативным считают определение уровня Lyso-GL3. Для подтверждения диагноза проводят молекулярно-генетическое исследование с целью выявления патогенной мутации гена GLA (в Российской Федерации все эти исследования выполняются бесплатно).
Н.Р. Носова. При анализе клинической картины обращали на себя внимание позднее развитие ГЛЖ и наличие ее не только у пробанда, но и его матери. Как указано выше, поражение внутренних органов при болезни Фабри, в отличие от некоторых других наследственных болезней, у мужчин обычно отмечается в возрасте 30-40 лет, а у женщин – в более старшем возрасте. Наследование болезни Фабри сцеплено с Х-хромосомой, поэтому у матери пациента обычно наблюдаются те или иные проявления заболевания, хотя фенотип его может отличаться. У пробанда с 18-летнего возраста отмечались снижение потоотделения, которое встречается у большинства мужчин с болезнью Фабри, и лимфедема. По данным регистра Fabry Outcomes Survey (n=714), частота лимфедемы при этом заболевании составила 16% у мужчин и 6% у женщин [11]. У матери пробанда была выявлена вихревидная кератопатия (коричнево-золотистые отложения в роговице в виде волнообразных линий, исходящих из одной центральной точки), которая является одним из клинических критериев диагноза болезни Фабри. По нашим данным, частота вихревидной кератопатии у 69 взрослых пациентов с болезнью Фабри составила 65,2%, в том числе 56,4% у мужчин и 76,7% у женщин [12]. В отличие от ГКМП, гипертрофия миокарда как у пробанда, так и его матери была выражена умеренно и не сопровождалась обструкцией выносящего тракта левого желудочка. У взрослых пациентов с болезнью Фабри обычно наблюдается поражение не только сердца, но и почек (альбуминурия/протеинурия, снижение скорости клубочковой фильтрации) и головного мозга (очаговые изменения в белом веществе при МРТ, транзиторные ишемические атаки/инсульт).
Е.А. Каровайкина. При болезни Фабри проводят заместительную терапию рекомбинантными препаратами α-галактозидазы А (агалсидазой альфа в дозе 0,2 мг/кг или агалсидазой бета в дозе 1 мг/кг), которые вызывают регресс ГЛЖ или по крайней мере замедляют прогрессирование кардиомиопатии. По данным D. Ger main и соавт., у пациентов с болезнью Фабри, начавших лечение в более молодом возрасте (18-30 лет), средняя масса миокарда левого желудочка снижалась на 3,6 г в год, в то время как без лечения у мужчин того же возраста она увеличивалась на 9,5 г в год (р В.В. Рамеев. Причиной утолщения стенок сердца мо жет быть не только гипертрофия кардиомиоцитов, но и инфильтрация миокарда нерастворимым фибриллярным гликопротеидом – амилоидом. В настоящее время известно около 30 амилоидогенных белков, однако более 95% случаев амилоидоза сердца обусловлены ALамилоидозом или реже транстиретиновым (ATTR) амилоидозом. AL-амилоидоз развивается при отложении моноклональных иммуноглобулинов у больных лимфоплазмаклеточными дискразиями, в том числе множественной миеломой. ATTR-амилоид (мутантный и дикого типа) образуется из транстиретина, синтезируемого в основном печенью и выполняющего функции транспортного белка тироксина и витамина А. Причи ной развития ATTR-амилоидоза дикого типа (стар ческого) считают возрастное снижение активности ферментных систем гепатоцитов, что приводит к пре имущественнои секреции нестабильных мономерных форм транстиретина, которые легко агрегируют в тканях с образованием амилоида. В основе наследственного ATTR-амилоидоза лежат мутации в гене TTR, сопровождающиеся синтезом транстиретина, который не способен образовывать тетрамеры и обладает очень высокой амилоидогенностью.
А.С. Рамеева. Пациентка Б., 50 лет, впервые обследована в клинике им. Е.М. Тареева в январе 2015 года. В течение года беспокоили боли в области сердца и нарастающая сердечная недостаточность. При эхокардиографии выявлено утолщение межжелудочковой перегородки и задней стенки левого желудочка до 14 мм, нарушение диастолической функции по рестриктивному типу. При коронарографии обнаружен умеренный стеноз правой коронарной артерии (50%). При обследовании в российском кардиологическом научном центре в декабре 2014 года определялись небольшая протеинурия (0,14 г/л), снижение вольтажа зубцов ЭКГ (рис. 4), увеличение толщины межжелудочковой перегородки и задней стенки левого желудочка до 18 мм, дилатация левого предсердия при отсутствии дилатации левого желудочка и снижения фракции выброса, при МРТ сердца – диффузное неравномерное субэндокардиальное накопление контрастного вещества. Выс ка зано предположение об амилоидозе, диагноз которого был подтвержден при биопсии миокарда. При исследовании крови методом Freelite отмечено резкое увеличение концентрации свободных легких цепей лямбда типа до 1383 мг/л (в норме 5,7-26,3 мг/л), указывавшее на наличие AL-амилоидоза. При трепанобиопсии диагностирована множественная миелома (увеличение числа плазматических клеток до 20%). Пациентке проводилась терапия бортезомибом, мелфаланом и дексаметазоном, на фоне которой нормализовалась концентрация свободных легких цепей лямбда типа и достигнута компенсация сердечной недостаточности.

В.В. Рамеев. Таким образом, у пациентки был диагностирован AL-амилоидоз с поражением сердца в рамках множественной миеломы. Заподозрить амилоидоз сердца позволяли возраст пациентки, быстрое развитие тяжелой сердечной недостаточности, которая плохо поддавалась симптоматической терапии, эхокардиографические признаки рестриктивного поражения сердца (увеличение левого предсердия при отсутствии дилатации левого желудочка и снижения фракции выброса), симметричное утолщение межжелудочковой перегородки и стенки левого желудочка без обструкции выносящего тракта, снижение вольтажа зубцов комплекса QRS на ЭКГ. Последний признак отличает амилоидоз сердца от ГЛЖ, хотя истинное снижение амплитуды QRS (менее 5 мм в отведениях от конечностей и менее 10 мм в грудных отведениях) наблюдается только у половины больных AL-амилоидозом сердца [14]. Однако даже при отсутствии низкого вольтажа комплексов QRS следует учитывать возможное его несоответствие степени ГЛЖ при эхокардиографии. Важное диагностическое значение имеют результаты МРТ сердца, которая позволяет не только измерить массу миокарда левого желудочка, но и выявить диффузное накопление гадолиния в субэндокарде [15].
В представленном наблюдении диагноз был подтвержден при биопсии миокарда, хотя для гистологического исследования могут быть использованы и другие ткани, более доступные для биопсии, в том числе слизистая оболочка прямой или двенадцатиперстной кишки, подкожно-жировая клетчатка, почка. На наличие AL-амилоидоза указывала моноклональная секреция лямбда-цепей иммуноглобулинов, выявленная с помощью метода Freelite, а также снижение отношения каппа- и лямбда-цепей до 0,01 (для AL-амилоидоза характерна величина этого показателя 1,65). У 7-10% больных AL-амилоидоз развивается в рамках множественной миеломы, для исключения которой всем пациентам следует проводить биопсию костного мозга.
Данный случай демонстрирует возможность “изолированного» поражения сердца при AL-амилоидозе, хотя у большинства пациентов наблюдаются и другие проявления, в том числе протеинурия/нефротический синдром, увеличение печени и селезенки, макроглоссия, периорбитальная пурпура, диарея, невропатия и/или ортостатическая гипотензия. У пациентки имелась небольшая протеинурия, однако она могла быть связана с застоем крови по большому кругу кровообращения.
Современная химиотерапия, включающая в себя ингибитор протеасом бортезомиб, позволяет добиться полного или частичного гематологического ответа у значительной части больных AL-амилоидозом, предупредить отложение амилоида в других органах и прогрессирование сердечной недостаточности.
П.П. Тао. Пациент В., 65 лет, русский, был обследован в клинике им. Е.М. Тареева в декабре 2015 года. В течение трех лет отмечается нарастающее снижение болевой, температурной и тактильной чувствительности в области кистей и стоп по типу “перчаток» и “носков», а в течение одного года – прогрессирующая застойная сердечная недостаточность. При электромиографии выявлены грубые аксонально-демиелинизирующие нарушения, наиболее выраженные в малоберцовых нервах, а при эхокардиографии – картина рестриктивного поражения сердца: дилатация левого предсердия, утолщение стенок левого желудочка, зоны гипокинезии в межжелудочковой перегородке, уплотнение эндокарда, нормальная фракция выброса левого желудочка. Уровень мозгового натрийуретического пропептида был повышен в 30 раз по сравнению с верхней границей нормы. При коронарографии обнаружен стеноз передней межжелудочковой ветви (65%) и правой коронарной артерии (75%). Проведены чрескожная коронарная ангиопластика и стентирование правой коронарной артерии, однако после вмешательства сердечная недостаточность сохранялась, появилась ортостатическая артериальная гипотензия. По данным эхокардиографии, толщина межжелудочковой перегородки достигла 22 мм, определялись множественные очаги зернистости в миокарде, фракция выброса левого желудочка снизилась с 57% до 45%. При МРТ сердца с контрастированием гадолинием на фоне выраженного утолщения стенок левого желудочка отмечено циркулярное субэндокардиальное диффузное накопление контрастного вещества в миокарде левого и передней стенки правого желудочков (рис. 5). Проводилась повторная биопсия слизистой оболочки прямой кишки, однако амилоид выявить не удалось. При иммунохимическом исследовании исключена моноклональная секреция легких цепей иммуноглобулинов, характерная для AL-амилоидоза. При молекулярно-генетическом исследовании обнаружена мутация гена TTR (Val30Met), подтверждающая диагноз наследственного ATTR-амилоидоза. При сцинтиграфии миокарда с 99mTcPYP выявлено накопление радиоизотопного препарата 2 степени, в связи с чем от биопсии миокарда было решено воздержаться. С целью восстановления тетрамерной структуры мутантного транстиретина пациент в течение 2 лет получает тафамидис 20 мг/сут. Переносимость лечения удовлетворительная, существенного прогрессирования амилоидоза не произошло.

В.В. Рамеев. Как и в предыдущем наблюдении, заподозрить амилоидоз у 65-летнего пациента позволяло типичное рестриктивное поражение левого желудочка, характеризующееся развитием тяжелой сердечной недостаточности при отсутствии дилатации и существенного снижения фракции выброса левого желудочка. При эхокардиографии определялись множественные очаги зернистости, которые нередко выявляют у пациентов с амилоидной инфильтрацией миокарда, а при МРТ сердца – диффузное накопление гадолиния в субэндокарде. В пользу системного амилоидоза свидетельствовала и периферическая полиневропатия, которая встречается как при AL-, так и семейном ATTR-амилоидозе и может предшествовать поражению сердца. В большинстве случаев развивается неуклонно прогрессирующая, симметричная дистальная невропатия, начинающаяся с сенсорных расстройств, в первую очередь болевой и температурной чувствительности, с последующим присоединением нарушений вибрационной и позиционной чувствительности и двигательных нарушений. Ранними симптомами невропатии бывают парестезии или мучительные дизестезии. Часто встречается синдром запястного канала, проявляющийся болями и парестезиями в I-III пальцах кисти с постепенной атрофией мышц тенара и обусловленный сдавлением срединного нерва в запястном канале амилоидом, откладывающимся в связках запястья [16].
Учитывая отсутствие моноклональной секреции легких цепей иммуноглобулинов и наличие мутации гена TTR, был установлен диагноз наследственного ATTRамилоидоза [17]. Диагноз амилоидоза должен быть подтвержден при гистологическом исследовании, однако результаты повторной биопсии прямой кишки оказались отрицательными. Тем не менее, наличие ATTRамилоидоза не вызывало сомнения с учетом типичной клинической картины и результатов молекулярно-генетического исследования. Кроме того, при сцинтиграфии было выявлено накопление 99mTcPYP в миокарде 2 степени (т.е. умеренное накопление, соответствующее таковому в костной ткани). В 2016 году в многоцентровом исследовании было показано, что накопление в миокарде 99mTcPYP 2-3 степени (рис. 6) при отсутствии моноклональной гаммапатии обладает 100% специфичностью в диагностике ATTR-амилоидоза сердца и фактически позволяет отказаться от биопсии миокарда [18]. Более того, сцинтиграфия с 99mTcPYP дает возможность дифференцировать ATTR-амилоидоз от AL-амилоидоза, при котором накопление радиоактивного препарата в миокарде отсутствует или не превышает 1 степени.

С середины 90-х годов ХХ века для лечения ATTRамилоидоза применяли трансплантацию печени, позволяющую восстановить синтез нормального транс тиретина. В последние годы более перспективной тактикой лечения считают медикаментозную стабилизацию тетрамерной структуры транстиретина и предотвращение образования амилоидогенных мономеров белка. Первый такой препарат – тафамидис – уже применяется в Европе и в Российской Федерации.
С.В. Моисеев. Представленные наблюдения иллюстрируют широкий спектр причин ГЛЖ неясной этиологии, которые включают в себя не только истинную гипертрофию миокарда, но и некоторые инфильтративные заболевания, такие как системный амилоидоз, имитирующие ГКМП. Разработать четкий алгоритм дифференциальной диагностики ГКМП достаточно сложно, учитывая вариабельность течения заболеваний, сопровождающихся ГЛЖ. Например, некоторые тяжелые генетические заболевания, такие как болезнь Помпе (гликогеноз II типа, связанный с дефицитом фермента кислой α-глюкозидазы в лизосомах), могут проявиться в возрасте 40-50 лет и старше, в то время как при системных заболеваниях, в том числе болезни Фабри или амилоидозе, экстракардиальные симптомы иногда отсутствуют. Ключевую роль в диагностике наследственных заболеваний, таких как ГКМП, ATTRамилоидоз, болезни Фабри, Помпе, Данона и др., играют изучение семейного анамнеза и молекулярногенетическое исследование.