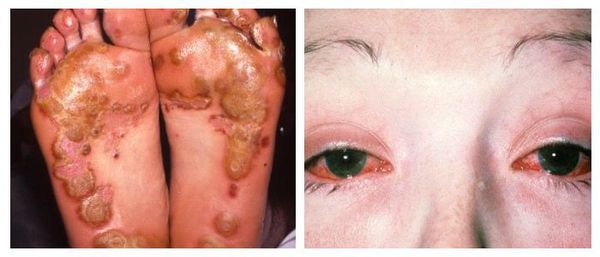
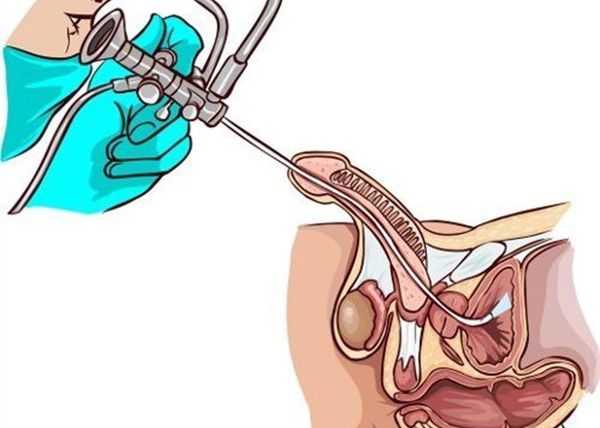
Что такое уретрит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Барашиков Д. В., уролога со стажем в 19 лет.
Определение болезни. Причины заболевания
Наиболее частый путь передачи — половой, реже воспалительный процесс инициируется условно-патогенной флорой. Уретрит может быть вызван бактериями, грибками или вирусами (например, вирусом герпеса).
Причины заболевания
Чаще всего уретрит вызывают инфекции, передающиеся половым путём, и условно-патогенные микроорганизмы: гоноккоки, хламидии, микоплазма, менингококки, вирус герпеса, аденовирус, бледная трепонема, уреплазма. Вероятность развития заболевания напрямую связана с образом жизни: количеством незащищенных половых актов, снижением иммунитета и несоблюдением гигиенических мероприятий. В зоне риска находятся мужчины и женщины 18-35 лет, ведущие активную половую жизнь и не использующие барьерный метод контрацепции.
Гораздо реже уретрит инициируется сопутствующими заболеваниями, воздействием агрессивных веществ (спермицидных лубрикантов, спиртосодержащих растворов) или травмами.
Предрасполагающими факторами для развития уретрита могут служить:
Симптомы уретрита
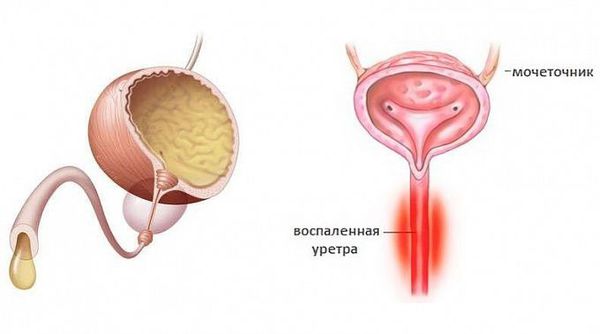
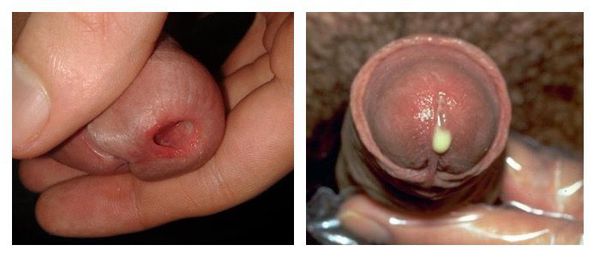
У достаточно большого количества пациентов уретрит изначально протекает со стёртыми проявлениями (торпидная или вялотекущая форма). Пациенты предъявляют жалобы лишь на скудное отделяемое из уретры по утрам на нижнем белье. В некоторых случаях возможно «склеивание» и незначительная гиперемия наружного отверстия уретры, разбрызгивание мочи при мочеиспускании. Цвет и прозрачность мочи обычно не меняется.
При торпидных уретритах воспалительный синдром достаточно часто не ограничивается передней уретрой, а распространяется на задний отдел, предстательную железу и шейку мочевого пузыря.
Тотальный уретрит характеризуется частыми, императивными позывами к мочеиспусканию, болью внизу живота и промежности. Нередко имеется примесь крови в моче, либо примесь гнойного отделяемого. Воспалительная реакция в остром периоде длится от нескольких дней до трёх недель.
Патогенез уретрита
У мужчин микрофлора уретры остается постоянной на протяжении всей жизни. Её представляют стафилококки, дифтероиды, диплококки, палочки и анаэробы (пептококки, бактероиды, энтеробактерии и клостридии). Микроорганизмы заселяют лишь первые несколько сантиметров мочеиспускательного канала — на остальном протяжении он почти стерилен. Реакция в канале нейтрально-щелочная.
В норме у женщин микрофлора уретры представлена теми же бактериями, что у мужчин, но в большем количестве. В небольшом количестве в уретре присутствуют лактобацилы и кишечная палочка. Бактерии свободно размножаются, не вызывая при этом воспаления. В медицине этот процесс называется колонизацией.
Различные инфекционные агенты, попадая на слизистую оболочку мочеиспускательного канала, адгезируются (сцепляются с поверхностью) и вызывают локальную воспалительную реакцию, либо персистируют (присутствуют в неактивном состоянии) в ней продолжительное время без клинических признаков заболевания.
Женщины более часто страдают клинически выраженными симптомами уретрита по сравнению с мужчинами, что связано с анатомическими особенностями строения мочеполовой системы — короткая уретра (около 1 см) и близкое расположение анального отверстия. Учитывая строение уретры, уретрит у женщин чаще приводит к развитию восходящей инфекции и может стать причиной бесплодия.
Классификация и стадии развития уретрита
Уретрит подразделяется по своей этиологии на:
По Международной классификации болезней МКБ-10 к уретриту и уретральному синдрому также относятся:
Классификация по локализации воспалительного процесса достаточно условная.
По глубине (степени) поражения выделяют (преимущественно у мужчин):
По клиническому течению выделяют уретриты:
Осложнения уретрита
Диагностика уретрита
Первоначально проводится стандартный осмотр и сбор анамнеза. Во время беседы врач должен выяснить, что именно беспокоит пациента, когда возникли первые симптомы, был ли в недавнем времени незащищенный половой акт, назначалось ли ранее лечение по поводу ИППП, имеются ли хронические заболевания.
Проведение 3-х стаканной пробы мочи позволяет косвенно определить уровень распространенности воспалительного процесса. Оценивается количество лейкоцитов в поле зрения:
Бактериологическое исследование (посев) отделяемого из уретры позволяет выявить патогенную и условно-патогенную микрофлору, ее титр (концентрацию) и чувствительность к антибиотикам. Диагностически значимым титром у женщин является 10х4, у мужчин — 10х3 КОЕ/мл.
Серологический метод – определение антител (иммуноглобулинов класса G, M и А) в венозной крови пациента к наиболее распространенным возбудителям уретрита. Используется как вспомогательный метод.
ПЦР – методика исследования отделяемого из уретры, крови или мочи, а также иных биологических жидкостей посредством полимеразной цепной реакции, с целью обнаружения в них определенных возбудителей.
Приемуществом метода является высокая чувствительность. Вероятность ложноотрицательного ответа ничтожно мала, а вероятность ложноположительного ответа составляет менее 1 %.
Наряду с лабораторными исследованиями, немаловажную роль играет проведение специфических исследований, таких как уретроцистоскопия или уретрография. В первом случае в мочеиспускательный канал вводят цистоскоп, с помощью которого визуализируют слизистую оболочку уретры, мочевого пузыря. При уретрографии диагностика проводится с использованием рентгеноконтрастного вещества и выполнения серии снимков для оценки проходимости и наличия патологических процессов в уретре.
Для исключения органических изменений и дифференциальной диагностики с другими заболеваниями, выполняется ультразвуковое исследование органов малого таза и верхних мочевых путей (мочевого пузыря, матки, придатков, простаты и семенных пузырьков, почек).
Лечение уретрита
В случае обнаружения у себя симптомов уретрита, необходимо обратиться к квалифицированному специалисту: урологу, гинекологу либо дерматовенерологу.
Терапия зависит от типа уретрита и направлена на устранение его причины. При гоноррейном уретрите необходима консультация дерматовенеролога с последующей антибактериальной терапией и контролем излеченности пациента и его полового партнера.
Лечение мужчин, ведущих половую жизнь, как правило, включает в себя инъекции цефтриаксона для лечения гонореи и пероральный приём азитромицина для лечения хламидиоза. Если обследование исключает гонорею и хламидиоз, то может применяться антибиотик триметоприм или фторхинолон (например, ципрофлоксацин). У женщин лечение такое же, как и лечение цистита. Для лечения инфекции, вызванной вирусом простого герпеса, могут потребоваться противовирусные препараты.
При негоноррейных бактериальных и грибковых уретритах основным методом является назначение антибактериальной и антимикотической терапии после верификации диагноза и определения чувствительности микрофлоры к антибиотикам (мазок, ПЦР диагностика, исключение гинекологических заболеваний и других воспалительных процессов, имеющих сходную клиническую картину).
В некоторых случаях возможно назначение эмпирической терапии, основанной на опыте лечения и частоте выявляемости возбудителя, обычно при недостатке точных данных. Сначала назначается препарат, а в дальнейшем врач оценивает, насколько он эффективен.
Параллельно базовой терапии пациенту назначают препараты, стимулирующие общий и местный иммунный ответ. Также применяют препараты для стимуляции местного иммунитета и профиллактики рецидивов. Доказана высокая эффективность препарата Уро-Ваксом при негонококковых бактериальных уретритах, вызванных E. coli.
С целью эвакуации возбудителя из мочевых путей и восстановления применяют местную терапию, включающую в себя инстилляции водного раствора хлоргекседина, колларгола, уропротекторов.
Для купирования внезапных и непреодолимых позывов к мочеиспусканию применяют ингибиторы М-холинорецепторов (солифенацин), селективные агонисты бета3-адренорецепторов (мирабегрон) и блокаторы альфа-адренорецепторов (тамсулозин). Механизм действия данных препаратов направлен на расслабление гладкомышечных клеток (снятие спазма) в строме простаты, шейке и мышечной оболочке мочевого пузыря.
Прогноз. Профилактика
Своевременное лечение бактериального уретрита и соблюдение рекомендаций гарантирует полное выздоровление. После санированного (пролеченного) бактериального уретрита возможно реинфицирование (повторное заражение) при незащищенных половых актах с инфицированным партнером. Поэтому при уретритах, вызванных ИППП, для профилактики рецидивов лечение обязательно должен проходить и половой партнёр.
Учитывая распространенность и многогранность клинической картины уретрита, а также риск развития осложнений, для профилактики рекомендуется придерживаться определенных правил поведения:
Уретрит у детей
Уретрит — это воспалительное заболевание уретры (мочеиспускательного канала). По своим анатомо-физиологическим особенностям уретра мальчиков и девочек отличается: у девочек она короткая (в возрасте 1 года приблизительно 2 см), более широкая и расположена в непосредственной близости к анальному отверстию, а у мальчиков — более длинная (в 1 год приблизительно 7–8 см) и узкая. Из-за такой особенности девочки чаще страдают воспалительными заболеваниями мочевыделительной системы, чем мальчики.
Содержание:
Причины возникновения уретрита
Уретрит является полиэтиологическим заболеванием, которое могут провоцировать следующие причины:
Виды уретрита
По этиологическому фактору выделяют следующие виды данного заболевания:
По клиническому течению выделяют следующие формы уретрита:
По степени распространенности воспаления уретрит бывает:
Симптомы уретрита
Основными симптомами заболевания являются:
Важно, что четко описать симптомы могут только дети старшего возраста. У маленького ребенка невозможно выделить характерный признак болезни. К тому же, инфекционный процесс зачастую протекает не локально (например, поражение распространяется не только на уретру, но и на мочевой пузырь). Поэтому для маленьких детей применяют такое сборное понятие, как инфекции мочевыводящих путей (ИМП).
Для того чтобы не пропустить ИМП, необходимо обратить внимание на следующие признаки:
Диагностика уретрита
Для диагностики данного заболевания необходимо прийти на консультацию к детскому урологу (для мальчиков и девочек) или гинекологу (только для девочек). Доктор соберет анамнез заболевания, проведет осмотр и, при необходимости, назначит дополнительные исследования:
Методы лечения уретрита
Лечением этого заболевания должен заниматься исключительно врач, поскольку самолечение может привести к нежелательным последствиям в будущем. Медикаментозную терапию доктор подбирает индивидуально, основываясь на причинах возникновения заболевания и данных диагностических исследований. Суть медикаментозного лечения острого уретрита заключается в назначении диетотерапии, антибиотикотерапии (препарат подбирается в зависимости от типа возбудителя), фитотерапии, витаминотерапии, пробиотиков, а также противовоспалительных и антигистаминных препаратов.
После курса терапии необходимо пройти дополнительное лабораторное обследование.
Лечение хронического уретрита в стадии обострения практически не отличается от лечения острой формы. В период ремиссии хронического процесса родителям нужно придерживаться следующих рекомендаций:
Последствия уретрита
Уретрит, который не вылечили полностью, имеет свойство переходить в хроническую форму. Кроме того, данное заболевание может стать причиной возникновения следующих патологий:
Во взрослом возрасте из-за нелеченной ИМП ребенок может столкнуться с проблемой бесплодия.
Антибиотики в лечении и профилактике инфекций мочевыводящих путей у детей
Инфекция мочевыводящих путей (ИМП) — рост микроорганизмов в различных отделах почек и мочевыводящих путей (МП), способный вызвать воспалительный процесс, по локализации соответствующий заболеванию (пиелонефриту, циститу, уретриту и т. д.). ИМП детей
Инфекция мочевыводящих путей (ИМП) — рост микроорганизмов в различных отделах почек и мочевыводящих путей (МП), способный вызвать воспалительный процесс, по локализации соответствующий заболеванию (пиелонефриту, циститу, уретриту и т. д.).
ИМП детей встречается в России с частотой около 1000 случаев на 100 000 населения. Довольно часто ИМП имеют тенденцию к хроническому, рецидивирующему течению. Это объясняется особенностью строения, кровообращения, иннервации МП и возрастной дисфункцией иммунной системы растущего организма ребенка. В связи с этим принято выделять ряд факторов, способствующих развитию ИМП:
В детском возрасте ИМП в 80% случаев развиваются на фоне врожденных аномалий верхних и нижних МП, при которых имеются нарушения уродинамики. В таких случаях говорят об осложненной ИМП. При неосложненной форме анатомических нарушений и расстройств уродинамики не определяется.
Среди наиболее часто встречающихся пороков развития мочевого тракта пузырно-мочеточниковый рефлюкс встречается в 30–40% случаев. Второе место занимает мегауретер, нейрогенная дисфункция мочевого пузыря. При гидронефрозе инфицирование почки происходит реже.
Диагностика ИМП строится на многих принципах. Необходимо помнить, что симптоматика ИМП зависит от возраста ребенка. Например, у новорожденных детей отсутствуют специфические симптомы ИМП и инфекция редко генерализуется.
Для детей младшего возраста характерны такие симптомы, как вялость, беспокойство, периодические подъемы температуры, анорексия, рвота и желтуха.
Для детей старшего возраста характерны лихорадка, боли в спине, животе и дизурические явления.
Перечень вопросов при сборе анамнеза включает следующие пункты:
Врач всегда должен стремиться более точно установить локализацию возможного очага инфекции: от этого зависит вид лечения и прогноз заболевания. Для уточнения топики поражения мочевого тракта необходимо хорошо знать клиническую симптоматику инфекций нижних и верхних мочевых путей. При инфекции верхних мочевыводящих путей значимым является пиелонефрит, который составляет до 60% всех случаев госпитализации детей в стационар (таблица).
Однако основу диагностики ИМП составляют данные анализов мочи, в которых главное значение имеют микробиологические методы. Выделение микроорганизма в посеве мочи служит основанием для постановки диагноза. Существует несколько способов забора мочи:
Распространенным непрямым методом оценки бактериурии является анализ на нитриты (нитраты, в норме имеющиеся в моче, при наличии бактерий преобразуются в нитриты). Диагностическая ценность данного метода достигает 99%, но у маленьких детей в связи с коротким пребыванием мочи в мочевом пузыре значительно снижена и достигает 30–50%. Необходимо помнить, что у маленьких мальчиков может быть ложноположительный результат из-за аккумуляции нитритов в препуциальном мешке.
В большинстве случаев ИМП вызывается одним видом микроорганизма. Определение в образцах нескольких видов бактерий чаще всего объясняется нарушениями техники сбора и транспортировки материала.
При хроническом течении ИМП в некоторых случаях возможно выявление микробных ассоциаций.
К другим методам исследования мочи относятся сбор общего анализа мочи, проба Нечипоренко и Аддиса–Каковского. Лейкоцитурия наблюдается во всех случаях ИМП, однако необходимо помнить, что она может быть, например, и при вульвите. Макрогематурия встречается у 20–25% детей с циститом. При наличии симптомов инфекции протеинурия подтверждает диагноз пиелонефрита.
Инструментальные обследования проводятся детям в период ремиссии процесса. Целью их является уточнение локализации инфекции, причины и степени повреждения почек. Обследование детей с ИМП на сегодняшний день включает:
Проведение инструментального и рентгенологического обследования должно выполняться по следующим показаниям:
Бактериальная этиология ИМС при урологических заболеваниях имеет отличительные особенности в зависимости от остроты процесса, частоты осложненных форм, возраста пациента и состояния его иммунного статуса, условий возникновения инфекции (амбулаторно или в стационаре).
Результаты исследований (данные НЦЗД РАМН, 2005) показывают, что у амбулаторных больных с ИМП в 50% случаев выделяются E. coli, в 10% — Proteus spp., в 13% — Klebsiella spp., в 3% — Enterobacter spp., в 2% — Morganella morg. и с частотой 11% — Enterococcus fac. (рисунок). Другие микроорганизмы, составившие 7% выделения и встречавшиеся с частотой менее 1%, были следующими: S. epidermidis — 0,8%, S. pneumoniae — 0,6%, Acinetobacter spp. — 0,6%, Citrobacter spp. — 0,3%, S. pyogenes — 0,3%, Serratia spp. — 0,3%.
В структуре внутрибольничных инфекций ИМП занимают второе место, после инфекций дыхательных путей. Следует отметить, что у 5% детей, находящихся в урологическом стационаре, развиваются инфекционные осложнения, обусловленные хирургическим или диагностическим вмешательством.
У стационарных больных этиологическая значимость кишечной палочки значительно снижается (до 29%) за счет увеличения и/или присоединения таких «проблемных» возбудителей, как Pseudomonas aeruginosa (29%), Enterococcus faec. (4%), коагулазонегативные стафилококки (2,6%), неферментирующие грамотрицательные бактерии (Acinetobacter spp. — 1,6%, Stenotrophomonas maltophilia — 1,2%) и др. Чувствительность этих возбудителей к антибактериальным препаратам часто непредсказуема, так как зависит от ряда факторов, в том числе и от особенностей циркулирующих в данном стационаре внутрибольничных штаммов.
Не вызывает сомнений, что основными задачами в лечении больных с ИМП являются ликвидация или уменьшение воспалительного процесса в почечной ткани и МП, при этом успех лечения во многом определяется рациональной антимикробной терапией.
Естественно, при выборе препарата уролог руководствуется прежде всего сведениями о возбудителе инфекции и о спектре антимикробного действия препарата. Антибиотик может быть безопасным, способным создавать высокие концентрации в паренхиме почек и моче, но если в его спектре нет активности против конкретного возбудителя, назначение такого препарата бессмысленно.
Глобальной проблемой в назначении антибактериальных препаратов является рост резистентности микроорганизмов к ним. Причем наиболее часто резистентность развивается у внебольничных и нозокомиальных больных. Те микроорганизмы, которые не входят в антибактериальный спектр какого-либо антибиотика, естественно, считаются резистентными. Приобретенная же резистентность означает, что изначально чувствительный к определенному антибиотику микроорганизм становится устойчивым к его действию.
На практике часто заблуждаются в отношении приобретенной резистентности, считая, что ее возникновение неизбежно. Но наука располагает фактами, опровергающими такое мнение. Клиническое значение этих фактов состоит в том, что антибиотики, которые не вызывают резистентности, можно использовать, не опасаясь ее последующего развития. Но если же развитие резистентности потенциально возможно, то и появляется она достаточно быстро. Другое заблуждение заключается в том, что развитие резистентности связывают с использованием антибиотиков в больших объемах. Примеры с наиболее часто назначаемым в мире антибиотиком цефтриаксоном, а также с цефокситином и цефуроксимом поддерживают концепцию о том, что использование антибиотиков с низким потенциалом развития резистентности в любых объемах не приведет к ее росту в последующем.
Многие считают, что для одних классов антибиотиков возникновение антибиотикорезистентности характерно (это мнение относится к цефалоспоринам III поколения), а для других — нет. Однако развитие резистентности связано не с классом антибиотика, а с конкретным препаратом.
Если антибиотик обладает потенциалом развития резистентности, признаки резистентности к нему появляются уже в течение первых 2 лет применения или даже на этапе клинических испытаний. Исходя из этого, мы можем с уверенностью прогнозировать проблемы резистентности: среди аминогликозидов — это гентамицин, среди цефалоспоринов II поколения — цефамандол, III поколения — цефтазидим, среди фторхинолонов — тровофлоксацин, среди карбапенемов — имипенем. Внедрение в практику имипенема сопровождалось быстрым развитием резистентности к нему штаммов P. aeruginosa, этот процесс продолжается и сейчас (появление меропенема не было сопряжено с такой проблемой, и можно утверждать, что она не возникнет и в ближайшем будущем). Среди гликопептидов — это ванкомицин.
Как уже указывалось, у 5% больных, находящихся в стационаре, развиваются инфекционные осложнения. Отсюда и тяжесть состояния, и увеличение сроков выздоровления, пребывания на койке, повышение стоимости лечения. В структуре внутрибольничных инфекций ИМП занимают первое место, на втором месте — хирургические (раневые инфекции кожи и мягких тканей, абдоминальные).
Сложности лечения госпитальных инфекций обусловлены тяжестью состояния больного. Часто имеет место ассоциация возбудителей (два и более, при раневой или катетер-ассоциированной инфекции). Также большое значение имеет возросшая в последние годы резистентность микроорганизмов к традиционным антибактериальным препаратам (к пенициллинам, цефалоспоринам, аминогликозидам), применяемым при инфекции мочеполовой системы.
На сегодняшний день чувствительность госпитальных штаммов Enterobacter spp. к Амоксиклаву (амоксициллин + клавулановая кислота) составляет 40%, к цефуроксиму — 30%, к гентамицину — 50%, чувствительность S. aureus к оксациллину составляет 67%, к линкомицину — 56%, к ципрофлоксацину — 50%, к гентамицину — 50%. Чувствительность штаммов P. aeruginosa к цефтазидиму в разных отделениях не превышает 80%, к гентамицину — 50%.
Существуют два потенциальных подхода к преодолению резистентности к антибиотикам. Первый заключается в профилактике резистентности, например путем ограничения применения антибиотиков, обладающих высоким потенциалом ее развития; столь же важными являются эффективные программы эпидемиологического контроля для предотвращения распространения в лечебном учреждении госпитальных инфекций, вызываемых высокорезистентными микроорганизмами (стационарный мониторинг). Второй подход — устранение или коррекция уже имеющихся проблем. Например, если в отделении интенсивной терапии (или в стационаре вообще) распространены резистентные штаммы P. aeruginosa или Enterobacter spp., то полная замена в формулярах антибиотиков с высоким потенциалом развития резистентности на антибиотики-«чистильщики» (амикацин вместо гентамицина, меропенем вместо имипенема и т.п.) позволит устранить или минимизировать антибиотикорезистентность грамотрицательных аэробных микроорганизмов.
В лечении ИМП на сегодняшний день используются: ингибиторозащищенные пенициллины, цефалоспорины, аминогликозиды, карбапенемы, фторхинолоны (ограничены в педиатрии), уроантисептики (производные нитрофурана — Фурагин).
Остановимся на антибактериальных препаратах в лечении ИМП подробнее.
Рекомендуемые препараты при инфекции нижних мочевых путей.
При инфекции верхних мочевых путей.
При госпитальной инфекции.
Для периоперационной антибактериальной профилактики.
Для антибактериальной профилактики при инвазивных манипуляциях: ингибиторозащищенные аминопенициллины — амоксициллин + клавулановая кислота.
Принято считать, что антибактериальная терапия амбулаторных больных с ИМП может проводиться эмпирически, основываясь на данных антибиотикочувствительности основных уропатогенов, циркулирующих в конкретном регионе в данный период наблюдения, и клиническом статусе пациента.
Стратегическим принципом антибиотикотерапии в амбулаторных условиях является принцип минимальной достаточности. Препаратами первого ряда служат:
Ошибочным является использование в амбулаторных условиях ампициллина и ко-тримоксазола, в связи с возросшей резистентностью к ним E. coli. Неоправданно назначение цефалоспоринов I поколения (цефалексин, цефрадин, цефазолин). Производные нитрофуранового ряда (Фурагин) не создают терапевтических концентраций в почечной паренхиме, поэтому их назначают только при цистите. В целях снижения роста резистентности микроорганизмов следует резко ограничить применение цефалоспоринов III поколения и полностью исключить назначение аминогликозидов в амбулаторной практике.
Анализ резистентности штаммов возбудителей осложненных уроинфекций показывает, что активность препаратов группы полусинтетических пенициллинов и защищенных пенициллинов может быть достаточно высокой в отношении кишечной палочки и протеев, однако в отношении энтеробактерий и синегнойной палочки их активность составляет до 42 и 39% соответственно. Поэтому препараты этой группы не могут быть препаратами эмпирической терапии тяжелых гнойно-воспалительных процессов органов мочевыделения.
Активность цефалоспоринов I и II поколений в отношении энтеробактера и протеев также оказывается очень низкой и колеблется в пределах 15–24%, в отношении кишечной палочки — несколько выше, однако не превышает активности полусинтетических пенициллинов.
Активность цефалоспоринов III и IV поколений существенно выше, чем у пенициллинов и цефалоспоринов I и II поколений. Наиболее высокая активность отмечена в отношении кишечной палочки — от 67 (цефоперазон) до 91% (цефепим). В отношении энтеробактера активность составляет от 51 (цефтриаксон) до 70% (цефепим), также высокая активность препаратов этой группы отмечается в отношении протеев (65–69%). В отношении синегнойной палочки активность этой группы препаратов низкая (15% у цефтриаксона, 62% у цефепима). Спектр антибактериальной активности цефтазидима наиболее высокий в отношении всех актуальных грамотрицательных возбудителей осложненных инфекций (от 80 до 99%). Высокой сохраняется активность карбапенемов — от 84 до 100% (у имипенема).
Активность аминогликозидов несколько ниже, особенно в отношении энтерококков, но в отношении энтеробактерий и протея высокая активность сохраняется у амикацина.
По этой причине антибактериальная терапия ИМП у урологических больных в стационаре должна основываться на данных микробиологической диагностики возбудителя инфекции у каждого больного и его чувствительности к антибактериальным препаратам. Начальная эмпирическая антимикробная терапия урологических больных может назначаться только до получения результатов бактериологического исследования, после которого она должна быть изменена согласно антибиотикочувствительности выделенного микроорганизма.
В применении антибиотикотерапии в стационаре следует придерживаться другого принципа — от простого к мощному (минимум использования, максимум интенсивности). Спектр используемых групп антибактериальных препаратов здесь значительно расширен:
Важной в работе детского уролога является периоперационная антибиотикопрофилактика (пре-, интра- и постоперационная). Конечно, не следует пренебрегать влиянием других факторов, снижающих вероятность развития инфекции (сокращение сроков пребывания в стационаре, качество обработки инструментария, катетеров, использование закрытых систем для отведения мочи, обучение персонала).
Основные исследования показывают, что послеоперационные осложнения предотвращаются в том случае, если высокая концентрация антибактериального препарата в сыворотке крови (и в тканях) создана к началу оперативного вмешательства. В клинической практике оптимальное время для антибиотикопрофилактики — 30–60 мин до начала операции (при условии внутривенного введения антибиотика), т. е. в начале анестезиологических мероприятий. Отмечен значительный рост частоты возникновения послеоперационных инфекций, если профилактическая доза антибиотика была назначена не в пределах 1 ч до проведения операции. Любой антибактериальный препарат, введенный после закрытия операционной раны, не повлияет на вероятность развития осложнений.
Таким образом, однократное введение адекватного антибактериального препарата в целях профилактики не менее эффективно, чем многократное. Только при длительном оперативном вмешательстве (более 3 ч) требуется дополнительная доза. Антибиотикопрофилактика не может продолжаться более 24 ч, так как в этом случае применение антибиотика рассматривается уже как терапия, а не как профилактика.
Идеальный антибиотик, в том числе и для периоперационной профилактики, должен быть высокоэффективен, хорошо переноситься больными, обладать невысокой токсичностью. Его антибактериальный спектр должен включать вероятную микрофлору. Для пациентов, длительно находящихся в стационаре до проведения оперативного вмешательства, необходимо принимать во внимание спектр нозокомиальных микроорганизмов с учетом их антибиотикочувствительности.
Для антибиотикопрофилактики при урологических операциях желательно использовать препараты, создающие высокую концентрацию в моче. Многие антибиотики отвечают этим требованиям и могут использоваться, например цефалоспорины II поколения и ингибиторозащищенные пенициллины. Аминогликозиды должны быть зарезервированы для пациентов, входящих в группы риска или с аллергией на b-лактамы. Цефалоспорины III и IV поколений, ингибиторозащищенные аминопенициллины и карбапенемы должны использоваться в единичных случаях, когда место операции обсеменено мультирезистентными нозокомиальными микроорганизмами. Все-таки желательно, чтобы назначение этих препаратов было ограничено лечением инфекций с тяжелым клиническим течением.
Существуют общие принципы антибактериальной терапии ИМП у детей, которые включают в себя следующие правила.
При фебрильном течении ИМП начинать терапию следует с парентерального антибиотика широкого спектра (ингибиторозащищенные пенициллины, цефалоспорины II, III поколений, аминогликозиды).
Необходимо учитывать чувствительность микрофлоры мочи.
Длительность лечения пиелонефрита составляет 14 дней, цистита — 7 дней.
У детей с пузырно-мочеточниковым рефлюксом антимикробная профилактика должна быть длительной.
При бессимптомной бактериурии антибактериальная терапия не показана.
В понятие «рациональная антибиотикотерапия» должен входить не только правильный выбор препарата, но и выбор его введения. Необходимо стремиться к щадящим и в то же время наиболее эффективным методам назначения антибактериальных препаратов. При использовании ступенчатой терапии, которая заключается в смене парентерального использования антибиотика на пероральный, после нормализации температуры, врач должен помнить о следующем.
Ниже представлены антибактериальные препараты в зависимости от пути их введения.
Препараты для перорального лечения ИМП.
• II поколения: цефуроксим;
• III поколения: цефиксим, цефтибутен, цефподоксим.
Препараты для парентерального лечения ИМП.
• II поколения: цефуроксим (Цефурабол).
• III поколения: цефотаксим, цефтриаксон, цефтазидим.
• IV поколения: цефепим (Максипим).
Несмотря на наличие современных антибиотиков и химиотерапевтических препаратов, позволяющих быстро и эффективно справляться с инфекцией и уменьшать частоту рецидивов путем назначения на длительный период препаратов в низких профилактических дозах, лечение рецидивов ИМП все еще представляет собой довольно сложную задачу. Это обусловлено:
Как известно, до 30% девочек имеют рецидив ИМП в течение 1 года, 50% — в течение 5 лет. У мальчиков до 1 года рецидивы встречаются в 15–20%, старше 1 года — рецидивов меньше.
Перечислим показания к антибиотикопрофилактике.
а) пузырно-мочеточниковый рефлюкс;
Длительность антибиотикопрофилактики чаще всего определяется индивидуально. Отмена препарата осуществляется при отсутствии обострений за время профилактики, но при возникновении обострения после отмены требуется назначение нового курса.
В последнее время на отечественном рынке появился новый препарат для профилактики рецидивов ИМП. Этот препарат представляет собой лиофилизированный белковый экстракт, полученный путем фракционирования щелочного гидролизата некоторых штаммов E. coli и носит название Уро-Ваксом. Проведенные испытания подтвердили его высокую эффективность с отсутствием выраженных побочных явлений, что возлагает надежду на его широкое использование.
Важное место в лечении больных с ИМП занимает диспансерное наблюдение, которое заключается в следующем.
Литература
С. Н. Зоркин, доктор медицинских наук, профессор
НЦЗД РАМН, Москва