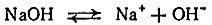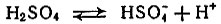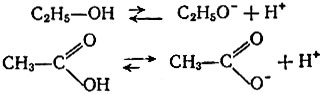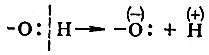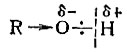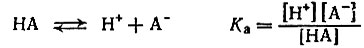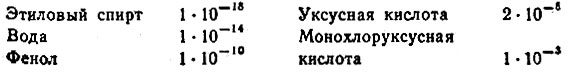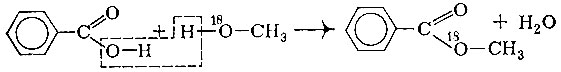Углерод кислород водород что это
Углерод, водород, кислород
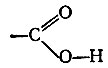
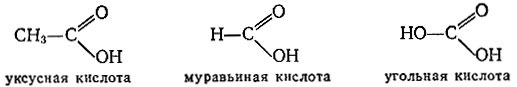
кислотная группа (карбоксил)
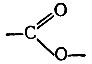
сложноэфирная группа
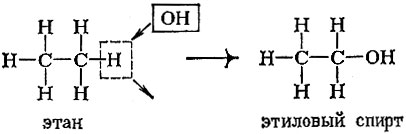
Сами названия групп многое говорят о них. Замена в молекуле углеводорода одного атома водорода на группу ОН (гидроксил) превращает углеводород в спирт. Вот как можно «перейти» от этана к этиловому спирту:
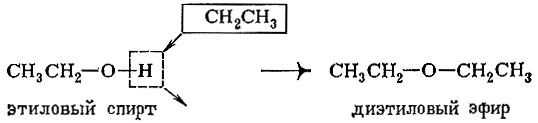
Из этилового спирта нетрудно «получить» диэтиловый эфир (обычный эфир, применяемый для наркоза). Для этого нужно водород гидроксильной группы «заменить» на радикал этил:
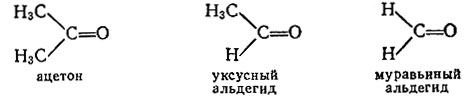
В карбонильной группе присутствует обычная двойная связь, только не между двумя углеродными атомами, а между углеродом и кислородом. Образование карбонильной группы можно представить так: в молекуле этилена один из углеродов заменяем на кислород:
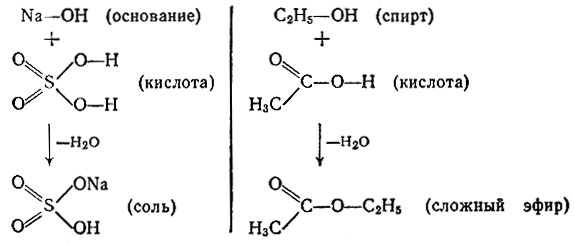
В органической химии спирты часто проявляют свойства кислот. Действительно, и кислоты и спирты при растворении в воде диссоциируют таким образом:
Поэтому и спирты, и кислоты дают с металлами соли:
Очевидно, что чем больше смещена в молекуле электронная пара к атому кислорода, тем легче отделится протон, тем легче диссоциирует соединение. В спиртах углеводородный радикал «нагнетает» электронную плотность на гидроксильную группу, электронная плотность между атомами кислорода и водорода в гидроксиле повышена, диссоциация происходит с трудом:
Мы говорим: более сильные, менее сильные. А как оценить количественно, во сколько раз одна кислота сильнее другой? Для таких оценок вводится понятие константы диссоциации кислоты. Константа эта равна произведению концентраций ионов Н+ и анионов кислоты А
, деленному на концентрацию молекул не диссоциировавшей кислоты НА:
Сопоставим константы диссоциации некоторых кислот:
Химические свойства кислородсодержащих органических соединений
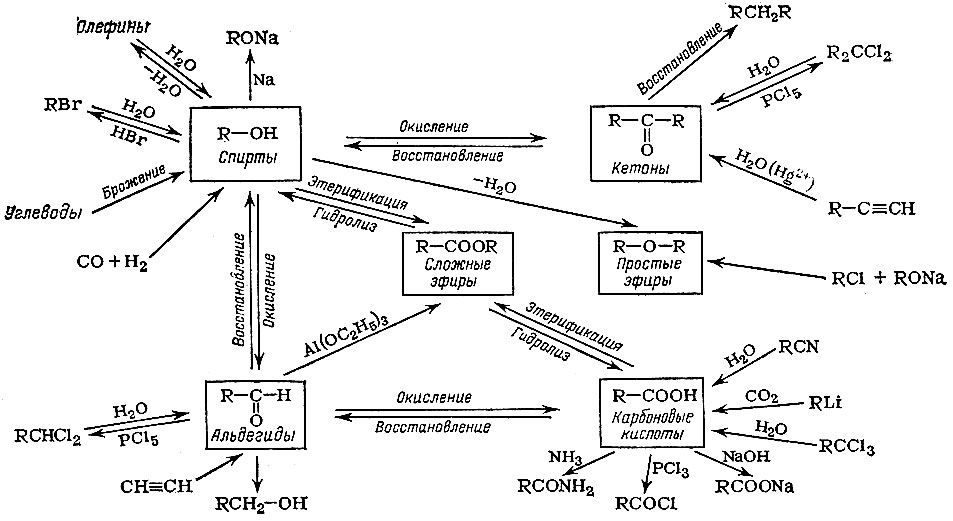
Мы не будем здесь обсуждать способы получения и свойства кислородсодержащих органических соединений. Основные реакции показаны на схеме. Отметим только, что в начале главы мы легко «превратили» в спирт этан, «заместив» атом водорода на гидроксильную группу. Разумеется, это просто только на бумаге, в действительности осуществить этот синтез довольно сложно.
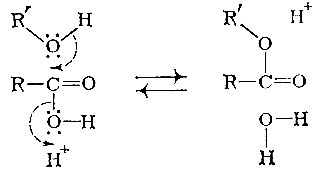
Но почему реакция идет именно так, каков ее механизм? Реакция этерификации протекает под действием иона водорода следующим образом:
Протон атакует гидроксильную группу кислоты. Разрывается связь гидроксила с углеродом и одновременно завязывается связь с подошедшим протоном, т. е. образуется вода. Молекула спирта атакует положительно заряженный углерод в остатке кислоты. При этом разрывается связь кислорода с водородом и «освободившаяся» пара электронов идет на образование новой связи с углеродом.
Реакция обратима, т. е. под действием воды и ионов Н+ сложный эфир омыляется с образованием спирта и кислоты. Для того чтобы понять, как проходит эта реакция, нужно написанное выше уравнение прочитать справа налево.
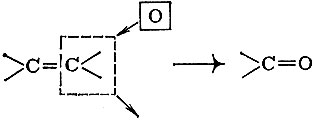
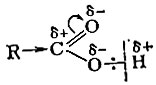
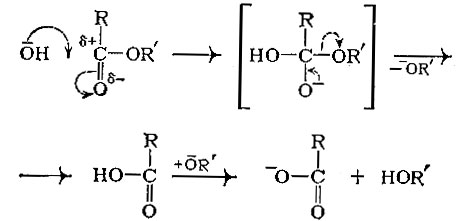
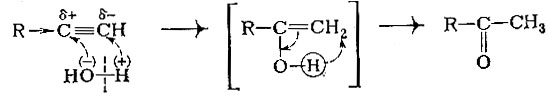
Но гидролиз сложного эфира можно провести и под действием ионов гидроксила. В этом случае первой стадией реакции будет атака отрицательно заряженного гидроксил-иона на углеродный атом, несущий частичный положительный заряд:
На этой схеме пунктирными стрелками обозначено смещение электронных пар, а в квадратные скобки заключен промежуточно образующийся комплекс.
LiveInternetLiveInternet
—Рубрики
—Музыка
—Поиск по дневнику
—Подписка по e-mail
—Постоянные читатели
—Сообщества
—Статистика
Углеводы. УглеРод, ВодоРод, КислоРод. Цитаты из Википедии.
Углеводы состоят из УглеРода, Воды: 2 ВодоРода и КислоРода.
Углево́ды — органические вещества, содержащие карбонильную группу и несколько гидроксильных групп
Гидроксильный радикал относится к реактивным формам кислорода и является наиболее активным компонентом оксидативного стресса. Он образуется в клетке в основном при восстановлении перекиси водорода в присутствии переходного металла (такого как железо).
Окислительный стресс (оксидативный стресс, от англ. oxidative stress) — процесс повреждения клетки в результате окисления
В некоторых случаях, однако, окислительный стресс используется организмом как защитный механизм. Иммунная система человека использует окислительный стресс для борьбы с патогенами, а некоторые реактивные формы кислорода могут служить посредниками в передаче сигнала
Нарушения в системе передачи сигналов могут привести к развитию рака, аутоиммунных заболеваний и диабета. Понимание механизмов передачи сигнала внутри клетки может привести к разработке методов лечения этих заболеваний и даже созданию искусственных тканей
Сахара́ — другое название низкомолекулярных углеводов: моносахаридов, дисахаридов и олигосахаридов.
Сахаров один из создателей первой советской водородной бомбы.
Её испытания состоялись 30 октября 1961/Белого Металлического Быка/ года посредством сброса с самолёта Ту-95В на ядерном полигоне «Сухой Нос» (остров Новая Земля). На обрывистых утёсах гнездится масса птиц, в особенности — гагар. 12 апреля 1961 года полет Гагарина.
Гагарин-«УглеРод 6 химический элемент»
«Сахаров и Хрущев /с Кузькиной матерью/» ВодоРод 1 химический элемент/«порождающий воду»/
но без КислоРода/порождающая кислоту/ Елена Боннэр» вода бы не образовалась, 8 химический элемент. Шутка
Влияние электромагнитных полей и излучений
Различается два типа электромагнитного излучения: ионизирующее/радиа́ция,/ и неионизирующее.
1.К ионизирующему излучению не относят видимый свет и ультрафиолетовое излучение, которые в отдельных случаях могут ионизировать вещество. Инфракрасное излучение и излучение радиодиапазонов не являются ионизирующими, поскольку их энергии недостаточно для ионизации атомов и молекул в основном состоянии
2.Радиобиология неионизирующих излучений изучает биологическое действие электромагнитных излучений, преимущественно в диапазоне частот от 3 кГц до 300 ГГц. В области постоянных и низкочастотных электромагнитных полей используют также термин магнитобиология.
Электромагнитные волны подразделяются на:
радиоволны (начиная со сверхдлинных),
терагерцевое излучение,
инфракрасное излучение,
видимый свет,
ультрафиолетовое излучение,
рентгеновское излучение и жёсткое (гамма-излучение) / Мистер Х-рентгеновские лучи Х/
Биологической активностью обладают высоковольтные линии электропередач.
Источники электромагнитных излучений, которые могут влиять на биологические объекты:
1.устройства беспроводной связи — Wi-Fi, Bluetooth, мобильные телефоны, высокочастотные средства связи;
2.компьютеры, мониторы, ТВ-экраны;
3.микроволновые печи, люминесцентные лампы, электрические моторы.
В опытах на животных изучались ЭМП/электро-магнитное поле/50 и 60 Гц. Воздействие ЭМП, подобно свету, непосредственно влияет на шишковидную железу, ухудшая биологический эффект мелатонина. Мелатонин регулирует ритмы гонадотропин-высвобождающих гормонов в гипоталамусе, влияя на фолликулостимулирующий гормон (ФСГ) и лютеинизирующий гормон (ЛГ), [15] а также эффективно снижает окислительный стресс.[16] Это может изменить производство половых гормонов, что приведет к изменениям в сперматогенезе и маскулинизации/процесс накопления вторичных половых признаков мужского пола у особи женского пола/.
Яркий свет блокирует синтез мелатонина, в то время как в темноте циркадный ритм выбросов мелатонина сохраняется благодаря ритмам супрахиазматического ядра./не было света раньше, детей было много/
Таким образом, в темноте секреция мелатонина усиливается, а днём — уменьшается
Радиационная травма живых клеток в значительной степени обусловлена образованием свободных радикалов. Наиболее часто поврежденной биомолекулой из-за ионизирующего излучения является ДНК. Воздействие ионизирующего излучения считается канцерогенным.
Рене Декарт назвал эпифиз/шишковидную железу/ «вместилищем души», будучи убеждённым в его уникальном месте в анатомии человеческого мозга, как структуры, которая является непарной.
H-водород, O-кислород, С-углерод.
Баяны
183K постов 12.1K подписчиков
Правила сообщества
Сообщество для постов, которые ранее были на Пикабу.
по-моему этот педагог не соответствует моральному образу учителя, да Тимурка?
Главное не курить во время сборки
Неуглеродные формы жизни
Неуглеродные формы жизни и альтернативная биохимия включает жизнь на основе кремния и кислорода, азота и фосфора, азота и водорода.
Главным претендентом на роль структурообразующего атома в альтернативной биохимии считается кремний. Он расположен в той же группе периодической системы, что и углерод, поэтому свойства их похожи. Но атомы кремния имеют большую массу и больший радиус, они сложнее образуют ковалентную связь, и это может помешать образованию биополимеров (класс полимеров, который встречается в природе в естественном виде и входит в состав живых организмов: белки, нуклеиновые кислоты, полисахариды, лигнин – NS). Кроме того, соединения кремния не столь разнообразны, как соединения углерода.
В то же время, например, соединения кремния и водорода – силаны – являются более жаропрочными, чем углеродно-водородные соединения. Поэтому ученые полагают, что кремниевая жизнь может существовать на планетах, средняя температура которых значительно превышает земную. В этом случае природным растворителем должна быть не животворящая для землян вода, а соединения с более высокой температурой кипения и плавления.
В декабре 2010 года исследователь из NASA Astrobiology Research Фелиса Вольфе-Симон сообщила об открытии бактерии GFAJ-1 из рода Halomonadaceae, способной при определенных условиях заменять фосфор мышьяком.
Соединения кремния, как считается, также должны быть более устойчивыми к серной кислоте. А вот по отношению к другим средам кремниевые соединения считаются менее устойчивыми по сравнению с углеродными.
Подобно углероду, фосфор может составлять цепочки из атомов, которые, в принципе, могли бы образовывать сложные макромолекулы, если бы он не был таким активным. Впрочем, в комплексе с азотом возможен вариант образования более сложных ковалентных связей, что делает возможным и возникновение большого разнообразия молекул, включая кольцевые структуры.
В атмосфере нашей планеты около 78% азота, но в силу инертности двухатомного азота энергетическая «стоимость» образования трехвалентной связи слишком высока. В то же время некоторые растения могут связывать азот из почвы в симбиозе с анаэробными бактериями, которые живут в их корневой системе. Если в атмосфере будет присутствовать значительное количество диоксида азота или аммиака, доступность азота будет выше. Кроме того, атмосфера экзопланет может быть насыщена и другими оксидами азота.
В аммиачной атмосфере растения, молекулы которых состоят из фосфора и азота, получали бы азот из атмосферы, а фосфор – из почвы. Клетки их окисляли бы аммиак для того, чтобы образовать аналоги моносахаридов, а водород выделялся бы как побочный продукт. Поэтому животные в таком случае будут вдыхать водород, расщепляя аналоги полисахаридов до аммиака и фосфора. Таким образом, энергетические цепочки формировались бы в обратной последовательности по сравнению с тем, что мы наблюдаем на Земле (на нашей планете в данном случае был бы распространен метан).
Авторское представление об экзопланете, на которой аммиак выполняет функцию воды / ©Ittiz
Недавно, по словам теоретика-кристаллографа, химика, физика и материаловеда, популяризатора науки Артема Оганова, их группа установила одну интересную особенность соединений азота и водорода. Выяснилось, что сжатые азотоводороды могут давать гораздо более разнообразную химию, нежели углеводороды (причем эти соединения существуют в термодинамически стабильном состоянии). А ведь именно разнообразие углеводородов, как было сказано выше, дает нам такую биологическую вариативность.
Между тем азотоводородов во Вселенной очень много. Так, планеты Уран и Нептун на 8% состоят из аммиака (относящегося к простейшим азотоводородам), которого там намного больше, чем на Земле. Помимо всего прочего соединения азота и водорода имеют низкую температуру плавления, которая растет с давлением (как и температура в недрах планет).
«Для ковалентных соединений азота с очень сильными направленными связями тоже будет характерна метастабильность – иными словами, мало того, что под давлением есть необычайно большое число стабильных соединений, там еще будет практически неограниченное число метастабильных соединений, – пишет Артем Оганов. – А если туда начать добавлять другие атомы: кислород, серу, – то химическое разнообразие превысит разнообразие органической химии. Это та область химии, которую мы пока что практически не знаем и которая вышла из наших расчетов».
Возможна ли жизнь на таких планетах, как Уран и Нептун? Неизвестно. «Потенциальная проблема состоит в том, что время жизни метастабильных соединений в планетных условиях (высокие температуры и давления) может оказаться недостаточно долгим», – заключает химик.
Углерод. Химия углерода и его соединений
Углерод
Положение в периодической системе химических элементов
Углерод расположен в главной подгруппе IV группы (или в 14 группе в современной форме ПСХЭ) и во втором периоде периодической системы химических элементов Д.И. Менделеева.
Электронное строение углерода
Электронная конфигурация углерода в основном состоянии :
+6С 1s 2 2s 2 2p 2 1s 

Электронная конфигурация углерода в возбужденном состоянии :
+6С * 1s 2 2s 1 2p 3 1s 

Атом углерода содержит на внешнем энергетическом уровне 2 неспаренных электрона и 1 неподеленную электронную пару в основном энергетическом состоянии и 4 неспаренных электрона в возбужденном энергетическом состоянии.
Физические свойства
Углерод в природе существует в виде нескольких аллотропных модификаций: алмаз, графит, карбин, фуллерен.
Графит — мягкое вещество серо-стального цвета, с металлическим блеском. Хорошо проводит электрический ток. Жирный на ощупь.
Карбин — вещество, в составе которого атомы углерода находятся в sp-гибридизации. Состоит из цепочек и циклов, в которых атомы углерода соединены двойными и тройными связями. Карбин — мелкокристаллический порошок серого цвета.
[=C=C=C=C=C=C=]n или [–C≡C–C≡C–C≡C–]n
Фуллерен — это искусственно полученная модифицикация углерода. Молекулы фуллерена — выпуклые многогранники С60, С70 и др. Многогранники образованы пяти- и шестиугольниками, в вершинах которых расположены атомы углерода.
Фуллерены — черные вещества с металлическим блеском, обладающие свойствами полупроводников.
В природе углерод встречается как в виде простых веществ (алмаз, графит), так и в виде сложных соединений (органические вещества — нефть, природные газ, каменный уголь, карбонаты).
Качественные реакции
Видеоопыт взаимодействия карбоната кальция с соляной кислотой можно посмотреть здесь.
Качественная реакция на углекислый газ CO2 – помутнение известковой воды при пропускании через нее углекислого газа:
При дальнейшем пропускании углекислого газа осадок растворяется, т.к. карбонат кальция под действием избытка углекислого газа переходит в растворимый гидрокарбонат кальция:
Видеоопыт взаимодействия гидроксида кальция с углекислым газом (качественная реакция на углекислый газ) можно посмотреть здесь.
Соединения углерода
Наиболее типичные соединения углерода:
| Степень окисления | Типичные соединения |
| +4 | оксид углерода (IV) CO2 гидрокарбонаты MeHCO3 |
| +2 | оксид углерода (II) СО муравьиная кислота HCOOH |
| -4 | метан CH4 карбиды металлов (карбид алюминия Al4C3) бинарные соединения с неметаллами (карбид кремния SiC) |
Химические свойства
При нормальных условиях углерод существует, как правило, в виде атомных кристаллов (алмаз, графит), поэтому химическая активность углерода — невысокая.
1.1. Из галогенов углерод при комнатной температуре реагирует с фтором с образованием фторида углерода:
1.2. При сильном нагревании углерод реагирует с серой и кремнием с образованием бинарного соединения сероуглерода и карбида кремния соответственно:
C + 2S → CS2
C + Si → SiC
При взаимодействии углерода с водородом образуется метан. Реакция идет в присутствии катализатора (никель) и при нагревании:
1.4. С азотом углерод реагирует при действии электрического разряда, образуя дициан:
2С + N2 → N≡C–C≡N
1.5. В реакциях с активными металлами углерод проявляет свойства окислителя. При этом образуются карбиды:
2C + Ca → CaC2
при недостатке кислорода образуется угарный газ СО:
2C + O2 → 2CO
Алмаз горит при высоких температурах:
Горение алмаза в жидком кислороде:
Графит также горит:
Графит также горит, например, в жидком кислороде:
Графитовые стержни под напряжением:
2. Углерод взаимодействует со сложными веществами:
2.1. Раскаленный уголь взаимодействует с водяным паром с образованием угарного газа и водорода:
C 0 + H2 + O → C +2 O + H2 0
ZnO + C → Zn + CO
Также углерод восстанавливает железо из железной окалины:
4С + Fe3O4 → 3Fe + 4CO
При взаимодействии с оксидами активных металлов углерод образует карбиды.
3С + СаО → СаС2 + СО
2.3. Концентрированная серная кислота окисляет углерод при нагревании. При этом образуются оксид серы (IV), оксид углерода (IV) и вода:
2.4. Концентрированная азотная кислотой окисляет углерод также при нагревании. При этом образуются оксид азота (IV), оксид углерода (IV) и вода:
Карбиды
| Ковалентные карбиды | Ионные карбиды | ||
| Метаниды | Ацетилениды | Пропиниды | |
| Это соединения углерода с неметаллами Например : Например : Например : Это соединения с металлами, при гидролизе которых образуется пропин Например : Mg2C3 | |||
| Частицы связаны ковалентными связями и образуют атомные кристаллы. Поэтому ковалентные карбиды химически стойкие. Окисляются только сильными окислителями | Метаниды разлагаются водой или кислотами с образованием метана и гидроксида или соли: Например : Al4C3 + 12H2O → 4Al(OH)3 + 3CH4 | Ацетилениды разлагаются водой или кислотами с образованием ацетилена и гидроксида или соли: Например: СаС2+ 2Н2O → Са(OH)2 + С2Н2 | |