Углерод — основа жизни всех органических молекул
Углерод — элемент номер шесть. Прямо в середине первой строки периодической таблицы химических элементов. Ну и что? Углерод основа жизни – это самый важный элемент живых организмов. Без этого элемента жизнь, какой мы ее знаем, не существовала бы.
Как вы увидите, шестой элемент периодической таблицы является центральным в соединениях, необходимых для жизни.
Значение углерода
Соединение, содержащееся главным образом в живых организмах, известно как органическое соединение.
Органические соединения составляют клетки и другие структуры организмов и осуществляют жизненные процессы. Углерод является основным элементом в органических соединениях, поэтому элемент необходим для жизни на Земле. Углерод основа жизни и она, какой мы ее знаем, не могла бы существовать. Теоретически, вроде бы возможны другие формы жизни, но человечество их не знает.
Соединения
Соединение — это вещество, состоящее из двух или более элементов. Соединение имеет уникальный состав, который всегда один и тот же. Мельчайшая частица соединения называется молекулой. Рассмотрим в качестве примера воду. Молекула воды всегда содержит один атом кислорода и два атома водорода. Состав воды выражается химической формулой H2O. Вода не является органическим соединением. Молекула воды всегда имеет такой состав: один атом кислорода и два атома водорода.
Что заставляет атомы молекулы воды «слипаться» вместе? Ответ — химические связи. Химическая связь-это сила, которая удерживает молекулы вместе. Химические связи образуются, когда вещества вступают в реакцию друг с другом. Химическая реакция-это процесс, который превращает одни химические вещества в другие. Для образования соединения необходима химическая реакция. Для разделения веществ в соединении необходима еще одна химическая реакция.
Почему этот элемент главный для жизни
Почему углерод так важен для жизни? Причина — способность образовывать устойчивые связи со многими элементами, в том числе и с самим собой. Это свойство позволяет шестому элементу образовывать огромное разнообразие очень больших и сложных молекул.
Однако миллионы органических соединений можно разделить всего на четыре основных типа: углеводы, липиды (жиры), белки и нуклеиновые кислоты.
Вы можете сравнить четыре типа в таблице ниже:
| Элементы | Тип соединений | Состав | Функции | Мономер (повторяющиеся звенья) |
| Углеводы | сахар, крахмал | углерод, водород, кислород | снабжает энергией клетки, накапливает энергию, формирует структуры тела | моносахарид |
| Липиды (жиры) | жирное масло | накапливает энергию, формирует клеточные мембраны, несет сообщения. | ||
| Белки | ферменты, антитела | помогает клеткам сохранять форму, формирует мышцы, ускоряет химические реакции, несет сообщения и материалы. | аминокислота | |
| Нуклеиновые кислоты | ДНК-РНК | содержит инструкции для белков, передает инструкции от родителей к потомству, помогает производить белки | нуклеотид Углеводы, белки и нуклеиновые кислоты-это крупные молекулы (макромолекулы), построенные из более мелких молекул (мономеров) в результате реакций дегидратации. В реакции дегидратации вода удаляется по мере соединения двух мономеров. Возникновение «жизненного» элемента углеродаКаждый атом углерода, находящийся на Земле и во Вселенной, возник в ядре красных гигантов при температуре около 100 миллионов градусов. Атомы углерода как сказано выше, являются основой любого живого организма, ибо обладают способностью соединяться в длинные цепочки и создавать сложные органические молекулы. Углеродные атомы, из которых построен человеческий организм и биосфера в целом, возникали в те далекие времена, когда еще не существовали Солнце и Солнечная система, когда не было еще даже полимерной цепи, из которой позднее родилось Солнце и все его семейство. Именно в звездах-гигантах возникали тогда из атомов гелия атомы углерода. Это произошло более семи миллиардов лет тому назад. Из звезд атомы углерода потом попали в межзвездное пространство. Там они смешались с межзвездным веществом, из которого позднее возникли полимерные цепи, включая и создание нашей Солнечной системы. Таким образом, углерод основа жизни которая переместилась из недр старых красных гигантов на нашу планету, а отсюда в земные растения и, наконец, вместе с пищей — в человеческий организм. Именно тогда зародилась жизнь на Земле. Можно сказать, что без красных гигантов, существовавших семь миллиардов лет назад, на Земле не было бы углерода, а, следовательно, и жизни. Итак, с точки зрения астрономии нашими далекими предками являются именно красные гиганты. Углерод — основа жизни на ЗемлеМы посвятили две статьи воздуху, без которого жизнь на нашей Углерод — простое неорганическое вещество, элемент таблицы Менделеева. Обозначается буквой «С» (Carboneum). В виде алмазов, графита и древесного угля известен человечеству с древнейших времен. Название carbone (углерод) впервые было введено в химическую науку французскими учеными. А. Лавуазье доказал, что уголь — это элементарное химическое вещество, а не носитель некоего невесомого флюида флогистона, отвечающего за горючие свойства веществ. Он же установил, что алмаз — это кристаллическая форма углерода. Три формы углеродаУглерод — удивительное вещество, физические свойства которого и даже внешний вид описать однозначно просто невозможно. Этот элемент — рекордсмен по количеству аллотропных модификаций. Три формы углерода:
Вещества, относящиеся к аморфным формам, не являются чистой формой углерода, но содержат углерод в очень значительных количествах. Для аморфного углерода характерна высокая теплоемкость, свойства полупроводников, невысокая плотность, относительно невысокая термостойкость — при температуре выше 1600 °С он превращается в графит. Как правило, их основой являются разные формы мелкокристаллического графита в виде неупорядочной структуры. Углеродные кластеры — сложные соединения с очень интересными свойствами. Им, а также другим перспективным материалам на основе углерода, мы посвятим одну из ближайших статей. Химические свойстваС химическими свойствами немного проще. В нормальных условиях углерод практически не вступает в реакции с другими элементами и веществами, инертен к кислотам, щелочам, галогенам. При высоких температурах проявляет сильные восстановительные свойства. Наиболее химически активны аморфные виды углерода, наиболее инертны — кристаллические. Графит по химической активности занимает серединное положение. При высоких температурах углерод окисляется кислородом (горит), образует несколько видов оксидов. Графит и аморфный углерод при высоких температурах Главное свойство углерода — способность соединяться в длинные цепи, причем эти цепи могут содержать как атомы углерода, так и другие атомы. Цепи могут замыкаться, разветвляться, образовывать циклы, быть разной длины, соединяться («сшиваться») между собой в разнообразные структуры. Такие углеродно-водородные цепи — основа всей органической химии. Следующая статья будет о содержании углерода в природе, его опасности и сферах применения. Углерод химические и физические свойства Углерод – это, наверное, один из самых впечатляющих элементов химии на нашей планете, который обладает уникальной способностью образовывать огромное множество различных органических и неорганических связей. Одним словом, углеродные соединения, которые обладают уникальными характеристиками – основа жизни на нашей планете. Что такое углерод В химической таблице Д.И. Менделеева углерод находится под шестым номером, входит в 14 группу и носит обозначение «С». Физические свойстваЭто водородное соединение, входящее в группу биологических молекул, молярная масса и молекулярная масса которого – 12,011, температура плавления составляет 3550 градусов. В агрегатном состоянии углерод твердое вещество, а кристаллическая решетка атомная. Углерод имеет следующие аллотропные модификации: Строение атомаАтом вещества имеет электронную конфигурацию вида 1S22S22P2. На внешнем уровне у атома 4 электрона, находящиеся на двух разных орбиталях. Если же брать возбужденное состояние элемента, то его конфигурация становится 1S22S12P3. К тому же атом вещества может быть первичным, вторичным, третичным и четвертичным. Химические свойства Пребывая в нормальных условиях, элемент инертен и во взаимодействие с металлами и неметаллами вступает при повышенных температурах: Получение углеродаУглерод в природе можно найти в виде черного графита либо же, что очень редко, в виде алмаза. Ненатуральный графит получают с помощью реакции кокса с кремнеземом. А ненатуральные алмазы получают, применяя тепло и давление вместе с катализаторами. Так металл расплавляется, а получившийся алмаз выходит в виде осадка. Добавление азота приводит к получению желтоватых алмазов, а бора – голубоватых. История открытияУглерод использовался людьми с давних времен. Грекам был известен графит и уголь, а алмазы впервые нашлись в Индии. К слову, в качестве графита люди часто принимали схожие по виду соединения. Но даже несмотря на это, графит широко использовался для письма, ведь даже слово «графо» с греческого языка переводится как «пишу». В настоящее время графит используется так же в письме, в частности его можно встретить в карандашах. В начале 18 века в Бразилии началась торговля алмазами, были открыты многие месторождения, а уже во второй половине 20 века люди научились получать ненатуральные драгоценные камни. На настоящий момент ненатуральные алмазы используются в промышленности, а настоящие – в ювелирной сфере. Роль углерода в организме человекаВ тело человека углерод попадает вместе с пищей, в течение суток – 300 г. А общее количество вещества в человеческом организме составляет 21% от массы тела. Из данного элемента состоят на 2/3 мышцы и 1/3 костей. А выводится из тела газ вместе с выдыхаемым воздухом либо же с мочевиной. Стоит отметить: без этого вещества жизнь на Земле невозможна, ведь углерод составляет связи, помогающие организму бороться с губительным влиянием окружающего мира. Таким образом, элемент способен составлять продолжительные цепи либо же кольца атомов, которые представляют собой основу для множества других важных связей. Нахождение в природе углеродаЭлемент и его соединения можно встретить повсюду. В первую очередь отметим, что вещество составляет 0,032% от общего количества земной коры. Одиночный элемент можно встретить в каменном угле. А кристаллический элемент находится в аллотропных модификациях. Также в воздухе постоянно растет количество углекислого газа. Большую концентрацию элемента в окружающей среде можно встретить в качестве соединений с различными элементами. Например, двуокись углерода содержится в воздухе в количестве 0,03%. В таких минералах как известняк или же мрамор, содержатся карбонаты. Все живые организмы несут в себе соединения углерода с иными элементами. К тому же остатки живых организмов становятся такими отложениями, как нефть, битум. Применение углерода Соединения этого элемента широко используются во всех сферах нашей жизни и перечислять их можно бесконечно долго, поэтому мы укажем несколько из них: Углерод это что для человекаУглерод образует четыре простых вещества – алмаз, графит, карбины и фуллерены, которые резко отличаются между собой по своим свойствам. Алмаз является бесцветным кристаллом и самым твердым из минералов. Он имеет высокий коэффициент преломления и обладает свойствами диэлектрика. Благодаря этим свойствам алмаз широко применяется в промышленности. Графит встречается в природе гораздо чаще, чем алмаз. Графит – это такая форма углерода, в которой каждый атом углерода связан с тремя соседями, образуя плоскую сетку. В результате он имеет слоистую структуру, причем связь между слоями осуществляется в основном за счет относительно слабых межмолекулярных сил. Все это определяет свойства графита – он мягок, легко расслаивается, хорошо проводит тепло, имеет серый цвет и металлический блеск, заметно электропроводен. Сажа, древесный уголь и другие угли, получаемые из органического и неорганического сырья, представляют собой мелкокристаллический графит, так что обычно термином «углерод» обозначают именно графит той или иной степени дисперсности. При стандартных условиях графит весьма инертен, но значительно более активен, чем алмаз. Он не реагирует с кислородом, водородом, галогенами. На него не действуют растворы кислот и щелочей. При нагревании графит сгорает в кислороде или на воздухе с образованием СО2. С другими неметаллами, кроме фтора и серы, он непосредственно не реагирует. Взаимодействие с металлами возможно только при высоких (1000-2000 ° С) температурах, а с водородом – еще и при высоких давлениях. Низкая реакционная способность графита позволяет использовать его как материал для тиглей, электродов, как замедлитель нейтронов в ядерных реакторах. Резкое различие в свойствах алмаза и графита обусловлено различным строением их кристаллов. Третья форма существования углерода – карбин – черный мелкокристаллический порошок, имеющий полупроводниковые свойства. Карбины более активны, чем графит. Четвертая форма – фуллерены. В них атомы углерода связаны многоцентровыми связями. При этом образуются правильные многогранники, в вершинах которых располагаются атомы. Наиболее характерны системы, содержащие 60 или 70 атомов, представляющие собой практически сферические частицы. Наиболее известны два оксида углерода. Оксид углерода СО – монооксид, угарный газ. При нормальных условиях не имеет цвета и запаха. Достаточно инертен при нормальных условиях. Он практически не растворяется в воде и с ней не реагирует. Молекула СО имеет самую высокую энергию связи среди двухатомных молекул, состоящих из разных атомов. Несмотря на высокую прочность СО легко сгорает, образуя СО2. Реакция протекает самопроизвольно с выделением большого количества тепла. Оксид углерода СО2 – диоксид углерода, углекислый газ – получается при сгорании любых углеродсодержащих веществ в присутствии воздуха. Является продуктом дыхания живых существ. Диоксид углерода проявляет отчетливые кислотные свойства. Он легко реагирует со щелочами и основными оксидами, образуя соли угольной кислоты – карбонаты. Диоксид углерода плохо растворим в воде. В природе углерод сосредоточен в карбонатных породах – известняках (СаСО3), образующих громадные залежи, и некоторых других карбонатах (MgСО3). Количество соединений углерода столь велико, что для их описания потребовалось выделить самостоятельное направление в химии – органическую химию. Число известных органических соединений углерода превышает 10 миллионов, тогда как число соединений всех остальных элементов составляет примерно 120 тысяч. Содержание в человеческом организме(вернуться к оглавлению)Так как углерод является основой всех соединений органической химии, то в человеческом организме он присутствует повсеместно. Он входит в состав аминокислот, составных частей белков, представляющих основу жизнедеятельности. Помимо этого, углерод является компонентом жиров и углеводов, веществ, обеспечивающих процесс жизнедеятельности живых организмов. Содержание в человеческом организме в процентном отношении к массе тела составляет 21 % от массы тела. Из них костная ткань – 36 %, мышечная ткань – 67 %. Биологическая роль(вернуться к оглавлению)Как уже было сказано выше, углерод является основной составляющей всех органических форм жизни. Он входит в состав белков, жиров, углеводов, нуклеиновых кислот, гормонов, ферментов, витаминов, то есть можно сказать, что углерод в той или иной степени важен для всех органов и систем живого организма, и всех, протекающих в них процессов, поддерживающих его жизнедеятельности. Углекислота (СО2), содержащаяся в крови, возбуждает дыхательный центр, расширяет мозговые сосуды, повышает возбудимость сердечной мышцы. Гидрокарбонаты калия (KHСО3) и натрия (NaHCO3) входят в состав буферных систем крови и тканей, поддерживающих рН организма. Уксусная кислота (СH3COОН) принимает участие в синтезе холестерина. Источники(вернуться к оглавлению)Основным источником углерода является пища, состоящая все из тех же углеродсодержащих веществ – белков, жиров, углеводов и других. При попадании в организм эти вещества под действие пищеварительной системы распадаются до мономеров, которые в дальнейшем используются нашим организмом для собственных нужд. В основе этого процесса лежат соединения, в состав которых входит углерод. Суточная потребность(вернуться к оглавлению)Суточная потребность углерода не нормируется, но существуют нормы потребления вышеперечисленных органических веществ с пищей, в состав которых входит углерод. Недостаток и избыток(вернуться к оглавлению)Вряд ли, представляется возможным оценить, как на организм влияет недостаток углерода, поскольку он входит в состав почти всех необходимых человеку веществ. Поэтому можно оценивать влияние нехватки лишь конкретных его соединений. То же относится и к избытку углерода. Например, при избытке углекислого газа СО2 в окружающей атмосфере наступает кислородное голодание. Токсичность(вернуться к оглавлению)Свободный углерод в виде сажи токсичен для человека. Длительный контакт с сажей или угольной пылью вызывает рак. Мельчайшая пыль угля вызывает изменение структуры легких, и как следствие нарушение их функций. Углерод в природе; его опасность и сферы примененияВ природе углерода не так уж и много, но он есть везде: В чистом виде и в значимых количествах углерод встречается только в виде алмазов и графитов. Но он — составная часть ископаемого топлива (уголь, нефть, газ, сланцы), торфа, битумов, природных минералов (мел, известняк, доломиты, карбонаты). Токсическое действие
Угарный газ и углекислый газ обладают токсическим действием, превышение ПДК этих газов в воздухе может вызвать летальный исход. Поэтому в закрытых помещениях большое внимание должно уделяться поглощению и удалению из воздуха углекислоты, выделяемой при дыхании. Токсическим действием обладает радиоактивный изотоп С-14. Встраиваясь в молекулы белков, особенно в ДНК и РНК, он может оказывать мутагенное воздействие, поэтому для него тоже установлены ПДК содержания в воздухе рабочего помещения. ПрименениеНет ни одной области промышленности, в которой в той или иной степени не использовался бы углерод. Расскажем об основных сферах его использования: • Основные виды ископаемого топлива на земле: нефть, уголь и газ — это соединения углерода. Они нужны для получения тепла, энергии, огромного количества химических материалов. |

 планете была бы невозможна. Теперь поговорим об углероде — элементе, который является основой жизни на земле. Ученые, уфологи и фантасты даже ввели в обиход термин «углеродная жизнь». И он вполне справедлив, так как все белки, аминокислоты, жиры, ДНК и РНК построены на основе углеводородных молекул.
планете была бы невозможна. Теперь поговорим об углероде — элементе, который является основой жизни на земле. Ученые, уфологи и фантасты даже ввели в обиход термин «углеродная жизнь». И он вполне справедлив, так как все белки, аминокислоты, жиры, ДНК и РНК построены на основе углеводородных молекул. Молекулы кристаллического углерода характеризуются правильной кристаллической решеткой. Большинство форм кристаллического углерода отличаются очень высокой твердостью и тугоплавкостью. Алмаз обладает высокой плотностью, почти не проводит тепло и ток. Графит, наоборот, имеет невысокую плотность и слоистое строение; проводит ток, может возгоняться, минуя жидкое состояние.
Молекулы кристаллического углерода характеризуются правильной кристаллической решеткой. Большинство форм кристаллического углерода отличаются очень высокой твердостью и тугоплавкостью. Алмаз обладает высокой плотностью, почти не проводит тепло и ток. Графит, наоборот, имеет невысокую плотность и слоистое строение; проводит ток, может возгоняться, минуя жидкое состояние.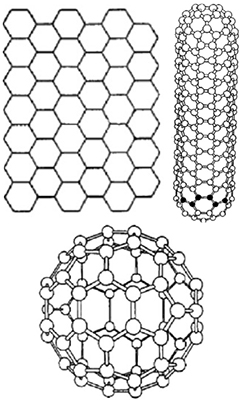 реагируют с водородом, азотом, фтором, галогенами, щелочными металлами, солями металлов, серой. В результате реакции с водородом и азотом получается синильная кислота. Взаимодействие большинства металлов, углерода, бора и кремния приводит к образованию карбидов. Углерод восстанавливает оксиды металлов до металлов. При определенных условиях удается преобразовать углерод, содержащийся в твердых видах топлива, в горючие газы (реакция газификации топлив очень важна для промышленности).
реагируют с водородом, азотом, фтором, галогенами, щелочными металлами, солями металлов, серой. В результате реакции с водородом и азотом получается синильная кислота. Взаимодействие большинства металлов, углерода, бора и кремния приводит к образованию карбидов. Углерод восстанавливает оксиды металлов до металлов. При определенных условиях удается преобразовать углерод, содержащийся в твердых видах топлива, в горючие газы (реакция газификации топлив очень важна для промышленности).

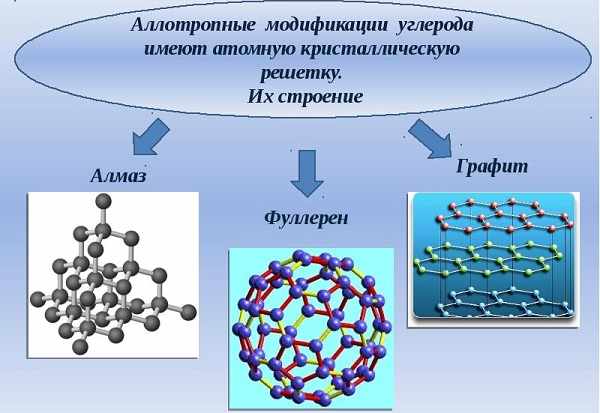
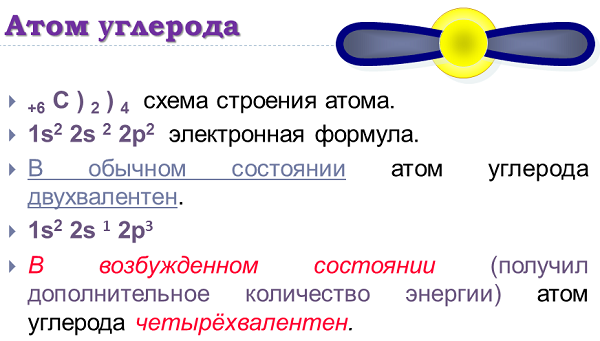
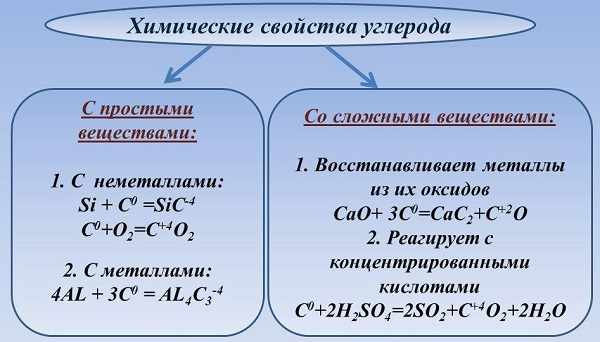





 в воздухе (углекислый газ и угарный газ), растворен в океанах и реках, залегает в ископаемых породах в земле, содержится в каждой клетке растения, животного, человека. Существует круговорот углерода в природе:
в воздухе (углекислый газ и угарный газ), растворен в океанах и реках, залегает в ископаемых породах в земле, содержится в каждой клетке растения, животного, человека. Существует круговорот углерода в природе:  При разработках угольных месторождений, при сжигании топлив, в процессе деятельности человека в воздух поступает большое количество аэрозолей углерода, попадающих в органы дыхания человека и животных. Регулярное вдыхание аэрозолей с высокой концентрацией углерода приводят к таким заболеваниям, как пылевой бронхит, антракоз. На всех производствах, связанных с углеродными аэрозолями и пылью, обязательно нормируется ПДК содержания алмазов, кокса, угля, углеродной пыли, сажи и др. Работники обязательно должны использовать средства защиты органов дыхания при работе с ними.
При разработках угольных месторождений, при сжигании топлив, в процессе деятельности человека в воздух поступает большое количество аэрозолей углерода, попадающих в органы дыхания человека и животных. Регулярное вдыхание аэрозолей с высокой концентрацией углерода приводят к таким заболеваниям, как пылевой бронхит, антракоз. На всех производствах, связанных с углеродными аэрозолями и пылью, обязательно нормируется ПДК содержания алмазов, кокса, угля, углеродной пыли, сажи и др. Работники обязательно должны использовать средства защиты органов дыхания при работе с ними.



