Лимфодиссекцией (или иначе лимфаденэктомией) называется хирургическое удаление лимфатических узлов при злокачественных опухолях. Лимфодиссекция не является самостоятельной операцией, а представляет собой часть хирургического противоопухолевого лечения.
Для чего проводится лимфодиссекция?
Злокачественные опухоли отличает способность образовывать метастазы, выходя за пределы первичного очага и начиная развиваться в других органах и тканях. Раковые клетки отделяются от первичной опухоли и распространяются по организму с током крови и лимфы, поражая в том числе и сами лимфатические узлы – сначала ближайшие.
Поэтому удаление вместе с первичной опухолью лимфатических узлов позволяет приостановить и даже предотвратить развитие метастазов. Результаты исследования удаленных при лимфодиссекции узлов помогают в составлении оптимальной программы дальнейшего лечения. Таким образом лимфодиссекция сочетает в себе непосредственно лечебную и диагностическую функции.
Показания к лимфодиссекции
Необходимость лимфодиссекции зависит от агрессивности конкретного заболевания и степени распространенности опухоли, то есть стадии рака.
Некоторые опухоли почти не метастазируют, поэтому при их лечении лимфодиссекция не применяется. Это, например, базальноклеточный рак. По той же причине в лимфодиссекции обычно нет необходимости на ранних стадиях рака.
Однако, для быстро метастазирующих видов рака лимфодиссекция является обязательной составляющей радикального лечения. При невозможности её проведения опухоль признается неоперабельной. Это касается, например, рака желудка, панкриатической карциномы, немелкоклеточной карциномы легкого.
В случае ряда заболеваний, — например, раке молочной железы, меланоме, плоскоклеточной карциноме кожи, — прежде чем проводить лимфодиссекцию, делают биопсию сторожевого лимфоузла, чтобы определить наличие в нем метастазов.
Сторожевым узлом называется ближайший на пути распространения опухоли лимфоузел. Чтобы обнаружить его, проводят картирование, выделяя пораженные ткани с помощью меченых изотопов или красящего вещества. После обнаружения сторожевой узел удаляется и передается на морфологическое исследование. Если в данном узле не выявлено следов поражения, то лимфодиссекцию не назначают, так как вероятность появления метастазов минимальна. Если же в сторожевом узле обнаружены опухолевые клетки, то без проведения лимфодиссекции прогноз ухудшается.
Метастатическое поражение шейных лимфатических узлов
Шейные лимфатические узлы являются частым местом метастазирования злокачественных опухолей, первичный очаг которых располагается в области головы и шеи. К ним, например, относятся плоскоклеточный рак верхних отделов дыхательных путей, а также метастазы рака слюнных желез и щитовидной железы.
Наиболее распространенным клиническим признаком является увеличивающееся образование шеи, которое обычно обнаруживается пациентом или его врачом. При подозрении на метастатическое поражения лимфатических узлов шеи для диагностики и определения наилучшей тактики лечения потребуется осмотр врачом-онкологом, инструментальные методы и биопсия.
Иногда новообразования вне области головы и шеи могут неожиданно метастазировать в шейные лимфатические узлы, что требует особенно тщательной диагностики для выявления первичного очага.
Лечение будет зависеть от типа и локализации первичной опухоли, которая распространилась в лимфатические узлы шеи, и, скорее всего, будет включать в себя комбинацию хирургического вмешательства, лучевой терапии и/или химиотерапии.
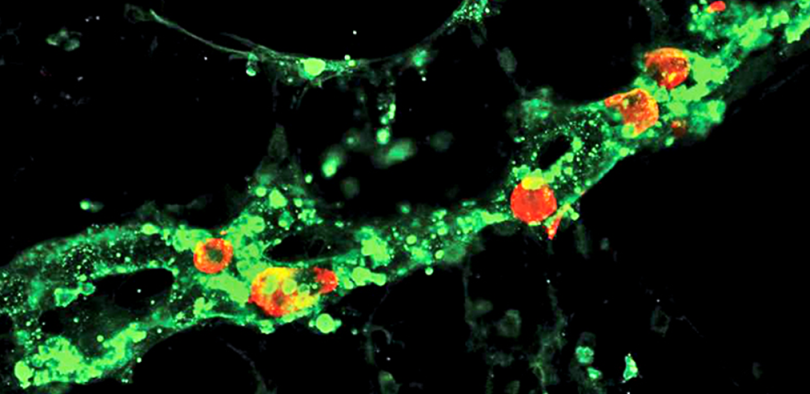
Иммунофлюоресцентная визуализация метастатических клеток меланомы (красные) внутри лимфатических сосудов (зеленые). Масштабная линейка: 100 мкм
(Science Advances/Michael Detmar Group ©)
Из чего состоит лимфатическая система шеи
Лимфатическая система шеи включает в себя сосуды и узлы.
Лимфатические капилляры — это тонкостенные структуры, состоящие из одного слоя эндотелиальных клеток. Они находятся во всех тканях организма и, объединяясь друг с другом, способствуют оттоку лимфатической жидкости в более крупные лимфатические сосуды.
Стенка лимфатических сосудов состоит из трех слоев: внутреннего слоя эндотелиальных клеток, среднего мышечного слоя и внешнего слоя соединительной ткани. В лимфатических сосудах гораздо больше клапанов, чем в венозных, при этом циркуляция лимфы полностью зависит от сжатия сосудов окружающими мышцами. Лимфатические сосуды дренируют лимфу в лимфатические узлы.
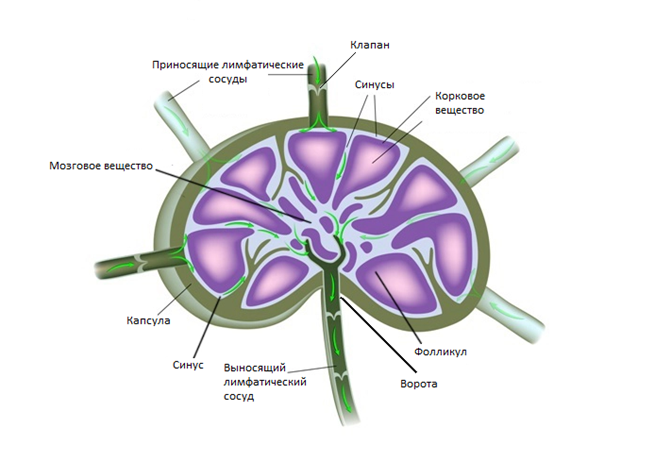
В среднем на каждой стороне шеи расположено до 75 лимфатических узлов. Снаружи узел покрывает капсула, под которой располагается субкапсулярные синусы – место куда попадает лимфатическая жидкость из приносящих лимфатических сосудов. Жидкость проходит сквозь ткань лимфатического узла, которая состоит из коркового и мозгового вещества, а затем выходит через ворота лимфатического узла и попадает в отводящие лимфатические сосуды. В итоге лимфа попадает в венозную систему в месте соустья внутренней яремной и подключичной вены.
Анатомическая структура лимфатического узла (Alila Medical Media/ Shutterstock ©)
Классификация лимфатических узлов шеи
На данный момент во всем мире рекомендована к использованию классификация Американского объединенного комитета по раку (American Joint Committee on Cancer (AJCC)) 8 издания от 2018 года:
Уровни лимфатических узлов шеи (Tenese Winslow LLC ©)
Диагностика
Осмотр
При пальпации шеи врач обращает внимание на расположение, размер, плотность и подвижность каждого узла. Особое внимание уделяется узлам, которые кажутся фиксированными к подлежащим сосудисто-нервным структурам и внутренним органам. Описание каждого узла становится важной частью медицинской документации, которая в дальнейшем может использоваться для оценки эффекта лечения.
Лучевые методы
Преимуществами УЗИ перед другими методами визуализации являются цена, скорость исследования и низкая лучевая нагрузка на пациента.
Ультразвуковыми признаками метастатического поражения лимфатических узлов может быть образование сферической формы, нарушение структуры, нечеткие границы, наличие центрального некроза и др.
Поскольку не всегда по УЗИ можно с уверенностью сказать является лимфатический узел пораженным или нет, иногда одновременно выполняют тонкоигольную аспирационную биопсию под ультразвуковым контролем с последующим цитологическим исследованием материала из этого узла. Результат цитологического исследования зависит от навыков врача УЗИ и качества образца (т.е. наличия достаточного количества репрезентативных клеток).
С появлением систем высокого разрешения и специальных контрастных веществ КТ позволяет обнаруживать лимфатические узлы, которые могли быть пропущены при иных методах диагностики.
Ценность МРТ – превосходная детализация мягких тканей. МРТ превосходит КТ в качестве предпочтительного исследования при оценке ряда новообразований головы и шеи, таких как основание языка и слюнные железы. Размер, наличие нескольких увеличенных узлов и центральный некроз – критерии, общие для протоколов исследования КТ и МРТ.
Этот новый метод визуализации все чаще используется для определения стадии опухолей головы и шеи. Метод основан на поглощении 2-фтор-2-дезокси-D-глюкозы (ФДГ) метаболически активными тканями. Исследование также может быть объединено с КТ, чтобы улучшить разрешение получаемого изображения и более точно определить расположение образования.
Биопсия
Биопсия — это удаление небольшого кусочка ткани для исследования под микроскопом или для тестирования в лаборатории на предмет наличия признаков злокачественности. В подавляющем большинстве случаев проводится тонкоигольная аспирационная биопсия. Врач, выполняющий биопсию, может использовать УЗИ или КТ для выполнения процедуры. Иногда тонкоигольная аспирационная биопсия не позволяет поставить окончательный диагноз, и требуются другие виды биопсии, такие как трепан-биопсия или эксцизионная биопсия.
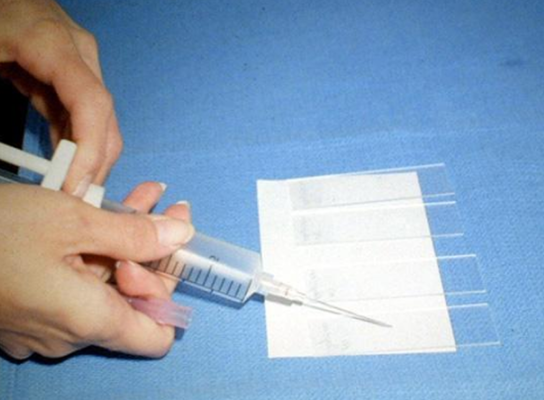 | 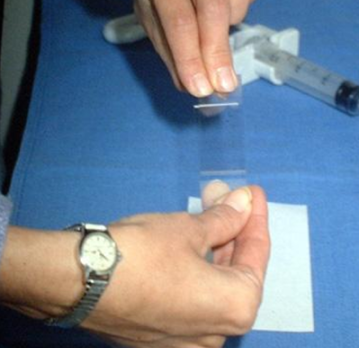 |
| Процесс приготовления предметных стекол для цитологического исследования. Материалом служит содержимое шприца после выполнения тонкоигольной аспирационной биопсии | |
План лечения
После определения диагноза и проведения всех диагностических исследований врач порекомендует оптимальный для пациента курс лечения. В конечном итоге лечение метастатического поражения лимфатических узлов зависит от типа и локализации первичной опухоли.
Существует три различных варианта лечения, которые могут быть использованы отдельно или в комбинации:
Хирургическое лечение
Хирургическое лечение обычно включает удаление лимфатических узлов шеи (лимфодиссекция) и последующее гистологическое исследование для точного определения стадии, так как это может существенно повлиять на дальнейшую тактику лечения. Хоть и не всегда, но чаще всего лимфодиссекция выполняется одновременно с удалением первичной опухоли.
Существуют различные виды лимфодиссекций:
Лучевая терапия
Лучевая терапия может быть назначена в качестве самостоятельного метода лечения в послеоперационном периоде, чтобы снизить вероятность рецидива либо в комбинации с химиотерапией в качестве самостоятельного или адъювантного лечения. Обычно адъювантная лучевая терапия необходима, если по результатам гистологического исследования обнаруживается несколько пораженных лимфатических узлов.
Химиотерапия
Химиотерапия обычно добавляется к лучевой терапии в качестве самостоятельного или адъювантного (послеоперационного) лечения. В некоторых случаях может использоваться индукционная химиотерапия с целью уменьшения объема образования и последующего хирургического вмешательства.
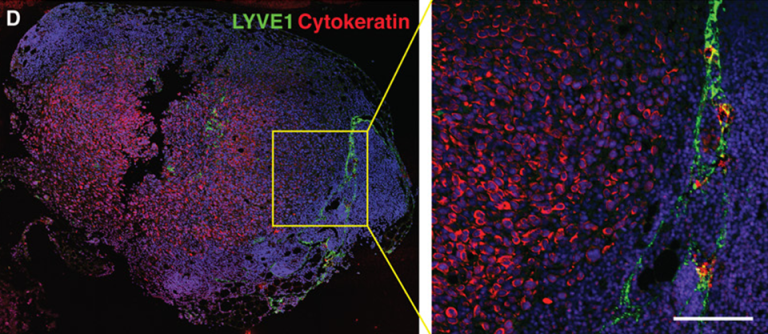
Иммунофлюоресцентная визуализация метастатически пораженного лимфатического узла с окраской на Цитокератин (красный) – маркер характерный для опухолевых клеток эпителиального происхождения. Масштабная линейка: 50 мкм
(Science Advances/Michael Detmar Group ©)
Прогноз
Метастазы в лимфатические узлы шеи могут возникать при онкологических заболеваниях различных локализаций, поэтому давать прогностические оценки для этой группы пациентов следует только после выявления первичной опухоли.
Факторы, влияющие на прогноз:
Наблюдение после лечения
Пациенты должны регулярно посещать своего специалиста по опухолям головы и шеи для оценки состояния на предмет любых признаков рецидива заболевания.
Стандартный график наблюдения
В первые 1–2 года осмотр и сбор жалоб рекомендуется проводить каждые 3–6 месяца, на сроке 3–5 лет – один раз в 6–12 месяцев. После 5 лет с момента операции посещать врача необходимо один раз в год или при появлении жалоб. У пациентов с высоким риском рецидива перерыв между обследованиями может быть сокращен.
Список литературы:
Авторская публикация:
Амиров Николай Сергеевич
Клинический ординатор НМИЦ онкологии им. Н.Н. Петрова
Под научной редакцией:
Раджабова З.А.
Заведующий отделением опухолей головы и шеи
НМИЦ онкологии им. Н.Н. Петрова,
врач-онколог, научный сотрудник, кандидат медицинских наук, доцент
Рекомендации для кистей и рук после удаления подмышечных лимфоузлов
Здесь приведена информация о том, как предотвратить развитие инфекции и уменьшить отечность кисти и руки после операции по удалению подмышечных лимфоузлов. Соблюдение этих рекомендаций поможет предотвратить развитие лимфедемы.
Информация о лимфатической системе
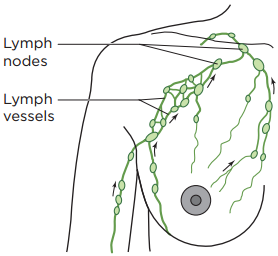
Рисунок 1. Нормальный отток лимфы
Лимфатическая система выполняет 2 функции:
Ваша лимфатическая система состоит из лимфоузлов, лимфатических сосудов и лимфатической жидкости (см. рисунок 1).
Подмышечные лимфоузлы — это группа лимфоузлов в подмышечной области (подмышке), которые отводят лимфатическую жидкость от молочной железы и руки. Количество подмышечных лимфоузлов у всех разное. Удаление подмышечных лимфоузлов — это операция по удалению группы таких узлов.
О лимфедеме
Иногда, в результате удаления лимфоузлов, лимфатической системе становится сложно справляться с выведением жидкости. В этом случае лимфатическая жидкость может накапливаться там, где были удалены лимфоузлы. Эта лишняя жидкость вызывает образование отека, который называется лимфедема.
Лимфедема может развиваться в руке, кисти, молочной железе или туловище со стороны, подвергнутой лечению (сторона, где были удалены лимфоузлы).
Признаки лимфедемы
Лимфедема может развиться внезапно или постепенно. Это может произойти спустя месяцы или годы после операции.
Следите за появлением следующих симптомов лимфедемы в руке, кисти, молочной железе и туловище со стороны, подвергнутой лечению:
Если у вас появился отек, вы можете заметить следующее:
Если у вас есть какие-либо признаки лимфедемы или возникли сомнения, позвоните вашему медицинскому сотруднику.
Снижение риска развития лимфедемы
Важно предотвращать развитие инфекции и отечность, чтобы снизить риск возникновения лимфедемы.
Предотвращение развития инфекции
Лимфедема может возникнуть у вас с большей вероятностью, если в затронутой лечением руке появится инфекция. Это происходит из-за того, что для борьбы с инфекцией ваш организм будет вырабатывать дополнительные белые кровяные тельца и лимфатическую жидкость, и эта жидкость не будет выводиться должным образом.
Соблюдайте эти рекомендации, чтобы снизить риск развития инфекции.
Если вы заметили какие-либо признаки инфекции (такие как покраснение, отек, более теплая, чем обычно, в этом месте кожа или болезненность), позвоните своему медицинскому сотруднику.
Уход за порезами и царапинами
Уход за ожогами
Сразу после операции
Небольшой отек после операции — это нормальное явление. Этот отек может сохраняться до 6 недель, но он носит временный характер и постепенно исчезнет. После операции у вас также могут быть болевые и другие ощущения, например покалывания и пощипывания. Следуйте этим рекомендациям, чтобы снять отек после операции.
Долгосрочная перспектива
Выполнение следующих действий может помочь снизить риск развития лимфедемы.
Когда следует обращаться к своему медицинскому сотруднику?
Позвоните своему медицинскому сотруднику, если у вас появились следующие симптомы:
Место и роль расширенной аорто-подвзошно-тазовой лимфаденэктомии в лечении рака нижнеампулярного отдела прямой кишки
Лимфогенное метастазирование является одной из причин того, что вероятность развития рецидива после операций по поводу рака прямой кишки весьма высока. Поэтому в хирургии рака прямой кишки система лимфооттока всегда рассматривалась как одна из главных мишеней, воздействие на которую могло бы улучшить отдаленные результаты.
Основные зоны регионарного метастазирования рака прямой кишки были определены Miles еще в 1908 г. Он показал, что распространение опухолевого процесса происходит в трех направлениях: восходящем, латеральном и нисходящем.
Частота их поражения представлена в табл. 1.
Основным достоинством этой классификации степени поражения лимфатического аппарата прямой кишки является то, что, в отличие от общепринятой классификации UICC (Union International Contra la Cancrum), при определении индекса N ориентируются не на количество пораженных лимфатических узлов, а на степень удаленности пораженного лимфатического узла от первичной опухоли.
Частота поражения различных групп лимфатических узлов при восходящем метастазировании
Частота метастатического поражения узлов, %
Takahashi T. et al., 1 997 [1 5]
Hida J. et al., 1997 [7]
Частота поражения различных групп лимфатических узлов при латеральном метастазировании
Частота метастатического поражения узлов, %
Takahashi T. et al., 1 997 [1 5]
Hida J. et al., 1997 [7]
Тем не менее, учитывая вариабельность анатомии лимфатического аппарата прямой кишки, довольно часто (до 80%) вышеупомянутые закономерности не соблюдаются, т.е. может не быть строго ориентированного регионарного метастазиро-вания рака прямой кишки. При раке нижне- и среднеампулярного отделов прямой кишки обнаруживаются метастазы в лимфатические узлы по ходу верхней прямокишечной артерии (в 9,4% и 14,3% соответственно), при раке же верхнеампулярного отдела в 19% наблюдений метастазы выявляются вдоль подвздошных сосудов.
Типы лимфаденэктомий
Первичный рак прямой кишки характеризуется тем, что опухоль остается длительное время локализованной и относительно медленно растет по сравнению с другими опухолями пищеварительного тракта. Локализованный и медленный рост характерен также и для метастазов в лимфатические узлы. Исходя из этой биологической особенности рака прямой кишки, было сделано предположение о том, что, увеличив объем лимфаденэк-томии, можно достичь снижения количества рецидивов.
Прежде всего, необходимо сказать, что подразумевается под понятием «увеличение объема лимфаденэктомии», поскольку именно терминологическая путаница зачастую обусловливает значительное расхождение в результатах у разных авторов. Для обозначения более полного удаления лимфатических коллекторов был предложен целый ряд терминов: «расширенная лимфа-денэктомия», «аорто-подвздошно-тазовая лимфа-денэктомия», «аортоподвздошная лимфаденэкто-мия с селективной тазовой лимфодиссекцией», «латеральная лимфодиссекция». Все это свидетельствует о том, что расширенная лимфаденэктомия не представляет собой единую стандартную методику, а является группой методов. Аор-то-подвздошная лимфаденэктомия, являющаяся неотъемлемой частью большинства методик и направлена на предотвращение метастазирования по восходящему пути, выполняется большинством хирургов сходным образом: производится высокая перевязка нижней брыжеечной артерии (у места отхождения от аорты), после чего отсе-паровывается париетальная фасция с клетчаткой и лимфатическими сосудами от аорты, нижней полой вены и общих подвздошных сосудов. А вот вопрос о способах удаления латеральных лимфатических коллекторов до сих пор является не решенным. Исторически сложившиеся школы западных и японских хирургов придерживаются двух противоположных точек зрения: если в Японии расширенная лимфаденэктомия с латеральной лимфодиссекцией активно практикуется вот уже несколько десятилетий, то в Европе и США от нее практически отказались.
Группы лимфатических узлов, удаляемые при различных типах лимфаденэктомий
Восходящий путь димфооттока
^тер^ьный путь димфооттока
Вновь интерес к расширенной лимфаденэктомии появился в 80-е годы, когда Heald и соавт. предложили выполнение тотальной мезоректумэктомии, т.е. удаление совокупности тканей и органов, находящихся в пределах фасциальной оболочки прямой кишки, включающей в себя параректальную клетчатку, сосуды и лимфатические узлы.
Несмотря на более чем положительные результаты (менее 5% местных рецидивов), большинство колоректальных хирургов не смогли их воспроизвести, в связи с чем вновь появился интерес к использованию более расширенных методов лимфа-денэктомии в хирургическом лечении рака прямой кишки.
Необходимо сказать о том, что включает в себя понятие «расширение лимфаденэктомии». T. Taka-hashi предложил выделять несколько вариантов лимфаденэктомии: ограниченная лимфаденэкто-мия, стандартная лимфаденэктомия и расширенная лимфаденэктомия. Группы лимфатических узлов, удаляемые при различных типах лимфаденэк-томий, представлены в табл. 3.
Однако такое деление не является общепринятым. Тотальной мезоректумэктомии соответствует ограниченная лимфаденэктомия в классификации T. Takahashi. Кроме того, было предложено производить высокую перевязку нижней брыжеечной артерии у места ее отхождения от аорты и удалять лимфатические узлы по ходу подвздошных сосудов. T. Takahashi рассматривает эту процедуру как стандартную лимфаденэктомию. Расширенная лимфаденэктомия включает в себя тотальную мезоректумэктомию, высокую перевязку нижней брыжеечной артерии, а также латеральную лимфодиссекцию, при которой удаляются узлы по ходу подвздошных сосудов и в запирательном пространстве.
Большинство авторов сходятся во мнении, что расширенная лимфаденэктомия мало влияет на показатели пятилетней выживаемости у больных с раком в стадии Dukes А. Данные по влиянию расширенной лимфаденэктомии на пятилетнюю выживаемость у пациентов с раком стадии Dukes В и Dukes С представлены в табл. 4 и 5.
Из приведенных публикаций видно, что данные по влиянию расширенной лимфаденэктомии на пятилетнюю выживаемость весьма противоречивы. Некоторые авторы показывают, что расширенная лимфаденэктомия увеличивает пятилетнюю выживаемость, другие считают, что она не оказывает никакого влияния или даже снижает пятилетнюю выживаемость. Вероятнее всего, это связано с несовершенством методик определения стадии опухолевого процесса, о которых упоминалось выше. По мнению R. Glass и соавт. [6], также высока доля субъективизма при выборе пациента для расширенной лимфа-денэктомии, в результате чего ей подвергаются пациенты с более поздней стадией заболевания чаще, чем пациенты с более ранней стадией, которым выполняется традиционная лимфодис-секция. В этом кроется еще одна из причин того, что данная операция не дает ожидаемого увеличения выживаемости. Кроме того, необходимо отметить, что сложилось два диаметрально противоположных мнения по вопросу о расширении лимфаденэктомии при операциях по поводу рака прямой кишки. Западные хирурги считают, что эффект этой процедуры весьма сомнителен и редко выполняют ее, в то же время японские хирурги полагают, что расширенная лим-фодиссекция высокоэффективна и должна рутинно выполняться при операциях по поводу рака прямой кишки.
Пятилетняя выживаемость у больных с раком Dukes В
Takahashi T. et al., 1 974-1 983 [1 5]
Koyama Y. et al. 1 984 [9]
Takahashi T. et al., 1 984-1 988 [1 5]
Hojo K. et al., 1 989 [8]
Пятилетняя выживаемость у больных с раком Dukes С
Takahashi T. et al., 1 974-1 983 [1 5]
Koyama Y. et al. 1 984 [9]
Takahashi T. et al., 1 984-1 988 [1 5]
Hojo K. et al., 1 989 [8]
Осложнения расширенной лимфаденэктомии
Влияние расширенной лимфаденэктомии на непосредственные результаты лечения недостаточно полно отражено в литературе. Некоторые авторы отмечают несколько большую продолжительность операции и кровопотерю. По мнению других, существенных различий по количеству послеоперационных осложнений между пациентами, подвергшимися расширенной и традиционной лимфаденэктомии, нет.
В последних работах описывается техника сохранения автономных нервов (nerve-sparing surgery) с целью предотвращения развития мочевой и половой дисфункций. Предлагается несколько вариантов этой методики:
Таким образом, метастатическое поражение лимфатических узлов значительно ухудшает прогноз для больного. Сравнение традиционных и современных методов определения лимфатических узлов показывает, что до 55% пораженных метастазами лимфатических узлов остаются не выявленными. Наименьшим последствием этого является неправильная оценка стадии заболевания. Более существенно то, что использование традиционной техники удаления прямой кишки ведет к оставлению части пораженных лимфатических узлов, а значит, к ухудшению отдаленных результатов у каждого четвертого оперированного. Это диктует необходимость внедрения в арсенал онкопроктологов методов различных видов лимфаденэктомий, несмотря на высокий процент дизурических и половых расстройств после таких вмешательств. Только такой подход может в дальнейшем способствовать предупреждению местных рецидивов и отдаленных метастазов, обеспечивая как можно более полное удаление путей лимфооттока от прямой кишки.
Несмотря на кажущуюся целесообразность выполнения латеральной лимфодиссекции у больных нижнеампулярным раком, такая операция не получила широкого распространения.
Причин подобного негативного отношения несколько.
1. Противоречивые данные о показателях 5-летней выживаемости после выполнения такого рода вмешательств. Однако в ряде случаев (особенно при включении в исследование только больных с распространенностью опухоли Dukes B и Dukes С) было показано увеличение показателей 5-летней выживаемости по сравнению со стандартной лимфаденэктомией (С-ЛАЭ). Следует отметить, что все исследования носили ретроспективный характер (табл. 6).
2. Усложнение и удлинение времени вмешательства наряду с увеличением кровопотери и объема перелитой крови, без увеличения госпитальной летальности по сравнению со стандартной хирургией (табл. 7).
3. Высокая частота мочеполовых расстройств, которые отмечаются всеми авторами (табл. 8).
С 1999 г. в ГНЦ колопроктологии начато проспективное рандомизированное исследование.
Критериями включения больных в исследование служили:
Критерии исключения больных из исследования.
Л. На дооперационном этапе:
Показатели 5-летней выживаемости после выполнения расширенной ЛАЭ по сравнению со стандартной ЛАЭ