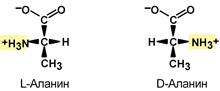
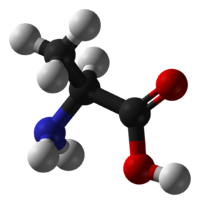
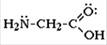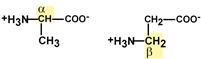Оптические изомеры аланина
Аминокислоты. Белки.
Вопросы экзамена
1. Аминокислоты. Классификация аминокислот. Номенклатура. Строение. Получение.
2. Химические свойства аминокислот: реакции карбоксильной группы, реакции аминогруппы. Отношение к нагреванию. Пептидная связь. Применение в медицине.
Белки и пептиды построены из остатков α-аминокислот.
Свойства белков во многом определяются строением и химическим поведением α-аминокислот.
Многие белки и пептиды применяются как лекарственные средства, это ферменты, гормоны, антибиотики, сыворотки.
Природные α-аминокислоты
В настоящее время известно свыше 100 природных α-аминокислот, из которых только 20 входят практически во все белковые молекулы (табл. 1).
12 из них могут синтезироваться в организме человека-заменимые, а 8-незаменимые не синтезируются, поступают с пищей.
Аминокислоты— органические бифункциональные амфотерные соединения, в состав которых входят карбоксильные группы –СООН и аминогруппы -NH2.
Простейший представитель — аминоуксусная кислота H2N-CH2-COOH (глицин)
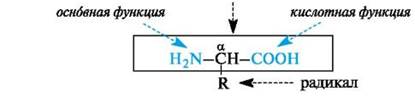
α-Аминокислоты имеют общую формулу:
· и различаются только строением радикала R.
Классификация и номенклатура
α-Аминокислоты классифицируют в зависимости от следующих признаков:
· По характеру радикала различают алифатические, ароматические и гетероциклические аминокислоты (см. табл.1).
Группа алифатических аминокислот наиболее многочисленна.
• В зависимости от количества функциональных групп различают кислые, нейтральные и основные.
Белковые α-аминокислоты*
* Сокращенные обозначения применяются только для записи аминокислотных остатков в молекулах пептидов и белков.
Систематические названия α-аминокислот практически не используются, хотя они, безусловно, допустимы.
Оптическая изомерия
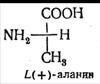
Стереоизомерия α-аминокислот, кроме глицина, связана с тем, что α-углеродный атом связан с четырьмя разными заместителями, поэтому все эти аминокислоты могут существовать в виде двух изомеров (энантиомеров), являющихся зеркальными отражениями друг друга (оптическая изомерия).
В состав белков животных организмов входят только L-аминокислоты.
Оптические изомеры аланина

ФИЗИЧЕСКИЕ СВОЙСТВА
По физическим свойствам аминокислоты резко отличаются от соответствующих кислот и оснований.
Все они кристаллические вещества, лучше растворяются в воде, чем в органических растворителях, имеют достаточно высокие температуры плавления; многие из них имеют сладкий вкус.
Эти свойства отчётливо указывают на солеобразный характер этих соединений.
Особенности физических и химических свойств аминокислот обусловлены их строением — присутствием одновременно двух противоположных по свойствам функциональных групп: кислотной и основной. α-аминокислоты являются амфотерными электролитами.
ПОЛУЧЕНИЕ α –АМИНОКИСЛОТ
1. Из карбоновых кислот по схеме –важнейший способ:
Уксусная кислота хлоруксусная
хлоруксусная кислота аминоуксусная к-та (глицин)
Аминокислоты обладают изомерией
Изомерия аминокислот в зависимости от положения аминогруппы
В зависимости от положения аминогруппы относительно 2-го атома углерода выделяют α-, β-, γ- и другие аминокислоты.
α- и β- формы аланина
Для организма млекопитающих наиболее характерны α-аминокислоты.
Изомерия по абсолютной конфигурации
В белке любого организма содержится только один стереоизомер, для млекопитающих это L-аминокислоты.
L- и D-формы аланина
Однако оптические изомеры могут претерпевать самопроизвольную неферментативную рацемизацию, т.е. L-форма переходит в D-форму.
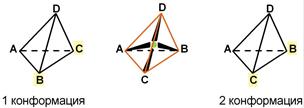
Как известно, тетраэдр – это довольно жесткая структура, в которой невозможно произвольным образом передвинуть вершины.
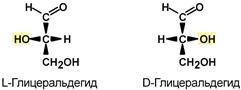
Точно так же для молекул, построенных на основе атома углерода, − за эталон конфигурации принята структура молекулы глицеральдегида, установленная с помощью рентгеноструктурного анализа. Принято, что в качестве маркера используют наиболее сильно окисленный атом углерода (на схемах его располагают сверху), связанный с асимметричным атомом углерода. Таким окисленным атомом в молекуле глицеральдегида служит альдегидная группа, для аланина – СООН группа. Атом водорода в ассиметричном углероде располагают так же, как в глицеральдегиде.
В дентине, белке зубной эмали, скорость рацемизации L-аспартата равна 0,10% в год. При формировании зуба у детей используется только L-аспартат. Такая особенность позволяет при желании определять возраст долгожителей. Для ископаемых останков наряду с радиоизотопным методом также используют определение рацемизации аминокислот в белке.
Деление изомеров по оптической активности
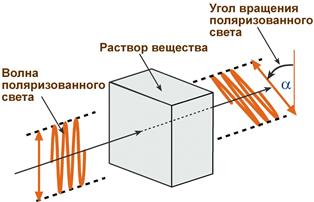
Наличие в аминокислоте ассиметричного α-атома углерода (хирального центра) делает возможным только два расположения химических групп вокруг него. Это приводит к особому отличию веществ друг от друга, а именно – изменению направления вращения плоскости поляризованного света, проходящего через раствор. Величину угла поворота определяют при помощи поляриметра. В соответствии с углом поворота выделяют правовращающие ( + ) и левовращающие (–) изомеры.
 |  | ||||||||||||||||||||||||||||||
| Аланин | |
 | |
 | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | (S)-2-аминопропановая (α-аминопропионовая) кислота |
| Сокращения | Ала, Ala, A GCU,GCC,GCA,GCG |
| Химическая формула | CН3-СН(NH2)-СООН |
| Физические свойства | |
| Отн. молек. масса | 89,09 а. е. м. |
| Молярная масса | 89,09 г/моль |
| Термические свойства | |
| Температура плавления | 295-316 °C |
| Классификация | |
| Рег. номер CAS | 56-41-7 |
| SMILES | C[C@H](N)C(O)=O |
Аланин (2-аминопропановая кислота) — алифатическая аминокислота. α-Аланин входит в состав многих белков, β-аланин — в состав ряда биологически активных соединений.
Аланин легко превращается в печени в глюкозу и наоборот. Этот процесс носит название глюкозо-аланинового цикла и является одним из основных путей глюконеогенеза в печени.
Содержание
Химические свойства
Синтез
Впервые аланин был синтезирован Штреккером в 1850 г. действием на ацетальдегид аммиаком и синильной кислотой с последующим гидролизом образовавшегося α-аминонитрила [1] :

В лабораторных условиях аланин синтезируют взаимодействием с аммиаком α-хлор или α-бромпропионовой кислоты [2] :

См. также
Примечания
Литература
Полезное
Смотреть что такое «Аланин» в других словарях:
АЛАНИН — Аланин … Энциклопедия Кольера
АЛАНИН — алифатическая аминокислота, a аланин, CH3CH2(NH)2COOH, входит в состав многих белков, b аланин, Н2NCH2CH2COOH, в состав ряда биологически активных соединений (кофермент аланин, пантотеновая кислота и др.) … Большой Энциклопедический словарь
АЛАНИН — (CH3C(NH2)COOH), бесцветная, растворимая АМИНОКИСЛОТА, широко распространенная в составе БЕЛКОВ, например, получаемых из шелка … Научно-технический энциклопедический словарь
АЛАНИН — аминопропионовая к та. В природе широко распространены два изомера. L ce A. заменимая аминокислота. Входит в состав разл. белков (в фиброине шёлка до 40% ), содержится в свободном состоянии в плазме крови. В составе муреина бактериальных… … Биологический энциклопедический словарь
АЛАНИН — Органическое соединение в продуктах разложения белковых веществ, иначе называемое амидопропионовая кислота. Словарь иностранных слов, вошедших в состав русского языка. Чудинов А.Н., 1910 … Словарь иностранных слов русского языка
аланин — сущ., кол во синонимов: 1 • аминокислота (36) Словарь синонимов ASIS. В.Н. Тришин. 2013 … Словарь синонимов
аланин — Аминокислота [http://www.dunwoodypress.com/148/PDF/Biotech Eng Rus.pdf] Тематики биотехнологии EN alanine … Справочник технического переводчика
Аланин — * аланін * alanine аминопропионовая кислота, аминокислота ( А. заменимая, А. незаменимая аминокислота). Особенно много А. в фибрине шелка (до 40%). Кодоны А. ГЦУ (, ГЦЦ (), ГЦА (), ГЦГ (). Одна из 20 аминокислот, входящих в состав белка: СН3 СН… … Генетика. Энциклопедический словарь
аланин — алифатическая аминокислота. α аланин, CH3CH(NH2)COOH, входит в состав многих белков, β аланин, H2NCH2CH2COOH, в состав ряда биологически активных соединений (кофермент аланина, пантотеновая кислота и др.). * * * АЛАНИН АЛАНИН, алифатическая… … Энциклопедический словарь
аланин — (син. l аланин) l аминопропионовая кислота, заменимая аминокислота; входит в состав белков организма … Большой медицинский словарь
Оптические изомеры
Химикам уже давно известно явление изомерии — когда два вещества имеют одну и ту же брутто-формулу (отражающую только количество разных атомов в веществе), но разные свойства — из-за разного порядка соединения атомов.
Особенно богата изомерами органическая химия. К примеру, этиловый спирт и диметиловый эфир имеют одну и ту же брутто-формулу: C2H6O, но структурная формула спирта — CH3–CH2–OH, а эфира — CH3–O–CH3. Эти вещества имеют разные свойства — как химические, так и физические (температура плавления, вязкость и т. д.).
В органической химии известны и так называемые оптические изомеры — молекулы, имеющие одинаковую структурную формулу, но не совместимые со своим зеркальным отражением. Простейший пример такой молекулы — это атом углерода с четырьмя разными заместителями. К примеру, СHClBrF или аланин CH3CHNH2COOH (рис. 1). Наличие у такой молекулы двух разных конфигураций связано с тем, что у атома углерода, образующего четыре одинарные связи, эти связи направлены к вершинам тетраэдра.
Оптические изомеры имеют одинаковый цвет, температуру кипения, плотность. Однако такие вещества обладают интересным физическим свойством — они вращают плоскость поляризации пропущенного через них поляризованного света. Один изомер будет вращать ее влево, другой — вправо.
Атом углерода с четырьмя разными заместителями называется хиральным атомом (от греческого heiros «ладонь» — тот же корень, что и в слове «хиромантия»). Чем больше хиральных атомов в молекуле, тем больше у вещества может быть оптических изомеров.
Интересно, что возможны органические вещества, которые имеют оптические изомеры, хотя в них формально нет ни одного хирального атома — центра изомерии.
Задача
Приведите пример органического вещества, не имеющего хиральных атомов, но при этом имеющего оптические изомеры, с минимальным количеством атомов углерода.
Подсказка 1
Для того чтобы молекула некоторого вещества не совпадала со своим зеркальным отражением, совершенно не обязательно, чтобы у нее был хотя бы один хиральный атом. К примеру, любая молекула в форме спирали будет оптически активной.
Подсказка 2
Кроме того, вспомните, к вершинам какой геометрической фигуры направлены четыре связи в хиральном атоме углерода.
Решение
Начнем с того, что для несовместимости со своим зеркальным отражением молекуле недостаточно быть просто несимметричной. Молекула может быть не равна своему отражению «на бумаге», но совместима с ним. Скажем, молекулу HCl мы можем просто повернуть (или посмотреть на нее с другой стороны). Мы можем также вращать части молекулы вокруг одинарных связей — а вот с двойными и тройными связями так поступать нельзя, они при этом рвутся.
Итак, если структура молекулы имеет такую пространственную асимметрию, что она не совмещается со своим зеркальным отражением, то молекула и ее отражение называются оптическими изомерами. Наша цель — попробовать придумать структуру, которая бы была несовместима со своим зеркальным отражением, имела бы минимальное количество атомов углерода, и при этом сами эти атомы не были бы хиральными центрами молекулы.
На первый взгляд, такой молекулой могли бы быть замещенные этилены, где вместо атомов водорода — четыре разных заместителя:
Однако несмотря на то, что у такого вещества есть изомеры (два произвольно выбранных заместителя у разных атомов углерода могут располагаться по одну сторону двойной связи или по разные), хиральными они не будут, так как молекулы с одной двойной связью — плоские; чтобы совместить их со своим зеркальным отражением, их достаточно просто повернуть на 180° вокруг оси, лежащей в плоскости молекулы и перпендикулярной двойной связи.
Существует вариант с тремя атомами углерода, который формально уже можно назвать решением нашей задачи. Четырехзамещенные аллены RR’C=C=CR»R»’ тоже содержат двойные связи, но их молекулы уже не плоские. Дело в том, что если у одного атома углерода есть две двойные связи, то их плоскости повернуты друг относительно друга на 90 градусов:
Эта молекула уже хиральна, и можно сказать, что задачу мы решили. Однако в ней есть «хиральный центр» — центральный атом углерода. Попробуем решить задачу другим способом.
Три атома углерода можно расположить по-другому — создав из них треугольник. У нас получится вещество циклопропан, С3H6:
Это хорошо известное вещество, которое до сих пор иногда используется в медицине в качестве средства для наркоза. Атомы углерода образуют жесткую плоскость. Каждый из них связан с двумя атомами водорода — один над плоскостью, другой — под ней.
Теперь заменим у двух атомов углерода по одному атому водорода на два других заместителя — к примеру, хлор и бром — так, чтобы они оказались по разные стороны от плоскости атомов углерода. Такое положение заместителей называется транс-изомером 1,2-дизамещенного циклопропана. (Если бы эти заместители располагались по одну сторону от плоскости, у нас получился бы цис-изомер, но он нас сейчас не интересует).
Внимательно посмотрим на получившуюся молекулу и представим себе ее зеркальное отражение:
Обе структуры, как бы мы ни крутили их в пространстве, друг с другом не совмещаются, а атома — хирального центра тут нет.
А теперь попробуем создать полный аналог хирального атома углерода — но без хирального центра. Вернемся к первоначальному атому, с которого мы начали (см. условие задачи). Четыре связи его направлены к вершинам тетраэдра. Давайте попробуем расположить по атому углерода в его вершинах и соединить их связями.
У нас получится углеродный скелет вещества C4H4 — тетраэдрана. Само это вещество еще не получено химиками, но его производные уже существуют в реальности. Если заместить в нём все атомы водорода на разные заместители, то получится вполне себе хиральная молекула, «хиральный центр» которой будет располагаться внутри тетраэдра:
Послесловие
Тема изомерии — одна из самых благодатных тем для игры ума. Даже в школьных олимпиадах по химии очень часто можно встретить задания с просьбой написать все изомеры того или иного вещества (иногда сами составители задач чего-то не рассчитывают, и на решение уходит много времени и очень много бумаги; у автора этой задачи на районной олимпиаде как-то ушло полтора часа и целая тетрадка).
Оптические изомеры — всего один из вариантов изомерии в органической химии, но очень важный.
К примеру, все основные аминокислоты, которые входят в состав наших белков, имеют формулу H2N–CH(R)–COOH — то есть все (кроме глицина, у которого R тоже представляет собой атом водорода) имеют асимметрический атом углерода и имеют оптические изомеры. И в нашем организме встречаются почти исключительно L-изомеры аминокислот (если не вдаваться в тонкости номенклатуры хиральных атомов, которых существует целых три типа, то можно назвать эти молекулы «левыми»). И биохимики до сих пор гадают, почему природа выбрала именно этот изомер — ведь при всех реакциях, когда из более простых веществ получаются вещества с хиральным атомом (без присутствия специфических катализаторов) образуется смесь двух изомеров в равных частях.
Синтетики тоже любят «поиграть» с оптической изомерией и при этом уже создали множество веществ без хирального атома — но с оптической активностью.
Кстати, можно создать хиральную молекулу вообще без заместителей. И она будет достаточно небольшой. Существуют так называемые ароматические углеводороды. Самый простой из них — бензол, C6H6. Его структуру учат в школе — плоский шестигранник. Вещество посложнее — нафталин. Это уже два соединенных по одной стороне бензольных кольца:
Три кольца можно уже соединять в линию — получится антрацен, а можно — под углом, и тогда у нас получится фенантрен:
Так вот, если продолжать соединять кольца под углом и дойти до шести колец, то крайние кольца упрутся друг в друга, им не хватит места, и плоскость молекулы нарушится. Вещество из шести колец называется гексагелицен, и его молекула уже представляет собой спираль. А значит, эта молекула может быть либо левой спиралью, либо правой, и будет иметь оптические изомеры.
Кстати, химики научились получать такие спирали даже из 12 бензольных колец, в них уже есть пара витков.
Более того, и оптическими изомерами весь ассортимент разнообразия химических веществ, как ни странно, не заканчивается.
Стоит сказать о возможности так называемой топологической изомерии. Что это такое? К примеру, существует вещество в форме кольца. Две молекулы этого вещества изомерны одной, в которой одно кольцо продето в другое. И такие молекулы уже есть. Класс веществ, в которых две или более частей молекул удерживаются механически, как звенья цепи, называются катенанами — от латинского catena «цепь» (см. Catenane). Биохимики научились получать катенаны из молекул ДНК, и более короткие структуры тоже складывали в цепочки.
А если представить себе катенан из четырех колец, то возможна изомерия между молекулой, в которой три кольца продеты в четвертое, и молекулой, в которых кольца соединены последовательно.
Изомерия в органической химии
Изомеры – это вещества, имеющие одинаковый состав (число атомов каждого типа), но разное взаимное расположение атомов – разное строение.
Изомерия – это явление существования веществ с одинаковым составом, но различным строением.
Например, формуле C4H10 соответствуют два изомерных соединения н-бутан с линейным углеродным скелетом и изобутан (2-метилбутан) с разветвленным скелетом:

При этом температура кипения н-бутана –0,5 о С, а изобутана –11,4 о С.
Виды изомерии
Структурные изомеры отличаются друг от друга взаимным расположением атомов в молекуле; стереоизомеры — расположением атомов в пространстве.
Структурная изомерия
Структурные изомеры – соединения с одинаковым составом, но различным порядком связывания атомов, т.е. с различным химическим строением. Молекулярная формула у структурных изомеров одинаковая, а структурная различается.
1. Изомерия углеродного скелета: вещества различаются строением углеродной цепи, которая может быть линейная или разветвленная.
Например, молекулярной формуле С5Н12 соответствуют три изомера:

2. Изомерия положения обусловлена различным положением кратной связи, функциональной группы или заместителя при одинаковом углеродном скелете молекул.

2.2. Изомерия положения кратной связи может быть вызвана различным положением кратной (двойной или тройной) связи в непредельных соединениях. Например, в бутене-1 и бутене-2:

2.3. Межклассовая изомерия – ещё один вид структурной изомерии, когда вещества из разных классов веществ имеют одинаковую общую формулу.
Например, формуле С2Н6О соответствуют: спирт (этанол) и простой эфир (диметиловый эфир):


Пространственная изомерия
Пространственные изомеры – это вещества с одинаковым составом и химическим строением, но с разным пространственным расположением атомов в молекуле. Виды пространственной изомерии – геометрическая (цис—транс) и оптическая изомерия.
1. Геометрическая изомерия (или цис-транс-изомерия).
Геометрическая изомерия характерна для соединений, в которых различается положение заместителей относительно плоскости двойной связи или цикла. Например, для алкенов и циклоалканов.
Двойная связь не имеет свободного вращения вокруг своей оси.
Поэтому заместители у атомов углерода при двойной связи могут быть расположены либо по одну сторону от плоскости двойной связи (цис-изомер), либо по разные стороны от плоскости двойной связи (транс-изомер). При этом никаким вращением нельзя получить из цис-изомера транс-изомер, и наоборот.
Например, бутен-2 существует в виде цис— и транс-изомеров

1,2-Диметилпропан также образует цис-транс-изомеры:

Геометрические изомеры различаются по физическим свойствам (температура кипения и плавления, растворимость, дипольный момент и др.). Например, температура кипения цис-бутена-2 составляет 3,73 о С, а транс-бутена-2 0,88 о С.
При этом цис—транс-изомерия характерна для соединений, в которых каждый атом углерода при двойной связи С=С (или в цикле) имеет два различных заместителя.
Таким образом, для соединений вида СH2=СHR и СR2=СHR’ цис—транс-изомерия не характерна.
2. Оптическая изомерия
Оптические изомеры – это пространственные изомеры, молекулы которых соотносятся между собой как предмет и несовместимое с ним зеркальное изображение.
Оптическая изомерия свойственна молекулам веществ, имеющих асимметрический атом углерода.
Асимметрический атом углерода — это атом углерода, связанный с четырьмя различными заместителями.

Такие молекулы обладают оптической активностью — способностью к вращению плоскости поляризации света при прохождении поляризованного луча через раствор вещества.
Например, оптические изомеры образует 3-метилгексан: