Кандидоз
Кандидоз — это инфекция, вызванная родом Candida. Род Candida насчитывает около 200 видов, которые присутствуют в продуктах питания, почве, растениях, некоторые входят в состав микрофлоры человека. Клинически значимыми являются несколько типов грибов, но ведущее значение в развитии кандидоза у человека имеют C.albicans и С.tropicalis.
Кандидозная инфекция чаще всего поражает слизистые оболочки рта, кишечника или влагалища.
Кандидоз вызывает широкий спектр симптомов: от самых легких, но распространенных форм, которые обычно обнаруживаются в ротовой полости и влагалище, до редких и тяжелых форм, ассоциированных с повреждением эндокарда, мозговых оболочек и развитием септицемии.
В соответствии с МКБ-10 выделяют:
Вульвовагинит или вагинит. Известны также как «молочница». Для заболевания характерны густые белые или желтые творожистые выделения из влагалища. Выделения сопровождаются зудом, жжением, отеком и покраснением интимной области, неприятным запахом. Реже отмечаются боль и дискомфорт во время мочеиспускания или во время полового акта. Беременные женщины или женщины с сахарным диабетом подвержены заболеванию в большей степени.
Кроме основных заметных симптомов, таких как молочница и белый налет на языке, кандида имеет следующие проявления: тяга к сладкому, раздражительность, апатия, ухудшение памяти, не способность к концентрации и вниманию, плохой сон, перепады настроения, запоры, метеоризм, постоянное чувство усталости.
К группам риска по кандидозу относятся следующие категории:
Защитные барьеры внутри организма
В патогенезе развития кандидоза немаловажную роль играют нарушения в работе органов пищеварения. Внутри организма существуют три барьера: механический, физико-химический и иммунобиологический, которые препятствуют колонизации слизистых оболочек и кожи патогенными микроорганизмами, а также обуславливают прямое противогрибковое действие в отношении кандиды.
Выработка секреторного иммуноглобулина A (IgA) слизистыми ротовой полости и кишечника является иммунологическим барьером, который защищает слизистые от колонизации грибами рода Candida.
Такие антибактериальные ферменты, как: лицозим, муцин, лактоферрин, пероксидаза, находящиеся в слюне, являются первыми линиями защиты. Длительное нахождение пищи в ротовой полости, а также отсутствие факта ее запивания водой или другими напитками увеличивают протективное действие компонентов слюны и снижают нагрузку на другие отделы желудочно-кишечного тракта. Агрессивная кислая среда желудка — следующий фактор неспецифической защиты. Пищеварение в двенадцатиперстной кишке, работа которой в равной степени зависит от деятельности поджелудочной железы и печени, способствует правильному усвоению углеводов, жиров и белков пищи и лучшему их всасыванию в тонком кишечнике. Кишечник является последней инстанцией, регулирующей поступление компонентов пищи в кровоток, поэтому от состояния энтероцитов, качества муциноподобной слизи и наличия симбиотической флоры будет зависеть его функция, в том числе и барьерная. Лечение кандиды в первую очередь начинается с восстановления функции кишечника.
Распространение кандиды — это результат, с одной стороны, нарушения барьерных функций желудочно-кишечного тракта, а с другой — создания самим человеком благоприятных условий для размножения дрожжей. К ним относится в первую очередь питание. Одним из ключевых факторов, от которого на 80 % зависит эффект при лечении кандидоза, является корректировка питания.
Список продуктов, которые способствуют размножению кандиды:
Список продуктов, которые улучшат состояние при кандидозе:
Анализы на кандидоз
Выявить кандиду непосредственно на видимых слизистых оболочках можно несколькими способами. Для этого проводят исследование методом ПЦР или выполняют культуральное исследование. В обоих случаях предметом исследования является мазок, взятый с места поражения. Оба метода определяют наличие главных виновников проблемы: грибов рода Candida на основе определения ДНК в образце или роста колонии грибов на питательной среде.
Оценить микробиоценоз тонкого кишечника позволяет исследование методом хромато масс-спектрометрии. Результаты анализа позволяют сделать заключение о состоянии пристеночной микрофлоры кишечника, выявить какие сообщества микроорганизмов находятся в дисбалансе. Материалом для исследования является цельная венозная кровь.
Анализ кала на дисбактериоз поможет сделать заключение о состоянии просветной микрофлоры толстого отдела кишечника. Наличие кишечной палочки, клебсиеллы, кандиды, некоторых видов стафилококков указывает на кандидоз.
Молочница во рту
Кандидоз полости рта — это воспалительное заболевание, которое развивается на фоне поражения слизистых оболочек грибами рода Candida. Обычно это связано с ухудшением местного и общего иммунитета. По данным исследований носителями этого грибка является до 90% взрослого населения, но при этом болезнь чаще всего не развивается, поскольку в обычных условиях возбудитель не действует агрессивно.
Причины кандидоза
Молочница во рту у взрослого человека — это поражение слизистой, которое может свидетельствовать о серьезных проблемах со здоровьем. Для размножения грибка необходимы особые условия. Чаще всего болезнь встречается у пациентов, пренебрегающих гигиеной полости рта. Наличие кариеса, воспалительных заболеваний десен повышает шансы на развитие грибкового воспаления. Это объясняется тем, что большое количество патогенных микроорганизмов истощает защитные механизмы.
Второй группой причин является ослабление иммунитета в связи с рядом заболеваний и состояний:
ВИЧ, сахарный диабет;
дистрофия, дефицит витаминов, минералов;
перенесенные операции, тяжелые инфекции и пр.
Существуют и специфические причины развития молочницы. Она может появиться после длительной и мощной антибактериальной терапии. Применение антибиотиков приводит к уничтожению полезной флоры и нарушению баланса. Это становится причиной активного размножения Candida.
Оральный кандидоз развивается и на фоне приема кортикостероидов в ингаляциях. Обычно поражение имеет вид эритемы и появляется на участках, где лекарство контактировало со слизистой: на небе, языке.
Особенности диеты влияют на вероятность развития кандидоза. Так, преобладание углеводов предрасполагает к активности грибка. Рост Candida и ее прикрепление к слизистой усиливаются в присутствии сахаров.
Вредные привычки повышают шансы на развитие лейкоплакии, плоского лишая и других заболеваний. В особенности речь идет о курении. Кандидоз часто развивается у пациентов с пирсингом языка.
Наличие съемных протезов также является фактором риска, если пациент не соблюдает правила гигиены. При отсутствии качественного очищения протез покрывается биопленкой, в составе которой много грибов. Дезинфекция является основной мерой профилактики болезни и частью комплексного лечения при прогрессирующем кандидозе ротовой полости. Если пациент не снимает конструкцию на ночь, это также повышает вероятность развития болезни. Слизистая оболочка долгое время остается без доступа кислорода, не омывается слюной — эти условия подходят для развития грибов и анаэробных микроорганизмов. Протез может травмировать слизистые, если не подходит по размеру. Микротравмы ослабляют местные защиты и способствуют началу развития грибковой инфекции. Травмы также могут быть связаны с острыми сколами зубов и пломб, химическими и термическими ожогами.
Сухость полости рта в связи с уменьшением слюноотделения, изменением вязкости слюны, ее состава — одна из причин кандидоза. Это может быть обусловлено другими заболеваниями, поэтому важно выяснить причины сухости, чтобы эффективно бороться с последствиями.
Кандидоз во рту у ребенка встречается чаще. Несформированность иммунной системы, заселение полости рта Candida из вагинального канала матери во время естественных родов приводят к тому, что развивается заболевание в раннем младенческом возрасте. Однако и дети старшего возраста могут страдать недугом, что связано с ослаблением иммунных сил.
Виды орального кандидоза и симптомы
Проявления орального кандидоза могут отличаться у разных пациентов. Это связано со степенью поражения слизистых, а также конкретным видом болезни. Выделяют четыре формы:
Несмотря на то что схема лечения для всех форм практически одинаковая, симптомы могут существенно отличаться. Рассмотрим их подробнее.
Острый псевдомембранозный кандидоз
Эта форма кандидоза слизистой рта может протекать бессимптомно. Отмечается незначительный дискомфорт из-за белой пленки или небольших бляшек, возвышающихся над слизистой. При легком течении появляется одна или несколько бляшек, они легко снимаются соскабливанием, а участок слизистой под ними имеет ярко-красный цвет. При тяжелом течении появляются крупные бляшки в большом количестве. Они могут сливаться, образуя крупные площади поражения. Иногда симптомы охватывают всю слизистую оболочку. При утолщении бляшек их удаление становится проблематичным. Тяжелое течение больше характерно для грудных детей, а также у взрослых пациентов после антибактериальной терапии, кортикостероидов, иммунодепрессантов.
Острый и хронический атрофический кандидоз
Острый атрофический кандидоз сопровождается сильным жжением. Белого налета может не быть, а слизистая оболочка становится ярко-красной. Многие пациенты отмечают металлический, кислый, соленый или горький привкус во рту. Характерным проявлением болезни является сухость в полости рта. Такая форма болезни чаще сопряжена с медикаментозной терапией.
При хроническом атрофическом кандидозе краснота и жжение менее выражены. Обычно болезнь развивается на фоне установки и ношения протезов.
Хронический гиперпластический кандидоз
Эта форма заболевания характерна для взрослых. Молочница ротовой полости может распространяться на слизистые щек, уголки рта и губы, спинку языка, мягкое небо. Одним из симптомов является появление белых бляшек, склонных к слиянию друг с другом. По мере развития болезни их поверхность становится шероховатой, грубой. Со временем элементы могут желтеть. Образования сливаются со слизистыми и удалить их невозможно.
Методы диагностики
Лечением занимается стоматолог-терапевт. Диагностика начинается с осмотра и подробного опроса: врач выяснит, какие препараты вы принимали в последнее время, есть ли хронические и инфекционные заболевания. В обязательном порядке проводится цитологическое исследование налета, взятого со слизистой. Это важно потому, что скопление негрибковой флоры можно легко спутать с грибковой инфекцией.
Соскоб выполняется в утреннее время, на голодный желудок, чистить зубы перед процедурой не нужно. Накануне важно отказаться от приема пищи, богатой углеводами, чтобы не спровоцировать рост патогенной флоры. Исследования позволяют не только точно определить возбудитель и вид гриба Candida, но и узнать чувствительность грибов к основным противогрибковым лекарствам. По результатам анализов врач определит грибок в полости рта и назначит медикаментозное лечение.
Особенности лечения
Основу лечения составляют системные и местные противогрибковые препараты. Сегодня они широко представлены на фармацевтическом рынке, но важно знать о том, что ежегодно уровень резистентности грибов Candida растет к основным средствам. Например, к таким препаратам, как «Флуконазол» устойчивость почти полная. Раньше это средство использовалось почти во всех случаях заболевания, но сегодня врачи вынуждены пересмотреть стандартные схемы терапии.
Лечение молочницы во рту у взрослых подбирается индивидуально. Выбор системного противогрибкового средства основывается на виде возбудителя, состоянии пациента и индивидуальных особенностей его здоровья. Существуют средства, к которым у инфекции минимальная устойчивость. Врач может назначит препараты на основе нистатина, производных имидазола и др.
Дополнительно обязательно используются местные средства:
растворы для полоскания полости рта;
гели и суспензии для аппликаций на пораженные участки;
местные таблетки и пастилки для рассасывания;
растворы для орошения и аэрозоли;
мази для закладывания в полости рта на ватно-марлевом тампоне и др.
Специалист может назначить аптечные антисептики или слабые солевые растворы для полоскания. Обычно используют растворы на основе йода, хлоргексидина, калия перманганата, генцианвиолета, натрия тетраборат в глицерине. Некоторые таблетки врач может порекомендовать закладывать за щеку.
Условия эффективного лечения
Эффективное лечение молочницы во рту предусматривает устранение основной причины. Очень важно санировать полость рта: вылечить зубы, разрушенные кариесом, удалить нежизнеспособные зубы и корни, которые уже не подлежат восстановлению. Это хронические очаги воспаления, поэтому одновременная санация сократит время лечения. Также следует удалить зубной камень и налет. Особенно это касается случаев кандидозного стоматита, связанных с травмированием десен острыми краями твердых зубных отложений.
Пациенты со съемными протезами должны быть повторно обучены гигиене и дезинфекции ортопедических конструкций. Если время пользования протезом подходит к концу, важно своевременно заменить его. Лечение кандидоза будет бесполезным, если человек будет пользоваться протезом неправильно и снова создавать в полости рта условия для размножения грибов.
Замене подлежат и неподходящие коронки, мостовидные протезы и другие конструкции. Также важно устранить сколы эмали, которые становятся источником травм для десен, слизистых оболочек щек и языка.
Курильщики должны по возможности сократить эпизоды курения или отказаться от вредной привычки. Если болезнь развилась на фоне приема кортикостероидов, важно разъяснить правила лечения: следует полоскать полость рта большим количеством теплой воды после распыления препарата.
При лечении кандидоза полости рта, развившемся на фоне антибактериальной терапии, следует принимать меры по восстановлению нормальной микрофлоры кишечника и полости рта. Может потребоваться консультация другого специалиста узкого профиля или терапевта: потребуется прием пробиотиков и пребиотиков.
Для всех пациентов, которые лечат кандидоз, действует несколько общих рекомендаций:
соблюдение гигиены полости рта;
отказ от пищи, богатой углеводами;
отказ от сладких напитков.
Необходимо исключить из рациона пищу, которая может раздражать слизистую: блюда, приготовленные с уксусом, маринады, острые, перченые продукты, копчености, кислые фрукты и ягоды. Также нельзя есть кондитерские изделия, выпечку на дрожжах, сахар. Лучше отдавать предпочтение теплым блюдам. Соблюдать такой режим питания нужно еще в течение 1,5−2 месяцев после выздоровления.
В ряде случаев целесообразно использовать зубные пасты с оксидазой глюкозы, лизоцимом, лактоферрином. Они способствуют улучшению защитных сил слизистой оболочки полости рта и могут быть частью комплексной профилактики развития воспалений. Выбор зубной пасты нужно согласовать с врачом, он порекомендует оптимальное средство, а также расскажет о том, какая щетка подойдет.
Профилактика кандидоза
Специфическая профилактика кандидоза в ротовой полости проводится только при наличии ВИЧ-инфекции, прохождении пациентом лучевой терапии, иммуносупрессивной или антибактериальной терапии. При отсутствии этих факторов риска врач даст рекомендации для конкретного случая.
Профилактика грибковых заболеваний у пациентов с сахарным диабетом, бронхиальной астмой, хроническими системными недугами предусматривает контроль над основной патологией. Важно регулярно наблюдаться у врача своего профиля, принимать назначаемые средства.
Если возникла необходимость в антибактериальной терапии, нужно придерживаться следующих правил:
принимать антибиотики только по назначению врача;
соблюдать достаточную длительность курса лечения — не отменять самостоятельно назначенные препараты при наступлении облегчения;
при необходимости длительного курса лечения или в случае повторной антибиотикотерапии принимать назначенные противогрибковые средства для профилактики.
При лечении бронхиальной астмы посоветуйтесь с врачом о возможности использования небулайзеров. После ингаляций важно полоскать полость рта, чтобы не допустить негативного воздействия компонентов лекарства на слизистые.
Если кандидоз рта часто рецидивирует, лучше пройти комплексное обследование: стандартную диспансеризацию или использовать конкретные методы диагностики, которые подберет врач. Грибковые инфекции слизистых могут быть проявлением основного заболевания, о котором вы не знаете. Обратитесь к терапевту, чтобы выяснить точные причины и вовремя принять меры.
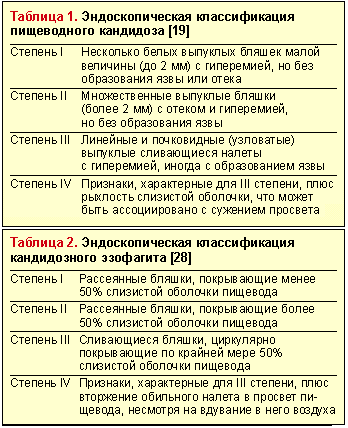
КАНДИДОЗ ПИЩЕВОДА
Кандидоз — инфекционное заболевание слизистых оболочек, кожи и внутренних органов, вызванное дрожжеподобными грибами рода Candida. Кандидоз пищевода (КП), являющийся проявлением висцерального кандидоза, занимает видное место среди инфекционных поражений пищевода. В последние годы прослеживается тенденция нарастания частоты КП, особенно у пациентов с нарушением иммунитета. Рост кандидозной инфекции в значительной степени обусловлен увеличением количества больных с ВИЧ-инфекцией, успехами в трансплантологии и иммуносупрессивной терапии, бесконтрольным использованием антибиотиков. КП встречается у 0,7-1,5% больных гастроэнтерологического профиля [5, 6].
Проблема тяжелых грибковых инфекций, вызываемых оппортунистическими патогенами, состоит в том, что они трудно поддаются лечению и могут приводить к летальному исходу. Было обнаружено, что смертность при инвазивных кандидозных инфекциях составляет 34% [16].
Благоприятные условия для развития инфекционного процесса создают различные нарушения физиологических, анатомических и иммунологических механизмов защиты организма. В качестве факторов, провоцирующих возникновение эзофагеального кандидоза, можно назвать использование антибиотиков, ингаляционных или инъекционных кортикостероидов, антацидную терапию или гипохлоргидрическое состояние, сахарный диабет, алкоголизм, последствия интоксикации, недоедание, пожилой возраст, нарушение моторики пищевода или пищеводную обструкцию, трансплантацию органов и костного мозга, энтеральное и особенно парентеральное питание и др. Ослабление иммунной системы может привести к возникновению кандидозной инфекции. При сахарном диабете повышенный уровень глюкозы в крови способствует росту грибов, так как гипергликемия ослабляет функцию гранулоцитов. Гипофункция паращитовидных желез и надпочечников приводит к нарушению кальциево-фосфорного обмена, что вызывает скрытую спазмофилию пищевода, тем самым снижая его местные защитные возможности [9]. Нарушения нутритивного статуса из-за недостатка белка в организме и низкой калорийности пищи влияют на состояние иммунной системы и создают предпосылки для развития кандидоза [3]. К факторам риска заболевания кандидозом относится снижение кислотности желудочного сока (рН 7,4 является оптимальной для роста грибов Candida, а при сдвиге рН до 4,5 рост грибов полностью угнетается) [3, 4, 7].
Патологические проявления КП разнообразны. Сначала пораженные участки пищевода имеют вид отдельных беловатых или желтоватых очажков, приподнятых над слизистой оболочкой. Позднее эти очажки могут сливаться, образуя плотные налеты с внедрением гриба в подслизистую оболочку или псевдомембранозные наложения с проникновением гриба в мышечную оболочку и сосуды [9]. Пленки, образующиеся на слизистой пищевода в особенно тяжелых случаях, могут почти полностью закрывать просвет пищевода. Налет состоит из слущенных эпителиальных клеток, которые смешиваются с грибками, клетками воспаления и бактериями. Микроскопическое исследование позволяет выявить равномерно окрашенные дрожжеподобные клетки и нити мицелия грибов Candida [9]. Истинное язвообразование наблюдается нечасто и в большинстве случаев отмечается у иммуносупрессированных больных с гранулоцитопенией [29]. Иногда возникает некроз стенки пищевода и развивается флегмонозное воспаление пищевода и средостения, что может стать одной из причин смерти больного [1].
Существует морфологическая классификация, согласно которой все случаи КП подразделяются на три группы в зависимости от степени тяжести процесса, то есть в зависимости от глубины поражения его стенки: 1-я группа — отдельные беловатые налеты с внедрением псевдомицелия гриба между эпителиальными клетками; 2-я группа — пленчатые налеты, сливающиеся между собой и образующие обширные поля, при этом нити псевдомицелия прорастают не только слизистую, но и подслизистую оболочку; 3-я группа — псевдомембранозные наложения, сочетающиеся с глубокими изменениями, при которых нити гриба глубоко проникают в толщу мышечной ткани [10].
Клинические проявления и осложнения. Симптомы заболевания практически отсутствуют у 25-30% пациентов, страдающих КП, особенно у иммунокомпетентных лиц. Тем не менее большинство пациентов предъявляют жалобы, связанные с поражением желудочно-кишечного тракта. Наиболее типичные клинические проявления КП — дисфагия и несколько реже одинофагия. Степень выраженности пищеводных симптомов колеблется от умеренного затруднения при глотании до резко выраженной боли, результатом чего являются неспособность принимать пищу и развитие вторичной дегидратации. При тяжелой одинофагии возможно наличие других причин или коинфекции, особенно у больных со СПИДом. Гораздо реже больные могут жаловаться на загрудинные боли, не связанные с глотанием, изжогу, тошноту, иногда рвоту с выделением пленок (псевдомембран), снижение аппетита и веса, появление жидкого стула со слизью (см. рисунок) [4, 9, 29].
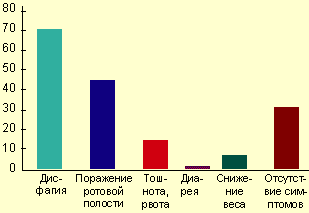 |
| Симптомы кандиозного эзофагита (R. S. Orlando, 1996) |
При КП может быть полезно физикальное исследование. Приблизительно две трети пациентов со
СПИДом и пищеводным кандидозом имеют кандидозный стоматит. КП наблюдается у больных с хроническим слизисто-кожным кандидозом, который относится к тяжелым формам кандидозной инфекции и чаще наблюдается при дисфункции надпочечников и околощитовидных желез [29].
Осложнения пищеводного кандидоза наблюдаются редко. Эзофагеальное кровотечение может наблюдаться при тяжелом течении болезни, сопровождающемся образованием эрозий, язв, и ассоциироваться с коагулопатией; возможно развитие перфорации. Описана вторичная обструкция просвета мицетомой. Редко возникает некроз с развитием флегмонозного воспаления пищевода и средостения [1]. В тяжелых случаях специфический эзофагит может осложниться развитием кандидамикозного сепсиса [6].
Диагностика. Подозрение на пищеводный кандидоз должно возникнуть у любого больного при наличии факторов риска развития пищеводной инфекции и жалоб на дисфагию и одинофагию. Наличие кандидозного стоматита подтверждает этот диагноз, но при его отсутствии поражение пищевода также не исключается.
Рентгенография пищевода с использованием бария обычно применяется для начальной оценки перед проведением эндоскопии. Однако на ранних стадиях кандидозного эзофагита рентгенологическое исследование пищевода не имеет большого диагностического значения, так как оно отражает лишь неспецифические изменения, общие для всех эзофагитов [2]. Классическими рентгенологическими признаками острого эзофагита, вызванного Candida spp., являются линейные или неправильной формы дефекты наполнения с четкими краями. При тяжелом течении кандидозного эзофагита происходит слияние повреждений, из-за чего большие дефекты наполнения иногда образуют скопления в виде гроздьев винограда [2]. Пищевод при этом приобретает «косматый» («ворсистый») вид, симулируя ульцерацию [25]. Наличие больших, хорошо очерченных язв не является признаком кандидозного эзофагита. Могут наблюдаться нарушение моторики и сужение просвета пищевода за счет псевдомембран. Следует помнить о том, что нормальная рентгенограмма пищевода с использованием бария не исключает пищеводного кандидоза. Из-за тяжелой одинофагии больной не сможет выпить барий, что затрудняет рентгеногрфию пищевода [29].
Более информативным для диагностики кандидозного эзофагита считается рентгенологический метод двойного контрастирования, эффективность которого достигает 70% [26].
Цитологическая щетка и баллонный катетер используются для быстрой диагностики пищеводных инфекций без эндоскопии. Эти инструменты могут быть легко введены через носовые ходы или рот сквозь защитный зонд, который предотвращает контаминацию. Материал, полученный на защищенной щетке или баллонном катетере после того, как они будут изъяты из пищевода, оценивается цитологически и культурально. Методика с использованием защищенных щеток имеет чувствительность 88% и специфичность почти 100% [26].
Цитологический метод предполагает окраску мазков-отпечатков или осадка смыва с цитологической щетки в поисках активных форм Candida — почкующихся дрожжевых клеток, псевдомицелия и мицелия. Культуральный метод предполагает помещение исследуемого материала на обогащенную глюкозой среду Сабуро или другие среды, чтобы затем по характеру образующихся колоний судить об этиологии инфекционного процесса в пищеводе.
Эндоскопическое исследование пищевода — наиболее чувствительный и специфический метод диагностики пищеводного кандидоза. Эндоскопическая картина КП характеризуется чаще всего наличием легко снимающихся фибринозных рыхлых наложений белого или желтого цвета, под которыми обнаруживается легкоранимая и/или отечная слизистая. Реже наблюдаются катаральный и эрозивно-язвенный эзофагит [19]. Candida spp. редко вызывает истинное язвообразование. Наличие язвы при кандидозном эзофагите нередко служит признаком дополнительного патологического процесса в пищеводе [29]. Существуют различные эндоскопические классификации пищеводного кандидоза (табл. 1 и 2).
В ходе эндоскопии пораженные участки слизистой могут быть подвергнуты щеточной биопсии для цитологического исследования или биопсии для гистологической диагностики. Когда эндоскопически идентифицируются язвы, многократное проведение биопсии помогает исключить наличие сосуществующих патологических процессов. Цитологическое исследование материала, полученного с помощью браш-биопсии, имеет более высокую ступень чувствительности, чем гистологическое исследование образцов биопсии при умеренном поверхностном кандидозе, потому что микроорганизмы могут быть вымыты с поверхности ткани при обработке биопсийного материала [19]. В редких случаях позитивная цитология при наличии отрицательной гистологии указывает на то, что речь идет скорее о колонизации, чем об инфекции. При более тяжелом кандидозном поражении пищевода наибольшее диагностическое значение имеет гистологическое исследование биоптатов слизистой с использованием специальной окраски на нейтральные мукополисахариды по Шиффу PAS (ШИК-реакция) или по Gomori гексаметилентетрамином серебра. Только гистологическое исследование демонстрирует инвазию мицелия или псевдомицелия гриба в глубь ткани пищевода.
Кожное тестирование и серологические тесты малоинформативны для диагностики пищеводного кандидоза.
Лечение. Существует множество пероральных и внутривенных медикаментов, которые используются для лечения кандидозного эзофагита. Несмотря на относительно широкий выбор препаратов, лечение КП является актуальной проблемой, так как некоторые лекарственные средства недостаточно эффективны, другие имеют серьезные побочные эффекты; кроме того, в настоящее время отмечается рост резистентности к антигрибковым препаратам.
При лечении КП первоначально должна быть назначена пероральная терапия, внутривенное введение используется лишь в случае рефрактерного течения заболевания или если имеются противопоказания к пероральному использованию медикаментов. Больным с умеренной степенью тяжести заболевания и минимальным нарушением иммунитета необходим сокращенный курс терапии с использованием системных абсорбируемых лекарственных препаратов типа орального азола. Иммунокомпрометированных больных после трансплантации и больных СПИДом с КП лучше лечить более длинными курсами азола. У пациентов с гранулоцитопенией, когда имеется существенный риск диссеминации Candida инфекции, оправданно использование внутривенных препаратов системного действия (азолов, амфотерицина B) [29].
Арсенал современных противогрибковых средств достаточно широк. Для лечения пищеводного кандидоза используют антигрибковые препараты нескольких групп. Наиболее эффективны препараты из группы азола. Перорально используют невсасывающиеся азолы (клотримазол, миконазол); однако более эффективны препараты системного действия из этой группы (кетоконазол, флуконазол и итраконазол). Эти препараты, подобно другим из группы азола, изменяют проницаемость клеточной мембраны грибов посредством цитохром P450 (CYP)-зависимого вмешательства в биосинтез эргостерола, что приводит к повреждению грибной клетки и ее смерти. Новые триазолы (итраконазол и флуконазол) имеют большее аффинное подобие, чем имидазолы (миконазол и кетоконазол) для грибных CYP-энзимов [14]. Хотя другие средства, такие, как миконазол, клотримазол и нистатин, могут быть использованы для лечения кандидозного стоматита, а также для профилактики пищеводного поражения, эти лекарственные средства менее эффективны в качестве основной группы препаратов для терапии КП [24].
Клотримазол и миконазол — препараты имидазолового ряда. В настоящее время выпускаются клотримазол в таблетках и миконазол для перорального применения. Однако они не всасываются в желудочно-кишечном тракте. Эти препараты могут использоваться при легком кандидозном поражении пищевода у лиц без иммунодефицита.
Кетоконазол (низорал, ороназол) является производным имидазола и при ежедневном приеме в дозе от 200 до 400 мг дает хороший эффект в лечении пищеводного кандидоза. У больных СПИДом, которым обычно требуются более высокие дозы кетоконазола, дневная доза может быть увеличена, если не возникает тошноты, до максимальной (800 мг). Кетоконазол хорошо проникает в различные органы и ткани, но плохо — через гематоэнцефалический барьер. Препарат хорошо всасывается в желудочно-кишечном тракте, но для оптимального всасывания требуется кислая среда. При желудочной гипохлоргидрии и использовании антацидных средств его биодоступность уменьшается. Для улучшения всасывания кетоконазол следует принимать за 2 часа до приема противоязвенных препаратов. Приблизительно у 10-25% больных СПИДом наблюдается снижение желудочной кислотной секреции. Кетоконазол же может вызвать временную блокаду синтеза тестостерона и кортизола [6, 8, 29].
Итраконазол (споранокс) относится к группе триазолов, подобно кетоконазолу, назначается в дозе 200 мг в день. Дальнейшее увеличение дозы удлиняет период полураспада препарата и повышает его эффективность. Всасывание интраконазола уменьшается при снижении pH желудочного сока [23]. Кетоконазол и итраконазол метаболизируются в печени и выделяются с желчью. Период полураспада этих двух препаратов составляет от 7 до 10 часов и от 24 до 42 часов соответственно [14]. Коррекции дозы у больных с почечной недостаточностью не требуется.
Флуконазол (дифлюкан, дифлазон, форкан, флюкостат — отечественный флуконазол) представляет собой водорастворимый триазол и назначается в дозе 100 мг в день. Флуконазол — это препарат, всасывание которого не зависит от pH желудочного сока и который значительно более эффективен при лечении пищеводного кандидоза при СПИДе, чем кетоконазол (200 мг ежедневно) [21]. Флуконазол доступен для перорального и внутривенного применения. Он минимально метаболизируется и выделяется неизмененным с мочой. Флуконазол отличается высоким тканевым тропизмом и не влияет на синтез андрогенов, хорошо проникает через гематоэнцефалический барьер. В отличие от кетоконазола и интраконазола он хорошо растворим в воде и минимально связывается белком. Препарат обладает длительным периодом полураспада (приблизительно 30 часов, если не нарушена функция почек, а наличие пищи или гипохлоргидрия не изменяют всасывание), что позволяет принимать его один раз в сутки. Показано, что введение флуконазола улучшает иммунные показатели по Т- и В-системам [18]. И флуконазол, и итраконазол можно принимать перорально в виде растворов. Эти формы могут быть более эффективны, чем таблетки, потому как усиливают локальный эффект и улучшают всасывание.
Неблагоприятные воздействия кетоконазола, флуконазола и итраконазола прежде всего зависят от дозировки и проявляются в виде тошноты, гепатотоксичности, замедления продукции стероидов и метаболизма циклоспорина [14]. В редких случаях кетоконазол может вызывать фатальный гепатит [12]. Незначительное увеличение аминотрансфераз — общий побочный эффект для всех трех препаратов, однако это не должно служить оправданием для их отмены. Влияние на стероидогенез наиболее выражено у кетоконазола. Обратимое замедление гонадального и надпочечного синтеза стероидов под воздействием кетоконазола может наблюдаться, когда доза превышает 400 мг в сутки [27]. В рекомендуемых дозах флуконазол и итраконазол не влияют на стероидогенез. В результате воздействия на печеночные микросомальные ферменты все три азола ингибируют метаболизм циклоспорина, что приводит к увеличению уровня циклоспорина в крови; этот эффект наиболее ярко выражен у кетоконазола [14].
Новейшим классом противогрибковых препаратов являются кандины, вмешивающиеся в синтез грибковой стенки. Они эффективны в отношении большинства видов Candida, в том числе C. krusei. Первые исследования показали, что капсофунгин, представляющий эту группу препаратов, оказался столь же эффективен при КП, как и амфотерицин В [16].
При лечении больных КП следует учитывать наличие резистентности, которая из-за широкого применения азолов в настоящее время значительно возросла. При развитии резистентности часто бывает полезно увеличить дозу азола. Если этого оказывается недостаточно, переходят на другой препарат из этой группы или используют пероральный раствор итраконазола [13], который нужно назначать в более высоких дозах из-за часто наблюдающейся перекрестной резистентности. Когда высокой дозы (то есть 400 мг ежедневно) флуконазола недостаточно, переходят на внутривенное введение амфотерицина B, при этом результат достигается в 90% случаев. Резистентность к амфотерицину наблюдается редко [29].
В табл. 3 представлено лечение кандидозного эзофагита в зависимости от функции лимфоцитов и гранулоцитов.
При лечении кандидозного эзофагита у больных СПИДом препаратами первого ряда являются кетоконазол и флюконазол, причем предпочтение следует отдавать флюконазолу. Из-за лучшей переносимости он прежде всего показан пациентам, находящимся на поздней стадии болезни, которые имеют много сопутствующих заболеваний. При нарушении глотания могут применяться парентеральные формы флуконазола. При неэффективности препаратов первого ряда используют лекарственные средства из группы резерва (амфотерицин В, итраконазол), которые более токсичные и/или более дорогие. Этиотропная терапия кандидоза пищевода, кроме основного курса лечения, требует проведения поддерживающего лечения, которое может быть пожизненным (табл. 4) [4].
Лечение кандидоза на фоне тяжелого иммунодефицита и лейкопении — задача сложная. Наряду с антигрибковой терапией актуально восстановление пула нейтрофильных лейкоцитов и их функциональной активности, так как нейтрофильные лейкоциты являются одним из основных звеньев механизма защиты от Candida spp. Предлагается в качестве дополнительного средства при лечении кандидозной инфекции на фоне нейтропении использовать гранулоцитарный колониестимулирующий фактор, который сокращает дефицит миелопероксидазы в нейтрофильных лейкоцитах и усиливает их кислородозависимую антикандидозную активность [7]. Получен хороший эффект от эндоскопического введения больным КП концентрата гранулоцитов и высокоинтенсивного импульсного лазерного излучения, что улучшает иммунные функции [5].
Таким образом, для достижения успеха у больных с тяжелыми грибковыми инфекциями, в том числе с кандидозом, целесообразен комплексный подход к диагностике и лечению. Повышению выживаемости будет способствовать оперативная диагностика с последующими подбором эффективной специфической противогрибковой терапии и проведением лечебных мероприятий, направленных на повышение числа гранулоцитов и стимуляцию фагоцитоза [16].
По вопросам литературы обращайтесь в редакцию