Рча сердца что можно после операции и что нельзя
РЧА в кардиологии. Показания и противопоказания.
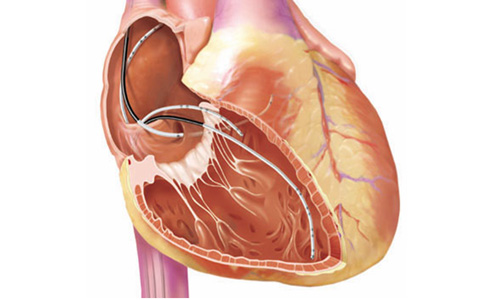
В настоящее время радикально решить проблему ускоренного проведения импульсов по сердечной мышце, лежащую в основе тахикардии, позволяет операция радиочастотной абляции (РЧА), или методика “прижигания сердца”. С помощью данной методики ликвидируется небольшой участок ткани, осуществляющий патологически частое возбуждение сердечной мышцы. Это осуществляется путем воздействия на ткань радиочастотных сигналов, оказывающих повреждающее действие. В результате дополнительный путь проведения импульсов прерывается, в то же время нормальные пути проведения импульсов не повреждаются, и сердце сокращается в своем обычном ритме, с частотой 60-90 ударов в минуту.
Показания для операции
Основными показаниями для проведения радиочастотной катетерной абляции являются нарушения ритма по типу тахикардии или тахиаритмии. К ним относятся:
Мерцательная аритмия – нарушение ритма, при котором мышечные волокна предсердий сокращаются по отдельности, изолированно друг от друга, а не синхронно, как при нормальном ритме. При этом создается механизм циркуляции импульса, и возникает патологический очаг возбуждения в предсердиях. Это возбуждение распространяется на желудочки, которые начинают также часто сокращаться, что вызывает ухудшение общего состояния пациента. Частота сердечных сокращений при этом достигает 100 – 150 ударов в минуту, иногда более.
Желудочковая тахикардия – частое сокращение желудочков, опасное тем, что быстро, еще до оказания помощи, может развиться фибрилляция желудочков и остановка сердца (асистолия).
ВПВ – синдром – заболевание, обусловленное врожденными нарушениями в проводящей системе сердца, в результате чего сердечная мышца предрасположена к опасным пароксизмальным тахикардиям.
Хроническая сердечная недостаточность и кардиомегалия (расширение полостей сердца), вследствие чего возникают нарушения ритма сердца.
Противопоказания
Несмотря на доступность и малую травматичность метода, он имеет свои противопоказания. Так, метод РЧА не может быть применен, если у пациента наблюдаются следующие заболевания:
Острый инфаркт миокарда,
Лихорадка и острые инфекционные заболевания,
Обострение хронических болезней (бронхиальная астма, декомпенсация сахарного диабета, обострение язвенной болезни желудка и др),
Тяжелая почечная и печеночная недостаточность.
Подготовка к процедуре
Госпитализация в стационар, где будет проводиться абляция, осуществляется в плановом порядке. Для этого пациент должен быть максимально обследован в поликлинике по месту жительства лечащим аритмологом, а также ему необходимо получить консультацию кардиохирурга.
Перечень обследования перед операцией включает в себя:
Общие анализы крови и мочи,
Анализ свертывающей системы крови – МНО, протромбиновое время, протромбиновый индекс, АЧТВ, время свертывания крови (ВСК),
УЗИ сердца (эхокардиоскопия),
ЭКГ, а при необходимости мониторирование ЭКГ по Холтеру (оценка сердечного ритма по ЭКГ за сутки),
ЧПЭФИ – чрезпищеводное электрофизиологическое исследование – может понадобиться в том случае, если врачу необходимо точнее установить локализацию источника патологического возбуждения, а также если нарушения ритма по ЭКГ не регистрируются, хотя у пациента сохраняются жалобы на приступообразное учащенное сердцебиение,
Пациентам с ишемией миокарда может быть показано проведение коронароангиографии (КАГ) перед операцией,
Исключение очагов хронической инфекции – консультация стоматолога и ЛОР-врача, а также уролога для мужчин и гинеколога для женщин – как и перед любой операцией,
Исследование крови на ВИЧ, вирусные гепатиты и сифилис.
После того, как пациент запланирован на операцию, он должен госпитализироваться в стационар за два-три дня до назначенной даты. За сутки до операции следует отказаться от приема антиаритмических или иных препаратов, могущих оказывать влияние на сердечный ритм, но только по согласованию с лечащим врачом.
Возможные осложнения
Операция абляции является малотравматичной, поэтому осложнения могут появиться в крайне редких случаях (менее 1%). Тем не менее, регистрируются следующие неблагоприятные состояния после операции:
Инфекционно-воспалительные – нагноения кожи в месте пункции, инфекционный эндокардит (воспаление внутренней полости сердца),
Тромбоэмболические осложнения – формирование тромбов вследствие травматизации сосудистой стенки и распространение их по сосудам внутренних органов,
Нарушения сердечного ритма,
Прободение артерий и стенки сердца катетером и зондом.
Образ жизни и прогноз после операции
Образ жизни после операции должен соответствовать следующим принципам:
Рациональное питание. В связи с тем, что основной причиной нарушений ритма сердца является ишемическая болезнь сердца, следует стремиться к профилактическим мерам, снижающим уровень”вредного” холестерина в плазме крови и предупреждающим его отложение на стенках сосудов, питающих сердечную мышцу. Самым главным из подобных мероприятий является снижение потребления животных жиров, продуктов фаст-фуд, жареной и соленой пищи. Приветствуется употребление зерновых, бобовых культур, растительных масел, нежирных сортов мяса и птицы, кисломолочных продуктов.
Адекватные физические нагрузки. Заниматься легкой гимнастикой, ходьбой и легким бегом полезно для здоровья сердца и сосудов, но должно быть начато через несколько недель после операции и только по разрешению лечащего врача.
Отказ от вредных привычек. Учеными давно доказано, что курение и алкоголь не только повреждают стенку сосудов и сердце изнутри, но и могут оказывать прямой аритмогенный эффект, то есть провоцировать пароксизмальные тахиаритмии. Поэтому прекращение курения и отказ от крепких спиртных напитков в больших количествах является профилактикой нарушений ритма.
В заключение необходимо отметить – несмотря на то, что РЧА является хирургическим вмешательством в организм, риск осложнений сравнительно не велик, а вот польза от операции несомненна – большинство пациентов, судя по отзывам, перестают испытывать неприятные симптомы и менее подвержены риску сосудистых катастроф, связанных с пароксизмами тахиаритмий.
Главный врач

БОНДАРЬ ВАЛЕРИЙ ВАСИЛЬЕВИЧ
Главный врач ГБУЗ «Никольская районная больница» ведёт личный приём граждан каждый понедельник и четверг с 13-00 до 16-00. Вы имеете возможность также задать вопрос в электронном виде.
Жизнь после радиочастотной аблации (РЧА)
Радиочастотная катетерная абляция (РЧА) сердца
РЧА сердца – хирургическое катетерное вмешательство, с использованием специальных катетеров, пункционно введенных в полость сердца через сосуды, и радиочастотной энергии, направленное на устранение нарушений сердечного ритма (аритмии).
Это один из самых современных методов лечения некоторых видов нарушений ритма сердца. Этот вид лечения относится к малоинвазивным вмешательствам, так как для его проведения не требуется никаких разрезов и доступов к сердцу, но иногда РЧА выполняется при операциях на открытом сердце.
Радиочастотная абляция проводится с помощью тонкого гибкого катетера-проводника, который вводится через кровеносный сосуд и подводится к источнику неправильного ритма в сердце, вызывающего аритмию. Далее по этому проводнику подается радиочастотный импульс, который разрушает участок ткани, отвечающий за неправильный ритм.
Радиочастотная (РЧ) энергия имеет широкий диапазон и зависит от сопротивления и диэлектрических свойств тканей. Радиочастотный ток – это ток с меняющейся полярностью при частоте от 30 кГц до 300 МГц. Все генераторы РЧ тока, используемые для аблации, работают в диапазоне 300 кГц — 1 МГц.
Жизнь после операции
Рекомендации пациентам после радиочастотной катетерной аблации фибрилляции предсердий (ФП):
Что можно после РЧА?
После РЧА можно сразу же отправиться домой. Пребывание в стационаре не требуется, и больничный не нужен. Если пациент не является профессиональным спортсменом и не занимается тяжелым физическим трудом, то образ жизни перестраивать практически не придется.
Каким должно быть питание и образ жизни после РЧА?
Все, что потребуется после РЧА – это ежедневно гулять не менее 40-60 минут, избегать сидячего образа жизни, посещения бани и горячих ванн. Ограничений по питанию нет, хотя злоупотреблять алкоголем первые 2 недели после операции настоятельно не рекомендуется.
Что нельзя делать после РЧА?
После РЧА в течение месяца нельзя заниматься силовыми тренировками в зале: поднимать штангу, приседать с утяжелениями и выполнять весь комплекс упражнений, «дающих» значительную нагрузку на вены. В первые несколько суток после РЧА не следует заниматься аэробикой, гимнастикой и на велотренажере. При этом необходимо совершать длительные прогулки в спокойном темпе.
Какой вес можно поднимать после РЧА абляции?
В первые 2-3 дня после РЧА не рекомендуется поднимать предметы весом свыше 3-5 кг. Через 1-2 месяца можно вернуться к привычным силовым нагрузкам.
Читайте другие статьи:
Больницы, в которых выполняют РЧА
Получить консультацию Вы можете, обратившись в BOSTI, написав или позвонив по номеру 0555 71 08 61.
Правила жизни пациентов после операции на открытом сердце (операции коронарного шунтирования)
У пациентов, которые перенесли операцию аорто-коронарного или маммаро-коронарного шунтирования, то есть операцию на открытом сердце, всегда много вопросов. Постараемся ответить на самые часто задаваемые.
Можно ли пить после шунтирования?
Алкоголь после шунтирования не противопоказан. Вопрос в его количестве. Алкоголь в умеренной дозе является даже профилактикой атеросклероза. Под умеренной дозой понимается один бокал (200 мл) вина в день для мужчины. Эквивалентом является 50 грамм крепких напитков. При этом нужно отметить, что именно в красном вине есть полифенолы, которые благотворно влияют на липидный обмен. Что касается женщин, то рекомендуемые дозы в два раза меньше, чему у мужчин. Доказано, что «непьющим» мужчинам и женщинам не стоит рекомендовать начинать употреблять алкоголь. К слову, в гранатовом соке также много полифенолов и его благотворное действие в плане профилактики атеросклероза тоже доказано.
Сколько живут после шунтирования?
После шунтирования жить можно достаточно долго. Например, не так давно у нас на коронарографии был пациент, с маммаро-коронарным шунтом 25 летней давности. По какому-то счастливому стечению обстоятельств во внутренней грудной артерии (a.mammaria) не формируются атеросклеротические бляшки. Это самый качественный и длительно живущий шунт. Эту операцию впервые в мире сделал профессор Колесов В.И., работавший в 1-м Ленинградском Медицинском институте. Венозные шунты имеют более ограниченное время жизни, чаще 8-10 лет. Кардиохирурги стараются подобрать оптимальную для пациента тактику операции, учитывая «важность» пораженной артерии и чаще комбинируют артериальные и венозные шунты. Иногда встречается полная артериальная реваскуляризация, что, конечно, прогностический очень хорошо для пациента. Надо отметит, что изменяющиеся (зарастающие) венозные шунты можно стентировать. Имплантация стента в полностью закрытый или суженный шунт встречается не так уж и редко. Иногда эндоваскулярные хирурги даже восстанавливают кровоток в собственных артериях пациента, даже если они были много лет закрыты. Все это становиться возможно благодаря современным эндоваскулярным (внутрисосудистым) технологиям.
Конечно, на время жизни после аорто-коронарного шунтирования также влияет наличие постинфарктных рубцов, их распространенность, снижение сократительной функции сердца, а также наличие сопутствующих заболеваний. Например, наличие сахарного диабета, особенно его декомпенсированной формы будет ухудшать прогноз. Самое важное, чтобы пациент соблюдал все предписания кардиолога: имел стабильное артериальное давление, целевые уровни «вредного» холестерина, следил за показателями углеводного обмена, а также сохранял рекомендованную двигательную активность.
Диета после шунтирования/питание после шунтирования
По поводу диеты можно выделить два основных направления: во-первых, это ограничение животных жиров. К животным жирам относятся продукты, изготавливаемые из мяса, молока, мясных субпродуктов. Также холестерина слищком много в яичном желтке и икре. Самая правильная диета для кардиологического пациента – это средиземноморская. Она богата овощами (кроме картофеля), зеленью, рыбой, морепродуктами, зерновыми. Употребление мяса должно свестись к 1-2 разам в неделю. Предпочтение следует отдавать нежирным сортам мяса – индейке, куриной грудке, дичи. Рыба может использоваться и речная, и морская. Морская рыба богата полиненасыщенными жирными кислотами, которые борются с процессом атеросклероза.
Во-вторых, нужно стараться избегать «простых» легкоусвояемых углеводов. К ним в первую очередь относятся сахар и белая мука. Эти рекомендации в большей степени относятся к пациентам с сахарным диабетом и нарушением толерантности к углеводам («преддиабет»)? Но и просто пациентам после шунтирования не повредят. Для этого стоит избегать мучного и сладкого. Гарниры должны быть представлены овощами, бурым или диким рисом, макаронами из твердых сортов пшеницы.
Реабилитация после шунтирования
Этап реабилитации после шунтирования очень важен. В общем от того насколько правильно будет проведен этот этап лечения зависит и дальнейшее выздоровление. Реабилитацию после шунтирования следует разделить на три этапа. Первый этап начинается еще в стационаре, когда пациент начинает делать под контролем врача по лечебной физкультуре дыхательные упражнения и начинает ходить. Второй продолжается в санатории, где постепенно увеличивают нагрузку в виде ходьбы под контролем специалистов и адаптируют пациента к повседневной жизни. Если операция шунтирования была плановая и послеоперационный период протекал спокойно, то переносимость нагрузки у пациента постепенно возрастает и становиться лучше, чем до операции. Собственно, для этого операция и делалась. Несмотря на то, что часто грудину во время операции открывают, а потом соединяют металлическими скобками, бояться, что она разойдется, не нужно. С другой стороны, нужно знать, что грудина срастается в течение 3-х месяцев и в течение этого времени надо ограничивать ассиметричные движения в верхнем плечевом поясе, отказаться от привычки закладывать руки за спину или носить что-то тяжелое в одной руке или на одном плече. У пациентов, которым делали операцию из миниинвазивного доступа очень повезло – с этими вопросами они не столкнуться. Третий этап- амбулаторный. Это самостоятельные тренировки в домашних условиях под четким руководством лечащего кардиолога, который с помощью нагрузочных проб может оценит в правильном ли режиме Вы тренируетесь.
Упражнения после шунтирования/Тренировки после шунтирования
Боли после шунтирования/Осложнения после шунтирования
Боли есть у всех пациентов после шунтирования в раннем послеоперационном периоде. Болит послеоперационная рана. Важно понимать, что сердце через несколько дней после операции коронарного шунтирования работает практически в «нормальном режиме». Плохое самочувствие пациента, помимо болей связано еще со снижением гемоглобина, иногда реакцией мозга на искусственное кровообращение. Важно:
Секс после шунтирования. Половая жизнь после шунтирования
Эректильная дисфункция частая проблема для наших пациентов, ведь по механизму возникновения она схожа с ишемической болезнью сердца, так как связана с недостаточным расширением артерий. Для большинства мужчин выходом из этой ситуации является прием ингибиторов фосфодиэстеразы 5 типа, то есть Виагры, Сиалиса и так далее. Сами эти препараты никакой дополнительной нагрузки на сердце не вызывают. Есть только одно важное правило – их ни в коем случае нельзя сочетать с нитропрепаратами (нитроглицерин, нитроспрей, нитросорбид, моночинкве, кардикет и так далее) из-за риска резкого снижения артериального давления. Если наши пациенты вынуждены принимать нитраты, то основные препараты для лечения эректильной дисфункции им противопоказаны.
Перелеты после шунтирования. Можно ли летать после шунтирования?
После шунтирования летать можно, если нет каких-либо других ограничений и послеоперационный период прошел спокойно. Первый перелет возможен через 10 дней. Об этом мы можем говорить с уверенностью, так как все наши пациенты, прооперированные в Германии возвращались на самолете домой именно в этот период. Все пациенты после шунтирования принимаю пожизненно малые дозы аспирина. А это хорошая профилактика артериальных тромбозов в том числе во время перелетов.
Одними из факторов риска длительных перелетов являются обезвоживание организма и застой крови в венах ног. Важно пить достаточно жидкости и, при длительных перелетах, не забывать вставать и разминаться.
Ключевую роль в жизни пациента после операции на открытом сердце играет врач-кардиолог. Поэтому принципиально важно найти врача, которому пациент доверил бы свое здоровье. Правильнее всего в этой ситуации ориентироваться на имидж клиники и на опыт конкретного доктора. Ошибкой будет надеяться на кардиохирурга, который проводил операцию. У сердечно-сосудистых хирургов совершенно другая специализация.
Чем чаще пульс, тем выше потребность мышцы сердца в кислороде и тем больше крови требуется сердцу для нормальной работы. Одна из важных задач кардиолога – обеспечить пациенту достаточно редкий пульс для уменьшения потребности сердца в крови, но и не слишком редкий, чтобы в головном мозге кровоток сохранялся на достаточном уровне. Обычно идеальный пульс для пациента после шунтирования- 55-60 уд/мин. Основные препараты, которые мы используем для урежения пульса это бета- адреноблокаторы (бисопролол, метопролол, небиволол и др). Они не только урежают пульс в покое, но и уменьшают реакцию пульса на физические и эмоциональные нагрузки.
После коронарного шунтирования 99% пациентов нуждаются в приеме статинов. Никакие побочные эффекты от приема статинов (по большому счету это только возможные боли в мышцах) не могут сравниться с той пользой, которую дает замедление процесса атеросклероза у наших пациентов.
Сразу после шунтирования походы к кардиологу будут достаточно частые. Это зависит от того как прошел послеоперационный период, были ли осложнения, находился ли пациент на реабилитации. В дальнейшем, когда состояние становиться стабильным, достаточно посетить кардиолога 1-2 раза в год. На приеме врач оценит давление, пульс пациента, выявит возможные проявления стенокардии, сердечной недостаточности. Оптимально выполнить нагрузочный тест- стресс- эхокардиографию, который поможет оценить работу сосудов сердца после операции. ЭКГ и УЗИ сердца в покое не дадут достаточной информации о функциональном состоянии сердца, а соответственно, косвенной информации о проходимости шунтов. Контроль липидограммы (расширенного анализа на холестерин) позволит врачу отрегулировать дозу статинов. Помните, что для пациентов, перенесших операцию на сердце, целевой показатель холестерина липопротеидов низкой плотности («вредный холестерин») 1,5-1,8 ммоль/л, что значительно ниже, чем у других категорий пациентов!
Пациентам, перенесшим операцию на сердце следует незамедлительно обратиться к врачу при проявления первых признаков стенокардии. Боли, жжение или тяжесть за грудиной, которые возникают при физической нагрузке, прекращаются при ее остановке и реагируют на прием нитроглицерина – это повод срочно обратиться к врачу, в т.ч. вызвав скорую помощь. Внезапно возникшие или прогрессирующие симптомы стенокардии часто являются предвестником скорого инфаркта.
Антиаритмическая терапия до и после инвазивных методов лечения фибрилляции предсердий.
Оксана Михайловна Драпкина, профессор, доктор медицинских наук:
– Тарасов Алексей Владимирович. «Антиаритмическая терапия до и после инвазивных методов лечения фибрилляции предсердий».
Алексей Владимирович Тарасов, кандидат медицинских наук:
– Добрый день, уважаемые коллеги. Я хочу обсудить очень интересный, очень актуальный вопрос – тактика ведения до и после различных инвазивных методов лечения фибрилляции предсердий. На сегодняшний день на всех международных российских площадках обсуждается точка приложения радиочастотной абляции для лечения фибрилляции предсердия. Но почему-то очень забывают, как вести пациентов после радиочастотной абляции, хотя таких пациентов все больше и больше. И порой мы не знаем, как это делать, что с этими пациентами делать, потому что возникает ряд достаточно серьезных дискутабельных вопросов и даже порой антирекламных вопросов, потому что пациенты приходят после, например, изоляции устья легочных вен, но с рядом незакрытых вопросов. И как их вести, что есть на сегодняшний день, какой наш опыт, я постараюсь вам представить.
На сегодняшний день лечение пароксизмальной формы фибрилляции предсердий, безусловно, это антиаритмическая терапия и какие-то инвазивные методы лечения. Основным инвазивным методом лечения фибрилляции предсердий является катетерная радиочастотная абляция устья легочных вен. В основном сейчас делают антральную абляцию устья легочных вен. Основным показанием к радиочастотной абляции устья легочных вен является симптоматическая параксизмальная форма фибрилляции предсердий, резистентная как минимум к двум антиаритмическим препаратам. На сегодняшний день обсуждается – к одному антиаритмическому препарату или как минимум к двум антиаритмическим препаратам. Но пока это как минимум два антиаритмических препарата вы должны своему пациенту дать, если они не работают, только тогда решать вопрос о лечения фибрилляции предсердий именно методом катетерной абляции.
Также очень важно отметить, что такие пациенты должны быть без органической патологии сердца, потому что больные с органической патологией сердца имеют другие механизмы, не обязательно эктопия из устьев легочных вен, здесь уже вовлечены процессы в предсердной ткани, и у таких пациентов радиочастотная абляция будет либо малоэффективна, либо 50/50.
Что мы имеем после радиочастотной абляции. Послеоперационный период можно разделить на три периода. Первый период составляет три месяца, его называют ранним послеоперационным периодом, некоторые его называют слепым послеоперационным периодом. Это самый проблемный период, потому что возникают как рецидивы старой фибрилляций предсердий, так и рецидивы новых предсердных тахиаритмий, и дальше я объясню, почему. И на третьем месяце мы должны принять решение, как быть дальше. Далее следует непосредственно послеоперационный период от трех до двенадцати месяцев наблюдения. И после двенадцати месяцев – поздний послеоперационный период.
Какие проблемы нас ждут в раннем послеоперационном периоде? Прежде всего, самое неприятное то, что 15% направленных больных на инвазивное лечение фибрилляции предсердия чувствуют себя первых два-три месяца даже хуже. И в этом-то и вопрос антирекламы так называемой. Врач, направивший больного на радиочастотную абляцию, потому получает этого пациента через одну-две недели, и пациент ему говорит: «Доктор, мне стало хуже». Действительно, у 15% пациентов после радиочастотной абляции идет ухудшение какое-то. И связано это ухудшение с тем, что у 45% – 50% возникают предсердные тахиаритмии. И сейчас мы уже говорим, что если взять все эти предсердные тахиаритмии, в 50% возвращается фибрилляция предсердия, рецидивы, ранние рецидивы, и 50% новые регулярные предсердные тахикардии. И самое неприятное, что именно новые предсердные тахикардии и составляют сложность в терапии, в диагностике, потому что под ними могут лежать как левопредсердное трепетание, предсердные тахикардии – эктопические, которые очень сложно поддаются медикаментозной терапии.
И вот как пример кардиограмма, где представлена в раннем послеоперационном периоде левопредсердное трепетание предсердий. Раньше мы вообще практически мало видели левопредсердных трепетаний. И именно после радиочастотной абляции стали появляться вот эти параксизмы, которые доставляют нам порой достаточные сложности в выборе тактики лечения. И вот как пример такой неустойчивый параксизм предсердной тахикардии, причем непрерывно рецидивирующий, порой они идут у таких пациентов именно в ранний послеоперационный период.
С чем же связана проблема раннего послеоперационного периода? Прежде всего, вот эти рецидивы связаны с воспалительной реакцией, обусловленной термическим повреждением предсердной ткани. Надо не забывать также об автономной нервной системе. Дело в том, что внутренняя поверхность сердца не имеет болевых рецепторов, но она имеет очень мощную автономную нервную систему, и эта нервная система возбуждается. И, безусловно, пока существует воспаление, происходит запуск вот этих предсердных тахикардий порой новых. И надо не забывать об отсроченном эффекте радиочастотной абляции – опосредованном формировании так называемого рубцового препятствия. Потому что пока существует зона воспаления, аритмия может проводиться, но когда формируется рубец, безусловно, защита как изоляции устья легочных вен здесь уже происходит прочнее.
Но ранние рецидивы фибрилляции предсердий либо новых предсердных тахиаритмий не являются таким эталоном, что радиочастотная абляция неэффективна. 60% больных с ранними рецидивами предсердных тахикардий далее имели четкие устойчивый синусовый ритм, и процедура считалась эффективной. Поэтому нельзя считать, что если у пациента ранние рецидивы фибрилляции предсердий либо другие какие-то предсердные тахикардии, это неэффективность процедуры. Но у тех пациентов, у которых мы имеем полную эффективность радиочастотной абляции и в ранний и поздний послеоперационный период, мы уже будем говорить об абсолютной эффективности радиочастотной абляции. Поэтому существует такая терминология как абсолютная эффективность и ранняя эффективность. Мы говорим о ранней эффективности, если приступов в первые три месяца не возникает.
Какие методы обследования нужно проводить таким пациентам? Сбор анамнеза, выявление симптомных приступов аритмии. Безусловно, после радиочастотной абляции пациенты более к себе относятся внимательно и предъявляют жалобы. Нередко они могут предъявлять жалобы на учащение ритма, либо даже какие-то болевые ощущения в области сердца. Больному необходимо проводить ЭКГ в 12-ти отведениях для определения как нарушений проводимости ритма сердца, так и нарушений аритмии. Необходимо проводить 1–7-суточное Холтеровское мониторирование ЭКГ для выявления асимптомных аритмий. Мы рекомендуем проводить Холтеровское мониторирование через месяц, через два, три для оценки дальнейшей тактики лечения.
Сейчас существуют еще такие методы как имплантируемый подкожный кардиомонитор, петлевые кардиомониторы, ЭКГ, которые позволяют мониторировать кардиограмму до трех лет. И на каждом визите доктор может снимать показания и оценивать асимптомные рецидивы фибрилляции предсердий.
Какова тактика ведения больных после радиочастотной абляции в ранний период? Мы должны определиться с антиаритмической терапией, необходимость антиаритмической терапии, с антитромботической терапией – это очень важно, я в конце об этом скажу. И мы можем воспользоваться немедикаментозными методами лечения в слепой период. Сейчас очень активно используется чреспищеводная электрическая стимуляция для восстановления именно новых тахикардий, например, левопредсердное трепетание предсердий. И имеет эффективность восстановления при проведении чреспищеводной стимуляции. Если у больного страдает гемодинамика, мы должны проводить электрокардиоверсию.
В чем вопрос антиаритмической терапии в ранний послеоперационный период. Сейчас нет четкости – нужно ли восстанавливать ритм этим пациентам или же стараться удерживать синусный ритм. Потому что пока нет четких конкретных данных, какой выбор тактики лучше «ритм-контроль» или «частота-контроль»? В консенсусе о катетрной и хирургической абляции фибрилляции предсердий от 2007 года в тактике ведения для удержания синусного ритма рассматривался только амиодарон. Но я абсолютно не согласен, потому что мы берем пациентов достаточно молодого возраста, мы берем пациентов без органической патологии. И потом после радиочастотной абляции сажать на амиодарон – на токсичный препарат абсолютно неоправданно. Поэтому в консенсусе от 2012 года предлагается более расширенный список антиаритмических препаратов: флекаинид, пропафенон, соталол, дофетилид или дронедарон. Но пока на сегодняшний день четких конкретных рекомендаций нет.
Тактика ведения именно на третьем месяце, когда прекращается слепой период. На третьем месяце мы должны четко понять, как быть дальше с этим пациентом, необходимо ли проводить повторную радиочастотную абляцию. Дело в том, что повторная радиочастотная абляция проводится достаточно часто (по многим авторам до 20% до 40%) – в нашей клинике до 40%, и это абсолютно нормальная тактика ведения пациентов. Но только после третьего месяца, когда пройдет воспаление, мы должны сказать, нужно ли проводить повторную радиочастотную абляцию или же не нужно. Если проанализировать поздние рецедивы предсердный тахиаритмий, если больному проводилась только одна радиочастотная абляция, поздние рецидивы возникают в 11% – 29% случаев. Если больному проводили как минимум две радиочастотные абляции, к сожалению, поздние рецидивы все равно случаются (по разным авторам от 7% до 24% случаев).
Какие причины возникновения поздних рецидивов предсердных тахиаритмий? Прежде всего, это возобновление проведения в зоне радиочастотной абляции устья легочных вен, когда наша изоляция начала пропускать импульс. И чаще, что возникает, это наличие триггеров, расположенных вне легочных вен. Нередко мы направляем больных на изоляцию устья легочных вен нельзя сказать запущенных, но уже когда время уходит. И из источника устья легочных вен эктопия опускается на предсердную ткань. Мы изолировали только устье легочных вен, но все предсердия мы не можем изолировать, поэтому, безусловно, эти триггеры начинают выстреливать и начинают давать поздние рецидивы. Но могу сразу сказать, что поздние рецидивы достаточно хорошо лечатся нашей современной антиаритмической терапией.
Я хочу представить наше интересное исследование, которое было начато еще в 2009 году на базе Московского областного кардиологического центра и дальше продолжено в ГНИЦ ПМ. Это был пилотный проект. Нами было обследовано 134 пациента, которым была проведена антральная изоляция устья легочных вен. И вот какие результаты мы получили. Ранние рецидивы предсердных тахикардий до трех месяцев возникали практически в 50% случаев. Но лишь только к повторной радиочастотной абляции пришли порядка 30% данных пациентов.
Следующий очень важный момент. У 30% больных преобладали регулярные предсердные тахикардии, то есть достаточно много было регулярных предсердных тахикардий, которые ставили наших врачей порой в тупик, как их лечить. И чаще всего превалировало левопредсердное трепетание предсердия. И в 20 % случаев были рецидивы фибрилляции предсердий.
Данные пациенты наблюдались до 12 месяцев, но больше нас интересовал именно слепой период, потому что у нас были выбраны различные тактики ведения пациентов, и одна группа пациентов вообще не принимала антиаритмических препаратов. Мы сейчас стали включать пациентов с имплантацией ревили (00:15:58) для исключения асимптомных рецидивов фибрилляции предсердий, и таких пациентов с имплантированными устройствами мониторирования у нас уже 39, но исследование не закончено, поэтому окончательные данные я вам не могу сказать.
Хочется сказать пока по полученным результатам. 36% больных продолжают прием антиаритмических препаратов даже после раннего послеоперационного периода. И здесь есть такое понятие как клиническая эффективность радиочастотной абляции. То есть мы уменьшаем количество приступов фибрилляции предсердий на 75%, больной себя чувствует лучше, чем до радиочастотной абляции. Но радиочастотная абляция полностью не убирает эти приступы. Но совместно с приемом антиаритмических препаратов пациента это устраивает, и приступы достаточно редки – два-три раза в год, и это нас устраивает.
На сегодняшний день наиболее эффективным антиаритмическим препаратом в послеоперационном периоде через три месяца и после радиочастотной абляции является препарат 1С класса – пропафенон. Но это больше у больных с рецидивами фибрилляции предсердий. Если же у больных появляются новые регулярные предсердные тахикардии, то здесь пропафенон нередко сочетается с верапамилом, либо отдельно верапамил – у таких пациентов показал хороший результат.
В конце презентации я хочу показать несколько слайдов о проблемах тромбоэмболических осложнений у таких пациентов. Нельзя сказать, что радиочастотная абляция абсолютно безопасная процедура, и в 0,6% возникают тромбоэмболические или кардиогенные инсульты, а в 1% случаев это транзиторные ишемические атаки. Но на сегодняшний день самый обсуждаемый вопрос – появление «немых» ишемических инсультов. И некоторые авторы пишут, что до 35% у таких пациентов определяются «немые» ишемические инсульты. С чем может быть связано появление такого большого количества? Не только с тромбоэмболическими проблемами, но надо понимать, что специфика процедуры радиочастотной абляции и появление воздушных эмболов тоже может вносить серьезный вклад в определение «немых» ишемических инсультов.
В чем проблема тромбообразования, появления тромбоэмболических осложнений? 1) Это большая зона повреждения эндотелия предсердий. 2) Установка транссептального интродьюсера и катетеров-электродов. 3) Оглушение предсердий – это очень важный момент. Это примерно как при кардиоверсии происходит оглушение предсердий, и создаются все условия для образования тромбов. И этот риск тромбоэмболических осложнений напрямую зависит от количества баллов по шкале CHA2DS2-VASc.
И вот пример позаимствован из одного американского журнала, статья вышла пару месяцев тому назад, где четко представлены данные чреспищеводного эхо, и мы видим мягкие тромбы на транссептальной перегородке. И на втором рисунке представлены обугленные элементы на конце электрода после удаления из транссептальной перегородки, которые могут являться причиной как небольших, так и серьезных мозговых нарушений. Но это с одной стороны, с другой стороны надо понимать, что есть проблема тромбоэмболоических осложнений, но есть проблема и кровотечений. И такая проблема, как тампонада перикарда происходит от 0,8% до 6% в зависимости от разных источников. Сосудистые осложнения возникают от 0% до 13%. Поэтому мы должны все-таки с одной стороны подготовить больного антикоагулянтами, но с другой стороны понимать, что есть риск кровотечений.
На сегодняшний день существует следующая тактика. Подготовка больных к радиочастотной абляции должна быть такая же, как при проведении электрической кардиоверсии. Для пациентов с фибрилляцией больше 48 часов, если мы берем радиочастотную абляцию, безусловно, обязательно нужно делать чреспищеводное эхо, потому что тромбоз ушка левого предсердия является противопоказанием для проведения данной процедуры. Через 4-6 часов после радиочастотной абляции мы должны назначить либо варфарин, либо новые оральные антикоагулянты. И, безусловно, на сегодняшний день очень обсуждается применение новых оральных антикоагулянтов при проведении радиочастотной абляции. Но пока четких данных нет, какой все-таки выигрывает из новых оральных антикоагулянтов. Отмена антикоагулянтной терапии должна проводиться на втором-третьем месяце (по европейским данным на втором месяце, на третьем месяце – по российским рекомендациям). Но если у больного есть хоть один балл по шкале CHA2DS2-VASc. мы должны продолжать назначать этому пациенту антикоагулянтную терапию, потому что мы не можем четко сказать, что у этого пациента не будет поздних рецидивов фибрилляции предсердий. На этом я хочу закончить свой доклад. Спасибо за внимание.