Разбор и решение задания №18 ОГЭ по химии
Определение характера среды раствора кислот и щелочей с помощью индикаторов. Качественные реакции на ионы в растворе.
В задании 18 ОГЭ по химии мы демонстрируем знания индикаторов и pH, а также качественные реакции на ионы в растворе.
Теория к заданию №18 ОГЭ по химии
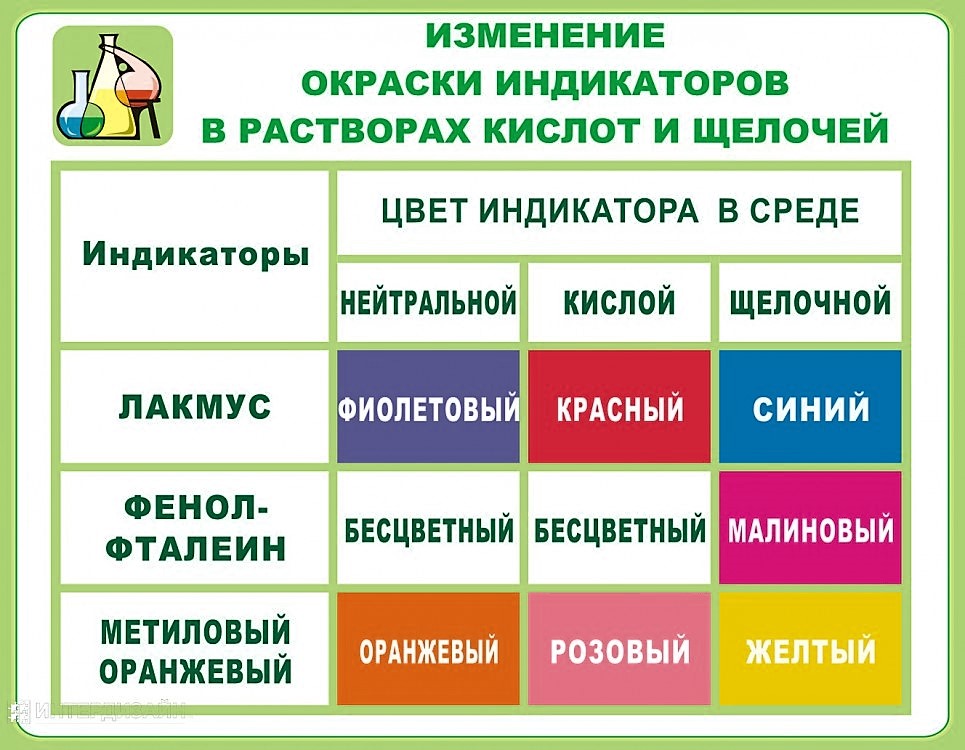
Индикаторы
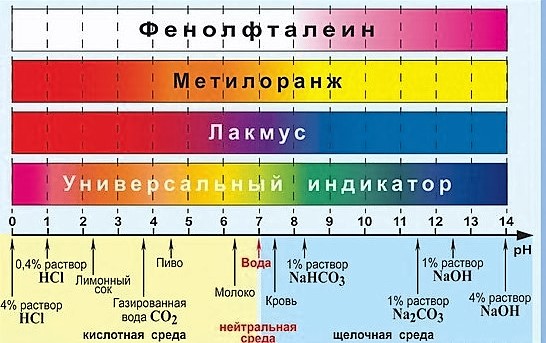
А вот ещё цвета индикаторов более подробно с жизненными примерами:
С индикаторами мы разобрались, перейдем к качественным реакциям на ионы.
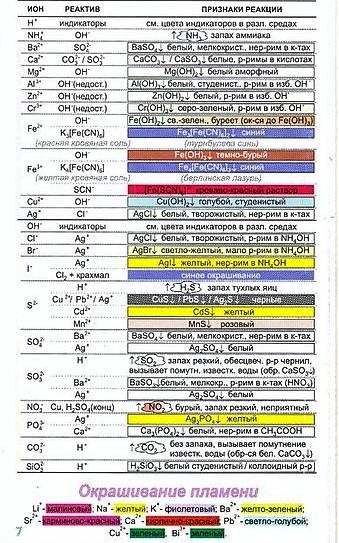
Качественные реакции на ионы
Качественные реакции на катионы и анионы представлены в таблице ниже.
Как правильно справиться с заданием 18 в тесте ОГЭ по химии?
Для этого необходимо выбрать качественную реакцию на один из предоставленных вариантов и убедится, что данный реактив не вступает в реакцию со вторым веществом.
Разбор типовых вариантов задания №18 ОГЭ по химии
Первый вариант задания
Установите соответствие между двумя веществами и реактивом, с помощью которого можно различить эти вещества.
А) Na2CO3 и Na2SiO3
Рассмотрим каждый случай.
Кислоты и щёлочи

И получается такое вещество, которое не относится ни к кислотам, ни к щелочам. Оно не способно вызывать ожоги. Но это будет только при правильной пропорции кислоты и щёлочи (иногда для верности пользуются фенолфталеином, он окрашивает щёлочь в слегка фиолетовый цвет).
Кислота и щёлочи — это как две противоположности. Но они очень важны при изготовлении таких вещей как: удобрения, пластик, мыла, моющие средства, красок, бумаги и даже взрывчаток. Это далеко не весь список.
Что такое кислота
Кислота — это и есть что-то кислое, оно характеризуется кислым вкусом. Кислота содержится в уксусе – уксусная кислота, в лимоне – лимонная кислота, в молоке – молочная кислота, в желудке – соляная кислота и т.п. Но это всё так называемые слабые кислоты, помимо них существуют кислоты с большей концентрацией (серная, синильная кислоты и т.д. хотя этот учёный пробовал). Они гораздо опаснее для человека и пробовать их не рекомендуется никому. Они способны разъесть одежду, кожу, вызвать тяжёлый ожог на коже, разъесть бетон и другие вещества. Например, соляная кислота нам нужна для того, чтобы желудок быстрее переваривал пищу, а также для уничтожения большинства вредных бактерий, которые приходят вместе с пищей.
Что такое щелочь?
Щелочь — это те вещества, которые хорошо растворяются в воде. При этом реакция сопровождается с выделением тепла, с увеличением температуры. Если щёлочь сравнивать с кислотой, то на ощупь она намного «мыльнее», то есть скользкая. Вообще, щёлочи не сильно отстают от кислот по разъеданию и по силе. Они также могут с лёгкостью разъесть древесину, пластик, одежду и тому подобное.
Кстати, из щёлочей делают мыло, стекло, бумагу, ткань и это не весь список. Щёлочь можно найти у себя на кухне, ну или в магазине под названием пищевая сода. Кстати, пищевая сода это очень хороший помощник всем домохозяйкам.
Кислоты и щёлочи – отличия
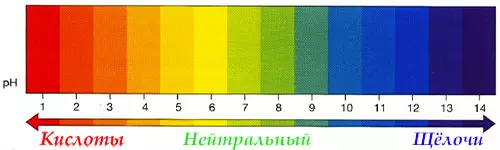
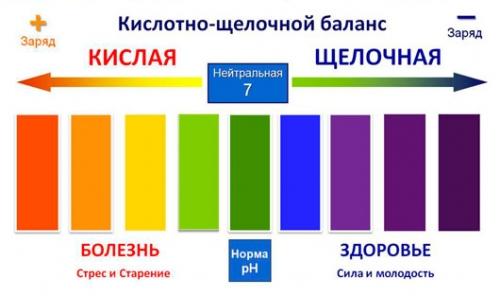
Кислоты и щёлочи отличают по показателям pH (шкала pH). Ниже Вы видите картинку – это специальная шкала, на которой имеются числа от 0 и до 14. Нулём обозначают самые сильные кислоты, а четырнадцатью – самую сильную щёлочь. Но какая же середина между этими числами? Может быть 5, может быть 7, а может быть 10? Серединой принято считать число 7 (нейтральное положение). То есть числа до 7 — это все кислоты, а больше 7 — это щёлочи.
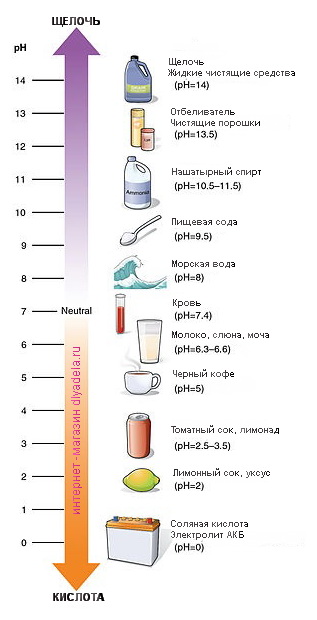
pH продуктов
Сильные кислоты и слабые кислоты
Есть некоторые кислоты, которые мы можем употреблять, в то время как работа с другими предполагает строгие меры безопасности.
Сильные кислоты — это те, которые полностью диссоциируют или ионизируются в водных растворах.
Один из способов визуализировать, как отличить слабые и сильные кислоты, по аналогии с игроками в регби:
Примеры сильных кислот
Среди известных сильных кислот выделяют:
Примеры слабых кислот
Обычно кислоты органических соединений известны как слабые:
Показатель кислотности растворов рН, механизм действия
Именно для этой шкалы разработаны специальные индикаторы — лакмусы. Это обычная полоска, которая реагирует на среду. В кислотной среде она окрашивается в красный цвет, а в щелочной среде – в синий цвет. Она необходима не только в химии, но и в быту.
Например, если у Вас есть аквариум, то немаловажную роль играет кислотность воды. От неё зависит вся жизнь аквариума. К примеру, показатель кислотности воды для аквариумных рыбок колеблется от 5 до 9 рН. Если будет больше или меньше, то рыбка будет чувствовать себя не комфортно, а может и вовсе умереть. Всё тоже самое и с растениями для аквариумов.
Работа с кислотами и щёлочами
Работа с кислотами и щёлочами требует большой внимательности и осторожности. Ведь при попадании на кожу они вызывают сильные ожоги. Старайтесь работать в проветриваемом помещении. Вдыхать пары щёлочей и кислот также не рекомендуется. Для личной безопасности стоит воспользоваться очками, перчатками и специальной одеждой, чтобы не повредить глаза, руки и любимую одёжку.
При работе с кислотами следует помнить, что сначала вливают кислоту в раствор (воду), а не наоборот. В противном случае произойдёт бурная реакция, которая сопровождается брызгами. А сам процесс добавления кислоты в раствор следует делать очень медленно, при этом контролировать степень нагрева сосуда и обязательно добавлять кислоту по стенкам сосуда.
При работе со щёлочами первым следует добавлять понемногу щёлочь. К тому же запрещено пользоваться стеклянной посудой, рекомендуют фарфоровую или специальную посуду.
При химической обработке металлов (оксидирование, анодирование, травление и др.) погружать в раствор и вынимать из раствора изделие следует с помощью специальных приспособлений или инструментов, но никак не руками, даже если они в резиновых перчатках. Кстати, щёлочь входит в состав некоторых батареек.
Запомните, что при химических ожогах кожи поражённое место нужно промыть сильной струёй проточной воды. И окончательно нейтрализовать: от кислот — 3%-ным раствором питьевой соды, а щёлочь — 1%-ным раствором уксусной кислоты.
Чем отличаются кислоты от щелочей
Кислоты и щёлочи отличают по показателям pH (шкала pH). Ниже Вы видите картинку – это специальная шкала, на которой имеются числа от 0 и до 14. Нулём обозначают самые сильные кислоты, а четырнадцатью – самую сильную щёлочь. Но какая же середина между этими числами? Может быть 5, может быть 7, а может быть 10? Серединой принято считать число 7 (нейтральное положение). То есть числа до 7 это все кислоты, а больше 7 это щёлочи.
Именно для этой шкалы разработаны специальные индикаторы — лакмусы. Это обычная полоска, которая реагирует на среду. В кислотной среде она окрашивается в красный цвет, а в щелочной среде – в синий цвет. Она необходима не только в химии, но и в быту.
Например, если у Вас есть аквариум, то немаловажную роль играет кислотность воды. От неё зависит вся жизнь аквариума. К примеру, показатель кислотности воды для аквариумных рыбок колеблется от 5 до 9 рН. Если будет больше или меньше, то рыбка будет чувствовать себя не комфортно, а может и вовсе умереть. Всё тоже самое и с растениями для аквариумов…
Кислоты
Кислоты — это соединения, содержащие водород и образующие ионы водорода (Н+) при растворении в воде. Ионы — это частицы с электрическим зарядом (см. статью «Химические связи»). Именно ионы придают кислотам их свойства, но существовать они могут только в растворе. Следовательно, свойства кислот проявляются исключительно в растворах. Молекула серной кислоты (H2SO4) состоит из атомов водорода, серы и кислорода. В состав соляной кислоты (НСl) входят водород и хлор. Кислота считается сильной, если большинство ее молекул распадаются в растворе, выделяя ионы водорода. Соляная, серная, азотная кислоты относятся к сильным. На контейнерах с сильными кислотами ставятся принятые во всем мире символы, означающие «опасно» и «высокая активность»Сила кислоты измеряется числом рН — водородным показателем. Сильные кислоты очень агрессивны; попав на поверхность предмета или на кожу, они прожигают её. На контейнерах с сильными кислотами ставятся принятые во всем мире символы, означающие «опасно» и «высокая активность».
Такие кислоты, как лимонная или уксусная, т.е. произведенные живыми организмами, называются органическими. Кислоты широко применяются в химической и медицинской промышленности, в производстве продуктов питания и синтетических волокон. Виноградный уксус содержит слабую кислоту, называемую уксусной. В помидорах есть органическая салициловая кислота. В цветных пятнах на коже морских улиток содержится кислота с неприятным вкусом, отпугивающая хищников. Для всех кислот характерно сходное поведение в химических реакциях. Например, при реакциях кислот с основаниями образуется нейтральное соединение — соль и вода. Реакции кислот с большинством металлов дают соль и водород. Реагируя с карбонатами, кислоты дают соль, углекислый газ и воду. Известный кулинарам пекарный порошок содержит гидрокарбонат натрия и винную кислоту. Когда в муку, содержащую пекарный порошок, добавляют воду, кислота и карбонат порошка вступают в реакцию, углекислый газ начинает выделятся в виде пузырьков, и это помогает тесту подниматься.
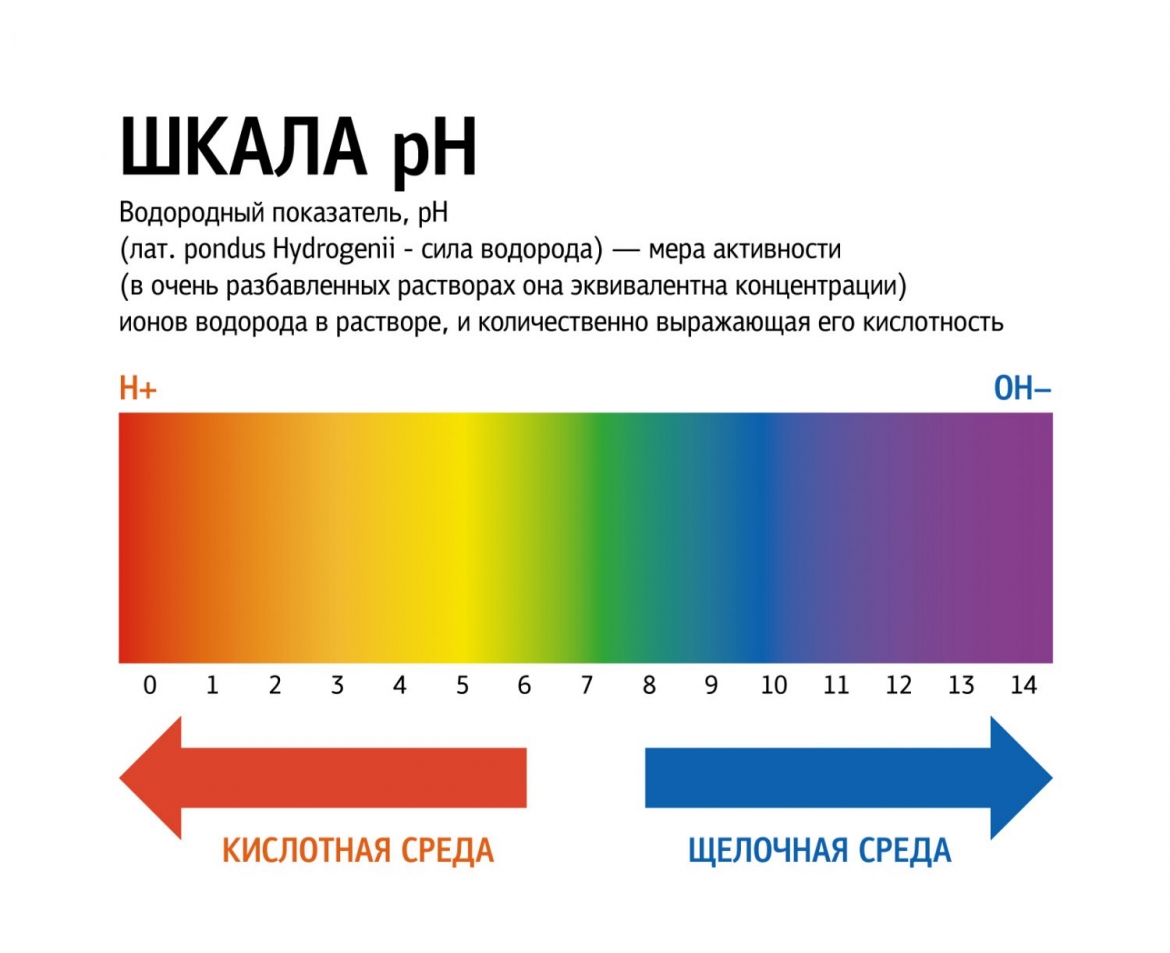
рН и индикаторы
Сила кислот и оснований определяется числом рН. Это мера концентрации ионов водорода в растворе. Число рН изменяется от 0 до 14. Чем меньше рН, тем выше концентрация водородных ионов. Раствор, рН которого меньше 7, — кислота. Апельсиновый сок имеет рН 4, значит, это кислота. Вещества с рН = 7 нейтральны, а вещества с рН больше 7 — основания или щелочи. рН кислоты или щелочи можно определить с помощью индикатора. Индикатор — это вещество, меняющее цвет при контакте с кислотой или щелочью. Так лакмус краснеет в кислоте и синеет в щелочи. Кислота окрашивает синюю лакмусовую бумажку в красные цвет, а красная лакмусовая бумажка в щелочи становится синей или фиолетовой. Лакмус получают из примитивных растений, называемых лишайниками. Другие растения, например, гортензия и краснокочанная капуста, также являются природными индикаторами.
Так называемый универсальный индикатор – это смесь нескольких красок. Он меняет цвет в зависимости от pH вещества. Он становится красным, оранжевым или желтым в кислотах, зеленым или желтым в нейтральных растворах и синим или фиолетовым в щелочах.
Серная кислота
Серная кислота играет важную роль в промышленности, прежде всего в производстве удобрений на основе суперфосфатов и сульфата аммония. Она также используется в производстве синтетических волокон, красителей, пластмасс, лекарств, взрывчатых веществ, моющих средств, автомобильных аккумуляторов. Когда-то серную кислоту называли минеральной кислотой, так как ее получали из серы — вещества, встречающегося в земной коре в виде минерала. Серная кислота очень активна и агрессивна. При растворении в воде она выделяет много тепла, поэтому ее нужно вливать в воду, но не наоборот — тогда кислота растворится, а вода поглотит тепло. Она — мощный окислитель, т.е. при реакциях окисления она отдает кислород другим веществам. Серная кислота также является осушителем, т.е. забирает воду, связанную с другим веществом. Когда сахар (C12H22O11) растворяется в концентрированной серной кислоте, кислота забирает у сахара воду, и от сахара остается пенящаяся масса черного угля.
Кислоты в почве
Цветы гортензии на кислотной почве синие, а на щелочной — розовыеКислотность почвы зависит от характера образовавших ее пород и от растущих на ней растений. На меловых и известняковых породах почва обычно щелочная, а на лугах, в песчаных и лесистых районах она более кислая. Кислотность также повышают кислотные дожди. Для земледелия лучше всего подходят нейтральные или слабокислые почвы, рН которых от 6,5 до 7. Разлагаясь, мертвые листья образуют органическую гуминовую кислоту и повышают кислотность почвы. Там, где почвы чересчур кислотные, в них добавляют измельченный известняк или гашеную известь (гидроксид кальция), т.е. основания, которые нейтрализуют кислоты почвы. Такие растения, как рододендроны и азалии хорошо растут на кислотных почвах. Цветы гортензии на кислотной почве синие, а на щелочной — розовые. Гортензия – природный индикатор. На кислотных почвах её цветы синие, а на щелочных розовые.
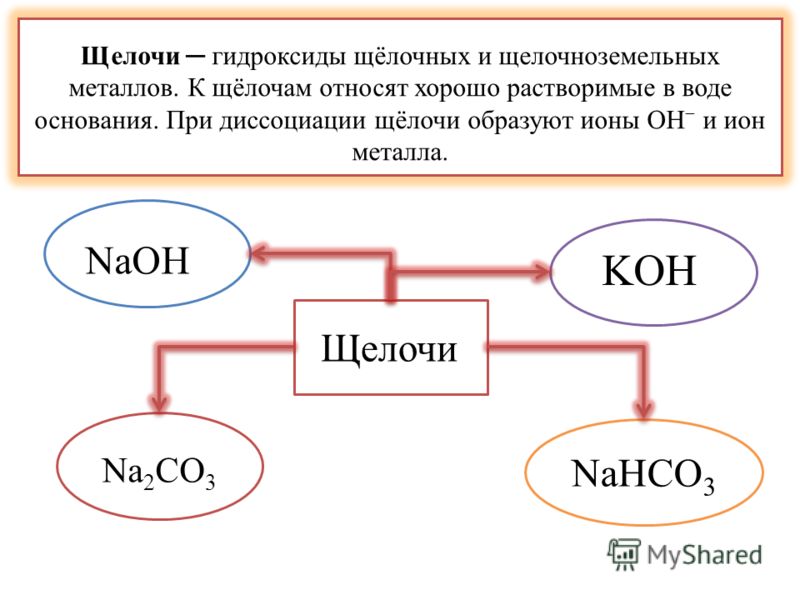
В настоящее время в химии принята теория Брёнстеда — Лоури и Льюиса, которая определяет кислоты и основания. В соответствии с этой теорией, кислоты — это вещества, способные отщеплять протон, а основания — отдавать электронную пару OH−. Можно сказать, что под основаниями понимают соединения, которые при диссоциации в воде образуют только анионы вида OH−. Если совсем просто, то щелочами называют соединения, состоящие из металла и гидроксид-иона OH−.
К щелочам принято относить гидроксиды щелочных и щелочно-земельных металлов. Все щелочи — это основания, но не наоборот, нельзя считать определения «основание» и «щелочь» синонимами.
Правильное химическое название щелочей — гидроксид (гидроокись), например, гидроокись натрия, гидроксид калия. Часто употребляются также названия, которые сложились исторически. Ввиду того, что щелочи разрушают материалы органического происхождения — кожу, ткани, бумагу, древесину, их называют едкими: например, едкий натр, едкий барий. Однако понятием «едкие щелочи» химики определяют гидроксиды щелочных металлов — лития, натрия, калия, рубидия, цезия.
Свойства щелочей
Щелочи — твердые вещества белого цвета; гигроскопичные, водорастворимые. Растворение в воде сопровождается активным выделением тепла. Вступают в реакции с кислотами, образуя соль и воду. Эта реакция нейтрализации является важнейшей из всех свойств щелочей. Кроме этого, гидроксиды реагируют с кислотными оксидами (образующими кислородосодержащие кислоты), с переходными металлами и их оксидами, с растворами солей.
Гидроксиды щелочных металлов растворяются в метиловом и этиловом спиртах, способны выдерживать температуры до +1000 °С (за исключением гидроксида лития).
Гидроксид натрия (едкий натр) используется в чистящих жидкостях, а также (как и гидроксид калия) для производства мыла. Мыло — это соль, образующаяся при реакции щелочей с кислотами растительных жиров. Жало осы выпускает щелочь, которую можно нейтрализовать кислотой, например уксусом.
Щелочи — активные химические реагенты, поглощающие из воздуха не только водяные пары, но и молекулы углекислого и сернистого газа, сероводорода, диоксида азота. Поэтому хранить гидроксиды следует в герметичной таре или, например, доступ воздуха в сосуд со щелочью организовать через хлоркальциевую трубку. В противном случае хим.реактив после хранения на воздухе будет загрязнен карбонатами, сульфатами, сульфидами, нитратами и нитритами.
Если сравнивать щелочи по химической активности, то она увеличивается при движении по столбцу таблицы Менделеева сверху вниз.
Концентрированные щелочи разрушают стекло, а расплавы щелочей — даже фарфор и платину, поэтому растворы щелочей не рекомендуется хранить в сосудах с пришлифованными стеклянными пробками и кранами, так как пробки и краны может заклинить. Хранят щелочи, обычно, в полиэтиленовых емкостях.
Именно щелочи, а не кислоты, вызывают более сильные ожоги, так как их сложнее смыть с кожи и они проникают глубоко в ткань. Смывать щелочь надо неконцентрированным раствором уксусной кислоты. Работать с ними необходимо в средствах защиты. Щелочной ожог требует немедленного обращения к врачу!
Применение щелочей
— В качестве электролитов.
— Для производства удобрений.
— В медицине, химических, косметических производствах.
— В рыбоводстве для стерилизации прудов.
Едкий натр. Самая популярная и востребованная в мире щелочь. Применяется для омыления жиров в производстве косметических и моющих средств, для изготовления масел в процессе нефтепереработки, в качестве катализатора и реактива в химических реакциях; в пищепроме.
Едкое кали. Применяется для производства мыла, калийных удобрений, электролитов для батареек и аккумуляторов, синтетического каучука. Также — в качестве пищевой добавки; для профессиональной очистки изделий из нержавеющей стали.
Гидроксид алюминия. Востребован в медицине как отличный адсорбент, антацид, обволакивающее средство; ингредиент вакцин в фармацевтике. Кроме этого, вещество применяется в очистных сооружениях и в процессах получения чистого алюминия.
Гидроокись кальция. Популярная щелочь с очень широким спектром применения, которую в быту знают под названием «гашеная известь». Используется для дезинфекции, смягчения воды, в производстве удобрений, едкого натра, «хлорки», строительных материалов. Применяется для защиты деревьев и деревянных сооружений от вредителей и огня; в пищепроме как пищевая добавка и реактив при производстве сахара.
Гидроокись лития. Востребованное соединение в химпроме как сырье; в стекольной, керамической, Фиксаналырадиотехнической индустрии; для производства смазочных материалов, электролитов; для поглощения вредных газов.
Гидроокись бария. Применяется в химпроме как катализатор, а также в пищепроме для очистки жиров, сахара.
• Кислоты и щелочи неспособны мирно сосуществовать даже одну секунду, находясь в соприкосновении. Перемешавшись, они мгновенно начинают бурное взаимодействие. Химическая реакция с ними сопровождается шипением и разогревом и длится до тех пор, пока эти ярые антагонисты не уничтожат друг друга.
• Кислотам свойственно образовывать кислую среду, а щелочам – щелочную.
• Химики отличают щелочь от кислоты по ее поведению с лакмусовой бумажкой или фенолфталеином.
Задания 33. Качественные реакции
51F997
Установите соответствие между формулами двух веществ и реактивом, с помощью которого можно различить эти вещества.
ФОРМУЛЫ ВЕЩЕСТВ
РЕАКТИВ
Ответ: А-5; Б-4; В-2; Г-1
Пояснение:
При пропускании аммиака через водный раствор лакмуса образуется гидрат аммиака – соединение, диссоциирующее в воде с образованием катионов аммония и гидроксид-анионов, следовательно, характер реакции среды становится щелочным, в результате чего раствор лакмуса окрашивается в синий цвет:
При пропускании хлороводорода через водный раствор HCl диссоциирует с образованием катионов водорода и хлорид-анионов:
Среда раствора становится кислой, и раствор лакмуса приобретает красный цвет.
Б) Азотную и соляную кислоты можно различить с помощью меди. Медь расположена в ряду активностей металлов правее водорода, поэтому взаимодействует только с кислотами-окислителями, например HNO3, соляная кислота медь не окисляет. В зависимости от концентрации азотной кислоты выделяются либо бурый газ, либо монооксид азота:
В) Сульфат натрия и нитрат калия можно различить, добавив их к растворам нитрата бария. С нитратом калия нитрат бария не реагирует. В случае с сульфатом натрия выпадает осадок белого цвета – BaSO4:
Алюминий является амфотерным металлом, и при взаимодействии его раствора соли со щелочью сначала выпадает осадок Al(OH)3, который затем в избытке щелочи превращается в растворимую комплексную соль – тетрагидроксоалюминат натрия:
A3BD96
Установите соответствие между формулами двух веществ и реактивом, с помощью которого можно различить эти вещества.
ФОРМУЛЫ ВЕЩЕСТВ
РЕАКТИВ
Ответ: А-2; Б-2; В-5; Г-5
Пояснение:
А) Отличить хлорид и сульфат калия можно с помощью щелочи Ba(OH)2, который, взаимодействуя с сульфатом, образует осадок белого цвета – BaSO4:
Хлорид калия с гидроксидом бария не реагирует.
Цинк является амфотерным металлом, и при взаимодействии его раствора соли со щелочью сначала выпадает осадок Zn(OH)2, который затем в избытке щелочи превращается в растворимую комплексную соль – тетрагидроксоцинкат бария:
В-Г) Различить растворы сильных кислот от растворов солей и щелочей можно с помощью соды – NaHCO3. При сливании растворов сильная кислота вытесняет слабую угольную из ее соли, в результате чего выделяется углекислый газ:
При взаимодействии соды со щелочью NaOH образуется средняя соль – карбонат натрия, однако видимые признаки реакции отсутствуют:
0877E2
Установите соответствие между формулами двух веществ и реактивом, с помощью которого можно различить эти вещества.
ФОРМУЛЫ ВЕЩЕСТВ
РЕАКТИВ
Ответ: А-4; Б-1; В-3; Г-2
Пояснение:
Алюминий является амфотерным металлом, и при взаимодействии его раствора соли со щелочью сначала выпадает осадок Al(OH)3, который затем в избытке KOH превращается в растворимую комплексную соль – тетрагидроксоалюминат калия:
Б) Различить растворы солей фосфата и сульфата натрия можно с помощью хлорида алюминия. С сульфатом натрия хлорид алюминия не реагирует, а с фосфатом натрия образует нерастворимую соль – фосфат алюминия:
В) Соляную кислоту и бромид калия можно различить с помощью железа. С соляной кислотой железо превращается в хлорид железа (II), кроме этого выделяется водород:
Г) Иодид калия и нитрат натрия можно отличить с помощью брома. Являясь более сильным окислителем по сравнению с йодом, бром вытесняет его из соли (с нитратом натрия бром не реагирует):
384A70
Установите соответствие между формулами двух веществ и реактивом, с помощью которого можно различить эти вещества.
ФОРМУЛЫ ВЕЩЕСТВ
РЕАКТИВ
А) пропанол-1 и фенол (р-р)
Б) крахмал и сахароза
В) пропанол-2 и глицерин
Ответ: А-3; Б-5; В-4; Г-1
Пояснение:
А) Отличить пропанол-1 от раствора фенола можно действием бромной воды. Для фенола ввиду наличия ароматического кольца характерны реакции электрофильного замещения. Влияние гидроксильной группы усиливает нуклеофильные свойства ароматического ядра, тем самым значительно облегчая замещение в орто- и пара-положениях. При приливании к водному раствору фенола бромной воды образующееся вначале помутнение при встряхивании исчезает. Дальнейшее прибавление бромной воды вызывает обильное выпадение белого осадка 2,4,6-трибромфенола:
Б) Крахмал и сахарозу можно отличить раствором йода.
20 – 30%) и амилопектина (
70 – 80%). Оба полисахарида содержат связанные между собой остатки α-глюкозы, но отличаются формой молекул и типом связи.
В амилозе остатки глюкозы связаны между собой (1→4)-глюкозидными связями, полисахаридная цепь имеет линейную структуру. Линейные молекулы амилозы содержат 200-300 углеводных остатков, ее молекулярная масса – несколько десятков тысяч. Молекула амилозы свернута в спираль, на каждый виток которой приходится шесть моносахаридных звеньев. Внутри спирали имеется канал диаметром около 0,5 нм, в котором могут располагаться подходящие по размеру молекулы, например I2. Комплекс амилозы с иодом имеет синий цвет, что используется для качественного обнаружения крахмала.
Амилопектин имеет разветвленное строение: остатки глюкозы в нем связаны не только (1→4), но и (1→6)-глюкозидными связями. Он состоит из гораздо более крупных молекул, чем амилоза: число остатков в них составляет несколько десятков тысяч, а молекулярная масса – несколько миллионов.
В) Пропанол-2 (изопропанол) и глицерин можно отличить свежеосажденным гидроксидом меди (II). Глицерин является трехатомным спиртом и в связи с наличием трех гидроксильных групп обладает более кислотными свойствами по сравнению с одноатомными спиртами, следовательно, может реагировать не только с щелочным металлами, но и с менее активными. Реакция глицерина со свежеосажденным гидроксидом меди (II) приводит к образованию темно-синего раствора глицерата меди (II):
Г) Толуол и бензол относятся к ароматическим углеводородам, однако толуол имеет один метильный радикал, который можно окислить перманганатом натрия (обесцвечивание раствора перманганата натрия). Само бензольное кольцо при этом к окислению устойчиво:
643645
Установите соответствие между формулами двух веществ и реактивом, с помощью которого можно различить эти вещества.