Универсальная газовая постоянная
Универса́льная га́зовая постоя́нная — термин, впервые введённый в употребление Д. Менделеевым в 1874 г. Численно равна работе расширения одного моля идеального газа в изобарном процессе при увеличении температуры на 1 К.
Содержание
Общая информация
В 1874 году Д. Менделеев вычислил значение константы в уравнении Менделеева-Клапейрона (уравнении состояния идеального газа) для одного моля газа, используя закон Авогадро, согласно которому 1 моль различных газов при одинаковом давлении и температуре занимает одинаковый объём (
В некоторых научных кругах эту постоянную принято называть постоянной Менделеева. Обозначается латинской буквой 
Входит в уравнение состояния идеального газа 
Удельная газовая постоянная (R/M) для сухого воздуха: 
Связь между газовыми константами
Универсальная газовая постоянная выражается через произведение постоянной Больцмана на число Авогадро, 
Примечания
См. также
Полезное
Смотреть что такое «Универсальная газовая постоянная» в других словарях:
универсальная газовая постоянная — Постоянная (R) в уравнении состояния для моля идеального газа (pv = RT), одинаковая для всех веществ. [Сборник рекомендуемых терминов. Выпуск 103. Термодинамика. Академия наук СССР. Комитет научно технической терминологии. 1984 г.] Тематики… … Справочник технического переводчика
универсальная газовая постоянная — molinė dujų konstanta statusas T sritis Standartizacija ir metrologija apibrėžtis Apibrėžtį žr. priede. priedas( ai) Grafinis formatas atitikmenys: angl. molar gas constant; universal gas constant vok. allgemeine Gaskonstante, f; ideale… … Penkiakalbis aiškinamasis metrologijos terminų žodynas
универсальная газовая постоянная — universalioji dujų konstanta statusas T sritis chemija apibrėžtis Idealiųjų dujų molinė būsenos lygties konstanta, lygi 8,314 J/K·mol. santrumpa( os) R atitikmenys: angl. gas constante per mole; universal gas constant rus. мольная газовая… … Chemijos terminų aiškinamasis žodynas
универсальная газовая постоянная — molinė dujų konstanta statusas T sritis fizika atitikmenys: angl. gas constant per mole; universal gas constant vok. ideale Gaskonstante, f; molare Gaskonstante, f; universelle Gaskonstante, f rus. универсальная газовая постоянная, f pranc.… … Fizikos terminų žodynas
универсальная газовая постоянная — Постоянная (R), входящая в управление состояния для моля идеального газа (pv = RT), одинаковая для всех идеальных газов … Политехнический терминологический толковый словарь
Газовая постоянная — Универсальная газовая постоянная R0 ≈ 8,314 кДж/(кмоль·K) фундаментальна физическая константа. Индивидуальная газовая постоянная R = R0/M, кДж/(кг·K) константа для газа или газовой смеси конкретной молярной массы … Википедия
универсальная газовая константа — molinė dujų konstanta statusas T sritis Standartizacija ir metrologija apibrėžtis Apibrėžtį žr. priede. priedas( ai) Grafinis formatas atitikmenys: angl. molar gas constant; universal gas constant vok. allgemeine Gaskonstante, f; ideale… … Penkiakalbis aiškinamasis metrologijos terminų žodynas
Газовая постоянная — универсальная физическая постоянная R, входящая в уравнение состояния 1 моля идеального газа: pv = RT (см. Клапейрона уравнение), где р давление, v объём, Т абсолютная температура. Г. п. имеет физический смысл работы расширения 1 моля… … Большая советская энциклопедия
ГАЗОВАЯ ПОСТОЯННАЯ — (обозначение R), универсальная постоянная в газовом уравнении (см. ЗАКОН ИДЕАЛЬНОГО ГАЗА), также называемая универсальной молярной газовой постоянной, равна 8,314510 ДжК 1 моль 1 … Научно-технический энциклопедический словарь
ГАЗОВАЯ ПОСТОЯННАЯ — (R), универсальная фнз. постоянная, входящая в ур ние состояния 1 моля идеального газа: pv=RT (см. КЛАПЕЙРОНА УРАВНЕНИЕ), где р давление, v объём моля, Т абс. темп pa. Г. п. по своему физ. смыслу работа расширения 1 моля идеального газа под пост … Физическая энциклопедия
Какое значение принимает универсальная газовая постоянная
Величины, характеризующие состояние газа, это m – масса газа,
V – объём газа, P – давление газа, T – температура газа. Эти величины называются параметрами состояния. Уравнение, связывающее параметры m, Р, V и T, называется уравнением состояния.
Уравнение состояния идеального газа – это уравнение Менделеева – Клапейрона
где m – масса газа; m – масса одного моля газа, тогда 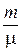
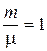
где R – универсальная газовая постоянная.
Выясним физический смысл универсальной газовой постоянной R.
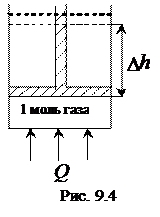
Пусть второе, конечное, состояние газа характеризуется параметрами V2, Р1, T2. При подводе тепла Q поршень приподнялся на высоту Dh в результате расширения газа при постоянном давлении P1. Газ совершил работу А по поднятию поршня:
где F – сила, действующая на поршень со стороны газа; P1 – давление газа на поршень. Давление P1 и сила F связаны соотношением
Записываем уравнение Менделеева – Клапейрона для 1 моля газа дважды: для первого состояния и для второго:
и вычтем из нижнего уравнения верхнее. Получим
где \(\Delta T\) – изменение температуры при переходе газа из начального состояния в конечное состояние. Так как
Теперь можно определить физический смысл универсальной газовой постоянной R.
Универсальная газовая постояннаяR равна работе, которую совершает 1 моль идеального газа при изобарическом расширении, если газ нагреть на один градус.
п V знак равно п р Т знак равно м р s п е c я ж я c Т <\ displaystyle PV = nRT = mR _ <\ rm
СОДЕРЖАНИЕ
Габаритные размеры
Из закона идеального газа PV = nRT получаем:
Поскольку давление определяется как сила, приходящаяся на область измерения, уравнение газа также можно записать как:
р знак равно ж о р c е а р е а × v о л ты м е а м о ты п т × т е м п е р а т ты р е <\ displaystyle R = <\ frac <<\ dfrac <\ mathrm
Площадь и объем равны (длина) 2 и (длина) 3 соответственно. Следовательно:
р знак равно ж о р c е ( л е п грамм т час ) 2 × ( л е п грамм т час ) 3 а м о ты п т × т е м п е р а т ты р е знак равно ж о р c е × л е п грамм т час а м о ты п т × т е м п е р а т ты р е <\ displaystyle R = <\ frac <<\ dfrac <\ mathrm
Поскольку сила × длина = работа:
р знак равно ш о р k а м о ты п т × т е м п е р а т ты р е <\ displaystyle R = <\ frac <\ mathrm
В противном случае мы также можем сказать, что:
Следовательно, мы можем записать R как:
Связь с постоянной Больцмана
Измерение и замена на определенное значение
Однако после переопределения базовых единиц СИ в 2019 году R теперь имеет точное значение, определенное в терминах других точно определенных физических констант.
Удельная газовая постоянная
р s п е c я ж я c знак равно р M <\ displaystyle R _ <\ rm
Так же, как постоянная идеального газа может быть связана с постоянной Больцмана, то же самое можно сделать и с постоянной газом путем деления постоянной Больцмана на молекулярную массу газа.
р s п е c я ж я c знак равно k B м <\ displaystyle R _ <\ rm
Еще одно важное соотношение исходит из термодинамики. Соотношение Майера связывает удельную газовую постоянную с удельной теплоемкостью для калорийно совершенного газа и термически совершенного газа.
Стандартная атмосфера США
Обратите внимание на использование киломолей, что дает коэффициент 1000 в константе. USSA1976 признает, что это значение не согласуется с приведенными значениями для постоянной Авогадро и постоянной Больцмана. Это несоответствие не является существенным отклонением от точности, и USSA1976 использует это значение R * для всех расчетов стандартной атмосферы. При использовании значения R по ISO расчетное давление увеличивается всего на 0,62 паскаль на 11 км (эквивалент разницы всего в 17,4 сантиметра или 6,8 дюйма) и на 0,292 Па на 20 км (эквивалент разницы всего в 33,8 см или 13,2 дюйма).
Также обратите внимание, что это было задолго до переопределения SI 2019 года, благодаря которому константе было присвоено точное значение.
ГАЗОВАЯ ПОСТОЯННАЯ
Смотреть что такое «ГАЗОВАЯ ПОСТОЯННАЯ» в других словарях:
ГАЗОВАЯ ПОСТОЯННАЯ — физическая постоянная, входящая в уравнение состояния 1 моля идеального газа; обозначается R, равна 8,314 Дж/(К.моль) = 1,987 кал/(К.моль) … Большой Энциклопедический словарь
ГАЗОВАЯ ПОСТОЯННАЯ — (R), универсальная фнз. постоянная, входящая в ур ние состояния 1 моля идеального газа: pv=RT (см. КЛАПЕЙРОНА УРАВНЕНИЕ), где р давление, v объём моля, Т абс. темп pa. Г. п. по своему физ. смыслу работа расширения 1 моля идеального газа под пост … Физическая энциклопедия
газовая постоянная — — [А.С.Гольдберг. Англо русский энергетический словарь. 2006 г.] Тематики энергетика в целом EN gas constant … Справочник технического переводчика
Газовая постоянная — Универсальная газовая постоянная R0 ≈ 8,314 кДж/(кмоль·K) фундаментальна физическая константа. Индивидуальная газовая постоянная R = R0/M, кДж/(кг·K) константа для газа или газовой смеси конкретной молярной массы … Википедия
газовая постоянная — физическая постоянная, входящая в уравнение состояния 1 моля идеального газа; обозначается R, равна 8,314 Дж/(K·моль) = 1,987 кал/(K·моль). * * * ГАЗОВАЯ ПОСТОЯННАЯ ГАЗОВАЯ ПОСТОЯННАЯ, физическая постоянная, входящая в уравнение состояния (см.… … Энциклопедический словарь
газовая постоянная — dujų konstanta statusas T sritis fizika atitikmenys: angl. gas constant vok. Gaskonstante, f rus. газовая постоянная, f pranc. constante de gaz, f … Fizikos terminų žodynas
газовая постоянная — газовая константа … Cловарь химических синонимов I
Газовая постоянная — универсальная физическая постоянная R, входящая в уравнение состояния 1 моля идеального газа: pv = RT (см. Клапейрона уравнение), где р давление, v объём, Т абсолютная температура. Г. п. имеет физический смысл работы расширения 1 моля… … Большая советская энциклопедия
ГАЗОВАЯ ПОСТОЯННАЯ — универс. физ. постоянная R, входящая в ур ние состояния идеального газа (см. Клапейрона уравнение); R = (8,314 510 ± 0,000 070) ДжДмоль*К). Удельной Г. п. наз. величина В = R/M, где М молярная масса … Большой энциклопедический политехнический словарь
ГАЗОВАЯ ПОСТОЯННАЯ — физ. постоянная, входящая в уравнение состояния 1 моль идеального газа; обозначается R, равна 8,314 Дж/(К х моль) = = 1,987 кал/(К х моль) … Естествознание. Энциклопедический словарь
Некоторые предположили, что было бы уместно назвать символ р то Константа Реньо в честь Французский химик Анри Виктор Рено, точные экспериментальные данные которого были использованы для расчета раннего значения константы; однако происхождение буквы р представить константу неуловимо. [3] [4]
Газовая постоянная находится в закон идеального газа, следующее:
п V = п р Т = м р s п е c я ж я c Т < displaystyle PV = nRT = mR _ < rm
Содержание
Размеры
Из закона идеального газа PV = nRT мы получили:
куда п давление, V объем, п количество молей данного вещества, и Т является температура.
Поскольку давление определяется как сила на единицу площади, уравнение газа также можно записать как:
р = ж о р c е а р е а × v о л ты м е а м о ты п т × т е м п е р а т ты р е < displaystyle R = < frac << dfrac < mathrm
Площадь и объем (длина) 2 и (длина) 3 соответственно. Следовательно:
р = ж о р c е ( л е п грамм т час ) 2 × ( л е п грамм т час ) 3 а м о ты п т × т е м п е р а т ты р е = ж о р c е × л е п грамм т час а м о ты п т × т е м п е р а т ты р е < displaystyle R = < frac << dfrac < mathrm
Поскольку сила × длина = работа:
р = ш о р k а м о ты п т × т е м п е р а т ты р е < displaystyle R = < frac < mathrm
Физическое значение р это работа на градус на моль. Он может быть выражен в любом наборе единиц, представляющих работу или энергию (например, джоули), единицы, представляющие градусы температуры по абсолютной шкале (например, Кельвин или же Ренкин), и любая система единиц, обозначающая моль или подобное чистое число, которое позволяет уравнение макроскопической массы и чисел фундаментальных частиц в системе, такой как идеальный газ (см. Константа Авогадро).
Вместо моля постоянную можно выразить, рассматривая нормальный кубический метр.
В противном случае мы также можем сказать, что:
Следовательно, мы можем написать р в качестве:
Связь с постоянной Больцмана
В Постоянная Больцмана kB (часто сокращенно k) может использоваться вместо газовой постоянной, работая с чистым подсчетом частиц, N, а не количество вещества, п, поскольку
куда NА это Константа Авогадро. Например, закон идеального газа в терминах постоянной Больцмана
Измерение и замена на определенное значение
По состоянию на 2006 год наиболее точное измерение р были получены путем измерения скорость звука cа(п, Т) в аргон при температуреТ из тройная точка воды в разных давление п, и экстраполяция до предела нулевого давленияcа(0, Т). Значение р тогда получается из соотношения
Однако после 2019 новое определение базовых единиц СИ, р теперь имеет точное значение, определенное в терминах других точно определенных физических констант.
Удельная газовая постоянная
| рспецифический для сухого воздуха | Единицы |
|---|---|
| 287.058 | Дж⋅кг −1 ⋅K −1 |
| 53.3533 | ft⋅фунт-сила⋅фунт −1 ⋅ ° R −1 |
| 1,716.49 | ft⋅фунт-сила⋅слизняк −1 ⋅ ° R −1 |
| На основе средней молярной массы для сухого воздуха 28,9645 г / моль. | |
В удельная газовая постоянная газа или смеси газов (рспецифический) дается делением молярной газовой постоянной на молярная масса (M) газа или смеси.
р s п е c я ж я c = р M < displaystyle R _ < rm
Точно так же, как постоянная идеального газа может быть связана с постоянной Больцмана, то же самое можно сделать и с постоянной газом путем деления постоянной Больцмана на молекулярную массу газа.
р s п е c я ж я c = k B м < displaystyle R _ < rm
Еще одно важное соотношение исходит из термодинамики. МайерЭто соотношение связывает удельную газовую постоянную с удельной теплотой для калорийно совершенного газа и термически совершенного газа.
Обычно, особенно в инженерных приложениях, удельную газовую постоянную представляют символом р. В таких случаях универсальной газовой постоянной обычно присваивается другой символ, например р чтобы отличить это. В любом случае контекст и / или единицы газовой постоянной должны давать понять, идет ли речь об универсальной или конкретной газовой постоянной. [6]
Стандартная атмосфера США
В Стандартная атмосфера США, 1976 (USSA1976) определяет газовую постоянную р ∗ в качестве: [7] [8]
Обратите внимание на использование единиц измерения в киломолях, что дает коэффициент 1000 в константе. USSA1976 признает, что это значение не соответствует приведенным значениям для постоянной Авогадро и постоянной Больцмана. [8] Это несоответствие не является существенным отклонением от точности, и USSA1976 использует это значение р ∗ для всех расчетов стандартной атмосферы. При использовании ISO значение р, расчетное давление увеличивается всего на 0,62паскаль на 11 км (эквивалент разницы всего в 17,4 сантиметра или 6,8 дюйма) и увеличение на 0,292 Па на 20 км (эквивалент разницы всего в 33,8 см или 13,2 дюйма).
Также обратите внимание, что это было задолго до переопределения SI 2019 года, которое дало константе точное значение.




