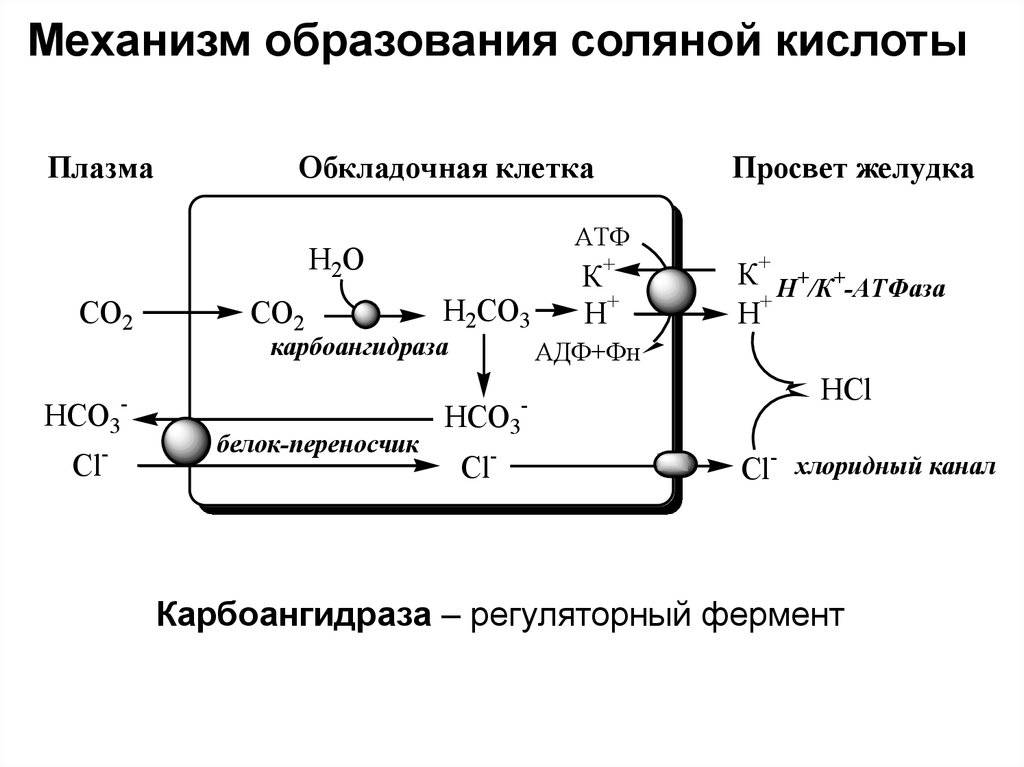
Какое общее название имеют соли хлороводородной кислоты
I. Физические свойства
Cоляная кислота (также хлороводородная, хлористоводородная кислота, хлористый водород) — раствор хлороводорода в воде, сильная одноосновная кислота. Бесцветная, прозрачная, едкая жидкость, «дымящая» на воздухе (техническая соляная кислота желтоватого цвета из-за примесей железа, хлора и пр.). В концентрации около 0,5 % присутствует в желудке человека. Максимальная концентрация при 20 °C равна 38% по массе, плотность такого раствора 1,19 г/см³. Молярная масса 36,46 г/моль.
II. Получение соляной кислоты
III. Химические свойства
3) Взаимодействие соляной кислоты с основаниями и аммиаком:
HCl + KOH → KCl + H2O
4) Взаимодействие соляной кислотыс солями:
Большинство хлоридов растворимы в воде (за исключением хлоридов серебра, свинца и одновалентной ртути).
IV. Применение соляной кислоты и ее солей
1. Соляная кислота входит в состав желудочного сока и способствует перевариванию белковой пищи у человека и животных.
2. Хлороводород и соляная кислота используются для производства лекарств, красителей, растворителей, пластмасс.
3. Применение основных солей соляной кислоты:
Hg2Cl2 (Рис.3. Каломель) – не ядовита, слабительное средство.
ZnCl2— для пропитки древесины против гниения, в медицине, при паянии.
V. Задания для повторения и закрепления
Задание №1
Задание №2
Расставьте коэффициенты методом электронного баланса в следующей реакции
Задание №3
Задание №4
Решите задачу:
Какое количество алюминия прореагирует с избытком соляной кислоты для получения 5,6 л водорода (н.у.)?
Кислые соли соляной кислоты: гидрохлорид, формула
Все, кто когда-либо изучал химию (начиная со школы и заканчивая аспирантурой), хоть раз сталкивался с таким понятием, как «гидрохлорид». Формула такого вещества тоже хоть раз, но встречалась. Редко кто не только не знает, что это за вещество, но и не помнит, что встречал такое понятие когда-то на занятиях по химии. Что же такое «гидрохлорид»? Химическая формула и свойства вещества будут рассмотрены в этой статье.
Соляная кислота
Необходимо разобраться, что такое соляная кислота, прежде чем узнать, что такое кислая соль соляной кислоты (гидрохлорид). Формула представлена ниже.

Кислые соли соляной кислоты
Формула (речь идет о гидрохлоридах) имеет общий вид: [основание] * HCl. Большинство кислых солей соляной кислоты являются бесцветными кристаллами. Если такое соединение имеет окраску, то это значит, что основание, с котором образован комплекс, придал кристаллам определенный цвет. Гидрохлориды весьма широко используются в фармацевтическом производстве.
Применение гидрохлоридов
Множество лекарств изготавливается именно на основе кислых солей хлороводородной кислоты. В качестве примеров можно привести такие вещества гидрохлорида, как полигексаметиленгуанидин, фенилпропаноламин, глюкозамин. Однако это далеко не полный список. Препараты на основе этих веществ используются для лечения позвоночника и суставов, для уничтожения микробов, для борьбы с воспалительными процессами (в верхних дыхательных путях, включая хронические заболевания). Это далеко не весь спектр областей применения лекарственных средств, а лишь малая их доля.
Витамин В6
Ни для кого не секрет, что витамин В6 является одним из наиболее важных витаминов, необходимых человеку для нормальной жизнедеятельности. Его нехватка вызывает головную боль, утомляемость, различные кожные заболевания, нарушения работы сосудов и т. д.
Витамин В6 используется также в качестве антидота при отравлениях гидразином.
Заключение
Итак, существуют не только неорганические соли хлороводородной кислоты, но и органические, которые являются комплексными соединениям. Наиболее распространено применение гидрохлоридов в фармакологии: великое множество препаратов изготавливаются на их основе или с содержанием этих веществ. Однако применение этих лекарственных средств требует особой внимательности, не допускающей превышения дозировки, назначенной специалистом. И ни в коем случае нельзя принимать препараты одновременно с алкоголем.
§ 55. Хлороводород, соляная кислота и их свойств (окончание)
Хлороводородная (соляная) кислота и её соли
Физические свойства. Концентрированная соляная кислота — бесцветный раствор, дымит во влажном воздухе, с резким запахом хлороводорода. Можно получить 40 %-й раствор соляной кислоты.
Химические свойства. Хлороводородная кислота имеет ряд свойств, характерных для большинства кислот.
К таким свойствам относятся:
1) изменение окраски индикаторов (лакмуса, метилоранжа) на красный;
2) взаимодействие с металлами, стоящими в ряду активности до водорода, с осно́вными и амфотерными оксидами, с основаниями, с солями слабых кислот:
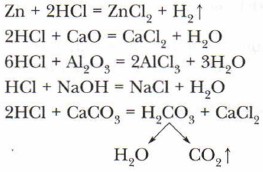
В этих реакциях получаются соли соляной кислоты — хлориды и другие продукты.
Особенное свойство соляной кислоты — реакция с раствором нитрата серебра. Используя эту реакцию, соляную кислоту можно отличить от других кислот.
Проделаем лабораторные опыты.

Белый творожистый осадок (AgCl) не растворяется в азотной кислоте.
Соли соляной кислоты называются хлоридами. Они все растворимы в воде, за исключением хлорида серебра и хлорида свинца (II).
Если добавить к раствору хлорида раствор нитрата серебра, то выпадет такой же творожистый белый осадок:
Нитрат серебра (или азотнокислое серебро) служит реактивом на соляную кислоту и её соли. Эта реакция называется качественной реакцией. С помощью этой качественной реакции распознают соляную кислоту и её соли.

Применение соляной кислоты. Соляную кислоту используют в разных областях народного хозяйства. В большом количестве её расходуют при травлении стали, перед покрытием стальных изделий слоем защитного металла (лужение, никелирование, хромирование). Перед этими процессами необходимо удалить плёнку оксидов с поверхности изделия. Недостаток этой операции заключается в том, что кислота реагирует не только с оксидом железа, но и с самим металлом. Чтобы избежать реакции кислоты с металлом, в кислоту добавляют специальные вещества, замедляющие нежелательную реакцию, — ингибиторы.
Соляную кислоту используют в производстве лекарств, красителей, ядохимикатов, пластмасс и других полимеров, а также для получения в лаборатории хлора и некоторых хлоридов.
Раствор соляной кислоты (0,5 %) назначают больным с пониженной кислотностью желудочного сока.
Свойства хлороводорода • Качественная реакция на соляную кислоту и её соли • Ингибитор







Какое общее название имеют соли хлороводородной кислоты
§8.7 Соли. Названия и классификация солей.
В предыдущих параграфах этой главы вы постоянно встречались с реакциями, в которых образуются соли.
Солями называются вещества, в которых атомы металла связаны с кислотными остатками.
NaCl – хлорид натрия,
Na 2 SO 4 – сульфат натрия,
СаSO 4 – сульфат кальция,
СаCl 2 – хлорид кальция,
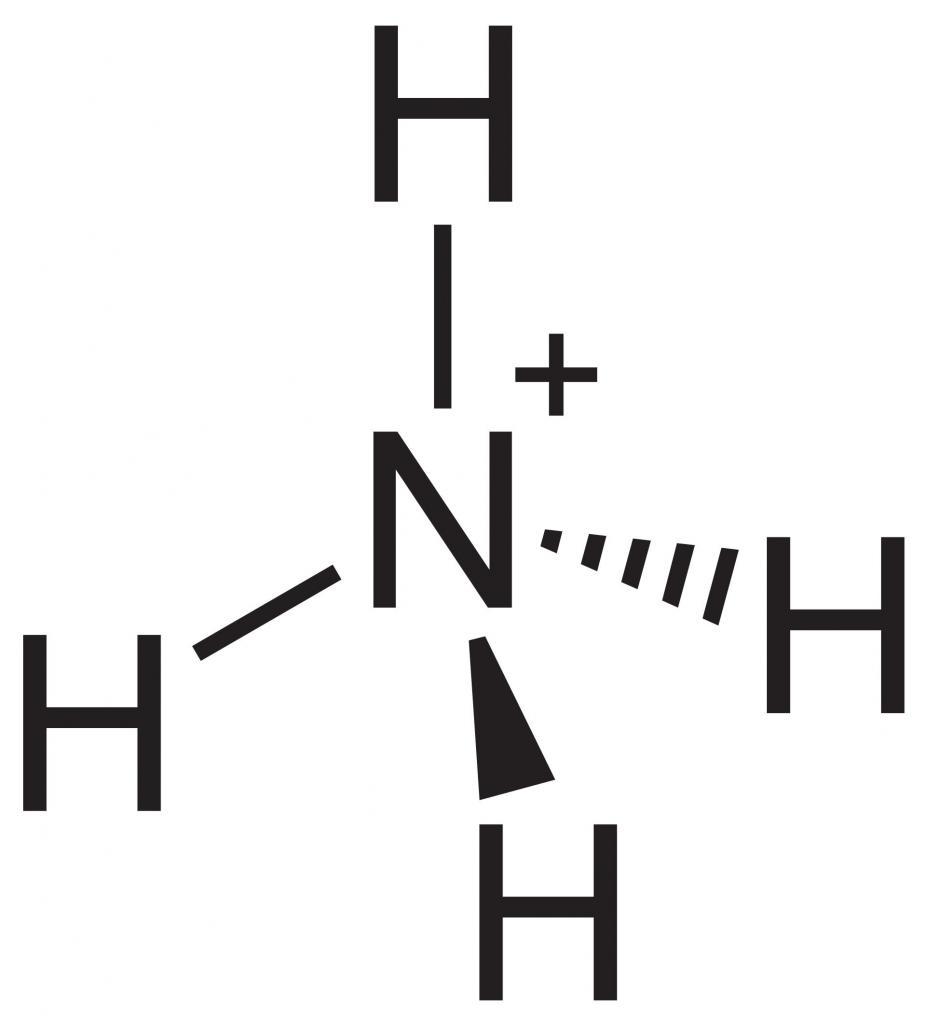
(NH 4 ) 2 SO 4 – сульфат аммония.
Формула соли строится с учетом валентностей металла и кислотного остатка. Практически все соли – ионные соединения, поэтому можно говорить, что в солях связаны между собой ионы металла и ионы кислотных остатков:
Na + Cl – – хлорид натрия
Ca 2+ SO 4 2– – сульфат кальция и т.д.
Названия солей составляются из названия кислотного остатка и названия металла. Главным в названии является кислотный остаток. Названия солей в зависимости от кислотного остатка показаны в таблице 8-6.
Таблица 8-6. Построение названий солей. В верхней части таблицы приведены кислородсодержащие кислотные остатки, в нижней – бескислородные.
Соль какой кислоты
Валентность остатка
Ca(NO 3 ) 2 нитрат кальция
Кремниевая H 2 SiO 3
Na 2 SiO 3 силикат натрия
PbSO 4 сульфат свинца
Na 2 CO 3 карбонат натрия
Фосфорная H 3 PO 4
AlPO 4 фосфат алюминия
Бромоводородная HBr
NaBr бромид натрия
Сероводородная H 2 S
FeS сульфид железа (II)
NH 4 Cl хлорид аммония
Фтороводородная HF
CaF 2 фторид кальция
Из таблицы 8-6 видно, что названия кислородсодержащих солей имеют окончания » ат «, а названия бескислородных солей – окончания » ид «.
В некоторых случаях для кислородсодержащих солей может использоваться окончание » ит «. Например, Na 2 SO 3 – сульфит натрия. Это делается для того, чтобы различать соли серной кислоты (H 2 SO 4 ) и сернистой кислоты (H 2 SO 3 ) и в других таких же случаях.
Любую соль можно получить соответствующей реакцией нейтрализации. Например, сульфит натрия образуется в реакции между сернистой кислотой и основанием (едким натром). При этом на 1 моль кислоты требуется взять 2 моля основания:
сульфит натрия (средняя соль)
Если взять только 1 моль основания – то есть меньше, чем требуется для полной нейтрализации, то образуется кислая соль – гидросульфит натрия:
гидросульфит натрия (кислая соль)
Кислые соли образуются многоосновными кислотами. Одноосновные кислоты кислых солей не образуют.
Кислые соли, помимо ионов металла и кислотного остатка, содержат ионы водорода.
Названия кислых солей содержат приставку «гидро» (от слова hydrogenium – водород). Например:
NaHCO 3 – гидрокарбонат натрия,
K 2 HPO 4 – гидрофосфат калия,
KH 2 PO 4 – дигидрофосфат калия.
Основные соли образуются при неполной нейтрализации основания. Названия основных солей образуют с помощью приставки «гидроксо». Ниже приведен пример, показывающий отличие основных солей от обычных (средних):
хлорид магния ( средняя соль)
гидроксохлорид магния ( основная соль)
Основные соли, помимо ионов металла и кислотного остатка, содержат гидроксильные группы.
Основные соли образуются только из многокислотных оснований. Одноокислотные основания таких солей образовать не могут.
В таблице 8-6 приведены международные названия солей. Однако полезно знать также русские названия и некоторые исторически сложившиеся, традиционные названия солей, имеющих важное значение (таблица 8-7).
Таблица 8-7. Международные, русские и традиционные названия некоторых важных солей.
Международное название
Традиционное название
В быту – как моющее и чистящее средство
Гидрокарбонат натрия
Натрий углекислый кислый
Пищевой продукт: выпечка кондитерских изделий
Применяется в технике
Натрий сернокислый
Лекарственное средство
Магний сернокислый
Лекарственное средство
Применяется в зажигательных смесях для головок спичек
В химии и в технике до сих пор сохраняется много старинных названий. Например, каустическая сода – вовсе не соль, а техническое название гидроксида натрия NaOH. Если обыкновенной содой можно почистить раковину или посуду, то каустическую соду ни при каких обстоятельствах брать в руки или использовать в быту нельзя!
Эти простые знания могут пригодиться в жизни – мало ли с какими веществами придется столкнуться в будущем.
** Строение солей аналогично строению соответствующих кислот и оснований. Ниже приведены структурные формулы типичных средних, кислых и основных солей.
В заключение приведем строение и название основной соли, формула которой, на первый взгляд, выглядит очень сложной: [Fe(OH) 2 ] 2 CO 3 – дигидроксокарбонат железа (III).
На самом деле, при рассмотрении структурной формулы такой соли становится ясно, что эта соль – продукт частичной нейтрализации гидроксида железа (III) угольной кислотой:
8.23. Закончите уравнения реакций. Определите, какие соли (средние, кислые, основные) получаются при данном мольном соотношении реагентов. Назовите эти соли.
в) 3Ca(OH) 2 + 2H 3 PO 4 =
г) Ca(OH) 2 + H 3 PO 4 =
Описание соляной кислоты: формула, свойства и применение
Кислоты – это химические соединения способные отдавать протон или принимать электронную пару с образованием ковалентной связи. Данный класс веществ имеет различные классификации: по числу атомов водорода, по происхождению, по силе. Соляная кислота является сильной, одноосновной неорганической кислотой.
Формула и другие названия соляной кислоты
В состав соляной кислоты входят два химических элемента: хлор и водород. Данная кислота состоит из двух атомов и имеет формулу: HCl. Стоит отметить, что соляная кислота – это тривиальное название (т.е. название, применяемое в обиходной речи химиков, не отражающее состава). По международной номенклатуре ИЮПАК вещество с формулой HCl принято называть хлороводородной кислотой. Иногда HCl называют хлористоводородной кислотой или хлористым водородом, также приемлемо название – хлорид водорода.
Физические свойства
Физические свойства HCl коррелируют с концентрацией данного соединения в растворе. Для того, чтобы не перегружаться цифрами, рассмотрим физические свойства хлористого водорода на примере его концентрированной формы (около 36%):
Химические свойства
Химические свойства хлорида водорода можно подразделить на общие (характерные для всех соединений, основным свойство которых является отдача протона) и специфические (характерные только для HCl). Общие свойства:
Специфические свойства соляной кислоты:
Получение соляной кислоты
Промышленный способ получения хлористого водорода заключается в горении водорода в хлоре и последующим растворением образовавшегося вещества в воде. Существует и другой способ получения хлороводородной кислоты, применяемый в лабораторных условиях. Суть способа заключается в реакции поваренной соли(NaCl) с концентрированно серной кислотой при нагревании. В результате получаются следующие соединения: гидросульфат натрия и хлорид водорода, если провести химическое взаимодействие между образовавшимися продуктами, то образуется сульфат натрия и 2 молекулы хлористого водорода. Приведем общее уравнение реакции: 2NaCl + H2SO4 = Na2SO4 + 2HCl.
Области применения
Хлорид водорода является ключевым реагентом в химической промышленности, однако данное соединение нашло себе применение во многих отраслях человеческого деятельности.
В химической промышленности
В химической промышленности хлористый водород применяют для синтез хлорорганических соединений, а хлорсодержащих солей различных металлов.
В металлургии
В металлургии HCl используется с целью очистки металла после лужения (процесса нанесения олова с целью защиты металла от коррозии).
В пищевой промышленности
33% раствор HCl активно применяют в пищевом производстве в качестве регулятора pH, предназначенного для очистки воды.
В быту
В домохозяйстве HCl используют в составе моющих, хлорсодержащих средств.
В сельском хозяйстве
В сельскохозяйственной деятельности HCl применяется в составе хлорорганических веществ, которые используются в качестве органических ядохимикатов.
В медицине
В медицинской практике применяют слабые растворы хлористого водорода с целью улучшения пищеварения.
В строительстве
В строительстве HCl используют для очистки красного кирпича от грязи. Также использование растворов HCl повышает морозостойкость и влагостойкость бетонных конструкций, что способствует постройке более долгоживущих зданий.
Интересные факты
Приведем ряд фактов о хлороводородной кислоте, которые удивят обывателя: