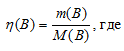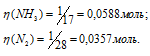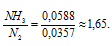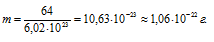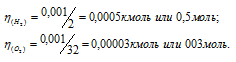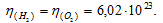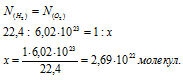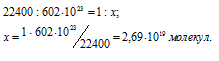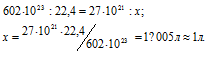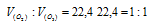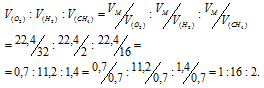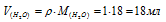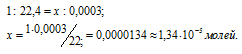Решите пожалуйста все:
1) Какое количество вещества (моль) содержится в 0,1 м3 водорода и (и. у.) в 0,1 кг этого газа?
2) Вычислите относительную плотность по воздуху газовой смеси, в которой объемные доли метана СН4 и этана С2Н6 равны 52% и 48% соответственно. Тяжелее или легче воздуха эта смесь?
3) При температуре 62 градуса Цельсия и давлении 1,01 * 10⁶ Па масса пара равна 0,24 * 10⁻³ кг и занимает объем 87 * 10⁻⁶ м³. Вычислите молярную массу вещества.
4) Определите давление 0,1 кг пропана в сосуде объемом 0,01 м³ при температуре минус 2 градуса Цельсия
Ответы и объяснения
m водорода = 0,1 кг = 100 г;
M водорода = 2 г/моль;
p водорода = 0,0000899 г/см³
V (количество вещества) = m/M = 100/2 = 50 моль
Ответ: 50 моль и 4,495 * 10⁻⁶ моль
M (СН4)= 16 г/моль;
M (С2Н6)= 30 г/моль;
M (воздуха)= 28,98 г/моль.
m (СН4)=16* 0,52 моль = 8,32 г
m (С2Н6)=30*0,48 моль =14,4 г
m (газовой смеси)= 8,32 + 14,4 = 22,72 г
M (газовой смеси) = 22,72 г / 1 моль = 22,72 г / моль
D (по воздуху) = M (газовой смеси) / M (воздуха) = 22,72 / 28,98 = 0,78
Ответ: D (по воздуху) = 0,78
Выразим малярную массу:
М=m*R*T/ p*v
M= 0,24 * 10⁻³ * 8,31 * 335 / 1,01 * 10⁶ * 87 * 10⁻⁶ = 668,124 / 87,87 * 10³ = 0,0076 кг/моль.
Ответ: 0,0076 кг/моль
М (пропана) = 0,04409 кг/моль.
Выразим давление:
p = m*R*T * v / M
p = 0,1 * 8,31 * 271 * 0,01 / 0,04409 = 51,1 Па
Какое количество молекул содержится в 0 1 моль водорода н у
Вычислите, сколько молекул содержится в 0,5 моль газообразного водорода
Имеется следующий перечень химических веществ: бром, магний, натрий, водород, бромид натрия, гидроксид натрия, хлорид аммония.
Напишите химические формулы каждого из указанных веществ.
1. Формулы простых веществ: водород — бром —
магний —
натрий —
2. Формулы сложных веществ: бромид натрия — гидроксид натрия —
хлорид аммония —
Какое из веществ, упоминаемых в перечне, соответствует следующему описанию: «При нормальных условиях является тяжёлой едкой жидкостью красно-бурого цвета с сильным неприятным «тяжёлым» запахом»? В ответе укажите название вещества.
Данному описанию соответствует бром
Из данного перечня выберите ЛЮБОЕ СЛОЖНОЕ вещество. Запишите его химическую формулу и укажите, к какому классу неорганических соединений оно относится. Ответ запишите в таблицу:
| Формула вещества | Класс соединения |
Формулу вещества введите в формате: Al2(SO4)3.
1. Бромид натрия — — соль (средняя соль).
2. Гидроксид натрия — — основный гидроксид (щёлочь).
3. Хлорид аммония — — соль (средняя соль).
Расчет числа молекул и объемов газообразных веществ
Решениие задач по химии на закон Авогадро
m(B)- масса вещества (В);
Ответ: в 1,65 раз число молекул NH3 больше числа молекул N2.
Задача 54.
Выразить в граммах массу одной молекулы диоксида серы.
Решение:
Находим молекулярную массу диоксида серы:
M(SO2) = 32 + (16 . 2) = 64г/моль.
Молекулярная масса численно составляет массу одного моля вещества, а значит, вес одного моля численно равен молекулярной массе и составляет 64г. Известно, что в одном моле любого вещества содержится 6,02 . 10 23 молекул данного вещества. Исходя из этого, рассчитаем массу в граммах одной молекулы диоксида серы:
Ответ: масса одной молекулы диоксида серы равна.
Задача 55.
Одинаково ли число молекул в 0,001кг Н2 и в 0,001кг О2? В 1 моле Н2 и в 1 моле 02? В 1л Н2 и в 1л О2 при одинаковых условиях?
Решение:
Молекулярные массы водорода и кислорода равны соответственно 2г/моль и 32г/моль. Отсюда находим количество водорода и кислорода, зная их массы:
Один моль любого вещества содержит 6,02 . 1023 молекул. Следовательно, в 0,001кг водорода и в 0,001кг кислорода содержится разное число молекул:
Так как имеется по одному молю водорода и кислорода, то количество молекул веществ будет одинаково:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 . 10 23 молекул. Отсюда рассчитаем количество молекул вещества, содержащихся в 1л водорода и в 1л кислорода:
Ответ: а) в 0,001кг водорода и в 0,001кг кислорода содержится разное число молекул; б) в одном моле водорода и в одном моле кислорода содержится одинаковое число молекул: в) в одном литре водорода и в одном литре кислорода содержится одинаковое число молекул.
Задача 56.
Сколько молекул содержится в 1,00 мл водорода при нормальных условиях?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 . 10 23 молекул. Отсюда рассчитаем количество молекул вещества, содержащихся в 1мл водорода из пропорции:
Ответ: 2,69 . 10 19 молекул.
Задача 57.
Какой объем при нормальных условиях занимают 27 . 10 21 молекул газа?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 . 10 23 молекул. Отсюда находим какой объём при нормальных условиях занимают 27 . 10 21 молекул газа, составив пропорцию:
Ответ: V=1л.
Задача 58.
Каково соотношение объемов, занимаемых 1 молем О2 и 1 молем О3 (условия одинаковые)?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Следовательно соотношение объёмов, занимаемых одним молем О2 и одним молем О3 иметь вид:
Ответ: 1:1
Задача 59.
Взяты равные массы кислорода, водорода и метана при одинаковых условиях. Найти отношение объемов взятых газов.
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Мольные массы кислорода, водорода и метана, соответственно равны 32 г/моль; 2г/моль; 16 г/моль.
Так как массы кислорода, водорода и метана одинаковы при одинаковых условиях, то отношение объёмов взятых газов находим из пропорции:
Ответ: 1:16:2.
Задача 60.
На вопрос, какой объем займет 1моль воды при нормальных условиях, получен ответ: 22,4л. Правильный ли это ответ?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Так как вода при нормальных условиях находится в жидкой, а не в газообразной фазе, то ответ, что 1моль воды займёт 22,4л не правильный. Учитывая, что молярная масса воды равна 18г/моль, а плотность равна единице, то правильный ответ будет равен:
Ответ: 18мл.
Задача 61.
Сколько молекул диоксида углерода находится в 1л воздуха, если объемное содержание СО2 составляет 0,03% (условия нормальные)?
Решение:
При нормальных условиях углекислый газ, содержащийся в 1л воздуха, занимает объём 0,0003л. Зная, что мольный объём любого газа занимает 22,4л, рассчитаем число молей углекислого газа в 0,0003л из пропорции:
Учитывая, что в одном моле вещества содержится 6,02 . 10 23 молекул, находим число молекул в 0,0003л газа:
Ответ: 8,07 . 10 18 молекул.
Какое количество молекул содержится в 0 1 моль водорода н у
Вычислите массу 0,5 моль газообразного водорода.
Имеется следующий перечень химических веществ: калий, хлор, алюминий, водород, хлорид калия, серная кислота, сульфат алюминия.
Какое из веществ, упоминаемых в перечне, соответствует следующему описанию: «Ядовитый газ жёлто-зелёного цвета, тяжелее воздуха, с резким запахом»? В окошке ответа укажите название вещества.
Данному описанию соответствует хлор
Из данного перечня выберите ЛЮБОЕ СЛОЖНОЕ вещество. Запишите его химическую формулу и укажите, к какому классу неорганических соединений оно относится в формате:
Вещество –____________________. Класс соединений – ____________________________.
1. — соль (средняя соль).
2. — кислота.
3. — соль (средняя соль).
Напишите химические формулы каждого из указанных веществ.
1. Формулы простых веществ: калий — хлор —
алюминий —
водород —
2. Формулы сложных веществ: хлорид калия — серная кислота —
сульфат алюминия —
Из приведённого перечня веществ выберите ЛЮБОЕ соединение, состоящее из атомов ТРЁХ элементов. Вычислите массовую долю кислорода в этом соединении. Запишите ответ в формате:
Вещества, состоящие из атомов трёх элементов: серная кислота и сульфат алюминия.
1. Если выбрана серная кислота, то: (или 65,3%).
2. Если выбран сульфат алюминия, то: (или 56,1%).
Ответ: 65,3 % или 56,1 %.
Масса водорода:
Вычислите, сколько молекул содержится в 0,5 моль газообразного водорода
Имеется следующий перечень химических веществ: бром, магний, натрий, водород, бромид натрия, гидроксид натрия, хлорид аммония.
Напишите химические формулы каждого из указанных веществ.
1. Формулы простых веществ: водород — бром —
магний —
натрий —
2. Формулы сложных веществ: бромид натрия — гидроксид натрия —
хлорид аммония —
Какое из веществ, упоминаемых в перечне, соответствует следующему описанию: «При нормальных условиях является тяжёлой едкой жидкостью красно-бурого цвета с сильным неприятным «тяжёлым» запахом»? В ответе укажите название вещества.
Данному описанию соответствует бром
Из данного перечня выберите ЛЮБОЕ СЛОЖНОЕ вещество. Запишите его химическую формулу и укажите, к какому классу неорганических соединений оно относится. Ответ запишите в таблицу:
| Формула вещества | Класс соединения |
Формулу вещества введите в формате: Al2(SO4)3.
1. Бромид натрия — — соль (средняя соль).
2. Гидроксид натрия — — основный гидроксид (щёлочь).
3. Хлорид аммония — — соль (средняя соль).
Из приведённого перечня веществ выберите соединение, состоящее из атомов нескольких элементов, один из которых — водород. Вычислите массовую долю водорода в этом соединении. Ответ округлите до сотых процента. Запишите ответ в формате:
Вещества, состоящие из атомов двух элементов: гидроксид натрия и хлорид аммония.
1. Если выбран гидроксид натрия, то: (или 2,50 %).
2. Если выбран хлорид аммония, то: (или 7,48%).
Ответ: 2,50 % или 7,48 %.
Количество молекул:
Ответ: молекул.
Вычислите массу 1,5 моль меди. Молярную массу меди считать равной 64 г/моль.
Имеется следующий перечень химических веществ: водород, хлор, медь, аргон, сульфат бария, сульфит натрия, серная кислота.
Напишите химические формулы каждого из указанных веществ.
1. Формулы простых веществ: водород — хлор —
медь —
аргон —
2. Формулы сложных веществ: сульфат бария — сульфит натрия —
серная кислота —
Какое из веществ, упоминаемых в перечне, соответствует следующему описанию: «При н. у. инертный одноатомный газ без цвета, вкуса и запаха»? В ответе укажите название вещества.
Данному описанию соответствует аргон
Из данного перечня выберите ЛЮБОЕ СЛОЖНОЕ вещество. Запишите его химическую формулу и укажите, к какому классу неорганических соединений оно относится. Ответ запишите в таблицу:
| Формула вещества | Класс соединения |
Формулу вещества введите в формате: Al2(SO4)3.
1. Сульфат бария — — соль (средняя соль).
2. Сульфит натрия — — соль (средняя соль).
3. Серная кислота — — кислота.
Из приведённого перечня веществ выберите ЛЮБОЕ соединение, состоящее из атомов ТРЁХ химических элементов. Вычислите массовую долю кислорода в этом соединении. Ответ округлите до сотых процента. Запишите ответ в формате:
Вещества, состоящие из атомов ТРЁХ элементов: сульфат бария, сульфит натрия, серная кислота.
1. Если выбран сульфат бария, то: (или 27,47 %).
2. Если выбран сульфит натрия, то: (или 38,09%).
3. Если выбрана серная кислота, то: (или 65,31%).
Ответ: 27,47 % или 38,09 % или 65,31 %.
Масса меди:
Вычислите объём 22,4 моля газообразного кислорода.
Имеется следующий перечень химических веществ: магний, сера, железо, кислород, сульфид железа(II), фосфат магния, сернистый газ.
Напишите химические формулы каждого из указанных веществ.
1. Формулы простых веществ: магний — сера —
железо —
кислород —
2. Формулы сложных веществ: сульфид железа(II) — фосфат магния —
сернистый газ —
Какое из веществ, упоминаемых в перечне, соответствует следующему описанию: «Кристаллы чёрного цвета с металлическим блеском»? В окошке ответа укажите название вещества.
Данному описанию соответствует сульфид железа(II)
Из данного перечня выберите ЛЮБОЕ СЛОЖНОЕ вещество. Запишите его химическую формулу и укажите, к какому классу неорганических соединений оно относится. Ответ запишите в таблицу:
| Формула вещества | Класс соединения |
Формулу вещества введите в формате: Al2(SO4)3.
1. Сульфид железа(II) —  — соль (средняя соль).
2. Фосфат магния —  — соль (средняя соль).
3. Сернистый газ —  — оксид (кислотный оксид).
Из приведённого перечня веществ выберите соединение, состоящее из атомов нескольких элементов, один из которых — сера. Вычислите массовую долю серы в этом соединении. Ответ округлите до сотых процента. Запишите ответ в формате:
Вещества, состоящие из атомов двух элементов, один из которых — сера: сульфид железа(II) и сернистый газ.
1. Если выбран сульфид железа(II), то: (или 36,36 %).
2. Если выбран сернистый газ, то: (или 50,00%).
Ответ: 36,36 % или 50,00 %.
Объём:
Ответ: л.
Вычислите объём 10 г газообразного кислорода.
Имеется следующий перечень химических веществ: углерод, кислород, хлор, водород, оксид железа(III), соляная кислота, хлорид железа(III).
Напишите химические формулы каждого из указанных веществ.
1. Формулы простых веществ: углерод — кислород —
хлор —
водород —
2. Формулы сложных веществ: оксид железа(III) — соляная кислота —
хлорид железа(III) —
Какое из веществ, упоминаемых в перечне, соответствует следующему описанию: «При нормальных условиях бесцветная, прозрачная, едкая жидкость, «дымящаяся» на воздухе»? В окошке ответа укажите название вещества.
Данному описанию соответствует соляная кислота
Из данного перечня выберите ЛЮБОЕ СЛОЖНОЕ вещество. Запишите его химическую формулу и укажите, к какому классу неорганических соединений оно относится. Ответ запишите в таблицу:
| Формула вещества | Класс соединения |
Формулу вещества введите в формате: Al2(SO4)3.
1. Оксид железа(III) — — оксид (амфотерный оксид).
2. Соляная кислота — — кислота.
3. Хлорид железа(III) — — соль (средняя соль).