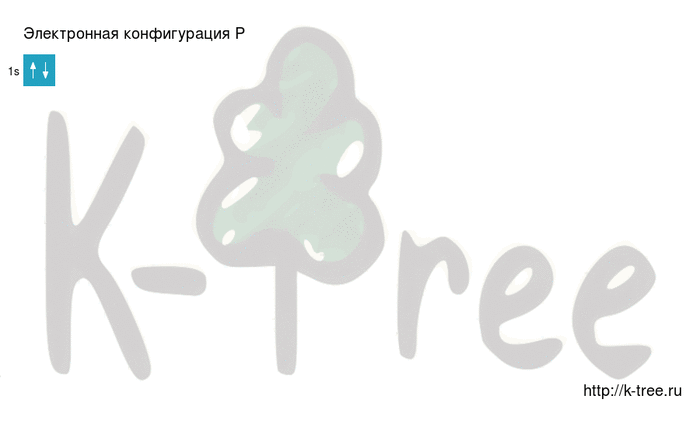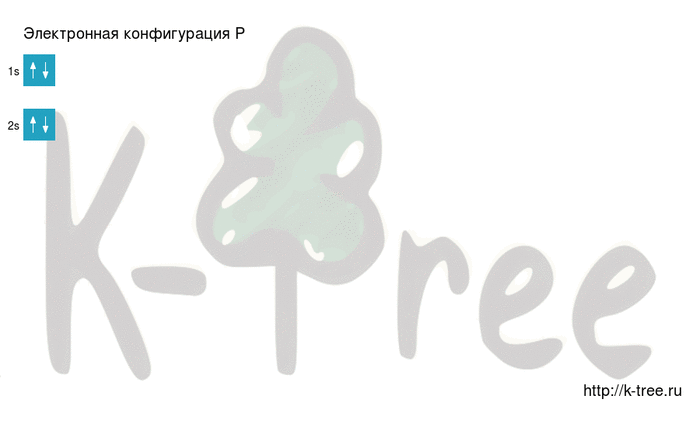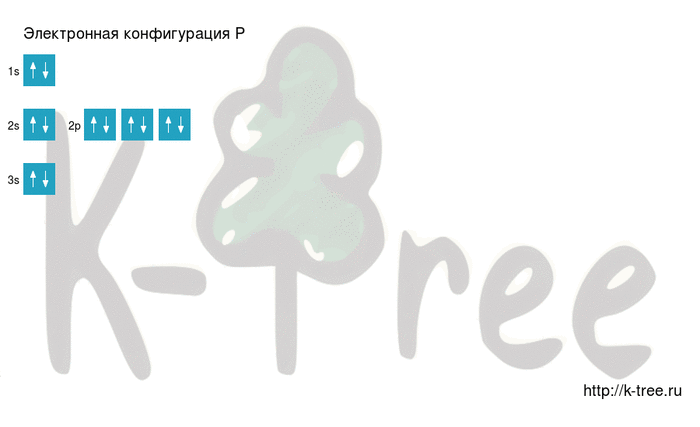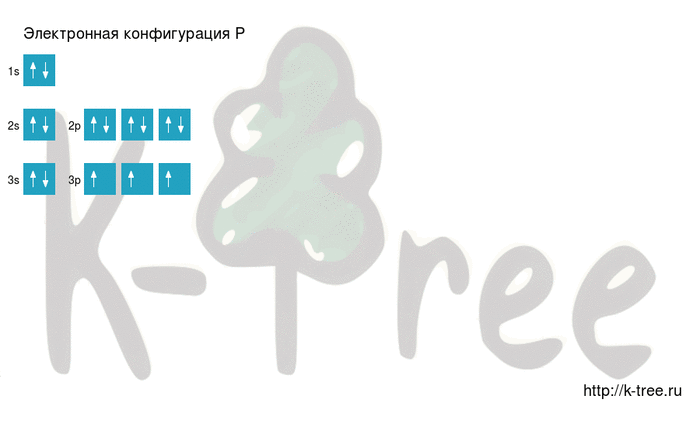Строение атома фосфора

Всего получено оценок: 287.
Всего получено оценок: 287.
Фосфор (Р) – типичный неметалл с относительной атомной массой 31. Строение атома фосфора определяет его активность. Фосфор легко вступает в реакции с другими веществами и элементами.
Строение
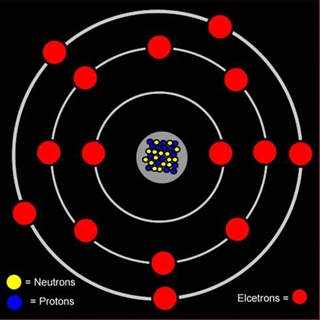
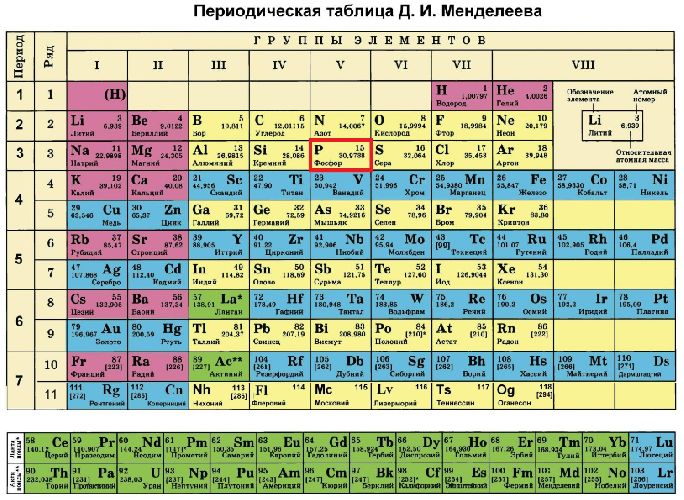
Строение атома элемента фосфора отражено в периодической таблице Менделеева. Фосфор расположен под 15 номером в пятой группе, третьем периоде. Следовательно, атом фосфора состоит из положительно заряженного ядра (+15) и трёх электронных оболочек, на которых находится 15 электронов.
Графически расположение строение атома выглядит следующим образом:
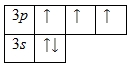
Фосфор относится к р-элементам. На внешнем энергетическом уровне в возбуждённом состоянии располагается пять электронов, которые определяют валентность элемента. В обычном состоянии внешний уровень остаётся незавершённым. Три неспаренных электрона указывают на степень окисления (+3) и третью валентность. Фосфор легко переходит из обычного в возбуждённое состояние.
Ядро состоит из 15 протонов и 16 нейронов. Чтобы посчитать количество нейронов, необходимо вычесть из относительной атомной массы порядковый номер элемента – 31-15=16.
Аллотропия
Фосфор имеет несколько аллотропических модификаций, отличающихся строением кристаллической решётки:
Белый фосфор – наиболее активная модификация элемента, которая быстро окисляется на воздухе, поэтому белый фосфор хранят под водой.
Свойства
Фосфор реагирует c простыми веществами – металлами и неметаллами, проявляя окислительно-восстановительные свойства. Основные реакции с фосфором описаны в таблице.
Фосфор P
Фосфор в таблице менделеева занимает 15 место, в 3 периоде.
| Символ | P |
| Номер | 15 |
| Атомный вес | 30.9737620 |
| Латинское название | Phosphorus |
| Русское название | Фосфор |
Как самостоятельно построить электронную конфигурацию? Ответ здесь
Электронная схема фосфора
Порядок заполнения оболочек атома фосфора (P) электронами: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s → 4f → 5d → 6p → 7s → 5f → 6d → 7p.
Фосфор имеет 15 электронов, заполним электронные оболочки в описанном выше порядке:
2 электрона на 1s-подуровне
2 электрона на 2s-подуровне
6 электронов на 2p-подуровне
2 электрона на 3s-подуровне
3 электрона на 3p-подуровне
Степень окисления фосфора
Ионы фосфора
Валентность P
Атомы фосфора в соединениях проявляют валентность V, IV, III, II, I.
Валентность фосфора характеризует способность атома P к образованию хмических связей. Валентность следует из строения электронной оболочки атома, электроны, участвующие в образовании химических соединений называются валентными электронами. Более обширное определение валентности это:
Число химических связей, которыми данный атом соединён с другими атомами
Валентность не имеет знака.
Квантовые числа P
Квантовые числа определяются последним электроном в конфигурации, для атома P эти числа имеют значение N = 3, L = 1, Ml = 1, Ms = ½
Видео заполнения электронной конфигурации (gif):
Результат:
Энергия ионизации
Перейти к другим элементам таблицы менделеева
Строение атома фосфора
Общие сведения о строении атома фосфора
Относится к элементам p-семейства. Неметалл. Обозначение – P. Порядковый номер – 15. Относительная атомная масса – 30,974 а.е.м.
Электронное строение атома фосфора
Атом фосфора состоит из положительно заряженного ядра (+15), внутри которого есть 15 протонов и 16 нейтронов, а вокруг, по трем орбитам движутся 15 электронов.
Рис.1. Схематическое строение атома фосфора.
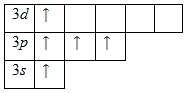
Распределение электронов по орбиталям выглядит следующим образом:
Внешний энергетический уровень атома фосфора содержит 5 электронов, которые являются валентными. Энергетическая диаграмма основного состояния принимает следующий вид:
Каждый валентный электрон атома фосфора можно охарактеризовать набором из четырех квантовых чисел: n (главное квантовое), l (орбитальное), ml (магнитное) и s (спиновое):
Наличие трех неспаренных электронов свидетельствует о том, что степень окисления фосфора равна +3. Так как на третьем уровне есть вакантные орбитали 3d-подуровня, то для атома фосфора характерно наличие возбужденного состояния:
Именно поэтому для фосфора также характерна степень окисления +5.
Примеры решения задач
| Задание | Определите число нейтронов в ядре изотопа титана с массовым числом 48. |
| Решение | Массовое число А указывает суммарное число протонов Z и нейтронов в ядре атома любого элемента: |
Атом титана имеет порядковый номер 22, следовательно, количество протонов в ядре равно 22 (Z=22). Тогда число нейтронов в ядре атома титана определим по формуле:
| Задание | Элемент состоит из двух изотопов в соотношении 2:3. Ядро первого изотопа содержит 10 протонов и 10 нейтронов. Определите атомную массу второго изотопа, если средняя относительная масса элемента равна 21,2. В ответе укажите на сколько нейтронов больше в ядре атома второго изотопа. |
| Решение | Относительная атомная масса первого изотопа равна: |
A1 = Z +n = 10 + 10 = 20 а.е.м.
Относительную атомную массу второго изотопа обозначим через A2.
Средняя относительная атомная масса элемента определяется суммой масс его изотопов с учетом их количества. Составим уравнение:
В ядре атома второго изотопа 10 протонов, следовательно, число, нейтронов будет равно n= A- Z =.22 — 10= 12. По условию задачи в ядре атома первого изотопа было 10 нейтронов. Значит, ядро атома второго изотопа содержит на два нейтрона больше, чем ядро первого изотопа.
Число протонов нейтронов электронов в атоме элемента (Таблица)
Число протонов нейтронов и электронов в атоме химического элемента (изотопа) можно определить, зная порядковый номер элемента в периодической таблице Менделеева и его атомную массу:
— Число протонов = число электронов = порядковый номер элемента
— Число нейтронов = атомная масса – число протонов
Вычислим число нейтронов в атоме на примере кислорода 16 O:
Таблица число протонов нейтронов электронов в атоме химического элемента
Справочная таблица содержит список элементов (изотопов) и их число протонов, нейтронов и электронов, а также атомную массу изотопа.
| Элемент, изотоп | Число протонов (= электронов) | Число нейтронов | Атомная масса изотопа |
| 1 H | 1 | 0 | 1,0078 |
| 2 H | 1 | 1 | 2,0141 |
| 3 He | 2 | 1 | 3,0160 |
| 4 He | 2 | 2 | 4,0026 |
| 6 Li | 3 | 3 | 6,0151 |
| 7 Li | 3 | 4 | 7,0160 |
| 9 Be | 4 | 5 | 9,0122 |
| 10 B | 5 | 5 | 10,0129 |
| 11 B | 5 | 6 | 11,0093 |
| 12 C | 6 | 6 | 12,0000 |
| 13 C | 6 | 7 | 13,0034 |
| 14 N | 7 | 7 | 14,0031 |
| 15 N | 7 | 8 | 15,0001 |
| 16 O | 8 | 8 | 15,9949 |
| 17 O | 8 | 9 | 16,9991 |
| 18 O | 8 | 10 | 17,9992 |
| 19 F | 9 | 10 | 18,9984 |
| 20 Ne | 10 | 10 | 19,9924 |
| 21 Ne | 10 | 11 | 20,9938 |
| 22 Ne | 10 | 12 | 21,9914 |
| 23 Na | 11 | 12 | 22,9898 |
| 24 Mg | 12 | 12 | 23,9850 |
| 25 Mg | 12 | 13 | 24,9858 |
| 26 Mg | 12 | 14 | 25,9826 |
| 27 Al | 13 | 14 | 26,9815 |
| 28 Si | 14 | 14 | 27,9769 |
| 29 Si | 14 | 15 | 28,9765 |
| 30 Si | 14 | 16 | 29,9738 |
| 31 P | 15 | 16 | 30,9738 |
| 32 S | 16 | 16 | 31,9721 |
| 33 S | 16 | 17 | 32,9715 |
| 34 S | 16 | 18 | 33,9679 |
| 36 S | 16 | 20 | 35,9671 |
| 35 Cl | 17 | 18 | 34,9689 |
| 37 Cl | 17 | 20 | 36,9659 |
| 36 Ar | 18 | 18 | 35,9675 |
| 38 Ar | 18 | 20 | 37,9627 |
| 40 Ar | 18 | 22 | 39,9624 |
| 39 K | 19 | 20 | 38,9637 |
| 40 K* | 19 | 21 | 39,9640 |
| 41 K | 19 | 22 | 40,9618 |
| 40 Ca | 20 | 20 | 39,9626 |
| 42 Ca | 20 | 22 | 41,9586 |
| 43 Ca | 20 | 23 | 42,9588 |
| 44 Ca | 20 | 24 | 43,9555 |
| 46 Ca | 20 | 26 | 45,9537 |
| 48 Ca* | 20 | 28 | 47,9525 |
| 45 Sc | 21 | 24 | 44,9559 |
| 46 Ti | 22 | 24 | 45,9526 |
| 47 Ti | 22 | 25 | 46,9518 |
| 48 Ti | 22 | 26 | 47,9479 |
| 49 Ti | 22 | 27 | 48,9479 |
| 50 Ti | 22 | 28 | 49,9448 |
| 50 V* | 23 | 27 | 49,9472 |
| 51 V | 23 | 28 | 50,9440 |
| 50 Cr | 24 | 26 | 49,9460 |
| 52 Cr | 24 | 28 | 51,9405 |
| 53 Cr | 24 | 29 | 52,9406 |
| 54 Cr | 24 | 30 | 53,9389 |
| 55 Mn | 25 | 30 | 54,9380 |
| 54 Fe | 26 | 28 | 53,9396 |
| 56 Fe | 26 | 30 | 55,9349 |
| 57 Fe | 26 | 31 | 56,9354 |
| 58 Fe | 26 | 32 | 57,9333 |
| 59 Co | 27 | 32 | 58,9332 |
| 58 Ni | 28 | 30 | 57,9353 |
| 60 Ni | 28 | 32 | 59,9308 |
| 61 Ni | 28 | 33 | 60,9311 |
| 62 Ni | 28 | 34 | 61,9283 |
| 64 Ni | 28 | 36 | 63,9280 |
| 63 Cu | 29 | 34 | 62,9296 |
| 65 Cu | 29 | 36 | 64,9278 |
| 64 Zn | 30 | 34 | 63,9291 |
| 66 Zn | 30 | 36 | 65,9260 |
| 67 Zn | 30 | 37 | 66,9271 |
| 68 Zn | 30 | 38 | 67,9248 |
| 70 Zn | 30 | 40 | 69,9253 |
| 69 Ga | 31 | 38 | 68,9256 |
| 71 Ga | 31 | 40 | 70,9247 |
| 70 Ge | 32 | 38 | 69,9242 |
| 72 Ge | 32 | 40 | 71,9221 |
| 73 Ge | 32 | 41 | 72,9235 |
| 74 Ge | 32 | 42 | 73,9212 |
| 75 As | 33 | 42 | 74,9216 |
| 74 Se | 34 | 40 | 73,9225 |
| 76 Se | 34 | 42 | 75,9192 |
| 77 Se | 34 | 43 | 76,9199 |
| 78 Se | 34 | 44 | 77,9173 |
| 80 Se | 34 | 46 | 79,9165 |
| 82 Se * | 34 | 48 | 81,9167 |
| 79 Br | 35 | 44 | 78,9183 |
| 81 Br | 35 | 46 | 80,9163 |
| 78 Kr * | 36 | 42 | 77,9204 |
| 80 Kr | 36 | 44 | 79,9164 |
| 82 Kr | 36 | 46 | 81,9135 |
| 83 Kr | 36 | 47 | 82,9141 |
| 84 Kr | 36 | 48 | 83,9115 |
| 86 Kr | 36 | 50 | 85,9106 |
| 85 Rb | 37 | 48 | 84,9118 |
| 87 Rb* | 37 | 50 | 86,9092 |
| 84 Sr | 38 | 46 | 83,9134 |
| 86 Sr | 38 | 48 | 85,9093 |
| 87 Sr | 38 | 49 | 86,9089 |
| 88 Sr | 38 | 50 | 87,9056 |
| 89 Y | 39 | 50 | 88,9058 |
| 90 Zr | 40 | 50 | 89,9047 |
| 91 Zr | 40 | 51 | 90,9056 |
| 92 Zr | 40 | 52 | 91,9050 |
| 94 Zr | 40 | 54 | 93,9063 |
| 93 Nb | 41 | 52 | 92,9064 |
| 92 Mo | 42 | 50 | 91,9068 |
| 94 Mo | 42 | 52 | 93,9051 |
| 95 Mo | 42 | 53 | 94,9058 |
| 96 Mo | 42 | 54 | 95,9047 |
| 97 Mo | 42 | 55 | 96,9060 |
| 98 Mo | 42 | 56 | 97,9054 |
| 100 Mo* | 42 | 58 | 99,9075 |
| 96 Ru | 44 | 52 | 95,9076 |
| 98 Ru | 44 | 54 | 97,9053 |
| 99 Ru | 44 | 55 | 98,9059 |
| 100 Ru | 44 | 56 | 99,9042 |
| 101 Ru | 44 | 57 | 100,9056 |
| 102 Ru | 44 | 58 | 101,9043 |
| 104 Ru | 44 | 60 | 103,9054 |
| 103 Rh | 45 | 58 | 102,9055 |
| 102 Pd | 46 | 56 | 101,9056 |
| 104 Pd | 46 | 58 | 103,9040 |
| 105 Pd | 46 | 59 | 104,9051 |
| 106 Pd | 46 | 60 | 105,9035 |
| 108 Pd | 46 | 62 | 107,9039 |
| 110 Pd | 46 | 64 | 109,9052 |
| 107 Ag | 47 | 60 | 106,9051 |
| 109 Ag | 47 | 62 | 108,9048 |
| 106 Cd | 48 | 58 | 105,9065 |
| 108 Cd | 48 | 60 | 107,9042 |
| 110 Cd | 48 | 62 | 109,9030 |
| 111 Cd | 48 | 63 | 110,9042 |
| 112 Cd | 48 | 64 | 111,9028 |
| 113 Cd* | 48 | 65 | 112,9044 |
| 114 Cd | 48 | 66 | 113,9034 |
| 116 Cd* | 48 | 68 | 115,9048 |
| 113 In | 49 | 64 | 112,9041 |
| 115 In* | 49 | 66 | 114,9039 |
| 112 Sn | 50 | 62 | 111,9048 |
| 114 Sn | 50 | 64 | 113,9028 |
| 115 Sn | 50 | 65 | 114,9033 |
| 116 Sn | 50 | 66 | 115,9017 |
| 117 Sn | 50 | 67 | 116,9030 |
| 118 Sn | 50 | 68 | 117,9016 |
| 119 Sn | 50 | 69 | 118,9033 |
| 120 Sn | 50 | 70 | 119,9022 |
| 122 Sn | 50 | 72 | 121,9034 |
| 124 Sn | 50 | 74 | 123,9053 |
| 121 Sb | 51 | 70 | 120,9038 |
| 123 Sb | 51 | 72 | 122,9042 |
| 120 Te | 52 | 68 | 119,9040 |
| 122 Te | 52 | 70 | 121,9030 |
| 123 Te | 52 | 71 | 122,9043 |
| 124 Te | 52 | 72 | 123,9028 |
| 125 Te | 52 | 73 | 124,9044 |
| 126 Te | 52 | 74 | 125,9033 |
| 128 Te* | 52 | 76 | 127,9045 |
| 130 Te* | 52 | 78 | 129,9062 |
| 127 I | 53 | 74 | 126,9045 |
| 124 Xe* | 54 | 70 | 123,9059 |
| 126 Xe | 54 | 72 | 125,9043 |
| 128 Xe | 54 | 74 | 127,9035 |
| 129 Xe | 54 | 75 | 128,9048 |
| 130 Xe | 54 | 76 | 129,9035 |
| 131 Xe | 54 | 77 | 130,9051 |
| 132 Xe | 54 | 78 | 131,9042 |
| 134 Xe | 54 | 80 | 133,9054 |
| 136 Xe* | 54 | 82 | 135,9072 |
| 133 Cs | 55 | 78 | 132,9055 |
| 130 Ba* | 56 | 74 | 129,9063 |
| 132 Ba | 56 | 76 | 131,9051 |
| 134 Ba | 56 | 78 | 133,9045 |
| 135 Ba | 56 | 79 | 134,9057 |
| 136 Ba | 56 | 80 | 135,9046 |
| 137 Ba | 56 | 81 | 136,9058 |
| 138 Ba | 56 | 82 | 137,9052 |
| 138 La* | 57 | 81 | 137,9071 |
| 139 La | 57 | 82 | 138,9064 |
| 136 Ce | 58 | 78 | 135,9072 |
| 138 Ce | 58 | 80 | 137,9060 |
| 140 Ce | 58 | 82 | 139,9054 |
| 142 Ce | 58 | 84 | 141,9092 |
| 141 Pr | 59 | 82 | 140,9077 |
| 142 Nd | 60 | 82 | 141,9077 |
| 143 Nd | 60 | 83 | 142,9098 |
| 144 Nd* | 60 | 84 | 143,9101 |
| 145 Nd | 60 | 85 | 144,9126 |
| 146 Nd | 60 | 86 | 145,9131 |
| 148 Nd | 60 | 88 | 147,9169 |
| 150 Nd* | 60 | 90 | 149,9209 |
| 144 Sm | 62 | 82 | 143,9120 |
| 147 Sm* | 62 | 85 | 146,9149 |
| 148 Sm* | 62 | 86 | 147,9148 |
| 149 Sm | 62 | 87 | 148,9172 |
| 150 Sm | 62 | 88 | 149,9173 |
| 152 Sm | 62 | 90 | 151,9197 |
| 154 Sm | 62 | 92 | 153,9222 |
| 151 Eu* | 63 | 88 | 150,9199 |
| 153 Eu | 63 | 90 | 152,9212 |
| 152 Gd* | 64 | 88 | 151,9198 |
| 154 Gd | 64 | 90 | 153,9209 |
| 155 Gd | 64 | 91 | 154,9226 |
| 156 Gd | 64 | 92 | 155,9221 |
| 157 Gd | 64 | 93 | 156,9240 |
| 158 Gd | 64 | 94 | 157,9241 |
| 160 Gd | 64 | 96 | 159,9271 |
| 159 Tb | 65 | 94 | 158,9253 |
| 156 Dy | 66 | 90 | 155,9243 |
| 158 Dy | 66 | 92 | 157,9244 |
| 160 Dy | 66 | 94 | 159,9252 |
| 161 Dy | 66 | 95 | 160,9269 |
| 162 Dy | 66 | 96 | 161,9268 |
| 163 Dy | 66 | 97 | 162,9287 |
| 164 Dy | 66 | 98 | 163,9292 |
| 165 Ho | 67 | 98 | 164,9303 |
| 162 Er | 68 | 94 | 161,9288 |
| 164 Er | 68 | 96 | 163,9292 |
| 166 Er | 68 | 98 | 165,9303 |
| 167 Er | 68 | 99 | 166,9320 |
| 168 Er | 68 | 100 | 167,9324 |
| 170 Er | 68 | 102 | 169,9355 |
| 169 Tm | 69 | 100 | 168,9342 |
| 168 Yb | 70 | 98 | 167,9339 |
| 170 Yb | 70 | 100 | 169,9348 |
| 171 Yb | 70 | 101 | 170,9363 |
| 172 Yb | 70 | 102 | 171,9364 |
| 173 Yb | 70 | 103 | 172,9382 |
| 174 Yb | 70 | 104 | 173,9389 |
| 176 Yb | 70 | 106 | 175,9426 |
| 175 Lu | 71 | 104 | 174,9408 |
| 176 Lu* | 71 | 105 | 175,9427 |
| 174 Hf* | 72 | 102 | 173,9400 |
| 176 Hf | 72 | 104 | 175,9414 |
| 177 Hf | 72 | 105 | 176,9432 |
| 178 Hf | 72 | 106 | 177,9437 |
| 179 Hf | 72 | 107 | 178,9458 |
| 180 Hf | 72 | 108 | 179,9466 |
| 181 Ta | 73 | 108 | 180,9480 |
| 180 W* | 74 | 106 | 179,9467 |
| 182 W | 74 | 108 | 181,9482 |
| 183 W | 74 | 109 | 182,9502 |
| 184 W | 74 | 110 | 183,9509 |
| 186 W | 74 | 112 | 185,9544 |
| 185 Re | 75 | 110 | 184,9530 |
| 187 Re* | 75 | 112 | 186,9558 |
| 184 Os | 76 | 108 | 183,9525 |
| 186 Os* | 76 | 110 | 185,9538 |
| 187 Os | 76 | 111 | 186,9558 |
| 188 Os | 76 | 112 | 187,9558 |
| 189 Os | 76 | 113 | 188,9581 |
| 190 Os | 76 | 114 | 188,9581 |
| 192 Os | 76 | 116 | 191,9615 |
| 191 Ir | 77 | 114 | 190,9606 |
| 193 Ir | 77 | 116 | 191,9626 |
| 190 Pt* | 78 | 112 | 189,9599 |
| 192 Pt | 78 | 114 | 191,9610 |
| 194 Pt | 78 | 116 | 193,9627 |
| 195 Pt | 78 | 117 | 194,9648 |
| 196 Pt | 78 | 118 | 195,9650 |
| 198 Pt | 78 | 120 | 197,9679 |
| 197 Au | 79 | 118 | 196,9666 |
| 196 Hg | 80 | 116 | 195,9658 |
| 198 Hg | 80 | 118 | 197,9668 |
| 199 Hg | 80 | 119 | 198,9683 |
| 200 Hg | 80 | 120 | 199,9683 |
| 201 Hg | 80 | 121 | 200,9703 |
| 202 Hg | 80 | 122 | 201,9706 |
| 204 Hg | 80 | 124 | 203,9735 |
| 203 Tl | 81 | 122 | 202,9723 |
| 205 Tl | 81 | 124 | 204,9744 |
| 204 Pb | 82 | 122 | 203,9730 |
| 206 Pb | 82 | 124 | 205,9745 |
| 207 Pb | 82 | 125 | 206,9759 |
| 208 Pb | 82 | 126 | 207,9767 |
| 209 Bi* | 83 | 126 | 208,9804 |
| 232 Th* | 90 | 142 | 232,0381 |
| 235 U* | 92 | 143 | 235,0439 |
* это нестабильные изотопы и с большим периодом полураспада, который равняется возрасту Вселенной.