Фвлж что это за процедура
Применение алгоритма HFA-PEFF для диагностики сердечной недостаточности с сохраненной фракцией выброса левого желудочка
Выявление сердечной недостаточности с сохраненной фракцией выброса левого желудочка (СНсФВ) у пациентов с артериальной гипертонией (АГ) высокого риска и симптомами СН по новому модифицированному алгоритму HFA-PEFF с применением пробы с пассивным подъемом ног и неинвазивной оценкой давления заклинивания легочной артерии (ДЗЛА).
Материалы и методы
В исследование включено 90 пациентов с АГ высокого риска, симптомами СН и фракцией выброса левого желудочка (ФВ ЛЖ) ≥ 50%. Для выявления СНсФВ использован алгоритм HFA-PEFF. Стресс-эхокардиографию проводили с применением пробы с пассивным подъемом ног, неинвазивную оценка ДЗЛА – с использованием уравнения Nagueh (1997) [ДЗЛА = 1,91+(1,24×E/e’)].
Согласно алгоритму HFA-PEFF пациенты были распределены на 3 группы: низкая вероятность/исключена СНсФВ ( Заключение
Алгоритм HFA-PEFF позволил подтвердить наличие СНсФВ у 58,9% пациентов с АГ, симптомами СН и ФВ ЛЖ ≥50%. Полученные данные демонстрируют целесообразность проведения стресс-эхокардиографии с пассивным подъемом ног для диагностики СНсФВ.
Несмотря на значительную заболеваемость и смертность, сердечная недостаточность с сохраненной фракцией выброса (СНсФВ) остается «загадкой» современной кардиологии. Прогноз пациентов с СНсФВ практически не изменился и по-прежнему считается неблагоприятным [1,2]. Отсутствие единого алгоритма диагностики и оценки прогноза СНсФВ, а также наличие «недочетов» в существующих рекомендациях являются одной из очевидных и важных проблем современной кардиологии.
В 2019 г. был опубликован документ, выпущенный под эгидой Европейского общества специалистов по сердечной недостаточности (HFA) и Европейского общества кардиологов (ESC) и предлагающий новый алгоритм диагностики СНсФВ – HFA-PEFF [3], который включает в себя клиническую оценку, ультразвуковое исследование сердца в покое и при нагрузке, определение уровня натрийуретического пептида (НУП), а также инвазивную оценку гемодинамики и определение этиологии сердечной недостаточности. Инвазивное изучение гемодинамики предполагает катетеризацию сердца, которая сопряжена с определенными сложностями и осложнениями, что ограничивает ее использование в рутинной клинической практике. В нашем исследовании мы использовали модифицированный алгоритм HFA-PEFF с неинвазивной оценкой давления заклинивания легочной артерии (ДЗЛА) с помощью эхокардиографии [4].
Целью исследования было выявление СНсФВ у пациентов с артериальной гипертонией (АГ) высокого риска и симптомами сердечной недостаточности (СН) по новому модифицированному алгоритму HFA-PEFF с применением пробы с пассивным подъемом ног и неинвазивной оценкой ДЗЛА.
Материал и методы
В проспективное исследование включали пациентов старше 65 лет или ≥55 лет при наличии ожирения и/или фибрилляции предсердий (ФП) и сахарного диабета (СД), у которых имелись артериальная гипертония и симптомы СН с ФВ ЛЖ ≥50%. Критерии исключения: индекс массы тела (ИМТ) ≥40 кг/м2, острый коронарный синдром или острое нарушение мозгового кровообращения в течение последних трех месяцев, онкологические заболевания, тяжелый порок клапанов сердца, заболевания, которые сопровождаются симптомами, сходными с таковыми СН (хроническая обструктивная болезнь легких, бронхиальная астма, анемия – концентрация гемоглобина менее 90 г/л).
Шаг 1 алгоритма HFA-PEFF аналогичен критериям диагностики СНсФВ в соответствии с действующими рекомендациями Европейского общества кардиологов 2016 г. [5]: оценка симптомов и признаков СН, выявление факторов риска и сопутствующих заболеваний, определение функционального класса (ФК) СН по NYHA с помощью теста с 6-минутной ходьбой, ЭКГ и стандартная эхокардиография (как минимум, измерение ФВ ЛЖ и конечного диастолического размера ЛЖ).
Шаг 2 включает оценку структурно-функциональных параметров миокарда и измерение уровня NT-proBNP. На этом этапе используется расширенный протокол эхокардиографии с тканевой допплерографией с выделением больших и малых критериев, которым присваиваются баллы (табл. 1). При сочетании большого и малого критериев в пределах одной области (структурная, функциональная, натрийуретические пептиды) баллы не суммируются. При наличии ТАБЛИЦА 1. Большие и малые критерии СНсФВ (Шаг 2)
(СДЛА >35 мм рт. ст.)
иОЛП >40 мл/м2 (ФП)
ИЛИ
иММЛЖ ≥149 г/м2
у мужчин или ≥122 г/м2
у женщин и ОТС >0,42
ИЛИ
BNP >80 пг/мл
ИЛИ
BNP >240 пг/мл
или
GLS 0,42
ИЛИ
ТСЛЖд ≥12 мм
ИЛИ
BNP 35-80 пг/мл
ИЛИ
BNP 105-240 пг/мл
Пациентам с промежуточной вероятностью СН (2-4 балла) проводится диастолическая стресс-эхокардиография с пассивным подъемом ног (Шаг 3) (рис. 1) [6]. Применение диастолической стресс-эхокардиографии позволяет выявить диастолическую дисфункцию на ранних стадиях, когда давление наполнения в ЛЖ остается нормальным в покое, но достигает патологических значений при нагрузке. При проведении пробы с пассивным подъемом ног происходит отток крови от нижних конечностей, увеличение притока венозной крови к сердцу и давления наполнения ЛЖ. Косвенными показателями давления наполнения ЛЖ при эхокардиографии являются параметры E/e’ и максимальная скорость трикуспидальной регургитации (ТРmax). Проба считается положительной при E/e’≥15 (2 балла) или при E/e’≥15 и увеличении скорости ТРmax >3,4 м/с (3 балла). Если у пациента определяется только увеличение ТРmax, проба считается отрицательной, так как нарастание этого показателя отражает физиологический ответ на физическую нагрузку и связано с увеличением легочного кровотока. ДЗЛА рассчитывали по уравнению Nagueh: ДЗЛА = 1,91+(1,24×E/e’), где Е – максимальная скорость раннего диастолического наполнения ЛЖ, измеренная при импульсно-волновой допплерографии, e’ – усредненная максимальная скорость раннего диастолического смещения септальной и латеральной частей кольца митрального клапана. Была выявлена тесная корреляция измерения ДЗЛА инвазивным методом и при эхокардиографии с применением тканевого допплера [4]. Косвенным показателем повышения давления в левых отделах сердца является увеличение ДЗЛА ≥15 мм рт. ст. в покое и ≥25 мм рт. ст. при нагрузке [6].

Результаты
Клинико-демографическая характеристика пациентов приведена в табл. 2. При поступлении наиболее распространенными симптомами были одышка при нагрузке (100%), слабость (57,4%) и отеки (35,0%).
| Показатель | Значение |
|---|---|
| Женщины, n (%) | 63(70,0) |
| Возраст, годы | 69,3±10,6 |
| Длительность АГ, годы | 15,8±7,8 |
| Индекс массы тела, г/м 2 | 28,3±4,9 |
| Ожирение, n (%) | 39 (33;43) |
| Функциональный класс СН, NYHA, n (%) | |
| II | 24 (26,7) |
| III | 47 (52,2) |
| IV | 19 (21,1) |
| Одышка, n (%) | |
| Легкая | 41 (45,6) |
| Умеренная | 41 (45,6) |
| Тяжелая | 8 (8,8) |
| Отеки нижних конечностей, n (%) | 45 (50,0) |
| NT-proBNP, пг/мл | 142 (50;220) |
| рCКФ, мл/мин/1,73 м 2 | 58,6 (48,6;72,9) |
| Фибрилляция предсердий, n (%) | 29 (32,2) |
| Пароксизмальная форма | 26 (28,9) |
| 3 (3,3)Постоянная форма | 3 (3,3) |
| Сахарный диабет 2 типа, n (%) | 40 (44,4) |
| Хроническая болезнь почек, n (%) | 41 (45,6) |
| Легочная гипертензия, n (%) | 67 (74,4) |
| 1 степень | 58 (64,4) |
| 2 степень | 6 (6,7) |
| 3 степень | 3 (3,3) |
| Фракция выброса левого желудочка, % | 58,1±5,3 |
| Диастолическая дисфункция, n (%) | |
| 1 тип | 41 (45,6) |
| 2 тип | 46 (51,1) |
| 3 тип | 0 (0) |
| Фибрилляция предсердий | 3 (3,3) |
| Гипертрофия левого желудочка, n (%) | 65 (72,2) |
| Среднее давление в легочной артерии, мм рт. ст. | 33,2±12,0 |
| Индекс объема левого предсердия, мл/м 2 | 27,4±10,7 |
| Индекс массы миокарда ЛЖ, г/м 2 | 113,6±21,2 |
| GLS | 17 (14,20) |
| E/e’ | 8,0±2,2 |
Результаты оценки наличия СНсФВ по алгоритму HFA-PEFF представлены на рис. 2. На втором этапе СНсФВ была выявлена у 36 (40,0%) из 90 пациентов и исключена у 8 (9,0%), в то время как 46 (51,0%) больным для установления диагноза потребовалась стрессэхокардиография (шаг 3). При проведении этого исследования у 17 (18,9%) пациентов отмечено увеличение E/e’ ≥15, а наличие СНcФВ подтверждалась увеличением ДЗЛА при проведении пробы с пассивным подъемом ног ≥25 мм рт. ст. Следует отметить, что у 4 (4,4%) из 90 пациентов имелись только малые критерии диагностики СНсФВ. Таким образом, при применении алгоритма HFA-PEFF у 53 (58,9%) из 90 пациентов была диагностирована СНсФВ.

Обсуждение
В нашем исследовании показана возможность использования модифицированного алгоритма HFA-PEFF, применение которого позволило выявить СНсФВ у 58,9% пациентов с АГ высокого риска с сохраненной ФВ и симптомами СН.
За последние десятилетия доля СНсФВ в структуре СН увеличилась с 41% до 56% [7]. Согласно данным крупного обсервационного исследования ЭПОХА-О-ХС среди всех больных с СН пациенты с ФВ ЛЖ более 50% составляют 56,8% [8]. В будущем можно ожидать дальнейшего роста числа таких пациентов в связи со старением населения. Однако в настоящее время нет единых критериев диагностики СНсФВ, которые отличаются как в рекомендациях кардиологических обществ, так и в рандомизированных клинических исследованиях. Хо и соавт. провели инвазивное исследование гемодинамики у 461 пациента с одышкой при нагрузке и ФВ ЛЖ≥50% и сопоставили частоту СНсФВ, установленной с использованием различных критериев [9]. Увеличение ДЗЛА было выявлено у 243 (52,7%) больных, в то время как по критериям Американской коллегии кардиологов/Американской ассоциации сердца 2013 г. СНсФВ была диагностирована у 416 (90,2%) пациентов, по критериям Евро пей ского общества кардиологов 2016 г. – у 205 (44,5%), а по критериям Американского общества сердечной недостаточности – у 55 (11,9%). Полученные данные демонстрируют ограниченные возможности современных рекомендаций. Авторы предложили фенотипировать пациентов с СНсФВ по клиническим и гемодинамическим параметрам, что, безусловно, имеет большое значение для их лечения. Таким образом, в действующих рекомендациях не учитываются неоднородность и коморбидность больных с СНсФВ, что обусловливает низкую специфичность и чувствительность предложенных критериев диагностики.
Новый алгоритм HFA-PEFF учитывает все современные аспекты диагностики СНсФВ, предполагает комплексное обследование пациентов и может стать альтернативой существующим рекомендациям. Наибо лее значимым преимуществом данного алгоритма явля ется тот факт, что авторы принимают во внимание особенности изменений уровней натрийуретических пептидов и индекса объема левого предсердия у пациентов с ФП.
Однако данный алгоритм имеет и ограничения. Заболевания опорно-двигательного аппарата, неврологические нарушения и ожирение могут препятствовать выполнению нагрузочной пробы. В свою очередь, инвазивная оценка гемодинамики, как было указано ранее, сопряжена с определенными сложностями выполнения и осложнениями. Например, в японском исследовании при проведении 576 процедур катетеризации правых отделов сердца было зарегистрировано 65 (11,3%) осложнений, 13 из которых были серьезными, включая 1 (2,3%) случай смерти [10]. В другом исследовании, проведенном специалистами из Уэльского кардиологического научно-исследовательского института, общая частота осложнений катетеризации правых отделов сердца составила 7,4%, а смертность – 0,7% [11].
В 2018 г. специалисты из Швеции провели исследование у 29 пациентов с симптомами СН, которым проводили эхокардиографию и катетеризацию правых камер сердца в покое и при нагрузке с пассивным подъемом ног. Было установлено, что у 41% пациентов с нормальным ДЗЛА в покое наблюдалось значительное его повышение при проведении пробы с пассивным подъемом ног [12]. Учитывая простоту выполнения пробы с пассивным подъемом ног, ее доступность, а также независимость от состояний, которые препятствуют проведению нагрузочных проб, представляется целесообразным проведение дальнейших исследований для оценки эффективности предложенного нами модифицированного алгоритма HFA-PEFF у большей популяции пациентов с симптомами СН.
Заключение
Частота выявления СНсФВ по модифицированному алгоритму диагностики HFA-PEFF у пациентов с АГ высокого риска и симптомами СН составила 58,9%. Применение нового алгоритма диагностики HFA-PEFF позволяет верифицировать СНсФВ с оценкой давления наполнения ЛЖ с помощью диастолической стрессэхокардиографии и неинвазивной оценки ДЗЛА.
Фракция выброса левого желудочка сердца: нормы, причины понижения и высокой, как повысить
Симптомы сниженной фракции выброса
Все симптомы, по которым можно заподозрить снижение сократительной функции сердца, обусловлены ХСН. Поэтому и симптоматика этого заболевания выходит на первое место.
Однако, согласно наблюдениям практикующих врачей УЗ-диагностики, часто наблюдается следующее – у пациентов с выраженными признаками ХСН показатель фракции выброса остается в пределах нормы, в то время как у лиц с отсутствующими явными симптомами показатель фракции выброса значительно снижен. Поэтому несмотря на отсутствие симптомов, пациентам с наличием сердечной патологии обязательно хотя бы раз в год выполнять эхокардиоскопию.
Итак, к симптомам, позволяющим заподозрить нарушение сократимости миокарда, относятся:
При отсутствии грамотного лечения систолической дисфункции миокарда такие симптомы прогрессируют, нарастают и все тяжелее переносятся пациентом, поэтому при возникновении даже одного из них следует получить консультацию врача-терапевта или кардиолога.
Нормальные показатели ФВ
Нормальное значение фракции выброса отличается у разных людей, а также зависит от аппаратуры, на которой проводится исследование, и от метода, по которому рассчитывают фракцию.
Усредненные значения составляют приблизительно 50-60%, нижняя граница нормы по формуле Симпсона составляет не менее 45%, по формуле Тейхольца – не менее 55%. Этот процент означает, что именно такое количество крови за одно сердечное сокращение необходимо протолкнуть сердцу в просвет аорты, чтобы обеспечить адекватную доставку кислорода к внутренним органам.
О запущенной сердечной недостаточности говорят 35-40%, еще более низкие значения чреваты скоротечными последствиями.
У детей в периоде новорожденности ФВ составляет не менее 60%, в основном 60-80%, постепенно достигая обычных показателей нормы по мере роста.
Из отклонений от нормы чаще, чем повышенная фракция выброса, встречается снижение ее значения, обусловленное различными заболеваниями.
Если показатель снижен, значит, сердечная мышца не может достаточно сокращаться, вследствие чего объем изгоняемой крови уменьшается, а внутренние органы, и, в первую очередь, головной мозг, получают меньше кислорода.
Иногда в заключении эхокардиоскопии можно увидеть, что значение ФВ выше усредненных показателей (60% и более). Как правило, в таких случаях показатель составляет не более 80%, так как больший объем крови левый желудочек в силу физиологических особенностей изгнать в аорту не сможет.
Как правило, высокая ФВ наблюдается у здоровых лиц при отсутствии иной кардиологической патологии, а также у спортсменов с тренированной сердечной мышцей, когда сердце при каждом ударе сокращается с большей силой, чем у обычного человека, и изгоняет в аорту больший процент содержащейся в нем крови.
Кроме этого, в случае, если у пациента имеется гипертрофия миокарда ЛЖ как проявление гипертрофической кардиомиопатии или артериальной гипертонии, повышенная ФВ может свидетельствовать о том, что сердечная мышца пока еще может компенсировать начинающуюся сердечную недостаточность и стремится изгнать в аорту как можно больше крови. По мере прогрессирования сердечной недостаточности ФВ постепенно снижается, поэтому для пациентов с клинически проявляющейся ХСН очень важно выполнять эхокардиоскопию в динамике, чтобы не пропустить снижение ФВ.
Важный метод диагностики
Исследование сердца ультразвуком
Эхокардиографическое исследование сердечно-сосудистой системы является очень важным и к тому же достаточно доступным методом диагностики. В ряде случае метод является «золотым стандартом», позволяя верифицировать тот или иной диагноз. Кроме того, метод позволяет выявить скрытую сердечную недостаточность, не проявляющую себя при интенсивных физических нагрузках. Данные об эхокардиографии (нормальных показателях) могут несколько разниться в зависимости от источника. Мы приводим нормы, предложенные Американской ассоциацией эхокардиографии и Европейской ассоциацией кардиоваскулярной визуализации от 2015 года.
Размеры камер сердца
Размеры камер сердца — параметр, который определяется для того, чтобы исключить или подтвердить перегрузку предсердий или желудочков.
Левое предсердие. Норма диаметра левого предсердия (ЛП) в мм для мужчин — ≤ 40, для женщин ≤ 38. Увеличение диаметра левого предсердия может свидетельствовать о сердечной недостаточности у пациента. Кроме диаметра ЛП, измеряется также его объем. Норма объема ЛП для мужчин в мм3 составляет ≤ 58, для женщин ≤ 52. Размеры ЛП возрастает при кардиомиопатиях, пороках митрального клапана, аритмиях (нарушениях ритма сердца), врожденных пороках сердца.
Правое предсердие. Для правого предсердия (ПП), как и для левого предсердия, методом ЭхоКГ определяются размеры (диаметр и объем). В норме диаметр ПП составляет ≤ 44 мм. Объем правого предсердия делится на площадь поверхности тела (ППТ). Для мужчин нормальным считается соотношение объем ПП/ППТ ≤ 39 мл/м2, для женщин — ≤33 мл/м2. Размеры правого предсердия могут увеличиваться при недостаточности правых отделов сердца. Легочная гипертензия, тромбоэмболия легочной артерии, хроническая обструктивная болезнь легких и другие заболевания могут стать причиной развития недостаточности правого предсердия.
ЭХО Кардиография (УЗИ сердца)
Левый желудочек. Для желудочков введены свои параметры, касающиеся их размеров. Так как практикующему врачу представляет интерес функциональное состояние желудочков в систолу и диастолу, существуют соответствующие показатели. Основные показатели размеров для ЛЖ:
Показатели диастолического и систолического объема и размера могут увеличиваться при заболеваниях миокарда, сердечной недостаточности, а также при врожденных и приобретенных пороках сердца.
Показатели массы миокарда
Масса миокарда ЛЖ может увеличиваться при утолщении его стенок (гипертрофии). Причиной гипертрофии могут быть различные заболевания сердечно-сосудистой системы: артериальная гипертензия, пороки митрального, аортального клапана, гипертрофической кардиомиопатии.
Межжелудочковая перегородка. Толщина МЖП у мужчин в мм — ≤ 10, у женщин — ≤ 9;
Оценка фракции выброса левого желудочка при помощи эхокардиографии: преимущества и ограничения метода

Сердце в человеческом организме – это насос. Подобно тому как для определения производительности техники используют разные параметры, такие как мощность в лошадиных силах, количество и размер цилиндров, ФВ ЛЖ является одним из показателей оценки функции сердца. Как и любой другой метод, оценка ФВ ЛЖ имеет свои преимущества и ограничения.
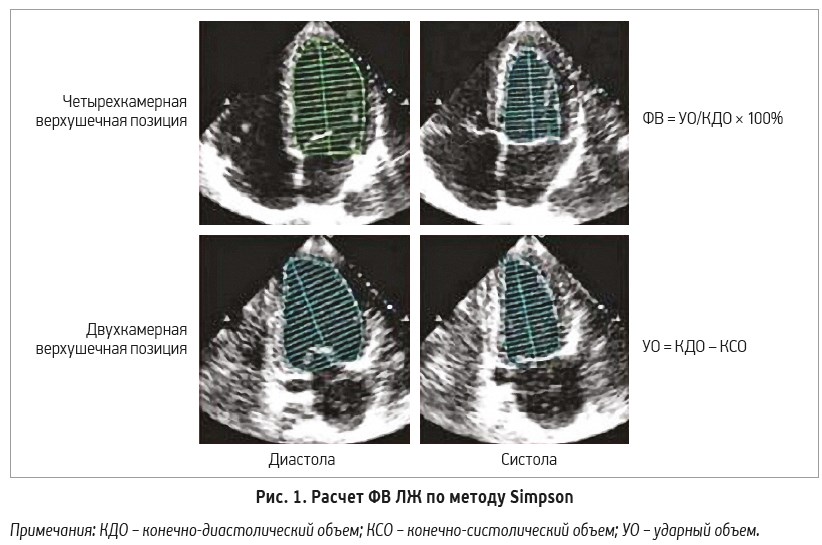
В соответствии с текущими рекомендациями (2015) ФВ ЛЖ (соотношение количества крови, выбрасываемой ЛЖ в аорту в каждый сердечный цикл, к объему ЛЖ, выраженное в процентах) рассчитывается по методу Simpson в двух позициях – четырех- и двухкамерной верхушечных позициях (рис. 1) [11, 12].
Одним из ограничений является плохое качество изображения, даже при условии выполнения 3D‑эхокардиографии, так как метод основан на оконтуривании внутренней границы эндокарда. Тем не менее ФВ ЛЖ является одним из самых часто используемых показателей в повседневной клинической практике, его измерение введено во все национальные руководства по эхокардиографии в качестве порогового значения для множества терапевтических стратегий [7].
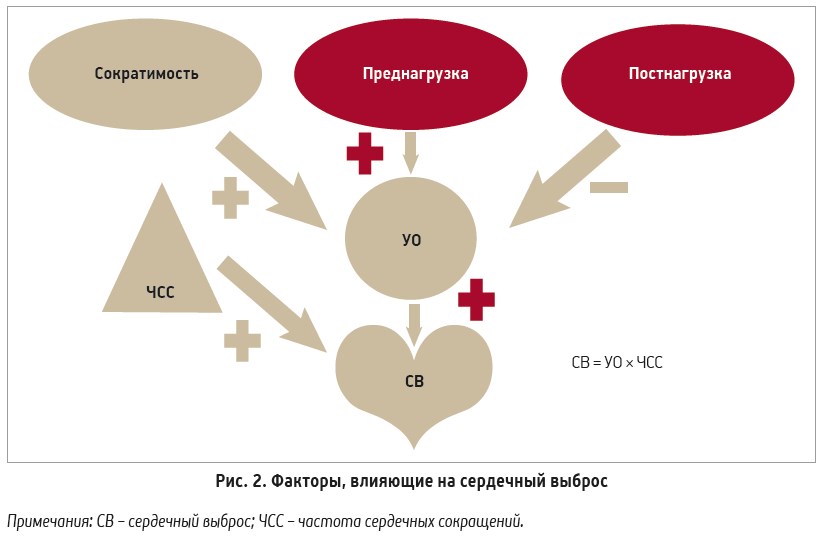
В то же время дальнейшее изучение говорит о том, что данный показатель не является идеальным для оценки функции ЛЖ. Оценка ФВ не дает представления о сердечном выбросе (СВ) – количестве крови, которое сердце как насос перекачивает за единицу времени (часто рассчитывают за 1 мин). В норме СВ составляет 3-4 л за 1 мин. На рисунке 2 представлены влияющие на данный показатель факторы.
ФВ ЛЖ – это суррогатный индекс сократимости миокарда, который не в полной мере отражает систолическую функцию ЛЖ, поскольку зависит от пред-, постнагрузки, объемов ЛЖ, ЧСС, клапанной патологии и не является прямым аналогом УО или СВ. Значение ФВ должно быть интерпретировано в каждом конкретном клиническом случае.
Ограничения метода
1. Контрактильный резерв. ФВ ЛЖ традиционно рассчитывается в покое, поэтому не известно, увеличится ли она при нагрузке (контрактильный резерв сердца). Клиницист не может использовать этот показатель для ответа на вопрос, почему у пациента одышка при физической нагрузке. Такая возможность появляется при проведении стресс-эхокардиографии либо спекл-трекинг стресс-эхокардиографии: ФВ ЛЖ или глобальная продольная деформация оцениваются изначально в покое, а затем во время физической или фармакологической нагрузки [3].
2. Клиническая ситуация, при которой у пациента «маленький ЛЖ» (концентрическая гипертрофия миокарда ЛЖ).
Проиллюстрировать это можно следующим образом.
Случай 1. У пациента А. КДО = 100 мл, КСО = 50 мл.
УО = 100 – 50 = 50 мл. ФВ = 50/100 × 100% = 50%.
Случай 2. У пациента В. КДО = 50 мл, КСО = 25 мл.
УО = 50 – 25 = 25 мл. ФВ = 25/50 × 100% = 50%.
Пациенты с разными объемами ЛЖ имеют одинаковую ФВ. Означает ли это, что у них одинаковая функция ЛЖ? ЧСС у обоих составляет 70 уд./мин. Даже при одинаковой ФВ ЛЖ пациенты имеют разный СВ.
Случай 1. У пациента А. СВ = 50 × 70 = 3500 мл/мин.
Случай 2. У пациента В. СВ = 25 × 70 = 1750 мл/мин.
Исходя из приведенных расчетов, у пациента В. гораздо худшая функция сердца, чем у пациента А.: даже при увеличении ЧСС до 110 уд./мин при нагрузке УО составит 1750 мл/мин, то есть больной не имеет резерва для улучшения функции сердца при нагрузке.
Таким образом, ФВ у пациентов с небольшими объемами ЛЖ не может служить адекватным показателем оценки функции. УО снижен у больных с концентрической гипертрофией ЛЖ и удовлетворительной ФВ, что очень важно для интерпретации показателя ФВ ЛЖ в клинической практике [13].
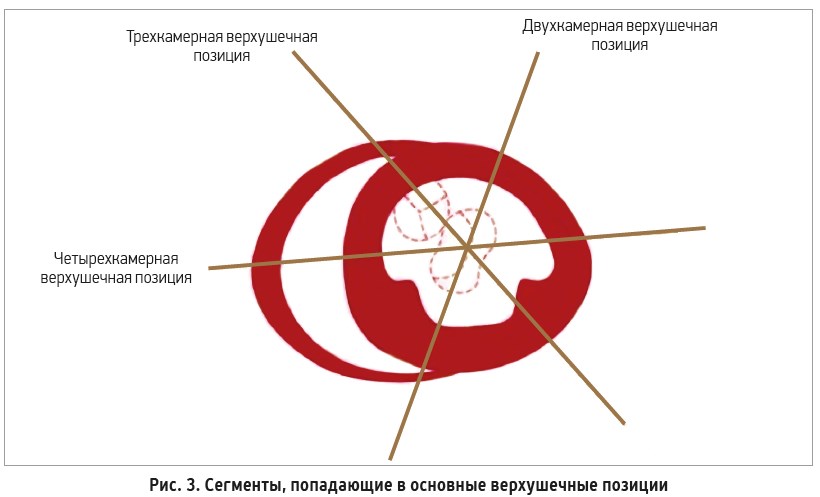
3. Положение «вне игры». При оценке ФВ ЛЖ по методу Simpson в двух позициях – четырех- и двухкамерной верхушечных – в измерение не включается трехкамерная верхушечная позиция (apical long-axis view); соответственно, антеросептальные и заднелатеральные сегменты ЛЖ не оцениваются при таком способе расчета ФВ (рис. 3).
Если у пациента имеют место нарушения локальной сократимости в вышеуказанных сегментах, измеренная ФВ ЛЖ будет выше реальной, а значит, не будет отражать истинную картину [5].
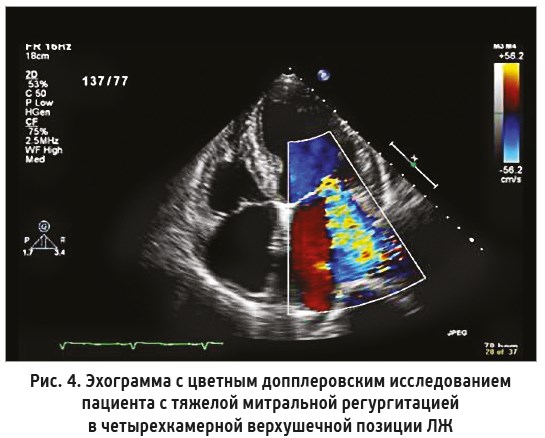
4. Изменение пред- и постнагрузки. Уменьшение постнагрузки отмечается при выраженной митральной недостаточности. Часть крови возвращается обратно в левое предсердие, часть – направляется в аорту. Сопротивление выбросу снижается, и значение ФВ ЛЖ оказывается значительно выше реального, при этом УО может быть снижен. Закрытие дефекта (устранение митральной недостаточности) обычно снижает абсолютное значение ФВ [8, 9].
На рисунке 4 митральная регургитация выглядит как сине-желтый поток (элайзинг-эффект) в полости левого предсердия.
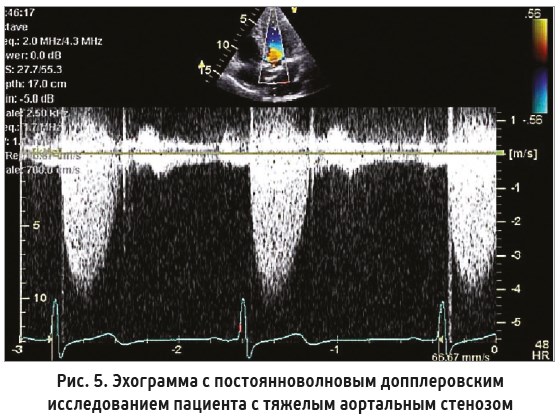
Повышение постнагрузки обычно фиксируется при аортальном стенозе, поскольку существует препятствие выбросу крови. В этой клинической ситуации после оперативного лечения по поводу аортального стеноза ФВ ЛЖ может увеличиваться. На рисунке 5 представлена эхограмма тяжелого аортального стеноза с систолическим градиентом давления 64 мм рт. ст.
5. Точность и воспроизводимость измерений. Точность измерений зависит от вида и производителя ультразвукового сканера, опыта оператора. Существуют достаточно большие внутри- и межлабораторные расхождения в оценке данного показателя не только при регистрации, но и при анализе записанных изображений. Ошибка измерения ФВ ЛЖ может достигать 10%, поэтому исследования в динамике рекомендуют проводить по возможности на одном приборе и одним оператором. Поскольку определение ФВ ЛЖ находится в пределах такой ошибки измерения, раннее снижение функции ЛЖ, вероятно, можно упустить [11].
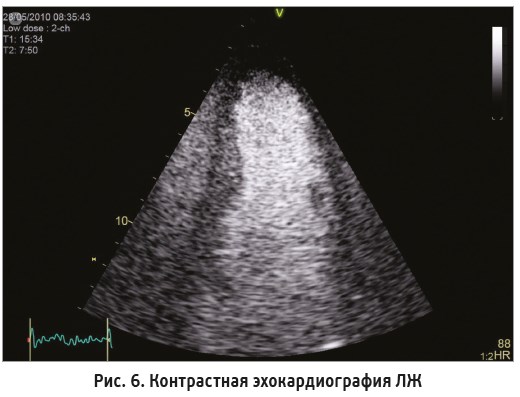
Точность исследования можно повысить путем контрастирования полости ЛЖ – с помощью так называемой контрастной эхокардиографии. На рисунке 6 представлена эхограмма ЛЖ при контрастном исследовании, полость ЛЖ заполнена белым (при ультразвуковом сканировании) контрастным веществом, при этом более четко контурируют стенки ЛЖ (черным цветом), в особенности эндокард.
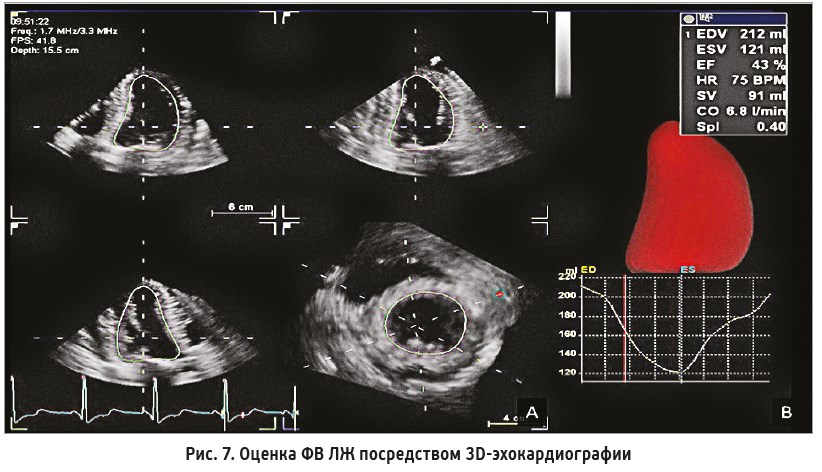
Качество и воспроизводимость исследования значительно повышает трехмерная (3D) эхокардиография, которая лишена недостатков двухмерного исследования и учитывает сегменты, визуализируемые в верхушечной трехкамерной позиции (рис. 7). Измерение ФВ ЛЖ путем трехмерной эхокардиографии является наиболее точным и перспективным методом при адекватном качестве визуализации, однако требует специальных программ постобработки и/или специального датчика [10].
6. Значительно сниженная ФВ ЛЖ. При дилатации полости и сниженной ФВ ЛЖ показатель УО может быть сохранен. Поэтому для оценки тяжести состояния пациентов с выраженной сердечной недостаточностью и сниженной ФВ рекомендуют ориентироваться на абсолютные размеры объемов и их динамику. По данным исследования [3], индексы КДО и КСО тяжелых больных дилатационной кардиомиопатией с низкой ФВ более чувствительны к выраженности сердечной недостаточности, чем показатель ФВ. Таким образом, целесообразно использовать конечные объемы в качестве показателей сердечной недостаточности. Адекватная количественная оценка тяжести сердечной недостаточности должна включать ЧСС (длительность сердечного цикла).
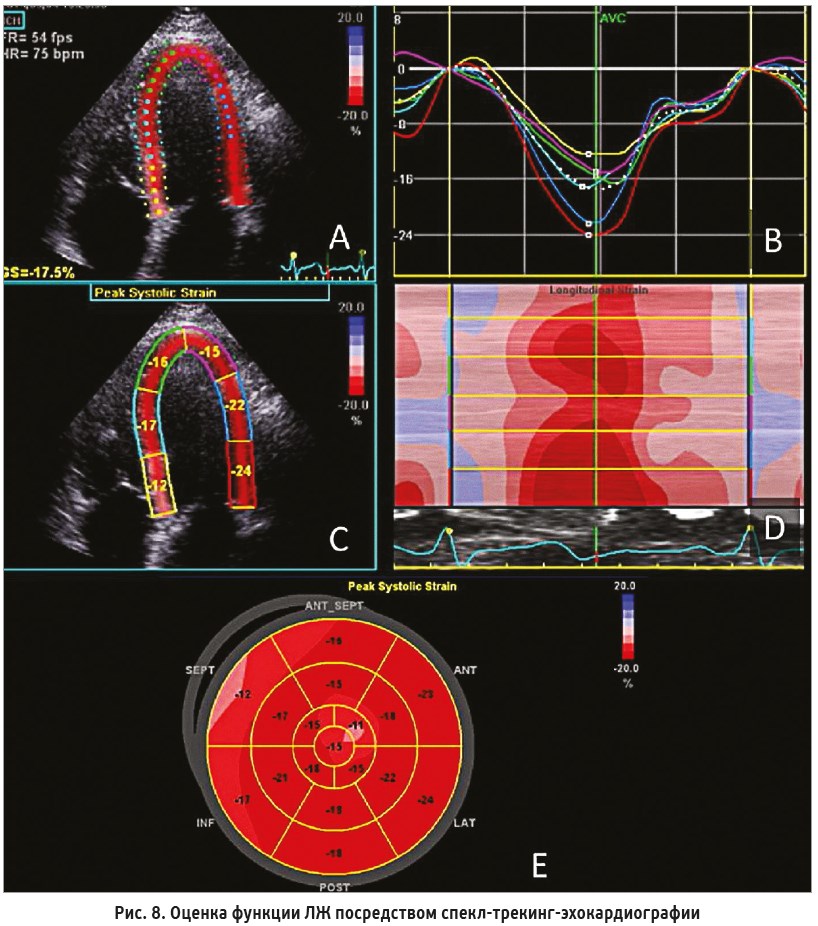
7. ФВ не учитывает продольную деформацию ЛЖ. Продольную деформацию ЛЖ оценивают с помощью спекл-трекинг-эхокардиографии (рис. 8). Принцип метода основан на отслеживании траекторий движения (tracking) в ходе сердечного цикла акустических маркеров миокарда (speckle) в серошкальном двухмерном ультразвуковом изображении с помощью специализированного программного обеспечения.
В результате компьютерной обработки траектории движения акустических пятен получают цифровые значения, графики и диаграммы деформации, а также значения ее скорости (глобальная деформация или глобальный продольный стрейн) и сегментов ЛЖ (региональная деформация или региональный стрейн) [1, 12, 15].
Деформация (S) – это величина, отражающая изменение длины мышечного волокна относительно исходного значения: S (%) = ∆L/L0, где L0 – исходная длина, ∆L – ее изменение. Деформация является положительной при удлинении либо утолщении волокна, отрицательной – при укорочении либо истончении.
Большинство экспертов придерживаются мнения, что продольное сокращение миокарда ЛЖ фактически отражает его насосную функцию по продольной оси, поэтому снижение данного показателя наступает значительно раньше, чем ФВ ЛЖ [11].
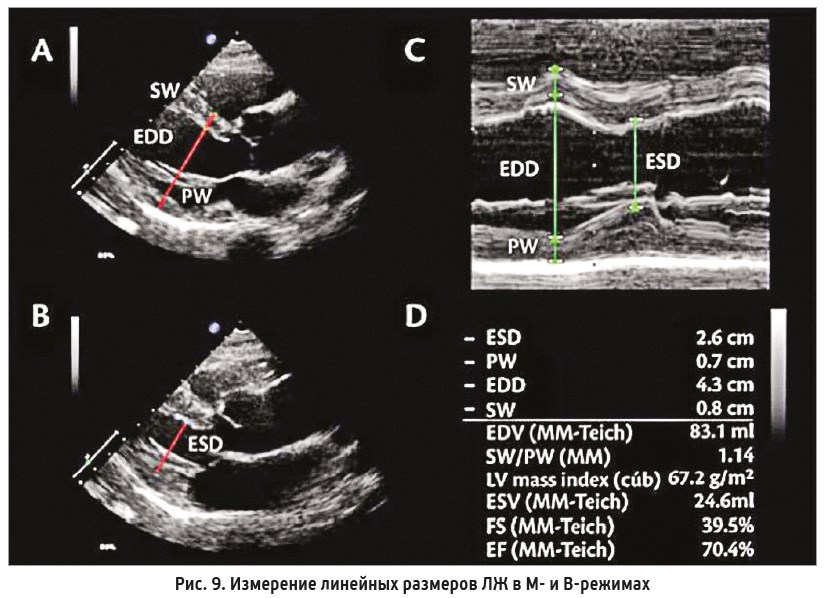
Существует еще один метод измерения ФВ ЛЖ – оценка по линейным размерам в М- или В‑режиме согласно формуле Teichholz (рис. 9). Рассчитывается следующим образом:
КДО = 7 × КДР 3 /2,4 + КДР
КСО = 7 × КСР 3 /2,4 + КСР
УО = КДО – КСО
ФВ = УО/КДО × 100%
Этот способ предполагает измерение внутренних размеров ЛЖ (конечно-диастолического и конечно-систолического) и толщины стенок на уровне кончиков створок митрального клапана. В то же время следует отметить, что оценка объемов и массы трехмерных структур по линейным или двухмерным измерениям несовершенна, так как основана на определенных геометрических моделях и допущениях, необходимых для преобразования линейных измерений в объемы [4].
Несмотря на то что расчет ФВ по формуле Teichholz часто используется в практике, оценка систолической функции ЛЖ с помощью линейных измерений некорректна при значительных нарушениях регионарной функции миокарда и не рекомендуется для применения в подобных случаях [5].
Исходя из приведенных данных, будущее оценки систолической функции ЛЖ состоит в совместном использовании и оценке ФВ и глобальной продольной деформации (глобального продольного стрейна).
Список литературы находится в редакции.
Медична газета «Здоров’я України 21 сторіччя» № 6 (475), березень 2020 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Під час XXII Національного конгресу кардіологів України, що відбувся 21-24 вересня, темою обговорення експертів стали практичні аспекти лікування артеріальної гіпертензії (АГ). Зокрема, значну зацікавленість аудиторії викликав тандемний виступ завідувачки відділу АГ та коморбідної патології ДУ «ННЦ «Інститут кардіології ім. М.Д. Стражеска» НАМН України» (м. Київ), доктора медичних наук Лариси Анатоліївни Міщенко та завідувачки відділення діагностики ДУ «Науково-практичний центр ендоваскулярної нейрорентгенохірургії НАМН України» (м. Київ), кандидата медичних наук Наталії Миколаївни Носенко, в якому було розглянуто особливості застосування сучасних антигіпертензивних препаратів з фіксованими комбінаціями (ФК) діючих речовин.
Коронарна хвороба, причиною якої є атеросклеротичне ураження вінцевих судин серця, – провідна кардіоваскулярна нозологія, що часто зумовлює клінічно значимі симптоми та стани (Meng et al., 2019). Фактори ризику розвитку коронарної хвороби розподіляються на модифіковані, тобто ті, на які можна впливати, та немодифіковані, що не піддаються корекції. До модифікованих факторів ризику належать психосоціальні чинники, надмірне вживання алкоголю, недостатня фізична активність, нездоровий спосіб життя, діабет, гіпертензія, надлишкова маса тіла й ожиріння, дисліпідемія, тоді як до немодифікованих – ускладнений сімейний анамнез щодо кардіоваскулярних захворювань, вік і стать.
Другого вересня за участі спеціалістів – сімейних лікарів та кардіологів – відбулося засідання Експертної ради, присвяченої оптимізації антикоагулянтної терапії в пацієнтів із неклапанною фібриляцією передсердь (ФП) і ролі сімейних лікарів у профілактиці інсульту в таких пацієнтів.
Артеріальна гіпертензія (АГ) – це рівень артеріального тиску (АТ), при якому переваги лікування за допомогою модифікації способу життя чи фармакотерапії однозначно переважають над ризиками. Доказова база свідчить, що таким рівнем АТ є ≥140/90 мм рт. ст. (ESC/ESH, 2018).





Warning: Use of undefined constant expert_review_likes - assumed 'expert_review_likes' (this will throw an Error in a future version of PHP) in /var/www/www-ars1963/data/www/ck62.ru/wp-content/themes/colormag/comments.php on line 93