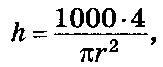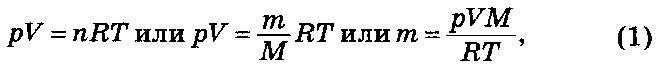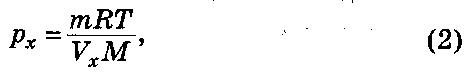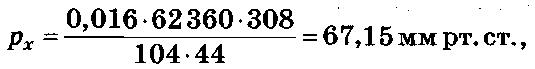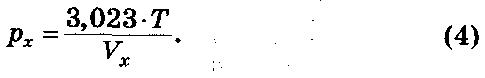Физиологические признаки
Смотреть что такое «Физиологические признаки» в других словарях:
ФИЗИОЛОГИЧЕСКИЕ ФОРМЫ РАСТЕНИЙ — новые формы растений, появляющиеся в результате изменения концентрации химических элементов в среде. У физиологических форм растений изменяются физиологические функции (фотосинтез, рост, развитие и др.), в то время как внешние морфологические… … Экологический словарь
Физиологические и биохимические свойства лучистых грибков — Лучистые грибки очень неразборчивы в выборе пищи. Они могут развиваться на скалах, где имеются только ничтожные количества питательных веществ, в грунтах, содержащих углеводороды, и в почвах, разлагая при этом гумусовые вещества,… … Биологическая энциклопедия
Признаки беременности — Раннее диагностирование беременности и определение её срока важно не только с точки зрения акушерства, но и из за того, что анатомические, физиологические и гормональные изменения[1], которые наступают после зачатия, могут оказывать существенное… … Википедия
Физиологические действия, состояния и процессы, их признаки — Имена существительные БЕСПА/МЯТСТВО, бесчу/вствие, забытьё, о/бморок. Внезапная потеря сознания, вызываемая болезненным состоянием или сильным душевным потрясением. ГО/ЛОД, аппети/т. Сильное желание есть, острое ощущение… … Словарь синонимов русского языка
Диагностические признаки скрываемой причастности человека к преступлению — Признаки изменения поведения виновных и невиновных лиц при контактах с сотрудниками ПОО образуют две основные группы: вербальные реакции и невербальные реакции. Вербальные (словесные) реакции лиц, дающих ложные объяснения, подразделяются на два… … Энциклопедия современной юридической психологии
Наркотические свойства трамадола — Содержание 1 Краткое описание медицинских свойств 2 Правовой статус … Википедия
Изменчивость — (биологическая) разнообразие признаков и свойств у особей и групп особей любой степени родства. И. присуща всем живым организмам, поэтому в природе отсутствуют особи, идентичные по всем признакам и свойствам. Термин «И.» употребляется… … Большая советская энциклопедия
наследственность — Категория. Эволюционный опыт предыдущих поколений живых организмов, запечатленный в генетическом аппарате. Специфика. Хранение, воспроизведение и передача наследственной информации происходит посредством дезоксирибонуклеиновой (ДНК) и… … Большая психологическая энциклопедия
Психофизиологическая проблема — вопрос об активном системном взаимодействии тела и психики. Исторически сложившийся научный спор о роли тела и психики в жизни человека, а также их взаимосвязи. Существуют различные взгляды на то, как соотносятся тело и психика, однако, данный… … Википедия
Пол — I совокупность генетически детерминированных признаков особи, определяющих ее роль в процессе размножения. Развитие признаков мужского (обозначают знакома Марса ♂ ) и женского (знак Венеры ♀ ) полов определяется хромосомными наборами (см.… … Медицинская энциклопедия
Физиологическая беременность
Беременность – физиологический процесс развития в женском организме оплодотворенной яйцеклетки, начинающийся с момента оплодотворения созревшей в яичнике яйцеклетки сперматозоидом. Оплодотворение обычно происходит в ампулярном, обращенном к яичнику, отделе маточной трубы.
Что необходимо знать о беременности
Благодаря ритмичным сокращениям трубы оплодотворенная яйцеклетка продвигается в полость матки. Во время этого продвижения яйцеклетка постепенно превращается в многоклеточный зародыш – плодное яйцо, густо покрытое нежными ворсинками – с их помощью оно прикрепляется к слизистой оболочке, выстилающей внутреннюю поверхность матки. С момента прикрепления начинается формирование сначала зародыша, а потом и плода, сопровождающееся перестройкой всех функций и систем организма женщины, которые по своей сути являются приспособительными реакциями, обеспечивающими благоприятные условия для развития плода.
На месте прикрепления зародыша ворсинки пышно разрастаются, и из них образуется так называемое детское место или плацента, соединенная с плодом пуповиной. Через плаценту от матери к плоду по кровеносным сосудам пуповины поступают питательные вещества и кислород, удаляются продукты обмена.
Физиологическая беременность продолжается в среднем 10 лунных месяцев (1 лунный месяц – 28 дней), т.е. 40 недель или 280 дней. Течение беременности принято разделять на триместры: первый начинается с оплодотворения и заканчивается в 12-13 недель, второй заканчивается в 28 недель, с этого же срока наступает третий триместр беременности, заканчивающийся родами.
Возможность беременности может и должна быть предположена у любой женщины детородного возраста, у которой не наступили месячные в срок или появилась аменорея (отсутствие менструации) в процессе регулярной половой жизни. Таким образом, первым признаком беременности обычно является отсутствие менструации в положенное время.
Спустя несколько дней после срока несостоявшейся менструации у большинства женщин появляется тошнота и даже рвота. Обычно рвота бывает один или два раза в день, утром, сразу после вставания с постели, но она не настолько сильна, чтобы вызвать заметное нарушение обмена веществ. Часто отмечается и учащение мочеиспусканий, которое, впрочем, может встречаться и у небеременных женщин в предменструальный период, однако у беременных оно более заметно.
Изменения молочных желез также отмечаются с самого начала беременности и особенно заметны у впервые беременных женщин. А примерно с 12-ой недели уже можно прощупать через переднюю брюшную стенку дно матки, которая на 20-ой неделе приближается к нижнему краю пупка, а на 36-ой – к мечевидному отростку грудины.
Повторнобеременные женщины раньше отмечают шевеления плода, чем впервые забеременевшие. Первые обычно замечают шевеления между 16 и 18 неделей, а вторые – между 19 и 21. Данные об этих ощущениях могут быть очень важны для определения срока беременности и предстоящих родов, поэтому женщина должна постараться запомнить дату появления первого шевеления плода.
Разумеется, существуют и более точные специальные методы диагностики беременности. Первоначально, особенно в сомнительных случаях, наступление беременности женщина может установить самостоятельно, воспользовавшись экспресс-анализом на беременность (тест-полоской, которую она может приобрести в аптеке).
В нашей Клинике мы можем провести и срочное исследование уровня хорионического гонадотропина, часто называемого «гормоном беременности». А современные диагностические ультразвуковые сканеры, такие, например, как используемый в Клинике «LeVita» «Sonix OP», позволяют установить беременность при уже при минимальном сроке в 2-3 недели. Точность диагностики возрастает при проведении трансвагинального сканирования – когда специальный датчик вводится в просвет влагалища и исследование проводится как бы изнутри (разумеется, при этом соблюдаются все санитарно-эпидемические требования).
Беременная женщина обязательно должна встать на учет в женской консультации и чем раньше, тем лучше: в начале беременности она еще точно помнит дни последней менструации, что важно для определения срока беременности, и точность её сведений можно уточнить простыми методами, например при гинекологическом осмотре.
Кроме того, именно в этот период врачу необходимо получить её исходные данные: об обычных для пациентки частоте пульса, величине артериального давления, уровне гемоглобина крови, массе тела – чтобы при их изменениях на более поздних сроках беременности быстро оценить сложившуюся ситуацию и, если нужно, без промедления принять необходимое решение. Тогда же врачу необходимо выявить и сопутствующие заболевания беременной, такие как гипертоническая болезнь или порок сердца, язвенная болезнь или сахарный диабет, которые могут оказать значительное влияние на течение беременности, состояние будущей матери и ее ребенка и соответствующим образом составить тактику ведения беременности.
Первичное медицинское обследование включает и определение таких важных параметров, как группа крови и резус-фактор, серологические тесты на сифилис, ВИЧ-инфекцию, гепатиты «В» и «С», а также показатели биохимического анализа кровы, данных коагулограммы (анализ на свертываемость) и т.д. Кроме того женщинам с определённой периодичностью проводится ультразвуковое исследование, допустимое при любом сроке: безвредность его подтверждена многочисленными исследованиями, проводящимися вот уже на протяжении более 50 лет во всем мире.
Если женщине больше тридцати пяти лет, то есть опасность возникновения у неё хромосомных аномалий, которые могут привести к развитию различных пороков развития плода (наиболее частая – болезнь Дауна). В этих случаях врач обычно рекомендует пройти специальное обследование – амниоцентез, при котором производится прокол стенки матки и плодного пузыря тонкой иглой, а полученная околоплодная жидкость направляется на анализ.
В целом беременность можно рассматривать как процесс продолжительного физического приспособления организма матери к удовлетворению потребностей растущего плода. Степень этого приспособления в целом превышает нужды плода, поэтому у женщины всегда имеются значительные резервы, позволяющие перенести периоды стресса или лишений без существенных изменений среды плода.
Каждая из систем организма женщины подвергается серьезным изменениям и испытаниям. Например, среднее артериальное давление, если не говорить о тенденции к небольшому падению в середине беременности, незначительно повышается, что облегчает перенос кислорода от матери к плоду. Говоря об изменениях со стороны сосудистой системы, заметим, что у беременных наблюдается расширение сосудов кожи, вследствие чего женщина меньше ощущает холод, но иногда может чувствовать себя хуже при жаркой погоде. По мере развития беременности движения диафрагмы значительно ограничиваются, и дыхание по своей природе становится частым и преимущественно грудным.
Прирост массы тела беременной отличается значительными индивидуальными колебаниями, но в среднем за время беременности женщина прибавляет в весе до 12 кг. Треть прироста, около 4 кг, набирается в первой половине беременности, а оставшиеся две трети – во второй. Более половины общего прироста массы тела обусловлено задержкой жидкости, которая распределяется между плазмой крови, плодом, плацентой, околоплодной жидкостью и остальными тканями. После резкого уменьшения массы тела в первые четыре дня после родов из-за отделения плода, плаценты, околоплодных вод и сокращения матки, а также учащенного диуреза, вес продолжает постепенно сокращаться на протяжении последующих 3 месяцев или около того.
Характерны и изменения молочных желёз – обычно женщины чувствуют их некоторое растяжение и болезненность. Вздутые устья желёзок ареолы вокруг соска могут выступать вверх, образуя так называемые бугорки Монтгомери. При достаточном освещении становится видимым набухание поверхностных вен, прежде всего идущих вокруг соска. Грудь теряет свою обычную мягкость и в ней можно прощупать тяжи набухших железистых протоков, идущих от периферии к соску наподобие спиц в колесе. После 14 недель появляются выделения из соска, прогрессирующие по мере развития беременности, причем молочные железы заметно увеличиваются в размере. После 16 недель становится заметной пигментация соска, особенно выраженная у смуглых женщин. У беременных усиливается и пигментация кожи, особенно выраженная на лице, вокруг сосков и белой линии живота. Это явление обусловлено увеличением количества циркулирующего меланоцитостимулирующего гормона. На животе и бедрах появляются продольные полоски — «стрии» длиной 5-8 см и около 0,5 см шириной. Вначале они розовые, но потом становятся более бледными и немного уплотненными. Новые родимые пятна появляются более чем у половины беременных женщин. Интенсивность работы сальных и потовых желез во время беременности также повышается.
Хотя справедливо считается, что беременность является физиологическим состоянием организма и многие женщины готовы к гармоничным отношениям с будущим ребенком, известно и то, что беременность – это периодом напряжения и нагрузки, и что лишь у немногих женщин она протекает без функциональных или органических нарушений разной степени выраженности.
Физиологические признаки что это
Физиологические (переходные) состояния новорожденных
Автор: врач-педиатр ДМЦ «Тигренок» Жарков П. А.
В вашей семье появился малыш и это действительно грандиозное событие в Вашей жизни. Все то время пока ваше чадо находилось у мамы в животе вы предвкушали его появление на свет, думали о том какого цвета у него будут глазки, волосики, как Ваша девочка или мальчик первый раз прижмется к Вам, обнимет своими ручками. Наверное, те чувства которые Вы испытываете сейчас можно назвать счастьем. И поэтому вы особенно внимательны к Вашему ребенку и волнуетесь как бы с ним не было чего-нибудь не так.
Во время внутриутробного развития малыш относительно ограничен от воздействий окружающего его маму мира. Ему тепло, постоянно поступают питательные вещества, откуда-то издали доносятся приглушенные звуки и т.п., однако с моментом рождения этот комфорт исчезает: до ребенка доносятся миллионы резких звуков, резкий свет, чьи то руки не дают спокойно полежать, кругом различные запахи, перепады температуры окружающей среды и постоянное тактильное раздражение, а малышу еще приходится самому дышать, сосать и как то приспосабливаться к новому и не очень приятному для него окружающему миру. В педиатрии есть такое понятие — физиологические то есть «правильные, не относящиеся к болезни» или переходные состояния новорожденного которые как раз и показывают как Ваш малыш адаптируется к своей новой жизни.
Что же мама может заметить?
1. Физиологическая желтуха новорожденных. Где-то на 2-3 день после рождения кожа, а иногда и слизистые (особенно глаз) Вашего малыша может приобретать желтоватый оттенок. Это состояние наблюдается приблизительно у 70% новорожденных и связано с тем что некоторые ферменты (важнейшие химические соединения приводящие к расщеплению тех или иных веществ) в организме ребенка пока не работают в полную силу и накапливается билирубин (специфический продукт обмена веществ) который и прокрашивает кожу и слизистые Вашей малютки. Стул и моча при этом сохраняют обычную окраску. Как правило желтуха угасает к 10-14 дню жизни и если самочувствие ребенка остается удовлетворительным, лечения не требуется. При заметном похудании, вялости, пассивности ребенка, а также если желтуха появилась в первые сутки жизни следует немедленно обратиться к педиатру, т.к. данное состояние не характерно для физиологической желтухи.
4. Затрудненное дыхание. В первые дни жизни маме может показаться что малыш «тяжело дышит». Периодически Ваш ребенок делает глубокий вдох и как будто «задерживает» дыхание, а потом делает медленный выдох. Дело в том что даже после рождения легкие функционируют неполностью и таким дыханием малыш подсознательно повышает давление в нижних дыхательных путях и «расправляет» легкие. Этот процесс, как правило, протекает не более 5 дней. Однако маме следует обратить внимание на то как ребенок дышит — если Вы слышите свист, хрипы или затруднение дыхания, а также если ребенок дышит слишком часто или слишком редко (в среднем новорожденный делает 30-50 дыхательных движений в минуту) или его дыхание «сбивается» и некоторое время малыш не дышит — необходимо немедленно обратиться к врачу.
5. Физиологическая потеря массы тела. В течение первых десяти дней жизни здоровый новорожденный может потерять до 10% от массы тела при рождении. Это связано, в первую очередь, с повышенным испарением жидкости при дыхании и недостаточным ее поступлением извне. Не забывайте что ранее начало грудного вскармливания способствует меньшим потерям массы.
В настоящей статье перечислены далеко не все переходные состояния новорожденных, однако наиболее наглядные и распространенные особенности представлены. Так или иначе, врачи медицинского центра «Тигренок» рекомендуют родителям обязательно обратиться к педиатру как можно скорее после выписки из родильного дома. Особенно это касается тех случаев когда имелась какая-либо патология во время беременности или родов или если у Вас есть какие-либо сомнения в здоровье Вашего малыша.
ГК «Униконс»
Продвижение и реализация комплексных пищевых добавок, антисептиков и др. продукции.
«Антисептики Септоцил»
Септоцил. Бытовая химия, антисептики.
«Петритест»
Микробиологические экспресс-тесты. Первые результаты уже через 4 часа.
«АльтерСтарт»
Закваски, стартовые культуры. Изготовление любых заквасок для любых целей.
ВНИМАНИЕ: Уважаемые клиенты и дистрибьюторы!
12. ФИЗИОЛОГИЧЕСКИЕ ПРИЗНАКИ
Совокупность характеристик, отражающих потребности дрожжевых организмов в определенных физико-химических условиях среды, относят к физиологическим признакам. Из этих признаков для целей идентификации используют следующие: способность к сбраживанию сахаров до углекислого газа и этанола в анаэробных условиях (брожение), усвоение безазотистых источников углерода путем их окисления в аэробных условиях (ассимиляция), потребление различных источников азота, рост на среде без витаминов, максимальные для роста температуры, способность расти при повышенном осмотическом давлении среды и пр. В технологическом смысле все перечисленные свойства имеют большее или меньшее значение.
Общими требованиями при проведении физиологических тестов являются использование при этом свежих (обычно 1–2-суточных) активно растущих культур дрожжей, высокоочищенных препаратов веществ, не содержащих примесей, которые могут обусловить ложные результаты, и культивирование организмов при оптимальных для их роста температурах.
12.1. ОПРЕДЕЛЕНИЕ ИНТЕНСИВНОСТИ БРОЖЕНИЯ И ДЫХАНИЯ
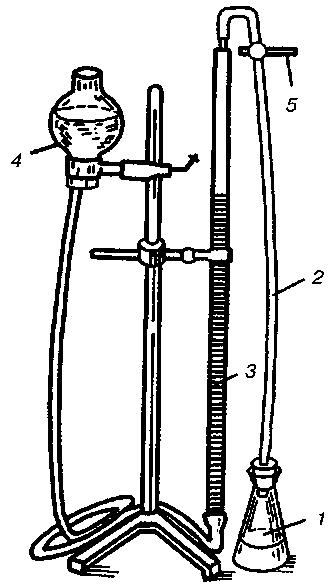
Уровни интенсивности дыхания (QO2) и интенсивности брожения (QCO2) измеряют у молодых клеток, исследуемых на одной стадии развития, культивируемых на одной и той же синтетической среде, содержащей глюкозу и полной с точки зрения содержания минеральных и азотсодержащих веществ, а также витаминов. Измерения производят на приборе для определения энергии дыхания и брожения микроорганизмов Одинцовой (рис. 28) или манометрическим способом на аппарате Варбурга (рис. 29) для газообмена.
Рис. 28
Прибор Одинцовой:
1 – бродильный сосуд; 2 – соединительная трубка; 3 – бюретка;
4 – уравнительный сосуд; 5 – трехходовой кран.
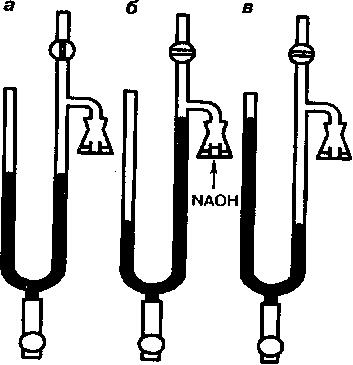
Рис. 29
Аппарат Варбурга:
а – исходное положение манометра; б – измерение интенсивности дыхания;
в – измерение интенсивности брожения.
В аппарате Варбурга и в приборе Одинцовой газометрическая часть состоит из тонких стеклянных трубок с делениями, снабженных пришлифованными кранами, позволяющими регистрировать выделяющийся углекислый газ (брожение) и поглощение кислорода (дыхание) дрожжами определенной массы в течение короткого времени.
Подготовка культуры. Чашки Петри с богатой питательной средой (сусло-агар с 0,3% дрожжевого автолизата) засевают экспериментальными расами.
Через 5–7 суток культивирования в термостате посев смывают с чашек стерильной водой, отфильтровывают и промывают также водой на воронке Бюхнера, затем отпрессовывают между листиками фильтровальной бумаги, и берут по весу для приготовления суспензии.
Для определения дыхания используют 0,5% отпрессованных дрожжей и однопроцентный раствор сахара (можно готовить из суспензии, приготовленной для определения брожения).
Длительность опытов – 2 ч при температуре 28°С.
Дрожжи по этим показателям различаются:
Для характеристики истинных бродильных свойств различных рас производственных дрожжей используют коэффициент – отношение интенсивности брожения к интенсивности дыхания (QCO2/QO2). Чем выше этот показатель, тем выше энергия брожения расы дрожжей в определенных условиях.
Работая на этих аппаратах, удобно вести исследования по влиянию условий культивирования дрожжей и воздействию факторов роста и активаторов брожения.
Процентное содержание дыхательного фермента клетки изменяется в зависимости от степени аэрации питательной среды. В противоположность этому интенсивность сбраживания является относительно постоянной в течение всего периода брожения и снижается только к его концу, когда число живых клеток уменьшается. Интенсивность сбраживания выражают в мм 3 газа на 1 мг дрожжей в час.
Лафон разделил дрожжи по этому признаку на шесть групп.
12.2. СБРАЖИВАНИЕ САХАРОВ
Для описания и идентификации микроорганизмов широко используют некоторые особенности их обмена веществ, выявляемые по способности изучаемого организма расти на принятых в настоящее время диагностических средах и вызывать те или иные превращения веществ, входящих в состав этих сред. Эмпирически давно отмечено, что немало характеристик дрожжей, в том числе и физиологических, взаимосвязаны. Подобные корреляции полезно помнить, так как они могут служить дополнительным контролем и предостеречь от грубых ошибок. Применительно к сбраживанию сахаров наиболее общими являются два правила:
Рис. 30
Накопление газа в поплавке:
1 – рост культуры сопровождается образованием газа;
2 – газ не образуется.
Наиболее простыми и общедоступными для установления способности дрожжей к сбраживанию сахаров являются методы:
Для получения концентрации 2% (раффинозы 4–6%) отдельные сахара растворяют в разведенном в соотношении 1:10 дрожжевом автолизате или в 0,5%-ном растворе дрожжевого экстракта. Использование в качестве растворителя дрожжевой воды не рекомендуется, поскольку она часто содержит значительные количества трегалозы, которая может сбраживаться дрожжами.
Чтобы обнаружить изменение рН, к среде добавляют индикатор – бромкрезоловый пурпурный – из расчета 2 см 3 1,6%-ного спиртового раствора на 1 л среды. При рН 6,8 индикатор имеет пурпурный, а при рН 5,2 – желтый цвет. Можно использовать в такой же концентрации бромтимоловый голубой, который при рН 6,0 желтого, а при рН 7,6 синего цвета.
С использованием трубок Дунбара. Растворы сахаров разливают по трубкам Дунбара и автоклавируют 15 мин при 112°С. При этом в слепом колене трубки нередко образуются пузырьки воздуха. Перед засевом, осторожно наклоняя трубку, их необходимо удалить. Посев производят культурами с сусло-агара или 0,1–0,2 см 3 суспензии клеток исследуемых дрожжей. Инкубация длится от 24 ч до 10 суток.
О способности к сбраживанию сахара свидетельствует образование газа в закрытом колене трубки.
С использованием поплавков. Приготовленные растворы сахаров разливают по пробиркам на 1/2 объема, в которые для определения газообразования опускают поплавки запаянным концом вверх (трубочки, диаметром 5–7 мм, длиной 35–45 мм, запаянные с одного конца). Горлышко пробирки закрывают большим пальцем и, осторожно переворачивая, заполняют поплавок жидкой средой. Пробирки закрывают ватно-марлевыми пробками и автоклавируют 20 мин при 0,1 МПа. После автоклавирования среда из поплавков вытесняется, но по мере охлаждения поплавки снова заполнятся.
Посев производят культурами с сусло-агара или 0,5–1,0 см 3 суспензии клеток исследуемых дрожжей.
При необходимости соблюдения анаэробных условий инкубирования, после посева поверхность среды заливают стерильным парафином, стерильным вазелиновым маслом или их стерильной смесью 1:1.
Инкубация длится от 24 ч до 10 суток.
О способности к сбраживанию данного углевода свидетельствует газообразование и вытеснение питательной среды из поплавка.
Посев в столбик полужидкого агара. В приготовленные растворы сахаров вносят 0,5% агара, 0,3% дрожжевого автолизата, кипятят до полного растворения, разливают в пробирки на 1/2 объема, автоклавируют 20 мин при 0,1 МПа. Из автоклава пробирки переносят в штатив и выдерживают вертикально до полного охлаждения.
Посев производят бактериологической иглой уколом до дна пробирки культурами с сусло-агара или суспензии клеток исследуемых дрожжей.
При необходимости соблюдения анаэробных условий инкубирования после посева поверхность среды заливают стерильным парафином, стерильным вазелиновым маслом или их стерильной смесью 1:1.
Инкубация длится от 24 ч до 10 суток.
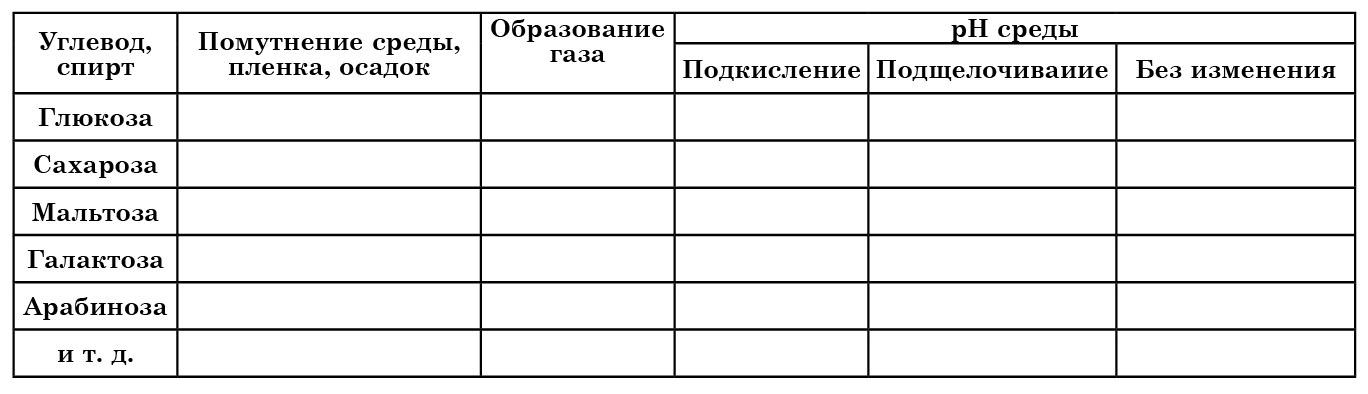
О способности к сбраживанию данного углевода свидетельствует газообразование и разрывы столбика полужидкого агара. Для учета полученных результатов можно использовать таблицу 13.
Показатели роста исследуемых культур дрожжей на средах с углеводами и спиртами
Микроорганизмы характеризуются неодинаковой способностью использовать различные углеводы и спирты в качестве единственных источников углерода и энергии. Перечень сахаров и других органических соединений, способность к сбраживанию (либо ассимиляции) которых определяют при идентификации дрожжей, включает:
Трисахариды
* Используются в тестах как на ассимиляцию, так и на брожение.
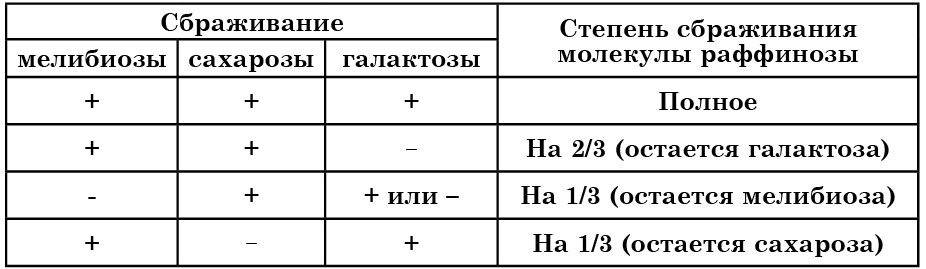
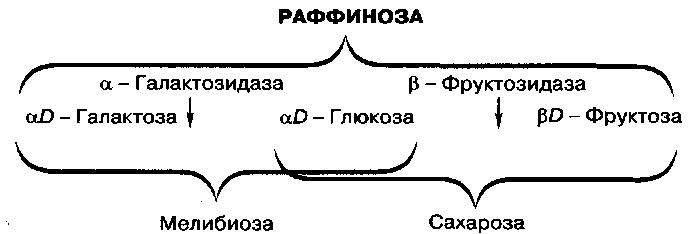
Возможные варианты сбраживания раффинозы дрожжами
Рис.31
Структура молекулы раффинозы
Из перечисленных углеводов специального рассмотрения требует раффиноза, поскольку этот трисахарид может по-разному сбраживаться дрожжами: полностью, на 2/3 или же на 1/3 молекулы, что учитывается при идентификации (табл. 14). О том, насколько полно и каким образом сбраживается раффиноза исследуемыми дрожжами, можно судить по способности к сбраживанию сахаров, входящих в состав молекулы раффинозы (рис. 31), или определением остаточных сахаров в среде.
12.3. ИЗБИРАТЕЛЬНОЕ СБРАЖИВАНИЕ ГЛЮКОЗЫ И ФРУКТОЗЫ
Известно, что в присутствии смеси глюкозы и фруктозы, такой как инвертный сахар, дрожжи сбраживают прежде всего глюкозу и после этого поглощают фруктозу. Но некоторые дрожжи ведут себя по-другому. При расчете процентного содержания сброженной глюкозы, когда 50% фруктозы уже сброжено, различают три категории дрожжей:
12.4. ЗИМАЗНАЯ, ИНВЕРТАЗНАЯ И МАЛЬТАЗНАЯ АКТИВНОСТЬ
Зимазная, инвертазная и мальтазная активность – основные с технологической точки зрения показатели ферментативной активности дрожжей.
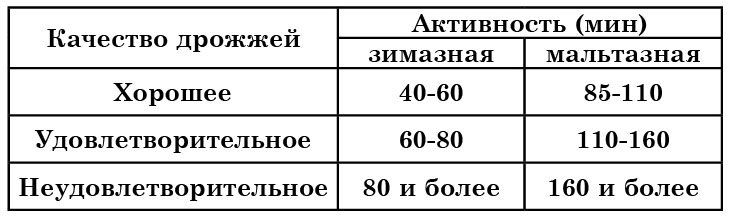
Например, для оценки качества хлебопекарных дрожжей приняты показатели ферментативной активности, представленные в таблице 15.
12.4.1. ГАЗОМЕТРИЧЕСКИЙ СПОСОБ
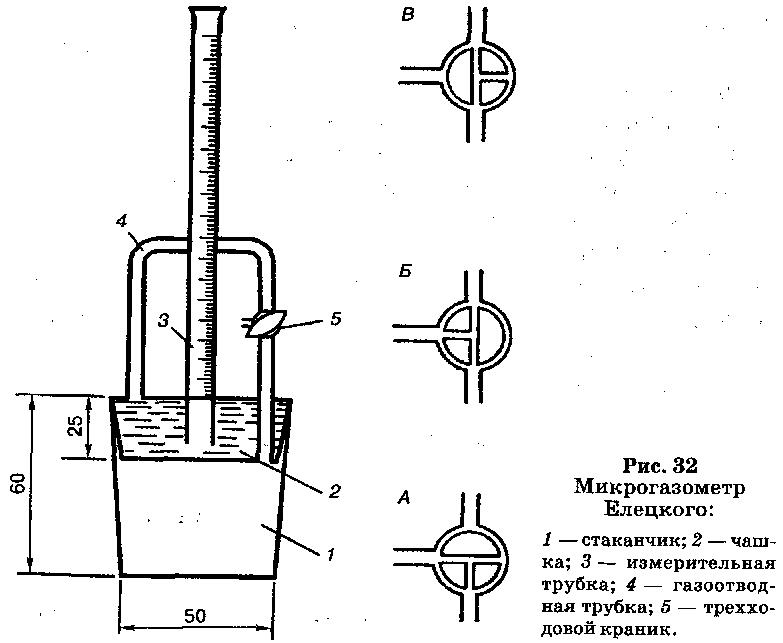
По скорости сбраживания дрожжами глюкозы, сахарозы и мальтозы определяют соответственно зимазную, инвертазную и мальтазную активность, выражаемую во времени, необходимом для выделения 10 см 3 СO2 из 5%-ного раствора сахара. Для определения пользуются микрогазометром системы Елецкого (см. рис. 32), изготовляемым на месте.
Прибор состоит из стаканчика 1 и манометрической крышки, соединяемых при помощи шлифованной поверхности. Диаметр стаканчика (внутренний) равен 50 мм, высота – 60 мм. Манометрическая крышка состоит из чашки 2 диаметром (внешний) 50 мм, высотой 25 мм и измерительной трубки 3 высотой 250 мм и внутренним диаметром 8–10 мм. В манометрической крышке имеется изогнутая газоотводная трубка 4 внутренним диаметром 3 мм с трехходовым краном 5, при помощи которого газоотводная труба соединяется как с внутренней камерой газомера – стаканчиком, так и с внешней средой.
Перед началом работы в манометрическую крышку заливают насыщенный раствор поваренной соли, подкрашенный метиленовым синим. Раствор наливают до основания измерительной трубки, и этот уровень принимают за ноль, все шлифы смазывают вазелином.
Подставив это значение в формулу, получим
0,5 г прессованных товарных дрожжей, или отпрессованных на воронке, или снятых с поверхности плотной агаризованной среды, помещают в стаканчик прибора, заливают 10 см 3 водопроводной воды температурой 35°С и размешивают. К полученной суспензии добавляют 10 см 3 10%-ного раствора сахара (глюкозы, сахарозы или мальтозы) и быстро закрывают стаканчик манометрической крышкой, предварительно переведя трехходовой кран 5 в положение А. Затем кран переводят в положение Б для выравнивания давления внутри прибора с атмосферным давлением. После этого кран переводят в положение В и прибор помещают в термостат при температуре 35°С, засекают время и наблюдают за прибором, пока не выделится 10 см 3 диоксида углерода и жидкость в измерительной трубке не поднимется на соответствующую высоту. Время, затраченное на выделение 10 см 3 газа, выраженное в минутах, называют зимазной, инвертазной или мальтазной активностью при использовании соответственно глюкозы, сахарозы или мальтозы.
После окончания анализа кран на газоотводной трубке переводят в положение Б, чтобы жидкость в трубке опустилась, и разъединяют манометрическую трубку и стаканчик. Из стаканчика выливают жидкость, ополаскивают его водой и вытирают досуха.
12.4.2. МАНОМЕТРИЧЕСКИЙ СПОСОБ***
Для определения ферментативной активности предлагается прибор (см. рис. 22), состоящий из колбы (100–120 см 3 ), газоотводной трубки с краном и чувствительного манометра (медицинский, для измерения артериального давления).
Перед началом работы измерить объем используемой колбы до нижнего края тщательно притертой резиновой пробки и объем проходящей через пробку газоотводной трубки. Для этого заполнить колбу и трубку водой, а затем измерить объем вместившейся жидкости мерным цилиндром. Полученную величину нанести на колбу и в дальнейшем использовать как «постоянную».
В колбу поместить 0,5 г прессованных дрожжей, залить 10 см 3 водопроводной воды температурой 35°С и размешать до однородной суспензии. Затем добавить 10 см 3 5%-ного раствора сахара (глюкозы, сахарозы или мальтозы) и закрыть колбу резиновой пробкой с газоотводной трубкой, соединенной с манометром. Для уравнивания давления в колбе с атмосферным давлением извлечь подвижную часть краника и сразу поместить его на место, тщательно притерев и совместив отверстия. Подготовленный таким образом прибор поместить в термостат при 35°С (308 К) и регистрировать время, за которое стрелка манометра достигнет необходимой отметки, соответствующей 10 см 3 выделенного углекислого газа.
Величину давления в определенном ранее объеме используемой колбы определить по уравнению Менделеева-Клапейрона:
где т – масса газа; М = 44 г; р = 700 мм рт. ст.; R = 62 360 мм рт. ст./моль К; V = 10 см 3 ;
Т = 308 К.
Таким образом, установлено, что в состоянии реального газа масса 10 см 3 диоксида углерода равна 0,016 г.
Для приведения давления газа в условия эксперимента формулу (1) преобразовали
где рх – показание манометра; m = 0,016 г; R = 62 360 мм. рт. ст./моль К; Т = 308 К;
Vх = 104 см 3 ; М = 44 г.
Значение Vх определяется вычитанием объема дрожжевой суспензии (20,5 см 3 ) из общего объема в системе (124,5 см 3 ). Тогда
где рх – давление, создаваемое газом массой 0,016 г и объемом 10 см 3 в используемом объеме Vх при температуре Т.
При условии, что в дальнейшей работе значения R, М и т будут использоваться как «постоянные», получится формула
На основании произведенных расчетов установлено, что, используя прибор с постоянным свободным объемом (в приведенном примере – 104 см 3 ), остается лишь регистрировать время, за которое стрелка манометра достигнет необходимой отметки (в приведенном примере – 67 мм рт. ст.).
Если за единицу измерения будет принят 1 Па, данная формула будет представлена как:
12.5. ПРОДУКТЫ БРОЖЕНИЯ
При брожении наряду с этиловым спиртом и углекислым газом образуется ряд побочных и вторичных продуктов. Эквивалентность между глицерином (Г) и суммой других вторичных продуктов: уксусной кислоты (У), янтарной кислоты (Я), 2,3-бутандиола (Б), ацетоина (А), остаточного свободного ацетальдегида (Э) – с коэффициентом при каждом из них, выведенным из химического уравнения, установлена аналитически.
Предложено уравнение, вытекающее из баланса спиртового брожения Нейберга:
5Я + 2У + Б + 2А + Э = Σ £ Г.
Это уравнение эквивалентности (Σ от 0,8 до 1,0) подтверждается для всех дрожжей, имеющих только бродильный тип обмена веществ. Для других групп дрожжей это отношение действительно только в условиях абсолютного анаэробиоза и не подходит для среды с доступом воздуха.
Для характеристики рас дрожжей, особенно промышленного назначения, необходимы сведения об образовании ими продуктов брожения, имеющих весьма важное значение в формировании конечного продукта.
12.6. ПОТРЕБНОСТЬ В ВИТАМИНАХ
Способность дрожжей синтезировать все необходимые для роста витамины или потребность в наличии каких-либо из них в среде используют при идентификации видов в качестве дополнительных характеристик. Нельзя недооценивать и технологическое значение этого фактора.
В некоторых случаях потребность в определенных витаминах присуща всем представителям рода. Например, все виды Hanseniaspora, Kloeckera нуждаются в инозите и пантотеновой кислоте. В других родах зависимость по каким-либо витаминам или способность расти на безвитаминной среде характерны для отдельных видов или даже разновидностей. Наиболее часто дрожжи нуждаются в обеспечении биотином и тиамином.
Постановка теста на способность к росту в среде без витаминов (см. табл. 6) и определение их значения как факторов роста осуществляются аналогично постановке тестов на способность к ассимиляции источников углерода. Поскольку дрожжи способны накапливать в клетках значительные количества витаминов, для приготовления инокулята в данном тесте используют культуры дрожжей, предварительно выращенные в безвитаминной среде.
Интенсивность брожения или накопления биомассы на жидких и плотных средах свидетельствует о значении данного витамина как фактора роста для исследуемой культуры дрожжей. Медленный и слабый рост на безвитаминной основе рассматривают как неспособность исследуемых организмов синтезировать все необходимые для роста витамины.
Для всех видов дрожжей, использующихся в промышленности, характерна специфическая потребность в том или ином факторе роста: мезоинозит, биотин, пиридоксин, тиамин, пантотеновая кислота, никотинамид, парааминобензойная кислота.
Для исследований используется безвитаминная среда.
Для анализа опытов используют нефелометрирование, или подсчет клеток в счетных камерах, а также взвешивание хорошо укупоренных пробирок.
В результате получают данные как по скорости роста и накопления биомассы, так и по скорости и пределу сбраживания сахара.
В результате построения витаминограмм можно отобрать тест-культуры для определения того или иного фактора роста – витамина.
12.7. РОСТ НА СРЕДАХ С ПОВЫШЕННЫМ ОСМОТИЧЕСКИМ ДАВЛЕНИЕМ
Под осмотической устойчивостью понимают приобретенную способность некоторых рас и культур дрожжей сохранять ферментативную активность в средах с относительно высоким осмотическим давлением. Это свойство следует отличать от осмофильности, которая является генетически закрепленным признаком отдельных родов и видов дрожжей, обитающих в специфических экологических условиях. *** При этом следует понимать, что дрожжи, устойчивые к высоким осмотическим давлениям, создаваемым в среде глюкозой, не всегда так же устойчивы к давлениям, создаваемым солями.
Определить способность культуры сохранять свою жизнедеятельность в средах с высоким осмотическим давлением важно не только для выделения и идентификации осмофильных дрожжей. Данный показатель имеет значение при выборе рас, используемых в производстве хлебопекарных дрожжей, как фактор, влияющий на стойкость готовой продукции и ее технологические особенности. Кроме того, в последние годы в селекции пивных и спиртовых рас все большее внимание уделяют осмотической устойчивости, исходя из технологических и экономических предпосылок.
12.7.1. ОТНОШЕНИЕ К КОНЦЕНТРАЦИИ ХЛОРИСТОГО НАТРИЯ
Устойчивость разных видов дрожжей к этому фактору заметно варьирует. Большую или меньшую чувствительность дрожжей к концентрации соли оценивают по их способности расти в среде, обеспечивающей хороший рост с 2,5 и 6,5% NaCl. Исследуют устойчивость чистой культуры дрожжей из лабораторной коллекции или выделенной из производственного либо природного субстрата.
Для этих целей можно использовать жидкие, полужидкие и плотные среды.
На жидких средах.
Дрожжевой автолизат. 0,5 см 3
Среду разливают в пробирки и стерилизуют при 0,1 МПа. Через 6–10 суток после посева по помутнению среды или образованию осадка регистрируют рост микроорганизмов и его интенсивность или отсутствие роста и делают заключение о чувствительности изучаемого микроорганизма к концентрации хлористого натрия.
Концентрация соли, при которой еще регистрируется рост исследуемой культуры дрожжей, принимается за показатель ее галотолерантности.
На жидких средах с использованием поплавков. *** Приготовленные солесодержащие среды разливают по пробиркам на 1/2–2/3 объема, в которые для определения газообразования опускают поплавки. Горлышко пробирки закрывают большим пальцем и, осторожно переворачивая, заполняют поплавок жидкой средой. Пробирки закрывают ватно-марлевыми пробками и автоклавируют 20 мин при 0,1 МПа. После автоклавирования среда из поплавков вытесняется, но по мере охлаждения поплавки вновь заполнятся.
Посев производят культурами с сусло-агара или 0,5–1,0 см 3 суспензии клеток исследуемых дрожжей.
При необходимости соблюдения анаэробных условий инкубирования после посева поверхность среды заливают стерильным парафином, стерильным вазелиновым маслом или их стерильной смесью 1:1.
Инкубация длится от 24 ч до 10 суток.
О способности исследуемой культуры дрожжей расти при данной концентрации соли свидетельствует газообразование и вытеснение питательной среды из поплавка.
Концентрация соли, при которой еще регистрируется рост исследуемой культуры дрожжей, принимается за показатель ее галотолерантности.
На полужидких средах. *** В жидкие фоновые среды (варианты 1 и 2) вносят 0,5% агара, кипятят до полного его растворения, разливают в пробирки на 1/2 объема, автоклавируют 20 мин при 0,1 МПа. Из автоклава пробирки переносят в штатив и выдерживают вертикально до полного охлаждения.
Посев производят бактериологической иглой уколом до дна пробирки культурами с сусло-агара или суспензии клеток исследуемых дрожжей.
При необходимости соблюдения анаэробных условий инкубирования после посева поверхность среды заливают стерильным парафином, стерильным вазелиновым маслом или их стерильной смесью 1:1.
Инкубация длится от 24 ч до 10 суток.
О способности исследуемой культуры дрожжей расти при данной концентрации соли свидетельствует газообразование и разрывы столбика полужидкого агара.
Концентрация соли, при которой еще регистрируется рост исследуемой культуры дрожжей, принимается за показатель ее галотолерантности.
На плотных средах. В жидкие фоновые среды (варианты 1 и 2) вносят 2,5% агара, кипятят до полного его растворения, переливают в коническую колбу на 1/2 объема, закрывают ватно-марлевой пробкой и автоклавируют 20 мин при 0,1 МПа. Сразу после автоклавирования разливают в заранее приготовленные стерильные высушенные чашки Петри. Когда агар полностью застынет, чашки необходимо подсушить.
Посев производят бактериологической петлей или шпателем Дригальского культурами с сусло-агара или суспензии клеток исследуемых дрожжей.
Объем инокулята должен предполагать обязательное получение изолированных колоний после инкубации, что позволит не только выявить наличие или отсутствие роста при определенной концентрации соли, но и определить возможное влияние на культуральные свойства, т. е. на состояние клеточной массы. ***
Инкубация длится от 24 ч до 10 суток.
При учете результатов регистрируют наличие или отсутствие роста дрожжей, его интенсивность и возможные отклонения в структуре колоний от таковых на контрольной среде.
Концентрация соли, при которой еще регистрируется рост исследуемой культуры дрожжей, принимается за показатель ее галотолерантности.
По разнице в подъемной силе. На технических весах берут две навески испытуемых дрожжей по 0,31 г каждая. К первой навеске добавляют 4,8 см 3 водопроводной воды, нагретой до 35°С, тщательно размешивают с помощью шпателя или пестика в фарфоровой чашке или в ступке, добавляют муку 85%-ного помола от 6,5 до 7,5 г (в зависимости от ее влажности) и быстро замешивают тесто, придавая ему форму шарика, не прилипающего к рукам.
Технологические параметры осмотической устойчивости хлебопекарных дрожжей
Шарик опускают в стакан или цилиндр с водой при температуре 32°С, засекают время и поддерживают эту температуру до всплывания шарика.
Ко второй навеске добавляют 4,8 см 3 3,35%-ного раствора поваренной соли, нагревают до 35°С и далее поступают так же, как с первой навеской.
Время, затраченное на всплывание шариков (мин), умножают на коэффициент 3,5 и получают величину подъемной силы, определяемую стандартным способом.
Шарик, замешенный на воде без соли, всплывает быстрее. Разница в подъемной силе дрожжей в зависимости от осмотического давления среды, выраженная в минутах, характеризует осмоустойчивость, которую рассматривают как косвенный показатель стойкости дрожжей.
Дрожжи с осмоустойчивостью в пределах 10–15 мин стойки при хранении и вполне пригодны для сушки.
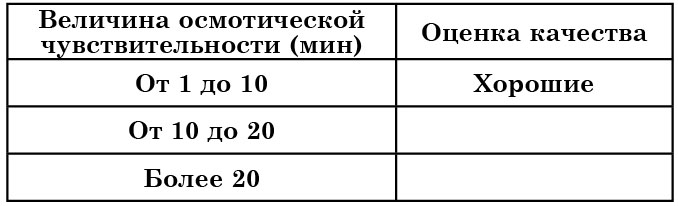
Для прессованных хлебопекарных дрожжей в зависимости от их осмотической устойчивости приняты показатели качества, указанные в таблице 16.
12.7.2. ОТНОШЕНИЕ К КОНЦЕНТРАЦИИ ГЛЮКОЗЫ
Стандартный метод. Готовят среду следующего состава.
Среду кипятят до полного растворения агара, автоклавируют 15 мин при 112°С и разливают по чашкам.
Посев на чашки производят бактериологической петлей или шпателем Дригальского культурами с сусло-агара или суспензии клеток исследуемых дрожжей.
Объем инокулята должен предполагать обязательное получение изолированных колоний после инкубации, что позволит не только выявить наличие или отсутствие роста при определенной концентрации глюкозы, но и определить возможное влияние на характер колоний, т. е. на состояние клеточной массы. ***
Инкубация длится от 24 ч до 10 суток.
Концентрация глюкозы, при которой еще регистрируется рост исследуемой культуры дрожжей, принимается за показатель ее осмотической устойчивости.
Основным недостатком метода можно считать обильное вытеснение сиропа на поверхность застывшего агара при высоких концентрациях сахара. Это исключает возможность получения изолированных колоний и их характеристики. ***
В полужидком глюкозно-дрожжевом агаре. *** Питательная среда включает следующие ингредиенты.
Дрожжевой автолизат. 0,5 см 3
Среду кипятят на медленном огне до полного растворения агара, разливают в пробирки высоким столбиком и стерилизуют при 0,1 МПа в течение 20 мин.
Полученный таким образом полужидкий агар застывает однородной массой, и независимо от концентрации глюкозы на поверхности среды нет капель вытесненного сиропа.
Посев исследуемой культуры производят бактериологической иглой глубоким уколом до дна пробирки.
При необходимости соблюдения анаэробных условий инкубирования после посева поверхность среды заливают стерильным парафином, стерильным вазелиновым маслом или их стерильной смесью 1:1.
Инокулированные среды инкубируют при 30°С в течение 7 дней.
Наличие роста регистрируют по образованию пузырьков газа и разрывам питательной среды по всей длине укола.
При учете результатов отмечают наибольшую концентрацию глюкозы, при которой еще регистрируется рост, и принимают ее за показатель осмотической устойчивости исследуемой культуры дрожжей.
12.8. ОТНОШЕНИЕ К ТЕМПЕРАТУРЕ
12.8.1. ОПРЕДЕЛЕНИЕ ОПТИМАЛЬНОЙ ТЕМПЕРАТУРЫ ДЛЯ РОСТА
В последние годы способность дрожжей к росту при определенных температурах все чаще вводят в ключи в качестве дифференцирующего признака. Подавляющее большинство дрожжей, имеющих технологическое значение, относится к мезофилам. Однако оптимальная температура для роста микроорганизмов этой группы имеет достаточно широкий диапазон. Поэтому необходимо определить температуру, обеспечивающую физиологически сбалансированный рост изучаемой культуры. Для этого штрихом бактериологической петлей или сплошным посевом шпателем Дригальского засевают в двух повторениях плотные питательные среды в чашках Петри или скошенные в пробирках. Посевы помещают в термостат с температурой 15, 20, 25, 30, 35, 40, 43, 45 и 48°С. Для низовых пивных дрожжей температурный интервал следует устанавливать в пределах технологических требований.
В зависимости от скорости роста через 3–5–7 суток отмечают интенсивность роста исследуемого организма визуально по 4-балльной шкале: «0» – отсутствие роста, «+» – слабый рост, «++» – хороший рост, «+++» – очень хороший рост.
После первого пассажа проводят второй пассаж, с той лишь разницей, что для каждой температуры посевным материалом служат клетки соответствующего предыдущего пассажа. Чашки вновь помещают в термостаты с различной температурой и через 3–5–7 суток отмечают рост и его интенсивность. Количество пассажей определяется исследователем, но, как правило, проводят три пассажа. Температура, при которой исследуемая культура дает одинаково интенсивный рост (без изменения культуральных признаков *** ) в как минимум трех пассажах считается оптимальной.
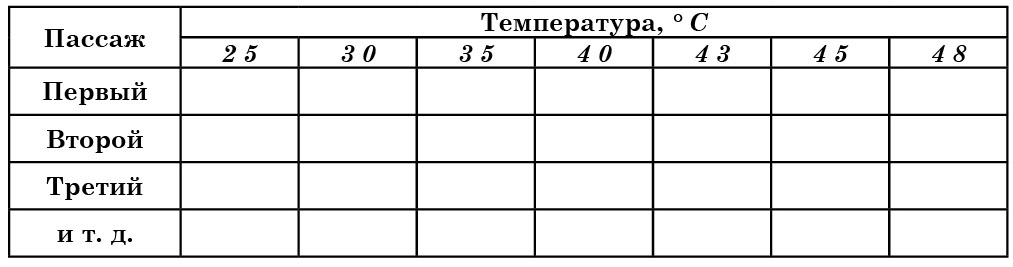
Интенсивность роста исследуемых дрожжей в зависимости от температуры
Для записи результатов наблюдений можно использовать таблицу 17.
На основании полученных результатов делают вывод об оптимальной температуре для роста изучаемой культуры.
При определении температуры, оптимальной для роста представителей психрофилов или термофилов, используют другие диапазоны температур: соответственно от –5 до 20° и от 50 до 80°С.
12.8.2. ХОЛОДО- И ТЕРМОУСТОЙЧИВОСТЬ ДРОЖЖЕЙ
Брожение сусла при температурах ниже 10°С и выше 30°С часто заканчивается недобродом, т. е. неполным сбраживанием сахаров сусла. Для сбраживания сусла при низких и высоких температурах целесообразно применять холодо- и термоустойчивые расы дрожжей.
Для отбора холодоустойчивых культур изучают бродильную способность (скорость и полноту сбраживания 18–20% сахаров в сусле) при температуре 7–10°С и отбирают те расы, которые начинают размножаться и сбраживают сусло быстрее и полнее других. При температуре 30–35°С этими дрожжами сбраживается лишь около 50% сахаров.
Для отбора термоустойчивых культур изучают бродильную способность при температуре 30–35°С и отбирают те расы дрожжей, которые начинают размножаться и сбра–живать сусло быстрее и полнее других при этой температуре.
Методика постановки опытов и контроль за ходом брожения описаны в п. 13.2.
Для получения более объективной информации следует использовать микроскопические методы оценки качественных и количественных параметров состояния исследуемых культур дрожжей. ***
Кроме того, важным показателем физиологического состояния исследуемой культуры и возможности ее технологического использования могут служить образующиеся в данных температурных условиях продукты брожения и степень отличия их количества от таковых при оптимальном температурном режиме. Для этого можно использовать формулу
5Я + 2У + Б + 2А + Э = Σ £ Г,
Целесообразно при отборе новых холодо- и термовыносливых рас дрожжей в качестве контроля брать музейные расы, обладающие этими свойствами.
12.9. СПИРТООБРАЗУЮЩАЯ СПОСОБНОСТЬ. КРИВЫЕ БРОЖЕНИЯ
Спиртообразующую способность оценивают по максимальному количеству спирта, которое могут образовать расы при сбраживании высокосахаристого сусла.
По окончании брожения определяют содержание спирта пикнометрическим методом, флотационным методом или окислением спирта бихроматом.
12.10. СПИРТОУСТОЙЧИВОСТЬ
Известно, что этиловый спирт действует токсично на все дрожжевые расы, но его ингибирующая концентрация варьирует в широком диапазоне. Присутствие в сусле незначительных количеств спирта оказывает слабое стимулирующее действие на размножение клеток. Но с увеличением концентрации спирта до 1,5–2,0% размножение клеток тормозится, а при 5,0% прекращается полностью. Токсические свойства этого соединения есть результат нарушения пористости и проницаемости клеточной мембраны, что, естественно, приводит к проблемам транспорта питательных веществ и дефициту доступной цитоплазме воды.
Сложность механизмов устойчивости дрожжевых клеток к этиловому спирту подтверждается и тем фактом, что выявлено более 250 генов, участвующих в этом процессе.
12.10.1. СТАНДАРТНЫЙ МЕТОД
В большинстве случаев расы, обладающие высокой спиртообразующей способностью, являются и спиртоустойчивыми. Под спиртоустойчивостью следует понимать способность рас проявлять жизнедеятельность при высоких концентрациях спирта в среде.
Для определения спиртоустойчивости рас дрожжей готовят разводки исследуемых рас на стерильной среде, содержащей 10–11% спирта и 2% глюкозы при температуре 25°С. Через 5 суток разводку каждой расы дрожжей вносят в количестве 1% в пропастеризованную или автоклавированную среду, содержащую 15% спирта и 2% глюкозы. Посев выдерживают при температуре 25°С и отмечают, на какие сутки в среде дрожжи размножились и начали бродить. О положительном результате свидетельствуют помутнение среды и газообразование.
Наиболее спиртоустойчивыми являются расы дрожжей, ранее других размножившиеся и забродившие в среде с 15% спирта, наименее спиртоустойчивые расы в такой среде не размножаются и не бродят.
Опыты удобно ставить в пенициллиновых флаконах, закрытых резиновыми пробками.
12.10.2. МЕТОД СЕРИЙНЫХ РАЗВЕДЕНИЙ ***
Инкубирование чистой культуры исследуемой расы дрожжей проводится в приборе, представляющем собой стеклянную бутылку с герметично закрывающейся трехходовой крышкой, исключающей испарение спирта при брожении. В сосуд наливается жидкая питательная среда и помещается стеклянный поплавок для последующей регистрации газообразования. Поплавок заполняется жидкой средой, прибор закрывается пробкой через марлевую салфетку и автоклавируется при 0,1 МПа в течение 20 мин.
В качестве субстрата используется глюкозно-дрожжевая среда, содержащая 5% глюкозы и 0,3% дрожжевого автолизата.
Далее в остывшую до комнатной температуры среду внести суточную сусло-культуру исследуемых дрожжей и этиловый спирт. Количество спирта должно соответствовать серии разведений от 10,0 до 14,0% и более (при необходимости) с шагом 0,5%. В контрольную пробу спирт не вносить.
Жидкая питательная среда, дрожжевая взвесь и этиловый спирт дозируются точно в соответствии с произведенными расчетами заданной концентрации спирта.
После составления питательной среды бутылки плотно закрыть и для исключения ошибки дополнительно покрыть резиновыми колпачками.
Инокулированные дрожжевой взвесью спиртосодержащие среды поместить в термостат при 30°С и инкубировать в течение 72 ч, регистрируя результаты каждые 24 ч.
Результаты брожения учитывать по четырехкрестной системе, регистрируя объем жидкости, вытесненной из поплавка углекислым газом.
Показателем спиртоустойчивости считать наибольшую концентрацию спирта, при которой еще регистрируются признаки брожения.
Для подтверждения результатов бродильной пробы по истечении 72 ч инкубации производятся посевы на сусло-агар из образцов с минимальным отрицательным результатом и выше.
Высокие концентрации этилового спирта в среде могут оказывать на дрожжевую клетку микостатическое действие, приводящее к остановке метаболических реакций брожения, но не к гибели клетки. Микоцидные концентрации этилового спирта превышают концентрации микостатические.
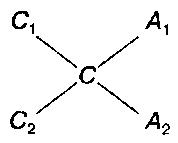
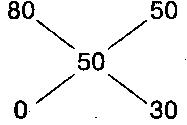
Правило креста. Правило смешивания растворов для получения заданной концентрации. Для получения раствора заданной концентрации из двух растворов пользуются следующей схемой:
где С – необходимая концентрация смеси, С1 – концентрация раствора и A1 – весовые количества раствора более высокой концентрации, С2 – концентрация раствора и A2 – весовое количество раствора более низкой концентрации.
П р и м е р. Из спирта крепостью 80% необходимо получить 50%-ный спирт. Как видно из схемы, для этого к 50 весовым частям 80%-ного спирта прибавляют 30 весовых частей воды.
12.11. КИСЛОТОУСТОЙЧИВОСТЬ
В годы, неблагоприятные для вызревания винограда, отдельные его партии могут поступать на переработку при величине рН сусла 2,5–2,9. Имеются наблюдения, что не все расы дрожжей могут полностью сбродить сахар в сусле с такой низкой кислотностью. Чтобы получить полностью выброженные высококислотные виноматериалы, рекомендуется применять кислотоустойчивые расы дрожжей.
Кроме того, одним из технологических приемов, предупреждающих инфицирование субстрата посторонней микрофлорой, является подкисление среды органическими или неорганическими кислотами. Важным при этом является использование рас, сохраняющих свои технологические свойства в кислой среде.
Нижняя граница рН устанавливается в соответствии с отраслевыми и технологическими особенностями.
Для отбора кислотоустойчивых культур для виноделия необходимо определять их бродильную способность в сусле с величиной рН 2,6 и содержанием сахаров 18% при температуре 25–27°С. При отсутствии в лаборатории сусла с такими кондициями его можно получить подкислением 10%-ным раствором винной кислоты и разбавлением водой обычного сусла с более высокой концентрацией сахаров и меньшей кислотностью.
Отбирают те расы дрожжей, которые начинают размножаться и сбраживают сусло быстрее и полнее других. В конце брожения необходимо определить остаточные сахара, чтобы убедиться в полном выбраживании их в сусле с рН 2,6 отобранной культурой.
Методика постановки опытов и контроль за ходом брожения описаны в п. 13.2.
Изменив сбраживаемый субстрат, температурный режим инкубации и величину рН, описанный метод можно применить для исследования кислотоустойчивости дрожжей, используемых в других отраслях промышленности.
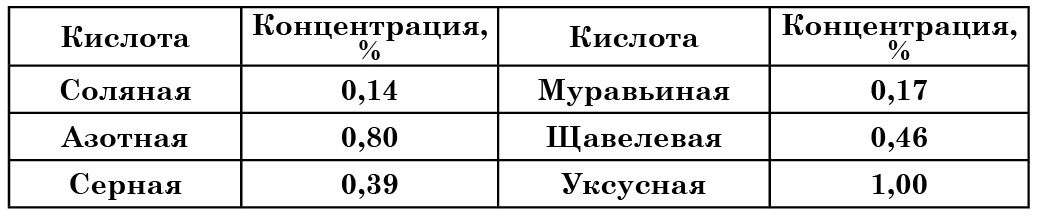
Предельно допустимые концентрации кислот для пивных дрожжей
Установлено, например, что через 24 ч пивные дрожжи погибают при концентрациях кислот, указанных в таблице 18.
12.12. ФЛОКУЛЯЦИЯ
Большое значение имеет способность дрожжей к оседанию, во многом определяемая их флокуляционной способностью. От этого свойства дрожжей зависят степень сбраживания, осветление продукта, редукция диацетила и т. д.
Способность дрожжей к флокуляции определяют по скорости оседания и величине осадка за определенный период.
12.12.1. ОПРЕДЕЛЕНИЕ ФЛОКУЛЯЦИОННОЙ СПОСОБНОСТИ
Метод позволяет выявить различия между хлопьевидными и пылевидными дрожжами.
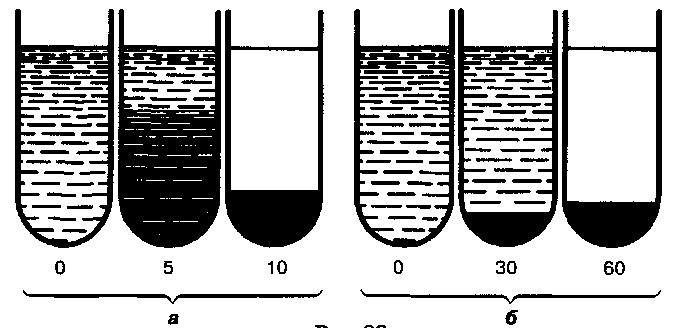
Суспензия хлопьевидных дрожжей быстро разделяется на два слоя и уже через 10 мин образуется осадок, который постепенно уменьшается благодаря уплотнению. У пылевидных дрожжей осадок образуется лишь через 30 мин и со временем увеличивается за счет дополнительного оседания взвешенных клеток (рис. 33).
Метод Иошида. Дрожжи из расчета 2–3 млн клеток в 1 см 3 вносят в 250 см 3 пивного сусла с концентрацией сухих веществ 8% и культивируют 2 суток при 25°С.
Рис. 33
Характер образования осадка у дрожжей:
а – хлопьевидных; б – пылевидных.
Сбраживаемое сусло тщательно перемешивают и по 10 см 3 вносят в бутылки диаметром 6 см, содержащие по 190 см 3 стерильного охмеленного сусла. Культивирование проводят при 11°С. Каждые сутки в бутылках измеряют оптическую плотность сбраживаемой жидкости на глубине 3 см от поверхности при λ = 630 нм и видимый или действительный экстракт.
Строят график: по оси ординат откладывают оптическую плотность, а по оси абсцисс – видимый или действительный экстракт. Полученная кривая характеризует флокуляционную способность дрожжей.
С точки зрения технологии следует обратить внимание на следующие параметры, характеризующие специфику процесса флокуляции:
По способности флокулировать пивные дрожжи сгруппированы в четыре класса:
Для производства пива низового брожения или лагерного пива используют штаммы дрожжей, относящиеся к 1-му и 2-му классу флокулирующих дрожжей. Способность дрожжей к флокуляции определяют любым из вышеперечисленных методов. Согласно методу Хельма, хорошо флокулирующие дрожжи полностью оседают в растворе ацетатного буфера через 10 мин, в то время как пылевидные дрожжи – через 60 мин. При использовании метода, предложенного чешскими специалистами, дрожжи, имеющие высокую флокуляционную способность, образуют осадок высотой 25–36 мм в стандартном объеме физиологического раствора в течение 12 мин.
12.13. ОБРАЗОВАНИЕ МИЦЕЛИЯ
Образование мицелия и псевдомицелия изучают на кукурузном или картофельно-глюкозном агаре методом пластинок, или культур на стекле (slide-culture).
Картофельно-глюкозный агар. 100 г промытого, очищенного и измельченного картофеля вымывают в 300 см 3 водопроводной воды в течение нескольких часов на холоде. Массу фильтруют через ткань и автоклавируют в течение 1 ч при 121°С. Для приготовления агаровой среды к 230 см 3 этой жидкости добавляют 770 см 3 водопроводной воды, 20 г глюкозы и 20 г агара и стерилизуют в автоклаве 15 мин при 112°С.
Приготовление препаратов. Расплавленную среду наливают в чашки Петри и в нее, зажав пинцетом, опускают и быстро вынимают стерильные предметные стекла. Покрытые пленкой агара стекла помещают на U-образную стеклянную подставку в другой чашке Петри и оставляют до полного застывания среды.
Посевы делают тонкими штрихами – по три на каждой пластинке параллельно короткой стороне стекла или по одному вдоль длинной стороны стекла. Стерильные покровные стекла накладывают на штрихи так, чтобы под ними не было пузырьков воздуха и чтобы часть штриха осталась непокрытой. На дно чашки наливают стерильную воду во избежание пересыхания слоя агара на пластинке.
Через 6–8 дней инкубации при 25°С стекла вынимают и, предварительно очистив их нижнюю поверхность от агара, помещают на столик микроскопа для наблюдений. На таких препаратах не нарушается естественное расположение клеток псевдомицелия, бластоспор или артроспор.
Образование мицелия и псевдомицелия наблюдают в анаэробных (под покровным стеклом) и в аэробных (вне стекла) условиях.
Так как на практике зачастую бывает трудно отличить ложный мицелий от истинного, особенно в культурах, где есть и почкование, и деление, то следует обращать внимание на следующее (рис. 34):
Рис. 34
Различия между истинным (а) и ложным (б) мицелием
12.14. ОПРЕДЕЛЕНИЕ ФЕНОТИПОВ: КИЛЛЕР, НЕЙТРАЛЬНЫЙ, ЧУВСТВИТЕЛЬНЫЙ
При описании различий между расами дрожжей сообщается о том, что все дрожжи Saccharomyces принадлежат к одному из трех фенотипов: киллер (К), нейтральный (N) или чувствительный (S).
Применение рас дрожжей определенных фенотипов (К, N или S) позволяет проконтролировать, в какой степени чистая культура, внесенная в нестерильное сусло, способна овладеть средой. Для этого необходимо определить процентное содержание дрожжей фенотипов K, N, S в спонтанно сбраживаемом сусле (контроль) и в отстоянном сусле, забродившем при внесении в него разводки чистой культуры дрожжей определенного фенотипа.
Техника определения фенотипов K, N, S состоит в следующем.
В чашки Петри разливают агаризованное (1,5%) виноградное сусло за 2–3 суток до использования, чтобы оно слегка подсохло и затем хорошо впитывало нанесенные на него дрожжевые суспензии.
Высушивать лучше в стерильном боксе под УФ-лампой в течение 3–5 ч, поставив перевернутое дно чашки на ребро ее крышки. ***
При работе на виноградном сусле для предотвращения гидролиза агара его 3%-ный водный раствор стерилизуют отдельно от сусла и смешивают при температуре 60–70°С в равных количествах.
Для лучшей контрастности зон подавления роста чувствительных культур в расплавленную среду можно добавлять перед розливом в чашки Петри стерильный 0,5%-ный водный раствор метиленового синего в количестве 1 см 3 на 200 см 3 среды.
Отдельную колонию штамма дрожжей, фенотип которого необходимо определить, изолируют иглой с плотной питательной среды и примерно в равном соотношении переносят на внутреннюю стенку пробирки с 0,5 см 3 стерильной водопроводной воды и уколом на чашку Петри с газоном культуры фенотипа S.
На одну чашку можно нанести в определенной последовательности до 30 уколов исследуемых штаммов.
Стерильно готовят водные суспензии тех же колоний в пробирках с 0,5 см 3 водопроводной воды и на других чашках Петри с сусло-агаром (без газона штамма фенотипа S). Делают петлей газоны исследуемых штаммов дрожжей диаметром около 1,5 см. На них в центр наносят уколом штамм фенотипа К, предварительно выращенный на сусло-агаре. На одну чашку можно нанести газоны десяти исследуемых штаммов в той же последовательности, что и на газоне штамма фенотипа S. Через 2 суток инкубации чашек Петри с посевами при температуре 25– 28°С определяют фенотипы штаммов.
Если вокруг колоний образовались зоны на газоне чувствительного штамма, то штаммы идентифицируются как киллеры. Штаммы, на газонах которых киллер образует зоны, являются чувствительными, остальные – нейтральными.
В качестве тестеров (индикаторных культур) можно использовать киллер и чувствительные расы коллекционных культур S. vini.