РОСПОТРЕБНАДЗОР по РТ
РОСПОТРЕБНАДЗОР по РТ
Что такое растительные стерины и есть ли в них польза?
Что такое растительные стерины и есть ли в них польза?
Растительные стерины – это незначительные по содержанию, но очень важные элементы клеточной оболочки растений, которые помогают снизить концентрацию холестерина в крови, предотвратить сердечные заболевания. В связи с этим производители стали добавлять растительные стерины в продукты питания. Однако, зачастую можно столкнуться с недобросовестными производителями, которые используют растительные жиры (стерины) вместо животных. Например, под видом масла и сыра в обороте находятся спреды и сырные продукты, что вводит потребителей в заблуждение.
Кроме того, молочные и кисло-молочные продукты включают в себя более 200 полезных для человека органических веществ, макро – и микроэлементов, в том числе белки, витамины, высокая биологическая ценность молочной продукции делает ее совершенно незаменимой в питании детей, пожилых и больных людей. Молочный жир содержит биологически активные жирные кислоты и является хорошим источником витаминов А и Д. Нехватка витамина Д приводит к различным заболеваниям, среди которых остеопороз у взрослых и рахит у детей. Витамин А необходим для обеспечения обменных процессов в органах зрения, он входит в состав зрительных пигментов и отвечает за сумеречное зрение.
© Управление Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека по Республике Татарстан (Татарстан), 2006-2017 г.
Эл. почта: org@16.rospotrebnadzor.ru (эл.адрес НЕ используется для
приема обращений, подача обращений в разделе «ПРИЕМ ОБРАЩЕНИЙ ГРАЖДАН»)
Информацию о зарегистрированных документах можно получить с 15:00 до 17:00 (в пятницу до 16:45; суббота, воскресенье – выходные дни)
по телефону: (843) 238 53 35
Дигидрокверцетин (Dihydroquercetin)
Владелец регистрационного удостоверения:
Лекарственная форма
Форма выпуска, упаковка и состав продукта Дигидрокверцетин
| Таблетки массой 0.25 г. | 1 таб. |
| Биологически активные компоненты, не менее: | |
| дигидрокверцетин | 25 мг |
Действие конкретного продукта определяется биологическими свойствами активных веществ, входящих в его состав.
В состав используемой биологически активной добавки к пище могут быть включены не все перечисленные ниже активные вещества.
Флавоноиды широко распространены в растительном мире. Они обладают выраженными антиоксидантными свойствами, различным флавоноидам присущи антиаллергенные, противовоспалительные, антивирусные, антибактериальные свойства и другие типы биологической активности. В растениях флавоноиды встречаются в виде флавоногликозидов и в свободном виде.
К основным классам флавоноидов относятся флаваноны (гесперидин, нарингин), дигидрохалконы, халконы, флаваны (катехин, антоцианидины), флаванонолы (дигидрофлавонолы), флавонолы (кверцетин, дигидрокверцетин, рутин), флавоны (апигенин, лютеолин), и изофлавоноиды.
Катехины – соединения растительного происхождения. Широко распространены в природе катехин и его диастереомер – эпикатехин. Обладают высокой биологической активностью: регулируют проницаемость капилляров. Катехины содержатся во многих растениях и продуктах растительного происхождения, являются сильными антиоксидантами. Обладают целым рядом полезных свойств, в т.ч. способствуют укреплению стенки капилляров, более эффективному использованию организмом аскорбиновой кислоты; задерживают развитие дегенеративных заболеваний костной ткани; способствуют улучшению состояния кожи; проявляют антибактериальные и противовоспалительные свойства; могут подавлять Helicobacter pylori, не затрагивая при этом полезные микроорганизмы кишечной биоты.
Антиоксидантные свойства катехинов в несколько раз сильнее, чем у витаминов С и Е.
Танины (дубильные кислоты) – органические вещества природного происхождения. Больше всего танинов содержится в коре дуба. Придают терпкий вкус фруктам, винам, содержатся в чае. Отличие дубильных веществ от других полифенольных соединений — это способность образовывать прочные водородные связи с белками.Обладают вяжущими, антибактериальными, кровоостанавливающими и противовоспалительными свойствами.
Антоцианидины – в растениях присутствуют в виде гликозидов (антоцианов). Придают растительным тканям разнообразную окраску – от розовой до черно-фиолетовой.
Витамин С (аскорбиновая кислота) обеспечивает синтез коллагена; участвует в формировании и поддержании структуры и функции хрящей, костей, зубов; влияет на образование гемоглобина, созревание эритроцитов.
Витамин Е (α-токоферола ацетат) обладает антиоксидантными свойствами, поддерживает стабильность эритроцитов, предупреждает гемолиз; оказывает положительное влияние на функции половых желез, нервной и мышечной ткани.
Каротиноиды (бетакаротен, лютеин, ликопин) являются природными органическими пигментами, синтезируемыми бактериями, грибами, водорослями, высшими растениями и коралловыми полипами; окрашены в желтый, оранжевый или красный цвета. Бетакаротен является предшественником витамина А. Оказывает антиоксидантное действие, обладает способностью инактивировать свободные радикалы в условиях гипоксии. Обладает иммуномодулирующим действием. Повышает устойчивость организма к инфекциям.
Панаксозиды – тритерпеновые гликозиды, основным источником является корень женьшеня. Повышают устойчивость организма к вредным физическим, химическим и биологическим факторам. Иммуностимулирующее действие их выражается в стимуляции продукции антител, сопровождающейся увеличением количества общего белка и гамма-глобулинов в крови. Панаксозиды стимулируют кроветворение, почти в 2 раза усиливают биосинтез нуклеиновых кислот, белков и жиров в костном мозге.Способствуют нормализации работы органов и различных функций организма.
Фитосомы что это такое
В настоящее время активно разрабатываются новые способы доставки ЛС с целью увеличения их биодоступности [6, 8]. Одной из таких систем являются фитосомы. В этих структурах водорастворимые растительные компоненты вступают в реакцию с фосфолипидами, при достижении равновесия между гидрофильными и гидрофобными радикалами, увеличивается способность преодоления липидного слоя клеточных мембран и растворения в желудочно-кишечных жидкостях [5].
Особый интерес представляют фитосомы с флавоноидами из-за широкого спектра фармакологической активности этих соединений. Однако гидрофильность данного класса существенно снижает их проницаемость через кожный барьер и всасывание в ЖКТ, следовательно, снижается биодоступность флавоноидов и оказываемый эффект [1].
Целью настоящего исследования стало информационно-аналитическое исследование свойств, способов получения и применения новой лекарственной формы – фитосомы.
Результаты исследования и их обсуждение
Строение и назначение фитосомы. Название «фитосома» недаром созвучно с «липосома». В состав обеих лекарственных форм входят липиды, однако строение фитосом существенно отличается от липосомальных лекарственных форм. В структуре липосомы активное вещество либо растворено внутри фосфолипидного «шарика», либо находится в слое мембраны, а также может быть конъюгировано на поверхности мембраны [16, 21]. Фитосома отличается от липосомы тем, что фитокомпонент ковалентно связан с полярной головкой фосфолипидов, являясь неотъемлемой частью мембраны. Некоторые липосомальные препараты действуют в водной среде или буферном растворе, тогда как фитосомы активны с растворителями, имеющими низкую диэлектрическую проницаемость [17, 18, 20].
Обобщая литературные данные, можно дать следующее определение понятию фитосома – это флавоноидная молекула, связанную по крайней мере с одной молекулой фосфатидилхолина. Она является молекулой-гибридом, обладающей высокой растворимостью в липидной и в водной средах. В водных средах фитосомы группируются в мицеллу [8, 10, 22].
Несмотря на разницу в строении, сходство фитосомы и липосомы проявляется в их предназначении. Как и липосома, фитосома используется для увеличения биодоступности лекарственного компонента, более направленной доставки, повышения эффективности действия и снижения терапевтической дозы лекарства [5, 16].
В фитосоме активное вещество хорошо преодолевает кожный барьер и предотвращает разрушение фитокомпонентов под действием пищеварительных ферментов и кишечных бактерий. Это приводит к улучшению терапевтической эффективности. Следовательно, дозы, требуемые для достижения желаемого эффекта, также снижаются [20].
На сегодняшний день известны фитосомы с экстрактами гинкго билоба, расторопши, виноградных косточек, боярышника, зеленого чая и женьшеня. Флавоноидные и терпеноидные соединения этих экстрактов хорошо связываются с фосфатидилхолином [5, 18, 19].
Эффективность фитосомальных лекарственных форм доказана клинически. Так, например, гепатопротекторные свойства плодов расторопши пятнистой связаны с присутствием в них силибина [9], который, однако, имеет ограниченную биодоступность. Были проведены клинические испытания силибина в виде фитосомы дозировкой от 240 до 360 мг в течение 150 дней [12]. В качестве контроля использовали «плацебо» (n = 117) или силибин вне комплекса (n = 49). Для оценки клинического действия были изучены энзимные уровни аспартат-аминотрансферазы (AST), аланин-аминотрансферазы (ALT) и гамма-глутамилтранспептидазы (GGT). Исследователи пришли к выводу, что фитосомальная форма силибина оказывает значительно более выраженный клинический эффект [16].
Способ получения фитосомы. Технология получения фитосом предполагает включение фосфолипидов (таких как фосфатидилхолин, фосфатидилэтаноламин, фосфатидилсерин) в стандартизованные растительные экстракты [5, 16].
Фитосомы получают реакцией взаимодействия между 1–2 молями фосфолипида с 1 молем активного растительного компонента (флавоноиды или терпеноиды) в апротонном растворителе (диоксан, ацетон, метиленхлорид, этилацетат). Затем комплекс выделяют путем выпаривания растворителя в вакууме или осаждением с реагентом, таким как алифатические углеводороды, путем лиофилизации или методом распылительной сушки. Наиболее оптимальное соотношение компонентов в фитосоме 1:1 [5, 10, 19].
В литературе встречается ряд методик получения фитосом. Например, для образования комплекса силимарина с соевым фосфатидилхолином 1:1 поступают следующим образом: к раствору 5 г силимарина в 100 мл ацетона добавляют 8 г реактива «Липоид S 100 (R) », при перемешивании при комнатной температуре. После полной солюбилизации реакционную смесь концентрируют в вакууме до объема 30 мл и приливают к 300 мл лигроина, при перемешивании. Осадок отстаивают в течение ночи, затем его отделяют фильтрованием, промывают лигроином и сушат в вакууме при 40 °С. Выход составляет 11,2 г комплекса. При изучении спектральных характеристик полученного фитосомального комплекса было установлено, что удельный показатель поглощения составляет 170,2 при 288 нм (растворитель – метанол) [7].
Вторым примером может служить методика получения фитосомы силибина с соевым фосфатидилхолином в соотношении 1:2. К суспензии, содержащей 4,82 г (0,010 моль) силибина в 75 мл диоксана, добавляют при перемешивании 15,4 г (0,020 моль) «Липоид S 100 (R) ». Через 4 часа реакционную смесь лиофилизируют. Выход составил 20 г комплекса светло-желтого цвета с удельным показателем поглощения, равным 106 при 288 нм в растворе метанола [7].
Для получения комплекса силибина с соевым фосфатидилхолином 1:0,3 раствор силибина в диоксане (2,41 г (0,005 моль) силибина на 100 мл диоксана) обрабатывают при 60 °С реактивом «Липоид S 100 (R) » массой 0,770 г (0,001 моль) в течение 1 часа. Реакционную смесь упаривают досуха в вакууме и остаток переносят в 100 мл хлороформа. Избыток силибина, присутствующий в виде осадка, удаляют фильтрованием, а маточный раствор, содержащий комплекс, выпаривают досуха в вакууме. Полученный остаток сушат при 30 °С под вакуумом. Выход составляет 2,3 г комплекса в виде белого желтоватого порошка. Удельный показатель поглощения метанольного раствора полученного комплекса равен 300 при 288 нм (CH3OH) [7].
Методика получения фитосомы экстракта гинкго билоба с соевым фосфатидилсерином заключается в следующем: 1,87 кг 20 % фосфатидилсерина суспендируют в 17,5 л этилацетата при комнатной температуре. Добавляют сухой экстракт гинкго билоба (0,65 кг) и перемешивают. Суспензию выдерживают в течение 1 часа при перемешивании при кипячении с обратным холодильником, затем фильтруют при 70–75 °C и концентрируют при давлении окружающей среды до получения мягкого осадка. Осадок сушат при 40 °C в течение 48 часов. Выход продукта: 2,23 кг комплекса экстракт гинкго билоба – фосфатидилсерин [3].
Интерес представляют фитосомы с индивидуальными флавоноидами, поскольку из-за разнообразия фармакологических эффектов этих соединений можно существенно расширить ассортимент лекарственных средств, обладающих хорошей биодоступностью.
Фитосомы кверцетина с фосфатидилхолином и холестерином получают с использованием метода тонкослойной гидратации с различным молярным отношением кверцетина, фосфатидилхолина и холестерина. Кверцетин и фосфатидилхолин растворяют в метаноле, а холестерин – в дихлорметане. Смесь помещают в круглодонную колбу и упаривают на роторном испарителе при 45 °С до образования пленки. Затем с помощью вакуумной сушки полностью удаляют органические растворители. Дополнительно готовый липидный тонкий слой подвергают воздействию потока газообразного азота и выдерживают в течение ночи при комнатной температуре, чтобы обеспечить полное удаление органических растворителей. Пленку увлажняют дистиллированной водой в роторном аппарате при 45 °С. Для уменьшения размера фитосомы применяют: диспергирование в ультразвуковой ванне при 45 °С, гомогенизацию в центрифуге с 20000 оборотов в минуту и метод ультразвуковой обработки [11, 12].
Физико-химическая оценка фитосом. Фитосомы можно охарактеризовать по форме, размеру, плотности распределения, % связанного вещества в объеме, количеству высвобождаемого вещества, стабильности [2, 6, 15].
В литературе встречается пример оценки свойств кверцетин-фосфатидилхолин-холестеринового фитосомального комплекса. Средний размер частиц фитосом, полученных при молярных соотношениях 1: 2: 0 и 1: 2: 0,2 кверцетина : фосфатидилхолина : холестерина, составил 79 нм и 82 нм соответственно. Анализ частиц, проведенный на приборе Malvern, Nano series, S90 Zetasizer, Великобритания, показал узкое распределение. При увеличении концентрации холестерина увеличивалась и толщина липидного бислоя. По результатам исследования эффективность инкапсуляции кверцетина в фитосоме была в пределах 96–98 % и не менялась в зависимости от изменений молярных соотношений компонентов системы. Анализ показал, что при добавлении холестерина стабильность фитосом возрастает за счет ограничения ацильных цепей фосфатидилхолина [9, 15].
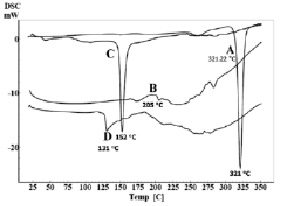
ДСК-термограмма чистого кверцетина (A), фосфатидилхолина (В), холестерина (С) и фитосомального комплекса (D)
Удельную теплоту плавления определяли с помощью дифференциального сканирующего калориметра (DSC 60, Shimadzu, Япония) [15]. Дифференциальные сканирующие (ДСК) термограммы чистого кверцетина, холестерина, фосфатидилхолина и фитосомального комплекса показаны на рисунке. Эндотермический пик кверцетина наблюдался в 321.22 °C (рисунок, А), соответствующий его точке плавления. ДСК-термограмма фосфатидилхолина и холестерина также показали эндотермические пики при 205 °С и 152.45 °С соответственно (рисунок, B, C). Термограмма фитосомального комплекса (рисунок, D) показала исчезновение эндотермического пика плавления кверцетина и значительное смещение эндотермического пика плавления холестерина в нижних точках плавления. Эти наблюдения показали, что кверцетин был молекулярно распределен на поверхности и внутри матрицы фитосомы и утратил свою кристаллическую структуру. Кверцетин и фосфатидилхолин образуют водородные связи между гидроксильными группами кверцетина и полярной части фосфатидилхолина [2, 15].
В литературе встречаются примеры определения удельной температуры плавления рутин-фосфатидилхолинового комплекса с помощью прибора Perkin Elmer JADE DSC, США. Также данный комплекс исследовали с помощью ИК-спектроскопии на Alpha FT-IR спектрофотометре (Bruker, Германия), образец исследовали на просвечивающем электронном микроскопе JEOL (JEM 2100), Япония [4, 13].
Выводы
1. По сравнению с традиционными лекарственными растительными формами фитосомы наиболее перспективны в доставке растительных экстрактов, т.к. абсорбция и биодоступность водорастворимых компонентов возрастает благодаря их взаимодействию с фосфолипидами.
2. В литературе присутствуют данные о фитосомах, содержащих преимущественно растительные экстракты, богатые флавоноидами, или индивидуальные флавоноиды. Однако данные о возможности включения других растительных гидрофильных, мало растворимых в воде соединений в липидные комплексы, отсутствуют. Это открывает широкие перспективы для исследователей в разработке методов получения новых фитосомальных комплексов.
3. Фитосомы – как лекарственная форма – новое, только развивающееся направление. Для его правильного становления необходима разработка единых подходов к оценке качества фитосом. В существующих литературных примерах методы физико-химической оценки этой лекарственной формы представлены крайне скудно или вовсе отсутствуют.
Фитосомы – эффективная помощь в лечении заболеваний
Отказ от ответсвенности
Обращаем ваше внимание, что вся информация, размещённая на сайте Prowellness предоставлена исключительно в ознакомительных целях и не является персональной программой, прямой рекомендацией к действию или врачебными советами. Не используйте данные материалы для диагностики, лечения или проведения любых медицинских манипуляций. Перед применением любой методики или употреблением любого продукта проконсультируйтесь с врачом. Данный сайт не является специализированным медицинским порталом и не заменяет профессиональной консультации специалиста. Владелец Сайта не несет никакой ответственности ни перед какой стороной, понесший косвенный или прямой ущерб в результате неправильного использования материалов, размещенных на данном ресурсе.
Чтобы витамины и лекарственные вещества лучше усваивались организмом, их выпускают в форме фитосом. Они позволяют добиваться превосходных результатов, в сравнении с простыми экстрактами растений.
Производство фитосом запатентовано и заключается в том, что определенные компоненты экстрактов трав связывают со специальным веществом фосфатидилхолином, которое было извлечено из сои. Любопытно, что именно из этого компонента состоят клеточные мембраны человека.
Внимание! Фитосома представляет собой мельчайшую каплю экстракта растения, которая заключена в оболочку из растительного лецитина.
Чем полезны фитосомы
При помощи фитосом улучшают сухие целебные экстракты, которые пользуются огромным спросом:
Препараты содержат терпеноиды, флавоноиды и компоненты, которые можно напрямую связать с фосфатидилхолином. Молекула этого вещества своей головной частью соединяется с компонентами водных экстрактов. А основа и концевая часть, в последующем, прикрывают связанную.
Этот способ помогает получить специальную клетку. Она защищает лекарственные вещества от бактерий, которые содержатся в кишечнике человека и от пищеварительного секрета. Таким образом, эти вещества не разрушаются.
Внимание! То, что растительные экстракты в такой форме более эффективно воздействуют на организм и лучше усваиваются, подтверждается многочисленными исследованиями.
Одним из самых распространенных веществ-фитосом является силифост. Это специальный лекарственный компонент – флавоноид, приготовление которого осуществляется из сырья расторопши. Его высоко оценивают из-за мощных защитных функций.
Исследования фитосом
Как показали исследования, проведенные на животных и людях, фитосом из расторопши будет усваиваться лучше, чем обычный силибин, полученный из экстракта или отвара расторопши.
В ходе одного из научных исследований изучалось выделение этого вещества у тех, кто столкнулся с проблемой удаления желчного пузыря. Чтобы получить образцы, учёные применяли дренажную Т-образную трубку.

Испытуемым назначили принимать фитосомы (одним) и обычный травянистый экстракт расторопши (другим). В результате было выявлено, что количество вещества, восстанавливающего печень и выделенного за 48 часов, у этих людей было различным. У тех, кто принимал фитосомы, показатель составил 11% процентов, а у тех, кто принимал обычный силимарин – 3%.
Фитосомы и обычные экстракты
Также было выявлено, что, применяя фитосомы виноградного семени и гинкго, можно добиться большего результата, в сравнении с лечением обычными экстрактами этих растений.
Проводилось исследование действия фитосомы гинкго среди больных с проблемами периферических кровеносных сосудов – симметричной гангрены и перемежающейся хромоты. Выяснилось, что фитосомы эффективнее воздействуют на больных (примерно на 30–60%), чем экстракты данных растений.

Эффективность воздействия на организм любого лекарства будет зависеть от введения достаточного количества активных соединений. Можно сделать вывод, фитосомы – это действительно ценное изобретение, которое способствует более эффективному усвоению целебных веществ организмом и успехам в лечении.
Отказ от ответсвенности
Обращаем ваше внимание, что вся информация, размещённая на сайте Prowellness предоставлена исключительно в ознакомительных целях и не является персональной программой, прямой рекомендацией к действию или врачебными советами. Не используйте данные материалы для диагностики, лечения или проведения любых медицинских манипуляций. Перед применением любой методики или употреблением любого продукта проконсультируйтесь с врачом. Данный сайт не является специализированным медицинским порталом и не заменяет профессиональной консультации специалиста. Владелец Сайта не несет никакой ответственности ни перед какой стороной, понесший косвенный или прямой ущерб в результате неправильного использования материалов, размещенных на данном ресурсе.
Гилоба
Состав и форма выпуска
Цены в аптеках
| Вещество | Количество |
|---|---|
| Экстракт листьев гинкго двулопастного | 40 мг |
Фармакологические свойства
Фармакодинамика. Капсулы Гилоба содержат экстракт из листьев гинкго двулопастного, который улучшает снабжение головного мозга кислородом и глюкозой. Активными веществами экстракта являются флавоноидные гликозиды, гинкголиды и билобалиды. Они расширяют кровеносные сосуды, улучшают кровоток, тормозят агрегацию тромбоцитов и, регулируя метаболизм, защищают клетки и ткани от повреждений, вызванных гипоксией. Гилоба улучшает мозговое кровообращение и метаболизм, предотвращает ухудшение умственной деятельности.
Фармакокинетика. Всасывается около 60% принятого внутрь экстракта. Препарат вступает в энтерогепатическую рециркуляцию с максимальной абсорбцией в первом цикле через 1,5 ч и во втором — через 12 ч. Период полувыведения — около 4,5 ч. За 72 ч 38% принятого внутрь экстракта выделяется через легкие, 22% — выводится с мочой и 29% — с калом.
Флавоноидные гликозиды всасываются в тонком кишечнике, максимальная концентрация в крови достигается через 2 ч после приема, период полувыведения гликозидов составляет 2–4 ч, а полностью они выводятся за 24 ч.
Показания Гилоба
нарушение мозгового кровообращения у лиц пожилого возраста, проявляющееся ухудшением памяти и умственных способностей, замкнутостью и беспокойством, головокружением, шумом в ушах, нарушением сна; нарушение периферического кровообращения в конечностях.
Применение Гилоба
по 1 капсуле 3 раза в сутки после еды, запивая водой. Первые признаки улучшения состояния отмечают через 1 мес после начала терапии. Для продолжительного эффекта Гилобу следует принимать не менее 3 мес.
Противопоказания
повышенная чувствительность к компонентам препарата, острый инфаркт миокарда, острая или хроническая гипотензия, сниженная свертываемость крови, эрозивный гастрит, пептическая язва желудка и двенадцатиперстной кишки в фазе обострения, период беременности.
Побочные эффекты
крайне редко — диспепсия, головная боль, кожно-аллергические реакции (гиперемия, отек, зуд). При возникновении реакций гиперчувствительности применение препарата следует прекратить.
Особые указания
редко препарат может вызывать нарушения со стороны ЖКТ у чувствительных пациентов. У пациентов со склонностью к гипотензии необходимо контролировать уровень АД ввиду сосудорасширяющего действия препарата.
Очень редко применение Гилоба может вызывать седативный эффект, поэтому рекомендуется оценить индивидуальную реакцию на препарат при управлении автотранспортными средствами или при выполнении других видов деятельности, требующих быстроты психомоторных реакций. Капсулы Гилоба не рекомендуется назначать в период беременности и кормления грудью, однако экспериментально не установлено отрицательного влияния препарата на плод.
Взаимодействия
с осторожностью назначают препарат одновременно с ацетилсалициловой кислотой и антикоагулянтами.
Передозировка
Симптомы: диарея, диспепсия, тошнота.
Лечение: необходимо снизить дозу или прекратить прием препарата. При необходимости назначают поддерживающую терапию.
Условия хранения
в сухом, защищенном от света месте при температуре 15–25 °С.