Финлепсин и Финлепсин ретард в терапии эпилепсии
(карбамазепин)
Финлепсин® и Финлепсин® ретард в терапии эпилепсии
Эпидемиология эпилепсии 11
Основные принципы лечения эпилепсии 13
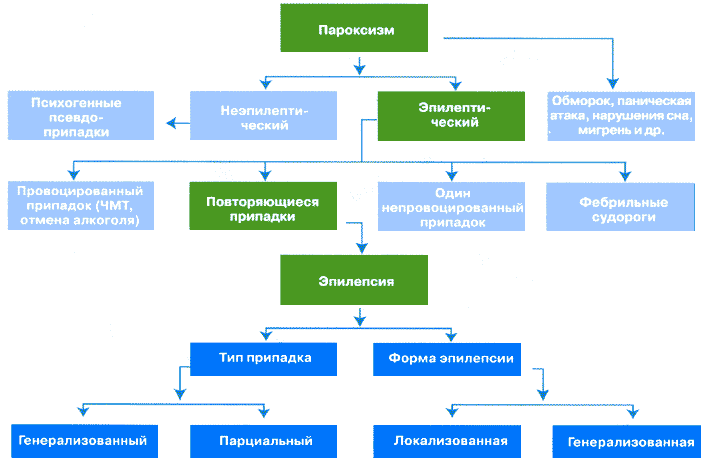
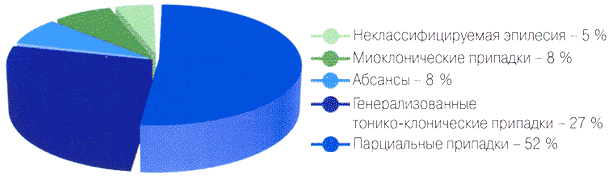
В структуре эпилепсии парциальные формы встречаются более, чем в половине случаев 1
Финлепсин®
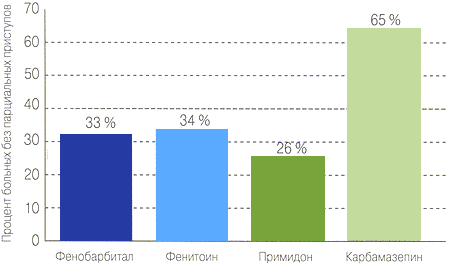
Препарат первого выбора при любых парциальных припадках (простых, сложных и вторично-генерализованных) 14
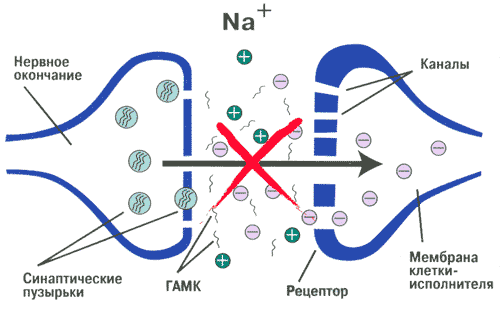
Механизм действия Финлепсина
Показания к применению Финлепсина® и Финлепсина® ретард 15
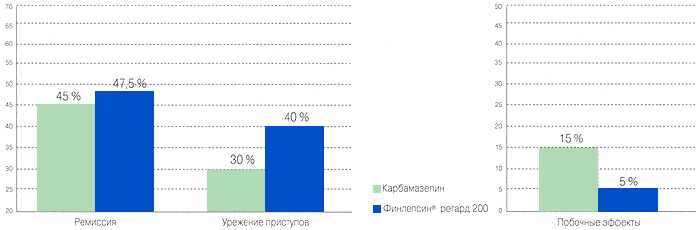
Преимущества Финлепсина® ретард перед обычной формой Карбамазепина при лечении парциальных приступов
Сравнительная эффективность Финлепсина® ретард и обычной формы Карбамазепина 2
Сравнительная безопасность Финлепсина® ретард и обычной формы Карбамазепина 2
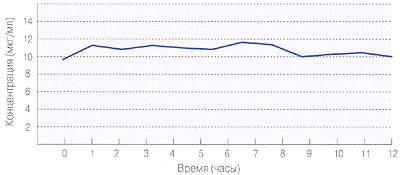
ФИНЛЕПСИН® РЕТАРД
обеспечивает стабильную концентрацию препарата в плазме крови 3
Активное вещество из микрокапсул высвобождается постепенно и равномерно. Кратность приема снижается до 1-2 раз в сутки.
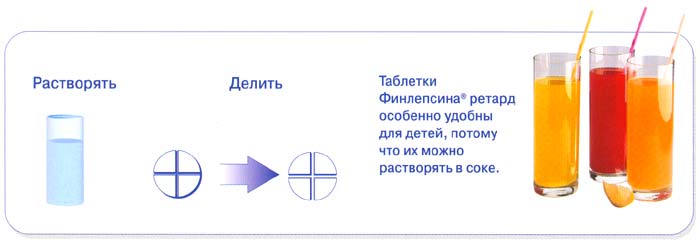
Таблетки Финлепсина® ретард можно 3
В структуре эпилепсии парциальные формы встречаются более, чем в половине случаев 7
Сравнительная эффективность Карбамазепина
Сравнительная безопасность Карбамазепина
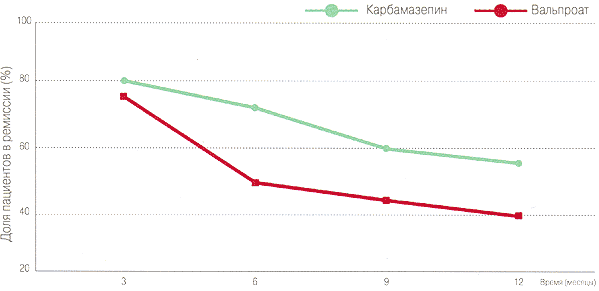
Сравнительная эффективность Карбамазепина и Вальпроата при лечении сложных парциальных приступов 9
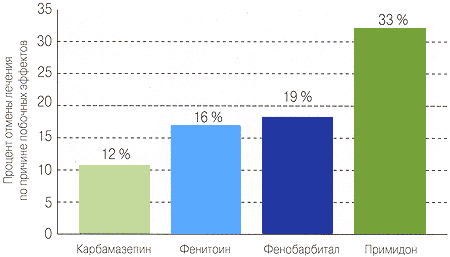
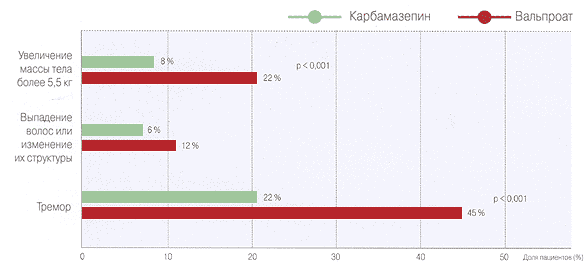
Сравнительная безопасность Карбамазепина и Вальпроата 4 (побочные эффекты на фоне лечения симптоматической эпилепсии по данным рандомизированного исследования 16 )
Основные принципы лечения эпилепсии 6
Преимущества назначения Финлепсина® ретард 200 и 400 мг
Спектр действия Финлепсина® 18
Финлепсин® ретард
Институт детской неврологии и эпилепсии
ИДНЭ (с 2006 года), ИДВНЭ (с 2016 года), ЦЗиР (с 2017) и ОЦМУ (с 2019) им. Святителя Луки
Что такое противоэпилептические препараты и на какие группы они делятся?
Еще во второй половине прошлого, XX века, эпилепсия считалась неизлечимым заболеванием. Развитие нейрофармакологии в последние десятилетия, синтез новых высокоэффективных антиэпилептических препаратов (АЭП), кардинальный пересмотр многих принципов ее лечения – все это позволило в настоящее время отнести эпилепсию к заболеваниям, которые поддаются лечению. АЭП выбирают в зависимости от формы эпилепсии и характера приступов.
Начинать лечение следует с препарата первого выбора при данной форме эпилепсии. Препарат обычно назначают в небольшой начальной дозе с постепенным ее увеличением до появления оптимального клинического эффекта или возникновения начальных признаков передозировки. При неэффективности препарата он постепенно отменяется и назначается следующий; при этом нельзя сразу переходить к комбинации препаратов, не использовав всех резервов монотерапии.
Препараты вальпроевой кислоты (Конвульсофин, Депакин и др.) – одна из наиболее эффективных групп АЭП.
Конвульсофин — кальциевая соль вальпроевой кислоты. Это современный препарат широкого спектра действия; он высоко эффективен практически при всех формах эпилепсии и типах эпилептических приступов. В настоящее время более чем 20-летний опыт применения вальпроатов свидетельствует, что они являются препаратами абсолютного выбора в лечении большинства форм генерализованной и идиопатической парциальной эпилепсии. В настоящее время доказано, что Конвульсофин обладает широким спектром антиэпилептической активности, как в отношении первично — генерализованных приступов (генерализованные судорожные, миоклонические, абсансы), так и парциальных (простых и сложных) и вторично — генерализованных пароксизмов. При этом Конвульсофин применяется как базовый препарат в качестве монотерапии, так и в комбинации с другими АЭП у детей и взрослых всех возрастов.
Дозировки Конвульсофина подбираются индивидуально и варьируют в широком диапазоне. Средняя доза может составлять 600-1500 мг/сут (20-40 мг/кг/сут). При необходимости и при тяжелых формах применяются значительно более высокие дозы. Среди побочных эффектов (ПЭ) вальпроатов наиболее значимы следующие: повышение аппетита и веса (редко – отказ от еды), изжога, тошнота, боли в животе, незначительно выраженное выпадение волос, дрожание рук. Необходимо контролировать уровень тромбоцитов в крови (возможно их снижение). При появлении ПЭ нужно проконсультироваться с лечащим врачом; при этом далеко не всегда возникает необходимость в отмене препарата.
Препараты группы карбамазепина (Финлепсин, Финлепсин – ретард, Тегретол) — также современные высокоэффективные АЭП. Финлепсин — препарат выбора в лечении симптоматических парциальных форм эпилепсии; при парциальных, первично – и вторично – генерализованных судорожных приступах. Применяется, как в монотерапии, так и в качестве добавочного препарата. Следует помнить, что препараты карбамазепина противопоказаны при абсансах и миоклонических приступах. Средняя суточная доза составляет 400-800 мг (около 20 мг/кг/сут). Предпочтение в лечении отдается пролонгированным формам, таким как Финлепсин – ретард. Основные ПЭ: двоение в глазах, сонливость, кожная сыпь, головная боль, снижение уровня лейкоцитов в крови.
Этосуксимид (Суксилеп). Суксилеп – препарат узкого спектра. Он высоко эффективен при абсансных и миоклонических приступах как в монотерапии, так и в комбинации с вальпроатами (Конвульсофином). При некоторых формах эпилепсии, например, синдроме Леннокса – Гасто, Суксилеп может применяться только в сочетании с другими АЭП. Средние дозы: 500-750 мг/сут (около 20 мг/кг/сут). ПЭ: тошнота, кишечные расстройства, сонливость. Примечательно, что препарат в большом количестве поступает в грудное молоко. Женщины, принимающие суксилеп в периоде лактации, должны отказаться от грудного вскармливания.
Топирамат (Топамакс) – препарат широкого спектра действия. Эффективен при всех типах парциальных приступов, а также при генерализованных судорожных. Применяется в лечении парциальных и генерализованных форм эпилепсии с наличием судорожных приступов. Средние дозы: 5-7 мг/кг/сут (200-400 мг/сут). Необходимо медленное наращивание дозы при введении препарата (обычно в течение 6-10 нед). ПЭ зависят, главным образом, от дозы топирамата и связаны с нарушением функции ЦНС: головокружение, утомляемость, сонливость, раздражительность, снижение концентрации внимания. Эти проявления обычно проходят вскоре после очередного повышения дозы. Возможно также появление парестезий (чувство ползания мурашек). Для предотвращения появления конкрементов в почках пациенты должны увеличить ежедневное потребление жидкости (щелочные минеральные воды). Препарат противопоказан больным с нарушением функции почек и при почечно-каменной болезни.
Бензодиазепины (клоназепам, антелепсин, клобазам, седуксен, радедорм, лорафен и др.). Бензодиазепины применяются только в качестве добавочных АЭП при резистентных формах эпилепсии. Особенно эффективны при миоклонических и фотосенситивных формах эпилепсии. Также назначаются при серийном учащении приступов, как препараты первой помощи. Обладают широким спектром ПЭ, прежде всего, в отношении ЦНС: выраженный седативный эффект, нарушение концентрации внимания, угнетение или возбуждение, шаткость, расстройство речи, слюнотечение, расстройства дыхания у детей раннего возраста. Категорически запрещено резко отменять бензодиазепины у больных эпилепсией – угроза учащения приступов и развития эпистатуса.
«Старые» АЭП: барбитураты (фенобарбитал, гексамидин, бензонал) и гидантоины (дифенин, фенитоин, дифантоин). Эффективны в лечении генерализованных судорожных и парциальных приступов. Фенобарбитал применяется в дозе 100-300 мг/сут (2-5 мг/кг/сут), а Дифенин – в дозе 100-400 мг/сут (3-8 мг/кг/сут). Европейская комиссия по антиэпилептическим препаратам в 1998 году рекомендовала врачам значительно сузить показания к применению данных препаратов у больных эпилепсией. Основанием для этого является негативное воздействие этих препаратов на ЦНС: вялость, сонливость, расстройство концентрации внимания, гиперактивность, снижение способности к обучению и др. Дифенин – тератогенный препарат, который нередко вызывает пороки развития у новорожденных. Он противопоказан для применения во время беременности.
К новым антиэпилептическим препаратам относятся топирамат, ламотриджин, тиагабин, вигабатрин, фелбамат, леветирацетам.
Следует помнить, что универсальных препаратов, которые были бы высоко эффективны во всех случаях, не давали побочных эффектов (ПЭ) и были бы недорогими – не существует. Назначение конкретного препарата, подбор дозировок, добавление или отмена АЭП должны производиться только лечащим врачом. Несоблюдение рекомендаций, самостоятельные манипуляции с препаратами, могут привести к тяжелым последствиям для пациентов, вплоть до развития эпилептического статуса.
Финлепсин или зептол что лучше пить
Пфайзер Эйч Си Пи Корпорэйшн
Противоэпилептические препараты за рамками эпилепсии (применение антиконвульсантов в лечении болевых синдромов)
Журнал: Журнал неврологии и психиатрии им. С.С. Корсакова. Спецвыпуски. 2013;113(4-2): 58-65
Давыдов О. С. Противоэпилептические препараты за рамками эпилепсии (применение антиконвульсантов в лечении болевых синдромов). Журнал неврологии и психиатрии им. С.С. Корсакова. Спецвыпуски. 2013;113(4-2):58-65.
Davydov O S. Antiepileptic drugs: over than epilepsy (anticonvulsants drugs use in different pain syndromes). Zhurnal Nevrologii i Psikhiatrii imeni S.S. Korsakova. 2013;113(4-2):58-65.
Пфайзер Эйч Си Пи Корпорэйшн
Пфайзер Эйч Си Пи Корпорэйшн
За прошедшие с момента появления первых антиконвульсантов годы появились обширная доказательная база и опыт применения этих препаратов в лечении различных форм эпилепсии, одновременно с этим наметился ряд точек приложения этих препаратов при лечении других заболеваний. В литературе имеются результаты исследования эффективности ПЭП при следующих заболеваниях и синдромах: невропатическая боль и фибромиалгия, мигрень, тревожные и биполярные расстройства, шизофрения, эссенциальный тремор [21].
Предпосылки для применения антиконвульсантов при невропатической боли
Ряд патофизиологических механизмов, характерных для невропатической боли, имеет аналоги при эпилепсии. Так, например, выявлено сходство между феноменом «взвинчивания», возникающим в задних рогах спинного мозга при невропатической боли, центральной сенситизацией и феноменом «киндлинга» или формирования «генераторов патологического возбуждения» в гиппокампальных нейронах при эпилепсии. Считается, что оба феномена, наряду с другими механизмами, возникают вследствие активации NMDA-рецепторов. Не удивительно, что антиконвульсанты показывают свою эффективность как с точки зрения уменьшения количества приступов эпилепсии, так и с точки зрения подавления интенсивности болевого синдрома [13, 17, 37].
Механизмы действия антиконвульсантов при болевых синдромах
Механизмы действия антиконвульсантов при невропатической боли различны. Антиболевой эффект таких препаратов, как карбамазепин, фенитоин, окскарбазепин, ламотриджин, вальпроаты, топирамат, принято объяснять уменьшением высокочастотной повторяющейся импульсации нейронов посредством блокирования потенциалзависимых натриевых и кальциевых каналов в периферических нервах. Ряд препаратов (например, фенобарбитал, тиагабин, топирамат, вигабатрин и вальпроаты) усиливают нервную передачу подавляющих боль импульсов, либо непосредственно блокируют нервную передачу возбуждающих импульсов. Прегабалин и габапентин имеют принципиально иной механизм действия, связанный с воздействием на альфа-2-дельта-субъединицу потенциалзависимых кальциевых каналов и подавлением процессов центральной сенситизации в заднем роге спинного мозга и в головном мозге. Обобщенные данные по механизмам действия антиконвульсантов представлены в табл. 1.
Помимо перечисленных в табл. 1 предполагаемых механизмов действия антиконвульсантов рассматриваются также их возможное опосредованное воздействие на различные нейротрансмиттерные системы и влияние на внутриклеточные процессы. На сегодняшний день обсуждается вопрос, является ли одинаковым механизм реализации терапевтического эффекта одного и того же антиконвульсанта при различных состояниях: эпилепсии, болевых синдромах, тревоге и др. через сходные механизмы или эти механизмы различаются [21].
На основании проведенного метаанализа и систематических обзоров такие авторитетные международные организации, как Европейская федерация неврологических обществ, Группа по изучению невропатической боли при Международной ассоциации по изучению боли и др., опубликовали рекомендации по терапии невропатической боли и выделили несколько направлений (линий) терапии этого состояния. В большинстве документов выделяют препараты первой линии, т.е. те препараты, с которых следует начинать лечение, а при неэффективности или непереносимости заменять на другой препарат этой же линии, а также средства второй и третьей линий, а в некоторых рекомендациях предлагается даже выделять препараты четвертой линии. Авторы рекомендаций сходятся в одном: на сегодняшний день среди антиконвульсантов только прегабалин и габапентин являются препаратами первой линии при терапии невропатической боли. Доказательства эффективности карбамазепина имеются только при тригеминальной невралгии [32] (табл. 3).
Важно подчеркнуть, что рассматриваемый подход к терапии невропатической боли основан на доказательствах, полученных в исследованиях, где учитывался опыт не только каждого специалиста, но были обобщены и соответствующие мировые данные [32]. Эти же позиции отражены и в рекомендациях группы российских экспертов [4].
Карбамазепин (тегретол, финлепсин, актинервал, зептол и др.) относится к ПЭП первого поколения и по химическому строению близок к трициклическим антидепрессантам. Карбамазепин имеет широкий спектр показаний, помимо других заболеваний включающий состояния, сопровождающиеся невропатической болью: невралгию тройничного нерва, языкоглоточную невралгию и болевую диабетическую полиневропатию. Большинство хорошо спланированных исследований проведены у пациентов с тригеминальной невралгией и лицевой болью, где препарат доказал свою эффективность. Данные по его эффективности при других типах невропатической боли ограничены (небольшое число проведенных испытаний и участвовавших пациентов). В связи с этим в ряде рекомендаций по лечению невропатической боли карбамазепин рекомендован как препарат первой линии терапии только для тригеминальной невралгии [17]. Карбамазепин обычно принимают независимо от приема пищи, с небольшим количеством жидкости. У взрослых лечение рекомендуют начинать с дозы 100-200 мг 1 или 2 раза в день, постепенно повышая ее не более чем на 200 мг в сутки, до купирования боли (в среднем это 800-1200 мг в день), а затем снижают ее до минимально эффективной дозы. В некоторых случаях может потребоваться доза 1600 мг в день, что предполагает тщательную титрацию и наблюдение за пациентом. Карбамазепин противопоказан при атриовентрикулярной блокаде, нарушении кроветворения, острой перемежающейся порфирии, в том числе в анамнезе, а также одновременно с ингибиторами моноаминоксидазы.
При применении карбамазепина зарегистрирован ряд серьезных побочных эффектов, таких как синдром Стивенса-Джонсона (на 1999 г. в мире зарегистрировано 544 случая), острый эпидермальный некролиз, агранулоцитоз, апластическая анемия, гепатит, нарушение почечной функции, эндокринные нарушения. К наиболее частым побочным эффектам (10% и больше) карбамазепина относятся: головокружение, атаксия, сонливость, крапивница, мультиорганные реакции гиперчувствительности, васкулиты, лейкопения, тошнота, рвота, отеки, повышение массы тела. Риск развития этих явлений повышен при учете неблагоприятных лекарственных взаимодействий. С осторожностью следует назначать карбамазепин у пожилых больных [5, 6].
Поэтому карбамазепин следует применять только при условии регулярного врачебного контроля. Перед началом лечения рекомендуется сделать анализ мочи, развернутый биохимический анализ крови, включая уровень мочевины. Эти показатели следует контролировать сначала еженедельно, а затем ежемесячно. В процессе лечения необходимо также регулярно контролировать функцию печени, состояние крови, в том числе концентрацию электролитов в сыворотке [14].
Окскарбазепин (трилептал) имеет структурное сходство с карбамазепином. Считается, что эффективность этих препаратов при эпилепсии вполне сопоставима, но окскарбазепин лучше переносится. Например, при применении препарата не зарегистрировано ни одного случая синдрома Стивенса-Джонсона. Для окскарбазепина было проведено несколько клинических исследований при тригеминальной невралгии с положительным результатом. Рекомендуемый режим дозирования 900-1800 мг в сутки. В ряде рекомендаций по лечению невропатической боли окскарбазепин показан как препарат первой линии терапии для тригеминальной невралгии. Окскарбазепин по этому показанию в России не зарегистрирован [17].
Габапентин в ряде международных рекомендаций признан препаратом первой линии терапии невропатической боли [32]. Помимо оригинального препарата нейронтин в России зарегистрирован ряд дженериков: гапентек, тебантин, габагамма, конвалис и др. В 9 крупных рандомизированных плацебо-контролируемых исследованиях была показана эффективность габапентина при постгерпетической невралгии и диабетической полиневропатии. По одному плацебо-контролируемому исследованию было проведено при фантомной боли, синдроме Гийена-Барре, невропатической боли различной этиологии, боли невропатического характера, вызванной онкологическим заболеванием, травме спинного мозга. По результатам клинических исследований препарат показал свое превосходство над плацебо при купировании боли и его хорошую переносимость больными [26].
В отсутствие нейротрансмиттеров в синаптической щели распространение импульса на следующий нейрон блокируется [13, 23].
Прегабалин (лирика) на сегодняшний день позиционируется во всех международных и Российских рекомендациях по лечению невропатической боли и болевой диабетической полиневропатии в качестве препарата первой линии терапии [4, 32]. Прегабалин, как и габапентин, относится к классу средств, имеющих высокую аффинность к альфа-2-дельта-протеину в центральной нервной системе. Прегабалин представляет собой дериват ГАМК и является по сути ее аналогом. В исследованиях на фоне приема препарата было продемонстрировано уменьшение высвобождения ряда нейротрансмиттеров (включая глутамат, норадреналин и субстанцию Р) в гипервозбужденных нейронах. Считается, что это вызвано модуляцией функции альфа-2-дельта-субъединицы потенциалзависимых кальциевых каналов. Прегабалин, уменьшая выделение нейротрансмиттеров, замедляет таким образом передачу нервного импульса на следующий нейрон, что в результате приводит к редукции болевого синдрома. Важно отметить, что прегабалин оказывает эффект только в условиях гипервозбуждения нейронов при патологических состояниях; его модулирующее действие приводит к переходу нейронов в нормальное состояние [13, 18, 23].
В литературе отражен обширный опыт постмаркетингового применения прегабалина. Так, в Германии было проведено его исследование при лечении 10 300 пациентов с такими формами патологии, как диабетическая полиневропатия, боль в спине с невропатическим компонентом, постгерпетическая и тригеминальная невралгия, алкогольная полиневропатия, другие различные полиневропатии и невропатическая боль вследствие опухоли. Достоверное снижение интенсивности боли отмечалось уже на 1-й неделе терапии. К 6-й неделе лечения прегабалином интенсивность боли снизилась в среднем на 62%, при этом у пациентов улучшались сон и настроение [24].
Имеется опыт использования препарата у пациентов с тяжелой, не купирующейся другими средствами, болью. В одном открытом исследовании [24] у пациентов с болью, рефрактерной к терапии габапентином, трициклическими антидепрессантами или другими препаратами, применение прегабалина достоверно уменьшало интенсивность боли по визуальной аналоговой шкале и выраженность тревоги и нарушений сна [25].
Препарат исследован также и при центральной невропатической боли у пациентов, перенесших травму спинного мозга, в ходе 12-недельного рандомизированного плацебо-контролируемого исследования. На фоне терапии прегабалином интенсивность боли у этой группы пациентов уменьшалась, начиная с 1-й недели терапии, а эффект сохранялся до конца курса лечения. Параллельно с обезболиванием применение препарата вызывало стойкое улучшение сна. Еще в одном исследовании прегабалин был эффективнее плацебо у пациентов с центральной постинсультной болью [30, 34].
Как уже указывалось, прегабалин хорошо переносится. Наиболее частыми побочными эффектами являются головокружение и сонливость. Как показывают данные клинических исследований, головокружение и сонливость на фоне приема прегабалина имеют транзиторный характер, возникая через 1-2 дня приема и прекращаясь на 2-4-й неделе терапии [25]. К другим побочным эффектам относятся: атаксия, дизартрия, нарушение внимания, эйфория, раздражительность, диплопия, сухость во рту, утомляемость, отеки, транзиторное повышение массы тела. Прегабалин не метаболизируется в печени и не связывается с белками плазмы, поэтому риск взаимодействия с другими лекарствами минимален.
Другие антиконвульсанты для лечения невропатической боли. Ламотриджин (ламиктал, конвульсан, ламолеп, ламиктор) является антиконвульсантом второго поколения и зарегистрирован для лечения эпилепсии и биполярных расстройств. При невропатической боли эффективность препарата была показана при болевой форме диабетической нейропатии, спинальной травме, тригеминальной невралгии, центральной постинсультной боли, однако в некоторых других исследованиях были получены противоречивые результаты. Топирамат (топамакс, топиромакс, макситопир и др.) показал эффективность в снижении боли при диабетической невропатии и спинальной травме, в других исследованиях эффект был недостаточным. Лакосамид (вимпат), на стадии клинических исследований вселявший определенные надежды на эффективность, не оправдал ожиданий в отношении терапии болевых синдромов. Следует также учитывать отсутствие невропатической боли в официальном перечне показаний для всех трех препаратов [18, 20, 38, 39].
Применение антиконвульсантов при мигрени, тревожных расстройствах и фибромиалгии
Применение антиконвульсантов при мигрени рассматривается только в рамках профилактической терапии приступов. Согласно рекомендациям Американской академии неврологии, для того чтобы начинать профилактическую терапию, таких приступов должно быть не менее 2 в месяц, или приступы должны быть тяжелыми, рефрактерными к лечению и приводящими к дезадаптации пациента [31]. Среди возможных механизмов профилактического действия антиконвульсантов рассматривается их влияние на систему ГАМК-глутамат или на внутриклеточные медиаторы (АТФ, ц-АМФ, протеинкиназа С и др.) посредством воздействия на кальциевые или натриевые каналы синапса. В США топирамат и вальпроаты зарегистрированы FDA для профилактики мигрени, но в России эти показания не фигурируют [31, 37].
Гипотетическую возможность применения большинства антиконвульсантов при тревожных расстройствах связывают с воздействием на трансмиссию ГАМК. Наиболее доказанным действием в отношении тревоги являются тиагабин, габапентин и прегабалин, причем последний официально зарегистрирован как в США, так и в России для лечения генерализованного тревожного расстройства. Механизм анксиолитического действия прегабалина связывают с пресинаптическим ингибированием высвобождения возбуждающих нейротрансмиттеров, а в качестве доказательства его эффективности опубликованы результаты более 7 рандомизированных плацебо-контролируемых исследований [35].
Одним из заболеваний, также до определенной степени поддающихся лечению антиконвульсантами, является фибромиалгия, или как ее еще называют, синдром индивидуальной гиперчувствительности к боли, заболевание, наиболее трудно поддающееся лечению. Из известных на сегодня антиконвульсантов в его лечении доказал свою эффективность только прегабалин, исследованный как в коротких, 8-недельных, так и в длительных, продолжительностью более года, исследованиях. Наличие достаточных доказательств позволило Европейской противоревматической лиге рекомендовать включение этого препарата в состав комплексной терапии фибромиалгии. Механизм действия прегабалина при фибромиалгии связывают с воздействием на процессы центральной сенситизации [12, 19].