Как работают бактериофаги
Как работают бактериофаги
о ткрытие пенициллина – первого антибиотика природного происхождения, воспринималось поначалу как шанс раз и навсегда победить инфекционные заболевания, уносившие миллионы жизней. Однако во второй половине прошлого века первоначальная эйфория пошла на убыль: выяснилось, что бактерии благодаря мутациям могут приобретать устойчивость к любому антибиотику и даже обмениваться между собой этими генами. Так началась «гонка вооружений» человека и бактерий.
Между препаратами бактериофагов и химическими антибиотиками существует принципиальное различие: антибиотик, в отличие от фагового препарата, убивает всё на своем пути, включая содружество полезных микроскопических обитателей организма.
Cовместная эволюция бактерий и фагов за последние 3 миллиарда лет привела к тому, что практически для любой болезнетворной бактерии имеется соответствующий вирус-«убийца».
В отличие от обычных антибиотиков, бактериофаги модифицируют свои генетические программы сами, что снимает проблему устойчивости. Результат – высокая избирательность: конкретный бактериофаг обычно эффективен в отношении лишь одного определенного бактериального вида или даже штамма бактерий.
Действие бактериофагов
Очень важным является то, что бактериофаги не трогают не «свои» бактерии, поэтому не вызывают гибель «хорошей» микрофлоры и, конечно, абсолютно безопасны для клеток высших организмов, включая человека.
При фаготерапии отсутствуют побочные эффекты, такие как аллергия, дисбактериоз, вторичные инфекции (например, грибковые), что нередко наблюдается при приеме антибиотиков. Бактериофаги могут применяться в комбинированной терапии с любыми лекарственными препаратами, включая антибиотики.

Препараты бактериофагов представляют собой раствор, используют их либо местно (например, на кожу или слизистые), либо принимают внутрь. В организме бактериофаги концентрируются в местах наибольшего поражения и размножаются до тех пор, пока находят бактерии-«мишени». После того, как бактерии-«мишени» закончились, фаги выводятся из организма.
Главная цель фаготерапии – остановить и повернуть вспять инфекционный процесс, чтобы дать иммунной системе организма возможность справиться с болезнью.
С помощью бактериофагов лечат

Инфекции мочеполовой системы

Инфекции органов дыхания
Инфекции желудочно-кишечного тракта

Ожоговые и раневые инфекции

Трофические язвы

Остеомиелит

Гнойно-воспалительные заболевания кожи и слизистых

Внутрибольничные инфекции
В идеальном случае перед началом лечения у конкретного больного следует выделить болезнетворную бактерию в культуру и подобрать бактериофаг из «коллекции» уже известных бактериальных вирусов.
Бактериофаги: современные аспекты применения
Бактериофаги: современные аспекты применения
Для современной медицины актуальнейшей проблемой является множественная устойчивость бактериальных возбудителей к антибиотикам и, как следствие, — вопрос: чем лечить больных? Резервы создания новых антибиотиков практически исчерпаны. Заболеваемость, вызванная полирезистентными бактериальными штаммами, в т.ч. госпитального происхождения, наносит колоссальный человеческий и экономический ущерб во всех регионах мира. Совершенно закономерно, что в такой ситуации мировая медицинская общественность вновь обратилась к бактериофагам — вирусам бактерий, их естественным врагам и регуляторам популяции. О них мы беседуем с Ольгой Сергеевной Дарбеевой, кандидатом медицинских наук, главным экспертом управления противобактериальных медицинских иммунобиологических препаратов ФГБУ «Научный центр экспертизы средств медицинского применения» Министерства здравоохранения РФ.
— Ольга Сергеевна, что такое бактериофаги? В чем заключается принцип их действия и какими преимуществами обладают по сравнению с антибиотиками?
— Бактериофаги широко распространены в природе — в пресноводных водоемах, морях и океанах, их выделяют из почвы, сточных вод, из клинического материала от больных. Являясь одними из древнейших обитателей Земли, по численности они достигают 10 в 30 фаговых частиц. По характеру жизненного цикла фаги разделяют на вирулентные и умеренные. Истинно вирулентные фаги (строго литические) убивают бактерию-хозяина. Адсорбируясь на поверхности микробной клетки, проникают в ее цитоплазму, где интенсивно размножаются, используя структурные компоненты клетки, и разрушают ее. Далее зрелые фаговые частицы, готовые к новому заражению, разрывают клеточную оболочку, и литический процесс повторяется с новыми бактериальными клетками. Именно вирулентные бактериофаги обладают наибольшим терапевтическим потенциалом, поскольку только они способны уничтожать клетки бактерий-хозяев.
Умеренные фаги способны к интеграции в геном бактерии в виде профага, или размножаются, не вызывая гибели бактерий. В медицине их используют в диагностических целях для внутривидового типирования.
В качестве антимикробных препаратов бактериофаги гораздо старше антибиотиков. Они активно применялись до открытия антибиотиков, которые быстро вытеснили фаги с рынка. Этому способствовали нестабильные результаты лечения фагами, объясняющиеся низким уровнем диагностики, когда они назначались без бактериологического подтверждения диагноза, определения фагочувствительности возбудителя, а также недостаточный уровень знаний о биологии фагов, условиях производства, хранения и применения.
В нашей стране фаготерапия успешно применялась при лечении и профилактике кишечных и гнойно-септических женских инфекций, в том числе, грибковых инфекций, детских инфекций, а также раневых инфекций, фаговые препараты выпускали несколько предприятий, организованных при НИИ вакцин и сывороток.
Сегодня бактериофаги выпускают на предприятиях по производству медицинских иммунобиологических препаратов, где проводится контроль качества на всех этапах производства. В начале 2000-х гг. крупнейшие фаговые производства вошли в состав ФГУП «НПО «Микроген» Минздрава РФ, в итоге остались самые сильные производства — филиалы в Нижнем Новгороде, Перми и Уфе.
Если антибиотики можно назвать тяжелой артиллерией, то бактериофаги — это снайперы, действующие направленно. Разрушая опасные микробы, они не подавляют собственную микрофлору, не обладают токсическим действием, не вызывают развития дисбактериоза или аллергических реакций, стимулируют различные механизмы иммунитета. На литическую активность фагов не влияет наличие резистентности бактерий к антибиотикам.
Если антибиотики вызывают массовую гибель бактерий, что может привести к токсическому шоку, то фаги действуют постепенно. Подчеркну, что бактериофаги не следует считать альтернативой антибиотикам. Они прекрасно сочетаются с антибиотиками при одновременном назначении в качестве дополнительной помощи. Как и в случае с антибиотиками, фаги назначают при наличии чувствительности возбудителя к фаговому препарату. Конечно, если состояние больного позволяет, вместо антибиотиков лучше использовать фаги, но если нужна быстрая помощь — необходимо назначение антибиотика.
Препараты бактериофагов — это стерильные очищенные фильтраты фаголизатов гомологичных видов бактерий, освобожденные от продуктов жизнедеятельности бактерий, эндо—и экзотоксинов, продуктов фаголизиса бактериальной клетки. Фаговые штаммы, входящие в состав препаратов, подобраны против наиболее часто встречающихся возбудителей бактериальных инфекций.
Специфическая направленность бактериофагов отражена в их названии: по составу они делятся на монопрепараты, содержащие вирулентные фаги бактерий одного рода или вида — стафилококковый, стрептококковый (в т.ч. энтерококковый), протейный, псевдомонас аэругиноза (синегнойный), клебсиелл пневмонии, коли, дизентерийный поливалентный, брюшнотифозный, сальмонеллезный гр. АВСДЕ), и комбинированные фаги, в составе которых монопрепараты. К комбинированным относятся: коли-протейный, клебсиелл поливалентный, пиобактериофаги поливалентные (очищенный, комплексный и Секстафаг®) — содержащие бактериофаги стафилококковый, стрептококковый, протейный, псевдомонас аэругиноза (синегнойный), клебсиелл, коли, а также Интести-бактериофаг, содержащий бактериофаги против шигелл, сальмонелл, стафилококков, энтерококков, протея, синегнойной палочки и энтеропатогенной кишечной палочки.
Лечебно-профилактические бактериофаги используют для перорального, наружного, местного, ректального применения, интраназального и конъюнктивального введения, введения в дренированные полости при лечении женских инфекций, в том числе, грибковых инфекций, детских инфекций, а также раневых инфекций.
— Ольга Сергеевна, как применяются бактериофаги в педиатрии?
— О бактериофагах как о наиболее щадящих антимикробных препаратах, не имеющих противопоказаний для назначения, лучше всего знали педиатры. В 1970—1990-е гг. ими активно лечили гнойно-воспалительные и кишечные инфекции новорожденных, детей раннего возраста. Бактериофаги, убирая патогенные бактерии, дают восстановиться нормальной микрофлоре. Сегодня в педиатрии, к сожалению, мало используют бактериофаги. Возможно, это недостатки преподавания в медицинских вузах или слабость отечественных производителей бактериофагов по сравнению с агрессивной политикой продвижения антибиотиков зарубежными фирмами. Однозначно это последствия трудных 1990-х годов, когда отечественная фармпромышленность не могла субсидировать пострегистрационные испытания и популяризацию своих препаратов. Очень хотелось бы, чтобы о бактериофагах больше рассказывали студентам-лечебникам медицинских вузов.
Заведуя лабораторией бактериофагов НИИ стандартизации и контроля медицинских иммунобиологических препаратов им. Л.А. Тарасевича более 20 лет, могу сказать, что мы инициировали и координировали клинические исследования по фаговой тематике в московском регионе. Наша лаборатория контролировала не только качество всех выпускаемых препаратов на соответствие нормативной документации, но и диапазон их действия в отношении возбудителей кишечных и гнойно-септических женских инфекций, в том числе, грибковых инфекций, детских инфекций, а также раневых инфекций из стационаров различного профиля.
Мы помогали производствам в сборе бактериальных штаммов современных возбудителей, в т.ч. для преодоления первичной фагоустойчивости, совместно с клиницистами участвовали в испытаниях новых препаратов. Консультировали клинических микробиологов и врачей, помогали госпитальным эпидемиологам крупных московских стационаров в организации использования бактериофагов для лечения и профилактики ВБИ.
Клиницисты ограничены стандартами лечения больных, а эпидемиологи, видя проблему глобально, могут предложить своему стационару или отделениям использовать фаготерапию и фагопрофилактику, в т.ч. с помощью целевых (для данного стационара) серий фаговых препаратов, адаптированных производителем к местным госпитальным штаммам. Особенность бактериофагов — возможность адаптации к циркулирующим среди населения бактериальным штаммам — возбудителям инфекций. Таким образом, преодолевая их первичную фагоустойчивость, можно создать промышленные серии препарата целевой направленности для этого региона.
Это качество фаговых препаратов неоценимо для решения проблемы госпитальных инфекций, поскольку ЛПУ несут большие потери от внутрибольничных инфекций, вызванных полирезистентными бактериальными возбудителями. По данным российских эпидемиологов, в стране ежегодно заболевают ВБИ около 2,5 млн пациентов и 320 тыс. медработников, а наносимый ими экономический ущерб достигает 5 млрд руб.
За этими цифрами стоят человеческие трагедии, когда развитие инфекций нивелирует результаты сложнейших хирургических операций или мероприятий по выхаживанию новорожденных. Отрадно отметить, что сегодня все чаще стали вспоминать о замечательных отечественных антимикробных препаратах. На состоявшихся в ноябре—декабре 2013 г. 3-м Международном конгрессе по профилактике госпитальных инфекций, 12-м Международном конгрессе детских инфекционистов и ежегодной конференции «Инфекции в онкологии» были представлены доклады по фаготерапии и фагопрофилактике.
Вместе с тем возросший интерес к бактериофагам спровоцировал негативную тенденцию в развитии фаговой проблематики — появление БАДов на их основе (в 2013 г. получено свидетельство о госрегистрации специализированного пищевого продукта) для применения работниками пищевых производств, а также в ЛПУ для профилактики госпитальных инфекций, о чем было сообщено на VI Ежегодном Всероссийском конгрессе по инфекционным болезням. В прениях этого форума, а также 3-го конгресса по госпитальным инфекциям специалисты подвергли сомнению саму идею использования бактериофагов в качестве БАДов, поскольку бактериофаги являются препаратами выбора в антибактериальной терапии и применяются после определения фагочувствительности. Их назначают наиболее ослабленному контингенту — детям раннего возраста и хроническим больным, неподдающимся антибиотикотерапии.
Бесконтрольное применение бактериофагов в виде БАДов может привести к формированию фагоустойчивости возбудителей. Кроме того, после регистрации фаговых БАДов за их качество отвечает только производитель, в отличие от лечебных фагов как лекарственных средств, подлежащих сертификации (каждая выпущенная серия) в аккредитованных экспертных структурах.
В заключение нашей беседы хочу еще раз подчеркнуть биологическую перспективность бактериофагов в роли лечебных препаратов при условии их обоснованного применения.
Что такое бактериофаги
Поделиться:
Инфекционные заболевания были бичом человечества до того момента, как начали появляться антибактериальные препараты. Обычно новую эру связывают с именем Флеминга и пенициллином. Однако на десять лет раньше было сделано открытие, которое, возможно, еще пригодится всем нам в будущем.
Убить убийцу
Говорят, война — это всегда огромный скачок в развитии хирургии. На самом деле не только: военные действия нередко способствовали продвижению онкотерапии и терапии инфекционных болезней.
Читайте также:
Медицина в годы ВОВ
Во время 1-й мировой войны канадский врач Феликс Д’Эррель изучал вспышку дизентерии среди солдат-французов. Это неприятное кишечное заболевание вызывается бактериями рода Shigellа, которых легко можно выделить из стула больных.
Врач заинтересовался случаем одного солдата, который полностью выздоровел, причем раньше, чем появилось улучшение у других, кого начали лечить одновременно с ним. Взяв у него пробы стула, Д’Эррель не обнаружил бактерий — что-то загадочное убило их.
Исследователь отфильтровал свой «материал», пропустив его через фильтр с настолько мелкими порами, что через них не могла бы пройти ни одна бактерия или какие-нибудь частицы испражнений. В полученный раствор врач добавил готовую культуру бактерий, взятых от другого больного, высадил все это в чашку Петри и стал ждать.
Читайте также:
Профилактика и лечение острых кишечных инфекций
Через некоторое время начался рост бактериальной культуры, однако колонии были разорванными — словно что-то неведомое разъедало их изнутри. Взяв мазки из «пустых» областей, Д’Эррель добавил их в «хорошие», здоровые колонии шигелл — и в них тоже образовались пустоты.
Практика, обогнавшая теорию
Поскольку к этому моменту наш соотечественник Дмитрий Ивановский уже открыл вирусы, Д’Эррель предположил, что невидимый глазу убийца бактерий относится именно к ним. Понимая важность своего открытия, исследователь дал вирусам, поражающим бактерии, отдельное имя — бактериофаги.
Увидеть фагов удалось только после изобретения электронного микроскопа, а выяснить, чтó именно происходит при их контакте с бактериями, — и того позже. Поэтому в течение многих лет идея Д’Эрреля отвергалась значительной частью ученых, которым было трудно представить себе вирус, поражающий бактерию, но не причиняющий вреда человеку. К тому же опыты канадца удавалось повторить не всем и не всегда.
Однако врач, не дожидаясь никаких теоретических подтверждений своего открытия, перешел к практике. Он не мог, имея в руках лекарство, видеть умирающих людей — и принялся лечить солдат фаговым раствором. Правда, сперва Д’Эррель убедился в его безвредности традиционным для таких энтузиастов способом: сперва пил бактериофаг, затем впрыскивал себе под кожу.
Естественное против искусственного
Выяснив, что для человека бактериофаг совершенно не опасен, Д’Эррель вылечил многих пациентов, что принесло ему известность. Его исследования даже стали основой для художественного романа «Эрроусмит», позднее экранизированного Голливудом. Фаговые лекарства успешно производились и применялись — но уже в 40-х годах энтузиазм начал угасать.
Причиной этого стало открытие Флемингом пенициллина и появление большого числа антибиотиков. Врачи настороженно относились к идее лечения людей с помощью вирусов, а тут у них появилась альтернатива. Антибиотики — химические вещества, полученные искусственно, — не были живыми и казались медикам более надежными. Фармацевтические компании уловили настроения врачебного сообщества и, прекратив выпуск фагов, принялись множить антибиотики.
Бактериофаги сегодня
В наше время, когда антибиотикорезистентность является глобальной и очень опасной проблемой, бактериофаги снова заинтересовали ученых.
У них есть свои недостатки — например, не просто узкий, а суперузкий спектр действия: каждый фаг «умеет» убивать только один штамм бактерий — даже не вид, а штамм. Из-за этого, кстати, и проваливались регулярно попытки повторить эксперименты Д‘Эрреля: дизентерия в двух разных частях армии, идентичная по симптомам и течению, могла быть вызвана разными «вариантами» шигелл.
Однако эту проблему сегодня может решить постепенное распространение такого диагностического метода, как полимеразная цепная реакция (ПЦР), которая точно определит штамм бактерии.
Бактериофаги не могут проникать через стенку клетки, поэтому они пока бессильны против тех возбудителей, которые паразитируют внутриклеточно. «Пока» — потому что активные исследования в этом направлении, возможно, помогут фагам пробираться в самые потаенные места.
А вот среди плюсов бактериофагов с ходу можно выделить два: во-первых, они совершенно безвредны для человека, поскольку вообще никак не взаимодействуют с его организмом — только с бактериями.
И, во-вторых, бактерий они убивают не всех, а значит, не имеют традиционного недостатка применения антибиотиков — возникновения дисбиоза. Так что сегодня бактериофаги стали перспективной областью — и в каком-то смысле новой надеждой человечества.
Товар по теме: [product strict=»(бактериофаг»](бактериофаг)
Фильтраты фаголизатов бактерий что это
ГОУ ВПО “Первый МГМУ им. И.М. Сеченова” Минздравсоцразвития РФ, Москва
Бактериофаги (от слов “бактерия” и греч. phagos – пожирающий; БФ), или фаги, – специфические вирусы бактерий, вызывающие их лизис (разрушение клеток) или изменяющие их свойства. Они впервые были обнаружены микробиологами Ф. Туортом (1915) в Великобритании и Ф. д’Эрелем (1917) во Франции. Однако изучить их морфологию удалось только после изобретения электронного микроскопа.
Биология бактериофагов
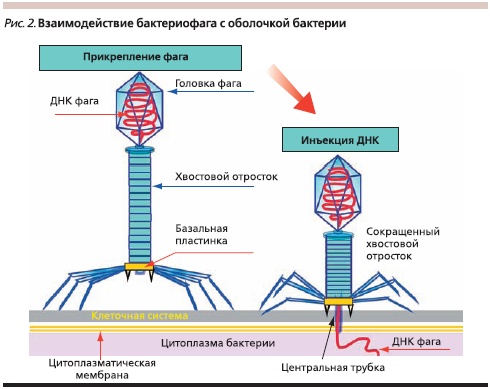
БФ состоят из белка – капсида, защищающего один тип нуклеиновой кислоты (ДНК или РНК, одно или двунитевые). Различают БФ с длинным отростком, имеющие сокращающийся или несокращающийся чехол, а также БФ с короткими отростками, аналогами отростков, без отростков и нитевидные (рис. 1, 2). Размер БФ колеблется от 20 до 800 нм (у нитевидных форм). БФ, имеющие форму сперматозоида, достигают до 200 нм длиной, состоят из хвостового отростка и головки икосаэдрического типа, содержащей нуклеиновую кислоту. Капсид головки и чехол хвостового отростка БФ состоят из полипептидных субъединиц, уложенных по икосаэдрическому (головка) или спиральному (отросток) типу симметрии. Хвостовой отросток имеет внутри полую трубку (стержень), через которую при инфицировании нуклеиновая кислота фага проходит из головки в бактерию. Чехол отростка заканчивается шестиугольной базальной пластинкой с шипами, от которых отходят фибриллы (нити). Базальная пластинка и хвостовые фибриллы участвуют в прикреплении БФ к бактериальной ячейке. Не все БФ имеют базальные пластинки и хвостовые фибриллы. В зависимости от жизненного цикла БФ могут быть вирулентными (литическими) или умеренными.
Вирулентные (литические) БФ для внедрения в бактерию адсорбируются на специфических рецепторах клетки, в т. ч. на липополисахариде, липопротеине, тейхоевых кислотах, протеинах, или даже на пилях. Специфичность рецепторов означает, что БФ может инфицировать только определенные бактерии. Попав в бактерию, БФ репродуцируется, формируя 200–500 фаговых частиц, и вызывает гибель бактерии. Это продуктивный (литический) тип взаимодействия. БФ с сокращающимся чехлом адсорбируются на клеточной стенке с помощью фибрилл хвостового отростка. Чехол хвостового отростка сокращается, и стержень с помощью ферментов (лизоцима) как бы просверливает оболочку клетки. Через канал трубки БФ нуклеиновая кислота инъецируется из головки в бактериальную клетку, а капсид БФ остается снаружи бактерии (рис. 2). Нуклеиновая кислота БФ направляет синтез его ферментов. При этом инактивируются ДНК и РНК хозяина. Нуклеиновая кислота БФ реплицируется и направляет синтез новых белков капсида. Происходят самосборка капсида вокруг фаговой нуклеиновой кислоты и формирование БФ, которые выходят из бактерии в результате ее лизиса, выталкивания или в некоторых случаях почкованием. Из бактерии высвобождается 200–1000 новых БФ, которые инфицируют другие бактериальные клетки.
Умеренные БФ взаимодействуют с бактериями по продуктивному или интегративному типу. Продуктивный тип умеренного фага, как и у вирулентных фагов, заканчивается лизисом бактерий. При интегративном типе ДНК умеренного фага встраивается в хромосому бактерии, реплицируется синхронно с бактериальным геномом, не вызывая ее лизиса (передается при делении бактерии). ДНК фага, встроенная в хромосому бактерии, называется профагом, а культура бактерий – лизогенной, сам процесс – лизогенией (от греч. lysis – разложение, genea – происхождение).
Хромосома умеренного фага лямбда, введенная в бактерию, вызывает либо лизис, либо лизогенизацию (проникшая в бактерию ДНК умеренного фага приобретает форму кольца и интегрирует в строго определенную область хромосомы). Ультрафиолетовое облучение индуцирует литический процесс с выходом фага. При лизогении фаги не образуются в результате “выключения” фаговых генов репрессором, кодируемым одним геном фага.
Профаги могут спонтанно или под действием индуцирующих агентов (ультрафиолетовые лучи, митомицин С и др.) дерепрессироваться, исключаться из хромосомы. Этот процесс заканчивается продукцией фагов (индукцией профага) и лизисом бактерий. Профаг придает бактерии новые свойства, что получило название фаговой конверсии (лат. conversio – превращение). Конвертироваться могут морфологические, культуральные, биохимические, антигенные и другие свойства бактерий. Например, наличие профага в холерном вибрионе обусловливает его способность продуцировать холерный экзотоксин.
БФ применяют для профилактики, лечения инфекций, а также для диагностики (например, для фаготипирования с целью выявления источника инфекции). Кроме того, БФ используют в генной инженерии в качестве векторов, переносящих участки ДНК; возможна также естественная передача генов между бактериями посредством трансдукции.
Фаготипирование – один из методов эпидемиологического маркирования. Применяется для выявления источника инфекции. Выделение бактерий одного фаговара от разных больных указывает на общий источник их заражения. При внутривидовой идентификации бактерий, т. е. при определении фаговара (фаготипа) бактерий с помощью фаготипирования, на чашку Петри с плотной питательной средой, засеянную чистой культурой возбудителя в виде “газона”, наносят капли различных диагностических типоспецифических фагов. Бактерии, чувствительные к фагу, лизируются (образуется стерильное пятно, “бляшка”, или т. н. негативная колония фага).
БФ – уникальное явление; они участвуют в разнообразных процессах:
Получение эффективных лечебно-профилактических БФ связано с тщательным и постоянным поиском штаммов с широким спектром (валентностью) действия на бактерии и высокой степенью их литической активности. Литическая активность и, следовательно, лечебная, а также профилактическая эффективность препаратов БФ зависят от видовой, инфравидовой принадлежности возбудителя, его рецепторных особенностей и факторов его микроокружения. Например, антитела и другие гуморальные белки могут заблокировать участки связывания бактерий с БФ, что исключает возможность парентерального введения последних. Кроме того, возможно быстрое формирование резистентности бактерий к применяемым БФ. Для получения лечебного эффекта при неблагоприятных бактериальных ассоциациях препараты БФ выпускают либо поливалентными, направленными против различных видов и сероваров одного возбудителя, либо комбинированными, содержащими БФ против различных видов возбудителя.
БФ не вызывают побочных реакций, не нарушают нормальную микрофлору. При дисбактериозе, нарушениях функций кишечника, обусловленных развитием местных воспалительных процессов, подавлении резидентной микрофлоры, происходит активация ряда условно-патогенных микроорганизмов и транзиторной микрофлоры. Эти обстоятельства поднимают значимость селективной деконтаминации, проводимой с помощью антибиотиков направленного действия и литических БФ.
БФ, обладая специфичностью действия против определенных возбудителей острых кишечных инфекций, могут также вносить вклад в развитие оральной толерантности. Известно, что организм человека проявляет пероральную (региональную) толерантность к собственной нормальной микрофлоре. Эта толерантность обусловлена блокадой активации сигнальных рецепторов (например, толл-подобных рецепторов – TLR и др.) к компонентам микрофлоры человека и активностью регуляторных T-лимфоцитов (Treg), которых в свою очередь активируют NKT-клетки (natural killer T cells). Компоненты (паттерны) БФ и разрушенных ими бактерий могут активировать определенные сигнальные рецепторы клеток организма, стимулирующие синтез антимикробных пептидов, подавляющих развитие наиболее агрессивных микробов (рис. 3). Срыв оральной толерантности влечет развитие различных нарушений, в т. ч. хронического гастрита, болезни Крона, неспецифического язвенного колита, некротизирующего энтероколита у детей, язвенной болезни желудка и двенадцатиперстной кишки.
Препараты БФ хранят при температуре 2–10 °С в сухом темном месте. БФ чувствительны к ультрафиолетовым лучам; даже их непродолжительное пребывание на свету приводит к утрате литической активности. Для защиты БФ от действия желудочного сока их выпускают в капсулах или таблетках, покрытых кислотоустойчивой оболочкой. Материалом защитного покрытия является нетоксичная целлюлоза, эстерифицированная уксусной и фталевой кислотами, образующая гладкую прозрачную пленку. Для детей из-за проблем проглатывания таблеток используют пектиновое покрытие. Пектин, обволакивая БФ, защищает их от разрушающего действия желудочного сока.
Нормализация микрофлоры, возможное участие БФ в поддержании колонизационной резистентности и оральной толерантности обеспечивают стабилизацию гуморального и клеточного звеньев иммунитета. Изредка применение БФ совпадает с ухудшением качества стула из-за массовой гибели чувствительных к нему бактерий. В этом случае для уменьшения интоксикации целесообразно назначать на ночь энтеросорбент – не ранее 3–4 часов после последнего приема БФ.
Препараты бактериофагов против возбудителей кишечных инфекций
Интести-бактериофаг жидкий содержит стерильные фильтраты фаголизатов шигелл (S. flexneri сероваров 1, 2, 3, 4, 6 и S. sonnei), сальмонелл (S. paratyphiA, S. paratyphiB, S. typhimurium, S. choleraesuis, S. infantis, S. oranienburg, S. enteritidis), энтеропатогенных кишечных палочек наиболее этиологически значимых сероваров (Escherichia coli О111, О55, О26, О125, О119, О128, О18, О44, О25, О20), протея (вульгарис и мирабилис), стафилококков, энтерококков и синегнойной палочки (Pseudomonas aeraginosa). Интести-бактериофаг (Bacteriophagum intestinalis fluidum) представляет собой прозрачную жидкость желтого цвета различной интенсивности.
Препарат предназначен для лечения и профилактики заболеваний желудочно-кишечного тракта, вызванных вышеуказанными бактериями, их сочетанием (в т. ч. бактериальной дизентерии, сальмонеллеза, брюшного тифа, паратифа, дисбактериоза, энтероколита, колита, диспепсии). Его назначают в остром периоде болезни: монотерапия при легких и стертых формах, при бактериовыделении; комбинированная терапия с другими антибактериальными средствами (при среднетяжелом течении) или иммуномодуляторами (при затянувшемся бактериовыделении). Залогом эффективности использования интести-бактериофага является определение фагочувствительности возбудителя и раннее применение препарата, который назначают перорально или ректально при помощи клизмы. Перорально интести-бактериофаг назначают 3–4 раза в сутки натощак за 1,0–1,5 часа до еды в течение 7–10 дней и в разовой дозе: детям до 6 месяцев – 5–10 мл, 6–12 месяцев – 10–15 мл, 1–3 года – 15–20 мл, старше 3 лет – 20 – 40 мл (см. таблицу). Для детей первых месяцев жизни назначенный препарат в первые двое суток разводят кипяченой водой в 2 раза. Если побочные осложнения отсутствуют (срыгивания, высыпания на коже), препарат назначают неразведенным. Перед приемом интести-бактериофага детям старше 3 лет и взрослым назначают раствор питьевой соды (0,5 чайной ложки на 0,5 стакана воды) или щелочную минеральную воду. В отсутствие колитического синдрома препарат назначают ректально 1 раз в день после опорожнения кишечника.
Бактериофаг дизентерийный поливалентный (в таблетках с кислотоустойчивым покрытием и в свечах) содержит стерильные фильтраты фаголизатов шигелл (S. flexneri и S. sonnei). Применяют с 6-месячного возраста для лечения и профилактики бактериальной дизентерии. Для лечения его применяют перорально 3 раза в сутки за час до еды в течение 5–7 дней и в разовой дозе: для детей от 6 месяцев до 3 лет – по 1 таблетке, 3–8 лет – по 1–2 таблетки, старше 8 лет – 2–3 таблетки. При слабовыраженном колитическом синдроме и в период реконвалесценции третий прием БФ внутрь можно заменить его ректальным применением: с 6 месяцев до 3 лет – 20–40 мл, с 3 до 8 лет – 40–60 мл, старше 8 лет – 60–80 мл.
С профилактической целью рекомендуют ежедневный прием препарата в зависимости от возраста: по 10–40 мл или 1–2 таблетки.
Бактериофаг сальмонеллезный групп A, B, C, D, E в таблетках с кислотоустойчивым покрытием, в свечах, жидкий содержит стерильные фильтраты фаголизатов сальмонелл (S. paratyphi A, S. paratyphi B, S. typhimurium, S. heidelberg, S. newport, S. choleraesuis, S. oranienburg, S. infantis, S. dublin, S. enteritidis, S. anatum, S. newlands). Для лечения его применяют перорально 3 раза в день за час до еды в течение 7–10 дней и в разовой дозе: для детей 6–12 месяцев – по 0,5 таблетки; 1–3 лет – по 0,5–1,0; 3–8 лет – по 1,0; старше 8 лет – по 2 таблетке. Третий пероральный прием можно заменить ректальным введением препарата. С профилактической целью БФ назначают детям по 1 таблетке и взрослым по 2 таблетке 2 раза в неделю.
Бактериофаг брюшнотифозный в таблетках с кислотоустойчивым покрытием содержит стерильный фильтрат фаголизата сальмонелл брюшного тифа (S. typhi). Препарат назначают для профилактики брюшного тифа внутрь за час до еды детям от 6 месяцев до 3 лет по 1 таблетке, а старше 3 лет и взрослым – по 2 таблетке 1 раз в 3 дня или каждый день до выздоровления.
Бактериофаг колипротейный жидкий содержит стерильные фильтраты фаголизатов энтеропатогенных (диареегенных) кишечных палочек (Escherichia coli наиболее распространенных серологических групп O20, O26, O33, O44, O55, O111, O119, O26, O124, O125, O127, O151), Proteusvulgarisи Proteusmirabilis. Препарат предназначен для лечения и профилактики заболеваний, вызванных вышеуказанными бактериями, а также дисбактериоза.
Сфера применения других препаратов бактериофагов многообразна; они используются как для местного применения (“раневые” бактериофаги), так и для приема перорально или ректально, в т. ч. в зависимости от формы выпуска:
В заключение следует отметить, что БФ и препараты БФ характеризуются многими положительными сторонами, они:
Информация об авторах:
Быков Анатолий Сергеевич – доктор медицинских наук, профессор кафедры микробиологии,вирусологии и иммунологии ГОУ ВПО “Первый МГМУ им. И.М. Сеченова” Минздравсоцразвития РФ.
Тел. 8 (495) 629-75-79, e-mail: bykov@imail.ru;
Быков Сергей Анатольевич – кандидат медицинских наук, ассистент кафедры клиническойиммунологии и аллергологии ГОУ ВПО “Первый МГМУ им. И.М. Сеченова” Минздравсоцразвития РФ.
Литература
1. Атлас по медицинской микробиологии, вирусологии и иммунологии / 2-е изд. Под ред. А.С. Быкова, А.А. Воробьева, В.В. Зверева. М., 2008. C. 272.
2. Дарбеева О.С., Жиленков Е.Л. Бактериофаги. Общая и санитарная микробиология с техникой микробиологических исследований: учебное пособие / Под ред. А.С. Лабинской, Л.П. Блинковой, А.С. Ещиной. М., 2004. C. 576.
3. Урсова Н.И., Минухина А.М. Бактериофаги. Клинико-иммунологическая эффективность иммунобиологических препаратов / Под. ред. М.П. Костинова, Н.В. Медуницина. М., 2008. C. 256.

 Читайте также:
Читайте также: