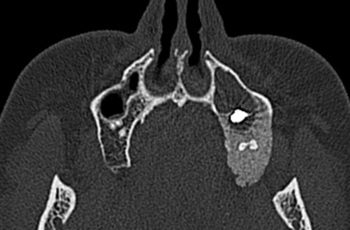
Фиброзная дисплазия. Виды и терапия заболевания
Фиброзная дисплазия – это заболевание костной системы, которое носит опухолевидный характер. Проявляется замещением костной структуры на соединительную ткань и приводит к патологическому развитию кости. Поражаются одна, либо несколько костей.
ДОСТУПНЫЕ ЦЕНЫ НА КУРС ЛЕЧЕНИЯ
Мягко, приятно, нас не боятся дети
ДОСТУПНЫЕ ЦЕНЫ НА КУРС ЛЕЧЕНИЯ
Мягко, приятно, нас не боятся дети
Фиброзная дисплазия – это системное заболевание костной ткани, которое, в основном, поражает костную систему женщин и диагностируется в позднем возрасте, хотя возможны первые проявления болезни и у детей. Дисплазия относится к болезням, которые порождают рак, хотя и не является им изначально, а только преобразуется в него со временем, если не прикладывать усилий по ее ликвидации. В бездействии переходит в состояние доброкачественной опухоли и тогда уже требует совсем иного лечения. Причины дисплазии не установлены, хоть и есть предположения о наследственной предрасположенности, но исследованиями это не подтверждено.
Виды фиброзной дисплазии
Течение болезни может быть острым, либо проходить в стадии ремиссии. Обострения могут происходить несколько раз в год.
Существует несколько видов фиброзной дисплазии, а именно:
В зависимости от того, где находится очаг болезни, она может проявлять себя по-разному, но иметь общие признаки для своего выявления. От вида дисплазии зависит ее течение и тяжесть формы, что влияет на лечение и проявление.
Основные признаки
Фиброзная дисплазия имеет основные симптомы, такие как деформация костного скелета и болезненность. Очень часто не представляется возможным обнаружить болезнь до ее проявления. Патологические переломы являются одними из первых вестников, сигнализирующих о нарушениях в костной системе, и именно при диагностике перелома уже можно обнаружить данный недуг.
При очаговом поражении страдают обычно такие зоны кости:
Могут страдать так же кости головы, лопаток, ребер и позвоночник. Из-за тяжести тела страдают чаще всего ноги, особенно бедро, что проявляется в виде деформаций, укорочения длины ног и как следствие хромота, боль при ходьбе.
При поражении малоберцовой кости не наблюдается никакой деформации, если же поражается большеберцовая кость, то происходит деформация голени, а также ее укорочение. Дисплазия седалищной кости разрушительно влияет на позвоночник, и если к ней добавляются еще очаги фиброзной дисплазии, то процесс искривления становится слишком выражен.
Очаговая форма протекает без выраженных симптомов, не причиняя вред остальным внутренним органам.
При тотальном поражении признаки заболевания дают о себе знать еще в раннем возрасте. В основном на начальном этапе все проходит бессимптомно.
Диагностика
Разнообразие симптомов не дает с точностью определить вид диагностики для постановки диагноза. Поэтому обычно заболевание определяют случайно, в ходе обследования, возможно, по каким- то другим причинам, например перелом ноги, либо же деформация кости или просто недомогание. Однако при обнаружении патологии, более точный диагноз помогает поставить:
Лечение и профилактика
Фиброзная дисплазия развивается еще во внутриутробном состоянии, поэтому лечению не поддается. К тому же не ясно, что становится причиной патологии, некоторые случаи и вовсе не поддаются объяснению. Можно произвести операционное удаление в очаге образования в некоторых случаях, но это существенных результатов может не оказать, либо, только приостановить на какое- то время развитие болезни. Поэтому проводится довольно часто именно ортопедическое лечение, с целью уменьшить проявление патологии. Хирургическое лечение проводится по показаниям врача в особых случаях. Сюда относят:
У детей применяется именно радикальное лечение, с резекцией всего очага патологии и замещением на имплантат. В дальнейшем медикаментозно корректируется рост стимуляцией остеобластов. Профилактические меры не выявлены, так как не выяснена этиология данного заболевания.
Дегенеративные изменения позвоночника
Специалисты ЦМРТ более 15 лет специализируются на диагностике и лечении заболеваний позвоночника. Читайте подробнее на странице Лечение позвоночника.
Дегенеративно-дистрофические заболевания позвоночника проявляются структурными и функциональными изменениями системы элементов позвоночных двигательных сегментов. В процесс могут быть вовлечены межпозвонковые диски, концевые пластины, фасеточные суставы, а в запущенных стадиях — позвоночный канал и спинной мозг. Симптомы вариативны, зависят от локализации, стадии заболевания. Диагностика подразумевает проведение КТ, МРТ. Лечение консервативное, в сложных случаях при деструкции позвонков, образовании грыж — оперативное.
Рассказывает специалист ЦМРТ
Дата публикации: 19 Мая 2021 года
Дата проверки: 30 Ноября 2021 года
Содержание статьи
Причины дегенеративных изменений позвоночника
Дегенеративно-дистрофические изменения позвоночного столба всегда вторичны и являются реакцией на механическую травму или нарушение обмена веществ. Дистрофия позвоночника может быть вызвана метаболическими причинами:
Симптомы дегенеративных изменений позвоночника
Клинические проявления поражения позвоночно-двигательных сегментов многообразны, зависят от отдела позвоночника, вовлечения нервно-сосудистых пучков. Симптомы включают:
Стадии развития дегенеративных изменений позвоночника
Остеохондроз — наиболее часто встречающаяся форма дегенеративного поражения позвоночного столба. На начальной стадии болезни изменения развиваются в пульпозном ядре. Структура утрачивает эластичность, теряет воду, что приводит к травматизации гиалиновых пластинок и прилегающих участков тел позвонков. По мере прогрессирования дегенерации появляются трещины, разрывы пластинок (узелки Шморля) и фиброзного кольца (протрузии и грыжи дисков). Другие компоненты — тела позвонков, связки, суставы — со временем вовлекаются в процесс с развитием остеосклероза.
Суставные поверхности смещаются, постепенно появляются подвывихи фасеточных суставов — остеоартроз (реберно-поясничный артроз). Дистрофические изменения в телах позвонков и последующее разрушение в терминальной стадии заболевания инициируют искривление позвоночного столба, стеноз канала.
Как диагностировать
После оценки жалоб и анамнеза дегенеративные изменения позвоночника подтверждают с помощью тестов визуализации, проводят:
Компьютерную томографию. КТ показывает патологию костных структур:
Магнитно-резонансное сканирование. МРТ визуализирует изменения мягких тканей и помогает обнаруживать:
Нейромиографию. НМГ назначают для исключения неврологической природы симптомов
Фиброз позвоночника что это такое
Синдром оперированного позвоночника
Синдром оперированного позвоночника — длительная или повторяющаяся хроническая боль в нижней части спины и/или в ногах после успешной с анатомической точки зрения операции на позвоночнике.
Сохранение болевого синдрома после хирургической декомпрессии поясничных и крестцовых корешков – достаточно частое явление. Рецидивы боли в спине после хирургического лечения грыж межпозвонковых дисков поясничного отдела позвоночника отмечают от 5 до 38% оперированных больных. На основании послеоперационных ревизий позвоночного канала было высказано предположение, что рецидив болевого синдрома у 36,4% оперированных вызван рубцово-спаечным процессом в эпидуральном пространстве, сдавливающим нервный корешок и сопровождающую его корешковую артерию. А в 28,2% случаев – сочетанием рубцово-спаечного процесса с рецидивом грыжи межпозвонкового диска.
Выделяются хирургические и нехирургические причины синдрома оперированного позвоночника.
К хирургическим причинам синдрома оперированного позвоночника относят:
К нехирургическим причинам относят:
Боль может быть вызвана изменениями практически всех структур позвоночного столба: межпозвонкового диска, синовиального соединения, мышц, связок, крестцово-подвздошного сочленения.
Лечение больных с диагнозом «синдром оперированного позвоночника» зачастую сопряжено с большими трудностями, так как ни консервативная терапия, ни повторные хирургические вмешательства на позвоночнике не дают адекватного уменьшения боли.
Специалистами Центра патологии спинного мозга нашей клиники предлагается наиболее эффективный на сегодняшний день метод лечения этой группы пациентов — эпидуральная стимуляция спинного мозга.
Пройти диагностику и лечение заболевания позвоночника и спинного мозга Вы можете, обратившись к специалистам Центра патологии спинного мозга нашей клиники или записавшись на прием к специалисту – нейрохирургу в любое удобное для Вас время.
Для получения подробной информации и записи на прием обращайтесь к нам по телефону контакт-центра: (495) 925-02-02 (круглосуточно).
Лечение периартикулярных болевых синдромов
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Заболевания мягких околосуставных тканей, или периартриты, – большая группа ревматических синдромов, при которых патологический процесс локализован в сухожилиях, сухожильных оболочках, фасциях, мышечно–сухожильных соединениях, суставных связках, энтезисах, суставных сумках [1,5]. В большинстве случаев эти заболевания сопровождаются хронической локальной болью в области одного сустава, усиливающейся при определенных движениях, связанных с нагрузкой на пораженную структуру. Периартикулярные поражения могут развиваться при многих ревматических заболеваниях, но чаще являются самостоятельным воспалительным или дегенеративным процессом. В отличие от артрита для периартрита характерно несоответствие между активными и пассивными движениями (обычно ограничение активных движений при нормальном объеме пассивных), усиление боли при строго определенных движениях, отсутствие припухлости сустава или локальная припухлость в проекции пораженного сухожилия. Несмотря на стойкий болевой синдром и нарушение функции, лабораторные и рентгенологические изменения отсутствуют [7].
Дегенеративные и воспалительные изменения мягких тканей могут сопутствовать остеоартрозу (ОА) или протекать в виде самостоятельных клинических синдромов. В отличие от ОА периартикулярные поражения часто развиваются в суставах, являющихся «исключениями» для идиопатического ОА: плечевом, локтевом, голеностопном, лучезапястном. В развитии периартикулярных синдромов имеют значение разнообразные факторы, как правило, способствующие перегрузке и микротравматизации пораженных структур:
• ортопедические аномалии;
• гипермобильность суставов;
• избыточная нагрузка;
• травма сустава;
• часто повторяющиеся стереотипные движения в суставе, вызывающие перегрузку и микротравматизацию определенной структуры;
• воспалительные и дегенеративные заболевания суставов.
Периартикулярные поражения составляют обширную группу ревматических заболеваний. Анатомические соотношения околосуставных тканей настолько тесны, что точная топическая диагностика поражения тех или иных структур достаточно сложна. Патологические изменения, первично возникшие в какой–либо одной структуре, распространяются в дальнейшем на прилежащие анатомические образования. Например, тендинит надостной мышцы, как правило, сопровождается субакромиальным бурситом. Тем не менее среди периартритов принято выделять следующие патологические процессы [2,4]:
• теносиновит – воспаление сухожильного влагалища;
• тендинит – воспаление сухожилия;
• бурсит – воспаление синовиальной сумки;
• энтезопатию – воспаление энтезиса – места прикрепления сухожилия или связки к кости или суставной капсуле;
• капсулит – поражение капсулы сустава;
• фасциит, апоневрозит – поражение фасций и апоневрозов;
• миофасциальный болевой синдром – изменения в скелетной мышце и прилегающей фасции.
Известны также генерализованные периартикулярные синдромы как невоспалительной (фибромиалгия), так и воспалительной (ревматическая полимиалгия) природы.
Морфологическая картина при периартрите характеризуется клеточной воспалительной инфильтрацией, выпотом в полость синовиальных влагалищ, дефектами отдельных мышечных фибрилл, очагами некроза, а в поздних стадиях – фиброзом, гиалинозом и обызвествлением [5].
Периартикулярные поражения являются одной из самых частых причин жалоб со стороны опорно–двигательного аппарата среди взрослого населения. Они могут быть локализованы в области любых суставов скелета. Как правило, это крупные суставы, несущие большую двигательную и весовую нагрузку. Основные клинические варианты периартикулярных поражений представлены в таблице 1.
Диагностировать периартикулярные поражения в большинстве случаев несложно. Боль чаще всего хорошо локализована и воспроизводится при простой пальпации соответствующей структуры. Для подтверждения диагноза можно провести дополнительные тесты [2,6]. Например, для подтверждения синдрома запястного канала следует воспроизвести сдавление срединного нерва и дизестезию в зоне его иннервации путем перкуссии по передней поверхности запястья дистальней проксимальной кожной складки (тест Тинеля) или сильного сгибания кисти (тест Фалена). Для подтверждения латерального эпикондилита можно провести тест резистивного активного разгибания: при разгибании кисти против сопротивления возникает боль. Для воспроизведения боли при медиальном эпикондилите можно воспользоваться тестом резистивного активного сгибания: активное сгибание кисти против сопротивления при супинированной руке вызывает боль. Аналогичным образом активные движения против сопротивления используются для определения повреждений вращающей манжеты плеча [7].
Для диагностики околосуставных поражений можно использовать УЗИ, которое позволяет визуализировать отек сухожилий и связок, бурсит, уточнить локализацию изменений, отличить периартрит от артрита.
Степень выраженности болевого синдрома при периартритах может варьировать от незначительной, когда пациент ощущает боль только при нагрузке на пораженные структуры, до выраженной, упорной, длительной боли, торпидной к лечению. Усугубляет прогноз наличие системной соединительнотканной патологии – гипермобильности суставов, сопутствующего астено–депрессивного синдрома.
Лечебные мероприятия при периартикулярных поражениях следует начинать с рекомендации ограничить физическую нагрузку на пораженную конечность. В легких случаях для уменьшения болевого синдрома достаточно не совершать вызывающие боль движения, временно прекратить спортивные тренировки. Целесообразно также применить иммобилизацию пораженной конечности с использованием лонгета. Положительный эффект оказывают также физические методы воздействия на пораженную область: ультразвуковая терапия, магнитотерапия, тепловые процедуры. С успехом применяются при периартритах нестероидные противовоспалительные препараты (НПВП) в виде мазей и гелей. В случае умеренного болевого синдрома этих мероприятий может быть достаточно.
При выраженной боли, связанной с периартикулярным поражением, требуются локальное введение глюкокортикоидов (ГКС) и системное применение НПВП. Прием этих препаратов позволяет быстро уменьшить боль, воспалительный отек околосуставных структур, ускорить восстановление движений в пораженном суставе. При выборе НПВП для лечения периартикулярного болевого синдрома следует учитывать такие параметры препарата, как быстрота и выраженность анальгетического эффекта в сочетании с хорошей переносимостью. Среди неселективных НПВП наиболее переносимыми считаются производные пропионовой кислоты, к которым относится кетопрофен (Фламакс). Этот препарат широко применяется не только в ревматологической практике, но и в хирургии, неврологии для лечения разнообразных болевых синдромов.
Кетопрофен после приема внутрь быстро абсорбируется из желудочно–кишечного тракта (ЖКТ). Он практически полностью (до 99%) связывается с белками плазмы. Кетопрофен уже через 1,5–2 ч достигает максимальной концентрации в плазме крови. В синовиальной жидкости концентрация препарата нарастает более медленными темпами, ее максимальные значения выявляются через 3–6 ч. Фармакологическими достоинствами кетопрофена у больных ревматологического профиля являются хорошее его проникновение в полость сустава и длительное поддержание в ней терапевтических концентраций. Лечебная концентрация кетопрофена в синовиальной жидкости держится в среднем 6–8 ч, но и через 12 ч содержание препарата остается выше, чем в плазме.
Эти данные позволяют с успехом использовать кетопрофен при лечении острых и хронических периартикулярных болевых синдромов. Период полувыведения кетопрофена составляет 1,6–1,9 ч, и это существенно ниже, чем у ряда других НПВП.
Известно, что лекарственные препараты с коротким периодом полувыведения представляют меньший риск для пациентов благодаря быстрой их элиминации в случае возникновения осложнений. Однако после приема 100 мг кетопрофена внутрь его лечебная концентрация поддерживается на протяжении 24 ч. Препарат не обладает кумулятивными свойствами. Как при пероральном, так и при внутримышечном пути введения кетопрофен не взаимодействует с другими препаратами, что имеет определенное значение при ведении больных с коморбидными состояниями.
Кетопрофен метаболизируется в печени и выводится из организма преимущественно почками. Его фармакокинетика не зависит от пола и возраста больных.
Основной механизм противовоспалительного действия кетопрофена, как и других НПВП, связан с торможением активности циклооксигеназы (ЦОГ) – ключевого фермента биосинтеза простагландинов. Возможными точками приложения фармакологической активности НПВП являются также синтез лейкотриенов и цитокинов, образование супероксидных радикалов, высвобождение лизосомальных ферментов, активация клеточных мембран, агрегация и адгезия нейтрофилов, функции лимфоцитов. Кетопрофен обладает «сбалансированной» активностью в отношении ингибиции ЦОГ–1 и ЦОГ–2, при этом он превосходит селективные и специфические ингибиторы ЦОГ–2 по эффективности и лишь незначительно уступает им по безопасности.
Кетопрофен (Фламакс и др.) характеризуется самым быстрым и мощным болеутоляющим эффектом среди НПВП. Его анальгетическая активность существенно выше по сравнению с диклофенаком и индометацином [8]. В реализации этого эффекта принимают участие многие физиологические процессы. Так, кетопрофен обладает отчетливой антибрадикининовой активностью, а брадикинин, как известно, понижает порог восприятия боли в очаге воспаления. Кетопрофен подавляет экспрессию ЦОГ–2 в задних рогах спинного мозга и ЦНС, блокирует болевые рецепторы и предотвращает перевозбуждение ноцицептивных структур. Кроме того, у кетопрофена имеются центральные механизмы регуляции боли: он влияет на таламические центры болевой чувствительности, блокируя синтез простагландинов в таламусе.
Особенностями кетопрофена являются его хорошая переносимость и высокая безопасность, что было отчетливо продемонстрировано во многих контролируемых исследованиях. Серьезные нежелательные явления, которые приводят к отмене препарата, встречаются лишь у 3–4% больных и обусловлены преимущественно воздействием на слизистую ЖКТ. Однако частота язвообразования даже при длительном его применении остается примерно такой же, как и при применении специфического ингибитора ЦОГ–2 – целекоксиба. Быстрая абсорбция в ЖКТ, легкое проникновение в полость сустава и длительное пребывание препарата в синовиальной жидкости снижает риск развития серьезных побочных явлений [9]. По данным мета–анализа зарубежных исследований, в которых принимало участие около 20 000 больных, препарат обладает низким риском развития ЖКТ–осложнений [10]. Такие же данные получены Н.В. Чичасовой и соавт. в клинико–эндоскопическом исследовании [11]. При высокой эффективности препарата частота образования язв верхних отделов ЖКТ в период его многомесячного использования оказалась низкой, не отличающейся от таковой при применении целекоксиба – селективного ингибитора ЦОГ–2. По данным Н.А. Шостак, кетопрофен также был сопоставим по переносимости с селективными ингибиторами ЦОГ–2 по данным анализа историй болезни пациентов, поступивших в стационар с желудочно–кишечным кровотечением [12]. В целом частота развития нежелательных явлений, в том числе гепатотоксических, нефротоксических, кардиотоксических, не превышает аналогичные показатели для селективных НПВП.
Режим дозирования препарата устанавливают индивидуально с учетом выраженности болевого синдрома. При острой боли целесообразно начать лечение с внутримышечного введения препарата в дозе 100 мг 1–2 раза/сут. в течение 2–3 дней. В дальнейшем возможен переход на пероральный прием капсул препарата в максимальной суточной дозе 300 мг.
Таким образом, Фламакс можно использовать в течение достаточно длительного времени для полного купирования болевого синдрома у пациентов с периартикулярными болевыми синдромами разной локализации. Рациональное применение разных форм этого препарата позволяет быстро уменьшить боль и воспаление в пораженных структурах околосуставных тканей.