Лечение фибрилляции и трепетания предсердий
Каковы рекомендации по проведению антитромботической терапии? Как выбрать препарат для профилактической антиаритмической терапии? Фибрилляция предсердий (ФП) — одна из наиболее часто встречаемых в клинической практике тахиаритмий, ее распространенност
Каковы рекомендации по проведению антитромботической терапии?
Как выбрать препарат для профилактической антиаритмической терапии?
Фибрилляция предсердий (ФП) — одна из наиболее часто встречаемых в клинической практике тахиаритмий, ее распространенность в общей популяции колеблется от 0,3 до 0,4% [1]. Выявляемость ФП увеличивается с возрастом. Так, среди людей до 60 лет она составляет приблизительно 1% случаев, а в возрастной группе старше 80 лет — более 6%. Около 50% пациентов с фибрилляцией предсердий в США — лица старше 70 лет, и более 30% госпитализированных в связи с нарушениями ритма сердца составляют больные с этой аритмией [2]. Трепетание предсердий (ТП) — существенно менее распространенная аритмия по сравнению с ФП. В большинстве стран ФП и ТП рассматриваются как разные нарушения ритма и не объединяются общим термином «мерцательная аритмия». На наш взгляд, подобный подход по многим причинам следует признать правильным.
Профилактика тромбоэмболических осложнений и рецидивов фибрилляции и трепетания предсердий
Фибрилляция и трепетание предсердий ухудшают гемодинамику, утяжеляют течение основного заболевания и приводят к увеличению смертности в 1,5-2 раза у больных с органическим поражением сердца. Неклапанная (неревматическая) ФП увеличивает риск ишемического инсульта в 2-7 раз по сравнению с контрольной группой (больные без ФП), а ревматический митральный порок и хроническая ФП — в 15-17 раз [3]. Частота ишемического инсульта при неревматической фибрилляции предсердий в среднем составляет около 5% случаев в год и увеличивается с возрастом. Церебральные эмболии рецидивируют у 30-70% больных. Риск повторного инсульта наиболее высок в течение первого года. Низкий риск инсульта у больных с идиопатической ФП моложе 60 лет (1% в год), несколько выше (2% в год) — в возрасте 60-70 лет. В этой связи у большинства больных с частыми и/или длительными пароксизмами фибрилляции предсердий, а также с ее постоянной формой должна проводиться профилактика тромбоэмболических осложнений. Метаанализ всех исследований по первичной и вторичной профилактике инсультов показал, что риск развития последних непрямые антикоагулянты уменьшают на 47-79% (в среднем на 61%), а аспирин — немногим более чем на 20%. При этом необходимо отметить, что при применении аспирина возможно статистически значимое снижение частоты случаев ишемического инсульта и других системных эмболий только при довольно высокой дозе препарата (325 мг/сут) [4]. В то же время в Copenhagen AFASAK Study [5] количество тромбоэмболических осложнений в группах больных, получавших аспирин 75 мг/сут и плацебо, существенно не отличалось.
В связи с этим больным с ФП, относящимся к группе высокого риска по тромбоэмболическим осложнениям: сердечная недостаточность, ФВ 35% и менее, артериальная гипертензия, ишемический инсульт или транзиторная ишемическая атака в анамнезе и др., — должны назначаться непрямые антикоагулянты (поддержание Международного нормализованного отношения — МНО — в среднем на уровне 2,0-3,0). Больным с неклапанной (неревматической) фибрилляцией предсердий, не относящимся к группе высокого риска, целесообразен постоянный прием аспирина (325 мг/сут). Существует мнение, что больным моложе 60 лет с идиопатической ФП, у которых риск тромбоэмболических осложнений очень низкий (практически такой же, как у людей без нарушений ритма), профилактическую терапию можно не проводить. Проведение антитромботической терапии у больных с ТП, очевидно, должно основываться на учете тех же факторов риска, что и при ФП, так как есть данные, что риск тромбоэмболических осложнений при ТП выше, чем при синусовом ритме, но несколько ниже, чем при ФП [6].
Международные эксперты предлагают следующие конкретные рекомендации по антитромботической терапии различных групп больных с фибрилляцией предсердий в зависимости от уровня риска тромбоэмболических осложнений [7]:
Международное нормализованное отношение должно контролироваться непрямыми антикоагулянтами в начале терапии не реже чем раз в неделю, а в последующем — ежемесячно.
В большинстве случаев больным с рецидивирующей пароксизмальной и персистирующей фибрилляцией предсердий при отсутствии клинических симптомов аритмии или незначительной их выраженности нет необходимости назначать антиаритмические препараты. У таких пациентов проводится профилактика тромбоэмболических осложнений (аспирин или непрямые антикоагулянты) и контроль ЧСС. Если выражены клинические симптомы, требуется противорецидивная и купирующая терапия, сочетающаяся с контролем ЧСС и антитромботическим лечением.
При частых приступах фибрилляции и трепетания предсердий эффективность антиаритмиков или их комбинаций оценивают по клинике, при редких приступах с этой целью проводят ЧПЭС или ВЭМ после 3-5-дневного приема препарата, а при применении амиодарона — после насыщения им. Для предупреждения рецидивов ФП/ТП у больных без органического поражения сердца используются антиаритмические препараты 1А, 1С и 3-го классов. Больным с бессимптомной дисфункцией ЛЖ или симптоматической сердечной недостаточностью, а также, вероятно, со значительной гипертрофией миокарда терапия антиаритмиками 1-го класса противопоказана в связи с риском ухудшения прогноза жизни.
Для профилактики пароксизмов фибрилляции и трепетания предсердий используются следующие антиаритмики: хинидин (кинилентин, хинидин дурулес и др.) — 750-1500 мг/сут; дизопирамид — 400-800 мг/сут; пропафенон — 450-900 мг/сут; аллапинин — 75-150 мг/сут; этацизин — 150-200 мг/сут; флекаинид — 200-300 мг/сут; амиодарон (поддерживающая доза) — 100-400 мг/сут; соталол — 160-320 мг/сут; дофетилид — 500-1000 мкг/сут. Верапамил, дилтиазем и сердечные гликозиды не должны применяться для противорецидивной терапии ФП и ТП у больных с синдромом Вольфа-Паркинсона-Уайта (ВПУ), так как эти препараты уменьшают рефрактерность дополнительного пути предсердно-желудочкового проведения и могут вызвать утяжеление течения аритмии.
У больных с синдромом слабости синусового узла и пароксизмами фибрилляции и трепетания предсердий (синдром брадикардии-тахикардии) имеются расширенные показания для имплантации электрокардиостимулятора (ЭКС). Постоянная электрокардиостимуляция показана таким пациентам как для лечения симптоматической брадиаритмии, так и для безопасного проведения профилактической и/или купирующей антиаритмической терапии. Для предупреждения и купирования приступов ФП И ТП у больных без ЭКС можно использовать антиаритмики 1А класса, обладающие холинолитическим действием (дизопирамид, новокаинамид, хинидин). При гипертрофической кардиомиопатии для профилактики пароксизмов тахиаритмии назначается амиодарон, а для урежения частоты желудочковых сокращений — бета-адреноблокаторы или антагонисты кальция (верапамил, дилтиазем).
Как правило, лечение антиаритмиками требует наблюдения за шириной комплекса QRS (особенно когда используются антиаритмические средства 1С класса) и продолжительностью интервала QT (при терапии антиаритмиками 1А и 3-го классов). Ширина комплекса QRS не должна увеличиваться более чем на 150% от исходного уровня, а корригированный интервал QT не должен превышать 500 мс. Наибольшим эффектом при профилактике аритмии обладает амиодарон [14, 15, 16, 17]. Метаанализ опубликованных результатов плацебо-контролируемых исследований, в которых приняли участие 1465 больных, показал, что применение малых поддерживающих доз амиодарона (менее 400 мг/сут) не вызывает увеличения поражения легких и печени по сравнению с группой плацебо [8]. Отдельные клинические исследования продемонстрировали более высокую профилактическую эффективность препаратов 1С класса (пропафенона, флекаинида) по сравнению с антиаритмиками 1А класса (хинидином, дизопирамидом). По нашим данным, эффективность пропафенона составляет 65%, этацизина — 61% [9, 10].
Выбор препарата для профилактической антиаритмической терапии пароксизмальной и персистирующей фибрилляции и трепетания предсердий
Можно согласиться с мнением, выраженным в международных рекомендациях по ведению больных с фибрилляцией предсердий [7], согласно которому противорецидивную терапию у больных без патологии сердца или с его минимальными структурными изменениями следует начинать с антиаритмиков 1С класса (пропафенона, флекаинида). Добавим к ним отечественные препараты этого же класса (аллапинин и этацизин), а также соталол; они достаточно эффективны и лишены выраженных экстракардиальных побочных действий. Если перечисленные антиаритмики не предотвращают рецидивов ФП/ТП или их использование сопровождается побочными эффектами, нужно переходить к назначению амиодарона и дофетилида. Затем при необходимости применяются препараты 1А класса (дизопирамид, хинидин) или нефармакологические методы лечения. Вероятно, у больных с так называемой «адренергической» ФП можно ожидать большего эффекта от терапии амиодароном или соталолом, а при «вагусной» ФП целесообразно начинать лечение с дизопирамида.
Ишемическая болезнь сердца, особенно при наличии постинфарктного кардиосклероза, и сердечная недостаточность увеличивают риск проявления аритмогенных свойств антиаритмических препаратов. Поэтому лечение фибрилляции и трепетания предсердий у больных с застойной сердечной недостаточностью, как правило, ограничивается использованием амиодарона и дофетилида. Если высокая эффективность и безопасность амиодарона при сердечной недостаточности и ИБС (включая ИМ) доказана достаточно давно, то аналогичные результаты в отношении дофетилида были получены в рамках недавних плацебо-контролируемых исследований DIAMOND CHF и DIAMOND MI [11].
Для пациентов с ишемической болезнью сердца рекомендуемая последовательность назначения антиаритмиков следующая: соталол; амиодарон, дофетилид; дизопирамид, новокаинамид, хинидин.
Артериальная гипертензия, приводящая к гипертрофии миокарда левого желудочка, увеличивает риск развития полиморфной желудочковой тахикардии «torsades de pointes». В связи с этим для предупреждения рецидивов ФП/ТП у больных с повышенным артериальным давлением отдается предпочтение антиаритмическим препаратам, существенно не влияющим на продолжительность реполяризации и интервала QT (1С класс), а также амиодарону, хотя и удлиняющему его, но крайне редко вызывающему желудочковую тахикардию. Таким образом, алгоритм фармакотерапии данного нарушения ритма при артериальной гипертензии представляется следующим: гипертрофия миокарда ЛЖ 1,4 см и более — использовать только амиодарон; гипертрофии миокарда ЛЖ нет или она менее 1,4 см — начинать лечение с пропафенона, флекаинида (иметь в виду возможность применения отечественных антиаритмиков 1С класса аллапинина и этацизина), а при их неэффективности использовать амиодарон, дофетилид, соталол. На следующем этапе лечения (неэффективность или появление побочных действий у вышеперечисленных препаратов) назначаются дизопирамид, новокаинамид, хинидин [7].
Вполне возможно, что при появлении новых результатов контролируемых исследований по эффективности и безопасности антиаритмических препаратов у больных с различными заболеваниями сердечно-сосудистой системы в вышеизложенные рекомендации по профилактике рецидивов пароксизмальной и персистирующей ФП будут внесены изменения, так как в настоящее время соответствующей информации явно недостаточно.
При отсутствии эффекта от монотерапии используют сочетания антиаритмических препаратов, начиная с половинных доз. Дополнением, а в ряде случаев и альтернативой профилактической терапии, как уже было сказано выше, может быть назначение лекарств, ухудшающих АВ проведение и урежающих частоту сокращений желудочков во время пароксизма ФП/ТП. Применение препаратов, ухудшающих проведение в АВ соединении, обоснованно и при отсутствии эффекта от профилактической антиаритмической терапии. При их использовании надо добиваться, чтобы ЧСС в покое составляла от 60 до 80 в минуту, а при умеренной физической нагрузке — не более 100-110 в минуту. Сердечные гликозиды малоэффективны для контроля ЧСС у больных, ведущих активный образ жизни, так как в подобных случаях первичным механизмом урежения частоты желудочковых сокращений является увеличение парасимпатического тонуса. Поэтому очевидно, что сердечные гликозиды могут быть выбраны только в двух клинических ситуациях: если больной страдает сердечной недостаточностью или имеет низкую физическую активность. Во всех остальных случаях надо отдавать предпочтение антагонистам кальция (верапамилу, дилтиазему) или бета-адреноблокаторам. При затянувшихся приступах фибрилляции или трепетания предсердий, так же как и при их постоянной форме, для урежения ЧСС можно использовать комбинации вышеперечисленных препаратов.
Купирование пароксизмов фибрилляции и трепетания предсердий
Первоочередной задачей при приступе тахисистолической формы ФП/ТП является урежение ЧСС, а затем, если пароксизм самостоятельно не прекратится, его купирование. Контроль за частотой сокращения желудочков (урежение до 70-90 в минуту) осуществляется внутривенным введением или пероральным приемом верапамила, дилтиазема, бета-адреноблокаторов, в/в введением сердечных гликозидов (предпочтение отдается дигоксину), амиодарона. У больных со сниженной сократительной функцией ЛЖ (застойная сердечная недостаточность или ФВ менее 40%) урежение ЧСС проводят только сердечными гликозидами или амиодароном. Перед купированием тахисистолических форм фибрилляции и трепетания предсердий (особенно трепетания предсердий) антиаритмиками 1А класса (дизопирамидом, новокаинамидом, хинидином) обязательна блокада проведения в АВ узле, так как упомянутые выше антиаритмические препараты обладают антихолинергическим действием (наиболее выраженным у дизопирамида) и могут существенно увеличить частоту сокращения желудочков.
Учитывая риск тромбоэмболии при затянувшемся пароксизме ФП, вопрос о его купировании должен быть решен в течение 48 часов, так как, если продолжительность приступа ФП превышает двое суток, необходимо назначение непрямых антикоагулянтов (поддержание МНО на уровне 2,0-3,0) в течение 3-4 недель до и после электрической или медикаментозной кардиоверсии. В настоящее время наиболее широко применяются непрямые антикоагулянты, являющиеся производными кумарина: варфарин и синкумар. Если продолжительность ФП неизвестна, использование непрямых антикоагулянтов до и после кардиоверсии также необходимо. Подобная профилактика тромбоэмболических осложнений должна проводиться и при трепетании предсердий.
Для фармакологической кардиоверсии используют следующие антиаритмики:
В международных рекомендациях по кардиопульмональной реанимации и неотложной кардиологической помощи [12] и рекомендациях АСС/АНА/ЕSС по лечению больных с фибрилляцией предсердий [7] отмечено, что купирование пароксизма у больных с сердечной недостаточностью или ФВ менее 40% целесообразно проводить в основном амиодароном. Применение других антиаритмиков должно быть ограничено из-за довольно высокого риска развития аритмогенных эффектов и отрицательного влияния этих препаратов на гемодинамику.
Применение верапамила и сердечных гликозидов противопоказано больным с ФП/ТП и синдромом Вольфа-Паркинсона-Уайта. При наличии последнего ФП/ТП купируют препаратами, ухудшающими проведение по пучку Кента: амиодароном, новокаинамидом, пропафеноном, флекаинидом и др.
Возможно пероральное купирование фибрилляции и трепетания предсердий хинидином, новокаинамидом, пропафеноном, флекаинидом, дофетилидом и др.
Трепетание предсердий (тип 1) может быть купировано или переведено в ФП частой транспищеводной или эндокардиальной ЭКС предсердий. Назначается стимуляция продолжительностью 10-30 сек с частотой импульсов, превышающей на 15-20% частоту предсердных сокращений, т. е. 300-350 (400) импульсов в одну минуту.
Когда ФП/ТП сопровождается тяжелой сердечной недостаточностью (сердечная астма, отек легких), гипотензией (систолическое давление менее 90 мм рт. ст.), нарастанием болевого синдрома и/или усугублением ишемии миокарда, показано немедленное проведение электроимпульсной терапии (ЭИТ).
При фибрилляции предсердий ЭИТ начинают с разряда мощностью 200 Дж, для бифазного тока энергия первого разряда меньше. Если он оказывается неэффективным, последовательно наносят разряды более высокой мощности (300-360 Дж). Трепетание предсердий часто купируется разрядом низкой энергии (50-100 Дж).
Электроимпульсная терапия также может быть выбрана для планового восстановления синусового ритма у больных с затянувшимися пароксизмами ФП/ТП. Медикаментозная кардиоверсия рекомендуется, если ЭИТ невозможна, нежелательна или с ее помощью не удалось восстановить синусовый ритм. При приступе ФП/ТП, продолжающемся более 48 ч, непрямые антикоагулянты перед кардиоверсией можно длительно не применять, если с помощью транспищеводной ЭхоКГ (ТПЭхоКГ) исключено наличие тромбов в предсердиях (в 95% случаев они локализуются в ушке левого предсердия). Это так называемая ранняя кардиоверсия: в/в введение гепарина (увеличение АЧТВ в 1,5-2 раза по сравнению с контрольным значением) или непродолжительный прием непрямого антикоагулянта (доведение МНО до 2,0-3,0) перед кардиоверсией и четырехнедельный прием непрямых антикоагулянтов после восстановления синусового ритма. По предварительным данным АСUТЕ multicentre study [13], частота тромбоэмболических осложнений существенно меньше при использовании ТПЭхоКГ и коротких курсов профилактической терапии гепарином или варфарином (при отсутствии тромба) или более длительном назначении непрямого антикоагулянта (при повторном обнаружении тромба после трехнедельного лечения варфарином) до ЭИТ, чем при традиционной терапии, проводимой «вслепую» непрямыми антикоагулянтами в течение 3-4 недель до и после электрической кардиоверсии, и составляет соответственно 1,2% и 2,9%. У больных, которые не получают антикоагулянты до кардиоверсии, тромбоэмболические осложнения развиваются в 1-6% случаев.
При тяжелых пароксизмах ФП и ТП, рефрактерных к медикаментозному лечению, применяют нефармакологические методы лечения: деструкцию АВ соединения с имплантацией электрокардиостимулятора, «модификацию» АВ соединения, имплантацию предсердного дефибриллятора или специальных электрокардиостимуляторов, радиочастотную катетерную деструкцию пути циркуляции импульса в правом предсердии при ТП и источников эктопической импульсации у больных с очаговой фибрилляцией предсердий, операции «коридор» и «лабиринт».
Литература
1. Kastor J. A. Arrhithmias. Philadelphia: W. B. Saunders company 1994. P.25-124.
2. Bialy D., Lehmann M. N., Schumacher D. N. et al. Hospitalization for arrhithmias in the United States: importance of atrial fibrillation (abstr) // J. Am. Coll. Cardiol. 1992; 19: 41A.
3. Wolf P. A., Dawber T. R., Thomas H. E., Kannel W. B. Epidemiologic assessment of chronic atrial fibrillation and risk of stroke: the Framingham study// Neurology. 1978; 28: 973-77.
4. The Stroke Prevention in Atrial Fibrillation Study Group Investigators. Stroke prevention in atrial fibrillation study: final results//Circulation. 1991; 84: 527-539.
5. Petersen P., Boysen G., Godtfredsen J. et al. Placebo-controlled, randomised trial of warfarin and aspirin for prevention of thromboembolic complications in chronic atrial fibrillation. The Copenhagen AFASAK study // Lancet. 1989; 1: 175-179.
6. Biblo L. A., Ynan Z., Quan K. J. et al. Risk of stroke in patients with atrial flutter // Am. J. Cardiol. 2000; 87: 346-349.
7. ACC/AHA/ESC guidelines for management of patients with atrial fibrillation//Circulation. 2001; 104: 2118-2150.
8. Vorperian V. R., Havighurst T. C., Miller S., Janyary C. T. Adverse effect of low dose amiodarone: a meta-analysis// JACC. 1997; 30: 791-798.
9. Бунин Ю. А., Федякина Л. Ф., Байрошевский П. А., Казанков Ю. Н. Комбинированная профилактическая антиаритмическая терапия этацизином и пропранололом пароксизмальной фибрилляции и трепетания предсердий. Материалы VII Российского национального конгресса «Человек и лекарство». Москва, 2000. С. 124.
10. Семыкин В. Н., Бунин Ю. А., Федякина Л. Ф. Сравнительная эффективность комбинированной антиаритмической терапии пропафеноном, верапамилом и дилтиаземом пароксизмальной фибрилляции и трепетания предсердий. Материалы VII Российского национального конгресса «Человек и лекарство». Москва, 2000. С. 123-124.
11. Sager P. T. New advances in class III antiarrhytmic drug therapy. Curr. Opin. Cardiol. 2000; 15: 41-53.
12. Guidelines 2000 for cardiopulmonary resuscitation and emergency cardiovascular care// Circulation. 2000; 102 (suppl I): I-158-165.
13. Design of a clinical trial for the assessment of cardiversion using transesophageal echocardiography (the ACUTE multicenter study) // Am. J. Cardiol. 1998; 81: 877-883.
14. Бунин Ю. А., Фирстова М. И., Енукашвили Р. Р. Поддерживающая антиаритмическая терапия после восстановления синусового ритма у больных постоянной формой мерцательной аритмии. Материалы 5-го Всероссийского съезда кардиологов. Челябинск, 1996. С. 28.
15. Bunin Y., Fediakina L. Low doses of amiodarone in preventing of paroxismal atrial fibrillation and flutter. International academy of cardiology. 2nd international congress on heart disease. Abstract book of the congress, Washington, USA, 2001.
16. Gold R. L., Haffajec C. I. Charoz G. et al. Amiodarone for refractory atrial fibrillation // Am. J. Cardiol. 1986; 57: 124-127.
17. Miller J. M., Zipes D. P. Management of the patient with cardiac arrhithmias. In Braunwald E., Zipes D., Libby P. (eds). Heart disease. A textbook of cardiovascular medicine. Philadelphia: W. B. Saunders company. 2001. P. 731-736.
Что такое мерцательная аритмия (фибрилляция предсердий)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Меркушин Д. Е., онколога со стажем в 11 лет.
Определение болезни. Причины заболевания
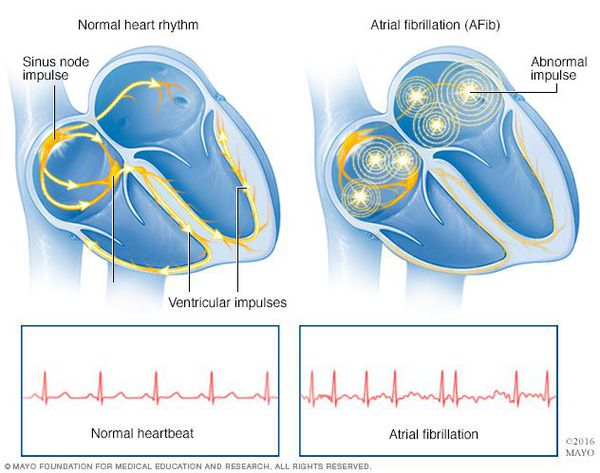
Мерцательная аритмия (фибрилляция предсердий) — нарушение ритма работы сердца, при котором отсутствует механическая систола предсердий и имеет место хаотичная электрическая активность их миокарда, состояние сопровождается нерегулярными сокращениями желудочков и гемодинамическими расстройствами.
Признаки фибрилляции предсердий на ЭКГ:
Распространенность фибрилляции предсердий в общей популяции населения составляет от 1 до 2%.
В большинстве случаев развитие фибрилляции ассоциировано с органической патологией органов сердечно-сосудистой системы, создающих субстрат для сохранения фибрилляции, однако появление данного симптомокомплекса не всегда укладывается в какую-либо нозологическую категорию, в такой ситуации говорят об изолированной фибрилляции предсердий.
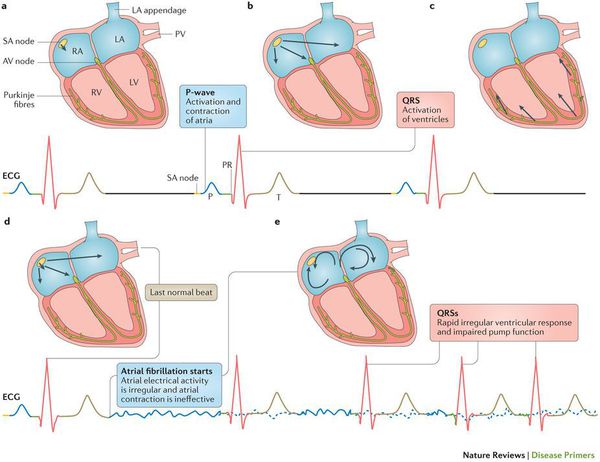
Строение и физиология сердца:
Заболевания, способствующие возникновению мерцательной аритмии
Среди ассоциированных с данной патологией заболеваний выделяют:
Факторы образа жизни, способствующие возникновению мерцательной аритмии
Чем опасна фибрилляция предсердий
Нарушение может приводить к развитию хронической сердечной недостаточности. Непоследовательное сокращение камер сердца способно значимо влиять на гемодинамику. Отсутствие скоординированного сокращения предсердий может снижать сердечный выброс примерно на 10 %. Такое снижение обычно хорошо переносится, кроме случаев с повышением частоты сокращений желудочков, когда ритм становится слишком частым (например, более 140 ударов/минуту) или когда у пациентов исходно имеется пограничный или сниженный сердечный выброс. В таких случаях может развиться сердечная недостаточность.
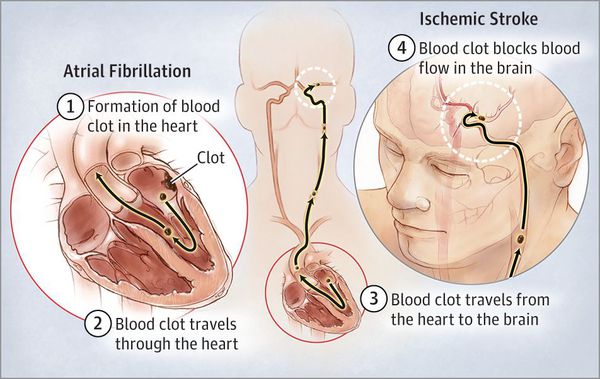
Развитие острого нарушения мозгового кровообращения. Риск развития ишемического инсульта составляет 1,5 % у лиц 50—59 лет и 23,5 % у лиц 80—89 лет. Особенно опасной является пароксизмальная фибрилляция предсердий с частыми срывами синусового ритма. Риск развития тромбоза церебральных сосудов особенно увеличивается в период срыва и восстановления синусового ритма. Выделяют т. н. атеротромботический подтип острого нарушения мозгового кровообращения по ишемическому типу.
Симптомы мерцательной аритмии
При фибрилляции предсердий отсутствует их эффективная механическая систола. При этом желудочки наполняются преимущественно пассивно за счет градиента давления между полостями сердца в период диастолы. В условиях увеличенной частоты сердечных сокращений не происходит достаточного наполнения желудочков, что приводит к гемодинамическим расстройствам различной степени выраженности.
Пациенты предъявляют жалобы на сердцебиение, чувство перебоя в ритме работы сердца, снижение работоспособности, повышенную утомляемость, одышку и сердцебиение при привычной ранее нагрузке. Кроме того, могут усугубляться симптомы уже существующих заболеваний сердечно-сосудистой системы.
Патогенез мерцательной аритмии
Хронические заболевания сердечно-сосудистой системы, а также состояния, характеризующиеся повышенной активностью РААС, вызывают структурное ремоделирование стенок предсердий и желудочков —пролиферацию и дифференцировку фибробластов в миофибробласты, синтез волокон соединительной ткани и развитие фиброза. Процессы ремоделирования камер сердца приводят к неоднородности проведения потенциала действия и к диссоциации сокращения мышечных пучков. При этом нарушается механическая систола предсердий и создаются условия для персистенции этого патологического состояния. [1]
Желудочки производят ненеритмичные сокращения, в итоге кровь задерживается в предсердиях, их объем увеличивается. Уменьшение наполнения желудочков, их частое сокращение, а также отсутствие эффективного сокращения предсердий могут приводить к снижению сердечного выброса и выраженным гемодинамическим расстройствам.
Из-за того, что кровоток в предсердиях замедляется из-за нарушения их механической систолы, а также из-за турбулентного перемешивания крови образуются тромбы, преимущественно в ушке левого предсердия.
Классификация и стадии развития мерцательной аритмии
Клинически различают несколько форм мерцательной аритмии, в зависимости от которых определяется тактика ведения пациента:
| Форма мерцательной аритмии | Описание |
|---|---|
| Впервые выявленная фибрилляцию предсердий | любой впервые возникший эпизод фибрилляции независимо от его причин и длительности |
| Пароксизмальная форма | периодические эпизоды фибрилляции предсердий длительностью до 7 суток с самопроизвольным прекращением |
| Персистирующая форма | эпизоды продолжительностью более 7 суток без самопроизвольного прекращения |
| Длительно персистирующая форма | эпизоды фибрилляции предсердий длятся более 1 года |
| Постоянная форма | присутствует постоянно |
В зависимости от присутствия искусственного клапана и поражений клапанного аппарата выделяют клапанную и неклапанную форму мерцательной аритмии.
Осложнения мерцательной аритмии
Чем опасна фибрилляция предсердий:
Таким образом, наблюдается тесная связь мерцательной аритмией с инсультом и сердечной недостаточностью.
Диагностика мерцательной аритмии
Обязательный минимум диагностики включает:
Могут применяться дополнительные методы обследования:
Лечение мерцательной аритмии
Экстренная помощь пациентам с острым приступом мерцательной аритмии
При впервые возникшем эпизоде фибрилляции предсердций каждому пациенту показана госпитализация в стационар круглосуточного пребывания. Госпитализация также показана пациентам с длительностью приступа более 24 часов.
Некоторой части пациентов с нечастыми пароксизмами фибрилляции предсердий допустимо самостоятельно принимать от 450 до 600 мг. Пропафенона однократно (терапия “таблетка в кармане”). Стоит отметить, что такой подход допустим лишь в случае эффективности и безопасности, проверенной при госпитализации.
Как вести себя в случае эпизода нарушения ритма
При возникновении одышки, головокружения, потере сознания, давящей боли за грудиной на фоне приступа самому пациенту или сопровождающему обязательно необходимо вызвать бригаду неотложной помощи.
Целями лечения мерцательной аритмии является:
Профилактика рисков формирования тромбов
Первостепенной задачей терапии фибрилляции предсердий является профилактика тромбососудистых осложнений.
При наличии патологии со стороны венозной системы нижних конечностей пациент должен быть проконсультирован сосудистым хирургом.
Чтобы снизить готовность тромбов к тромбообразованию, применяются прямые и непрямые антикоагулянты.
Показания для антикоагулянтной терапии и выбор препарата определяются риском тромбоэмболии, который рассчитывают по шкале CHADS2. Если сумма баллов по шкале CHADS2 ≥ 2, то при отсутствии противопоказаний показана длительная терапия пероральными антикоагулянтами. Однако антикоагулянтная терапия опасна кровотечениями. Для оценки риска данного осложнения разработана шкала HAS-BLED. Сумма баллов ≥ 3 указывает на высокий риск кровотечения, и применение любого антитромботического препарата требует особой осторожности.
К антикоагулянтам непрямого действия относится антагонист витамина К варфарин. Препарат относится к группе антиметаболитов и нарушает синтез в печени X фактора свертывания.
К прямым антикоагулянтам относят гепарин и низкомолекулярные препараты гепарина (фраксипарин, эноксапарин и др.). Перевод пациентов с непрямого антикоагулянта на прямой рекомендован при необходимости хирургического лечения в связи с удобством коррекции терапевтического диапазона дозы.
К новым непрямым антикоагулянтам относят препараты прямые ингибиторы тромбина (дабигатран) и ингибиторы Xа фактора свертывания крови (препараты из группы ксабанов — апиксабан, ривароксабан, эдоксабан). Препараты обладают эффективностью, сопоставимой с приемом варфарина при минимуме гемморагических осложнений. Доказательная база у препаратов существует на данный момент только по проблеме неклапанной фибрилляции предсердий. Эффективность препаратов относительно клапанной фибрилляции предсердий в настоящее время является предметом клинических исследований. Поэтому при наличии врожденной и приобретенной патологии клапанного аппарата и наличии искусственного клапана сердца единственным препаратом из группы антикоагулянтов по-прежнему остается варфарин.
Восстанавливать или не восстанавливать синусовый ритм
Выбор стратегии ведения проводится индивидуально. Учитывается возраст пациента, выраженность симптомов фибрилляции предсердий, наличие структурной патологии миокарда, физическая активность.
Удержание стабильного сердечного ритма
Длительная терапия фибрилляции предсердий предполагает выбор стратегии — поддержания синусового ритма или контроля частоты сокращений сердца.
При пароксизмальной фибрилляции возможно рассмотреть тактику поддержания синусового ритма.
При персистирующей и постоянной форме, пожилом возрасте, низкой физической активности и удовлетворительной субъективной переносимости фибрилляции большинство специалистов склоняются к тактике контроля ЧСС, т. к. восстановление синусового ритма и его последующий срыв сопровождаются изменениями реологических свойств крови и повышенным риском внутрисосудистого тромбообразования, а тактика поддержания синусового ритма не улучшает отдаленный прогноз у пациентов.
Контроль ЧСС
Стратегия контроля частоты сердечных сокращений предполагает регулярный прием частотоурежающих препаратов из группы сердечных гликозидов, бета-адреноблокаторов, блокаторов Са++ каналов и антиаритмиков III класса (амиодарон, дронедарон), а также используются их комбинации.
При подборе препаратов важно знать, есть ли у пациента трепетание предсердий. Это нарушение часто сочетается с фибрилляцией. Если доктор не учтёт это сочетание при подборе терапии, препараты будут воздействовать только на фибрилляцию, а трепетание сохранится. Это чревато развитием сердечной недостаточности: трепетание приводит к нему быстрее, чем фибрилляция.
Сегодня не существует точного ответа на вопрос о целевом уровне ЧСС при фибрилляции предсердий. Клинические и методические рекомендации основаны на мнении экспертов в области кардиологии.
Первоначально рекомендуется снизить частоту сокращения желудочков до уровня менее 110 ударов в покое и при физической нагрузке. Если урежение частоты сокращения желудочков не приводит к исчезновению ограничений физической активности, то целесообразно снизить частоту их сокращений до 60-80 в покое и 90-115 в минуту при физической нагрузке.
Из бета-адреноблокаторов применяются:
Среди недигидроперидиновых антагонистов Са++ назначают:
Из антиаритмиков III класса используют:
Имеются клинические данные об эффективности омега-3 полиненасыщенных жирных кислот в комплексной терапии фибрилляции предсердий, в частности эйкозапентаеновой и докозагексаеновой. По данным многоцентровых плацебо-контролируемых клинических исследований FORWARD и OPERA, доказано влияние омега-3 полиненасыщенных жирных кислот на снижение риска внезапной смерти и общую летальность пациентов, имеющих хроническую сердечную недостаточность, и пациентов, перенесших острый инфаркт миокарда. [3]
По данным исследования GISSI-Prevenzione, назначение омега-3 полиненасыщенных жирных кислот позволяет снизить рецидивы фибрилляции предсердий уже через 3 недели от старта терапии. Максимальный эффект наблюдается через год непрерывного приема препарата. [4]
Стратегия контроля синусового ритма не исключает стратегию контроля частоты сердечных сокращений. Уменьшение частоты желудочковых сокращений до целевого уровня позволяет уменьшить клиническую симптоматику фибрилляции предсердий во время неизбежных срывов ритма работы предсердий.
Тактика контроля ритма не имеет существенного преимущества перед тактикой контроля частоты сокращений сердца в плане прогноза сердечно-сосудистой смертности, однако значительно уменьшает выраженность клинической симптоматики, возникающей при данном заболевании.
Препараты для восстановления синусового ритма
Для поддержания синусового ритма при фибрилляции предсердий рекомендуется применение следующих препаратов:
При развившемся пароксизме фибрилляции предсердий синусовый ритм восстанавливается спонтанно самостоятельно в течение нескольких часов или суток (до 7 суток).
При выраженной клинической симптоматике заболевания, а также если в дальнейшем будет выбрана стратегия поддержания синусового ритма, необходима медикаментозная кардиоверсия.
Для профилактики тромбососудистых осложнений пациенту предлагается прием 500 мг. ацетилсалициловой кислоты (кишечнорастворимую таблетку необходимо разжевать перед приемом) или 2 тб. (150 мг) клопидогрела.
Электрическая кардиоверсия
Электрическая кардиоверсия постоянным током быстро и эффективно переводит фибрилляцию предсердий в синусовый ритм. Предпочтение данному виду восстановления синусового ритма отдается при нестабильной гемодинамике (нарастающим симптомам хронической сердечной недостаточности) и появлению ишемии миокарда по ЭКГ/ЭХО-КС.
Радиочастотная катетерная абляция
Данные о выполнении радиочастотной абляции в терапии первой линии у пациентов с фибрилляцией предсердий остаются противоречивыми, в то время как у пациентов с рецидивирующей фибрилляцией эта процедура является максимально оправданной и эффективной.
Выявлены неблагоприятные факторы, увеличивающие частоту рецидивов после проведения данной процедуры : дилатация левого предсердия, возраст старше 65 лет, длительность заболевания, количество ранее проведенных процедур, а также недостаточность аортального и митрального клапанов.
Виды оперативного вмешательства при мерцательной аритмии
При мерцательной аритмии применяются хирургические методы лечения. Одним из вариантов является операция типа «лабиринта» Кокса. Суть операции заключается в изоляции задней стенки левого предсердия, каватрикуспидального и кавакавального перешейка и исключение из кровотока устья левого предсердия. Таким образом, операция создает электрический лабиринт ходов для распространения возбуждения, через которые импульс из синоатриального узла находит путь к предсердножелудочковому узлу, предотвращая формирование волн «re-entry». Операции типа “лабиринт” Кокса в основном использовались у пациентов, подвергающихся другим открытым операциям на сердце. Выполнение подобных сочетанных операций при мерцательной аритмии приводит к уменьшению рецидивов фибрилляции, трепетания предсердий и предсердных тахикардий, однако не влияет на общую смертность. Отбор пациентов на подобные методы хирургического лечения должен осуществляться на мультидисциплинарном консилиуме специалистов.
Хирургическая изоляция ушка левого предсердия выполнялась кардиоторакальными хирургами в течение нескольких десятилетий, однако проспективные рандомизированные исследования влиянии на частоту развития ишемического инсульта у пациентов после хирургического лечения в настоящее время отсутствуют.
Прогноз. Профилактика
Пароксизмальная и персистирующая формы фибрилляции предсердий могут оказаться, поводом для освобождения от труда с выдачей листка нетрудоспособности. Ориентировочный срок для освобождения от труда с целью купирования приступа — 7-10 дней; для подбора противорецидивной терапии требуется в среднем от 7 до 18 дней. [6] Критериями закрытия листка временной нетрудоспособности являются: