Фето фетальный синдром что
Частота сопутствующих ВПС в этой группе детей значительно превышает среднюю в популяции, составляя около 7%. Особенно высока выявляемость пороков среди близнецов-реципиентов (12%); наиболее частым из них является легочный стеноз (4,8—9,6%).
Естественное течение синдрома фето-фетальной трансфузии.
До 90% беременностей заканчиваются преждевременными родами. В 25% случаев один из близнецов (чаще донор) погибает внутриутробно. Еще 10% умирают вскоре после рождения. Более половины родившихся детей нуждаются в искусственной вентиляции легких. У 13% имеются внутрижелудочковые кровоизлияния III—IV степени или перивентрикулярная лейкомаляция. У близнецов-доноров в 10% случаев развивается почечная недостаточность, приводящая к смерти около 60% из них.
Среди выживших детей высок процент поражений центральной нервной системы (задержка речи и умственного развития, детский церебральный паралич).
Выраженная гипертрофия миокарда в выводном отделе правого желудочка может приводить к снижению потока крови через желудочек и легкие, что сопровождается нарушением их развития и прогрессированием легочного стеноза вплоть до атрезии клапана.
Клиническая симптоматика синдрома фето-фетальной трансфузии.
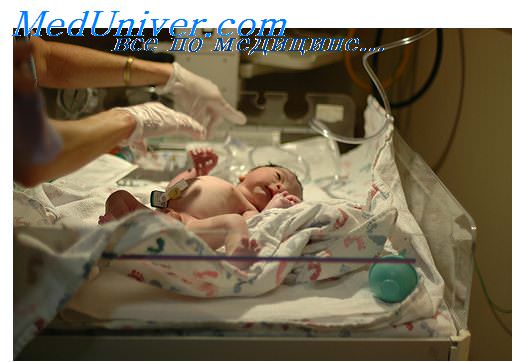
У новорожденного, перенесшего синдром фето-фетальной трансфузии в качестве донора, можно отметить бледность, тахикардию, нарушения периферической циркуляции. Тяжесть состояния близнеца-реципиента в большинстве случаев бывает обусловлена полицитемией, гипербилирубинемией, сердечной недостаточностью. Разница в массе тела между новорожденными превышает 15%. При внутриутробной гибели одного из близнецов у выжившего ребенка высока опасность развития ДВС-синдрома и почечной недостаточности.
У новорожденных с синдромом фето-фетальной трансфузии нередко выявляется артериальная гипертензия. Причиной этого у бывших доноров может быть активация ренин-ангиотензиновой системы в ответ на хроническую гипово-лемию. Причиной гипертензии у реципиентов может быть повышение в плазме уровня эндотелина-1 — потенциального сосудосуживающего вещества. Так как увеличенный уровень ренина может передаваться от донора к реципиенту, это вносит дополнительный вклад в дисфункцию сердечно-сосудистой системы у последнего.
Лечение синдрома фето-фетальной трансфузии.
Основная терапия проводится во внутриутробном периоде. В качестве вариантов лечения используют периодический декомпрессионный амниоцентез, создание сообщения между оболочками, лазерную фотокоагуляцию плацентарных анастомозов, перевод беременности в моноплодную. Это позволяет повысить выживаемость для отдельных плодов до 65—90%.
При лечении близнецов-доноров используют 10% раствор глюкозы, эритроцитарную массу и препараты железа. Близнецам-реципиентам показаны заменные переливания свежезамороженной плазмы для снижения гематокрита.
Артериальная гипертензия новорожденных и легочный стеноз лечатся по соответствующим принципам.
— Вернуться в оглавление раздела «Кардиология.»
Фето-фетальный трансфузионный синдром ( Синдром фето-фетальной трансфузии )
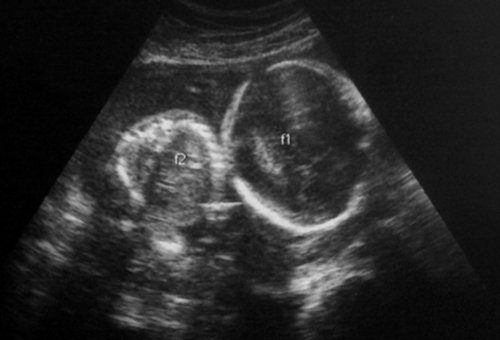
Фето-фетальный трансфузионный синдром (ФФТС) – это тяжелое осложнение многоплодной монохориальной беременности, при которой из-за анастомозов в сосудистой сети плаценты возникает дисбаланс кровотока у плодов. Проявлениями служит диспропорциональность развития близнецов, многоводие в пузыре «рецепиента» при маловодии у «донора», ряд серьезных пороков развития обоих плодов, их внутриутробная гибель. Диагностика производится на основании картины ультразвуковых исследований, эхокардиографии и допплерографии, выполняемых обычно во второй половине беременности. Для сохранения беременности осуществляют лазеркоагуляцию плацентарных анастомозов, периодическое амниодренирование, окклюзию пуповины более пострадавшего плода для сохранения другого.
МКБ-10
Общие сведения
Причины
Морфологической предпосылкой для развития фето-фетального трансфузионного синдрома является наличие в хорионе анастомозов между сосудистыми сетями обоих плодов. При монохориальной беременности они выявляются в 60-90% и могут быть поверхностными и глубокими. Поверхностные вено-венозные и артерио-артериальные анастомозы способны транспортировать кровь в обоих направлениях (в зависимости от давления) и выравнивают объемы крови между близнецами. Строение глубоких анастомозов таково, что артериальная кровь, поступающая в котиледон плаценты из системы одного ребенка, переходит в венозную сеть другого. Предполагается, что превалирование количества глубоких сосудистых соединений в хорионе над числом поверхностных и становится причиной появления синдрома.
Факторы, приводящие к возникновению большего количества глубоких анастомозов, на сегодняшний момент неизвестны. Предполагается, что они возникают из-за патологии формирования плаценты «донора», в результате чего сосудистое сопротивление в ней растет, и формируются шунты, связывающие его с сосудами «реципиента». Обсуждается возможность влияния позднего разделения близнецов, тератогенных факторов, недостаточного кровоснабжения матки женщины. Выяснение точных причин ФФТС осложняется поздней диагностикой этого состояния и непредсказуемостью его появления.
Патогенез
Считается, что возникновение фето-фетального трансфузионного синдрома может произойти на разных сроках вынашивания, причем позднее возникновение осложнения благоприятней в прогностическом отношении. Иная точка зрения заключается в том, что предпосылки для ФФТС возникают еще на этапе разделения плодов (4-12 дни гестации), а выраженность и срок появления дальнейших нарушений зависит от количества глубоких анастомозов и степени дисбаланса кровообращения близнецов. Первоначально возникает простой переток крови от «донора» к «реципиенту», который не отражается на скорости развития и других характеристиках обоих плодов.
Уменьшение объема циркулирующей крови у близнеца-донора постепенно приводит к явлениям плацентарной недостаточности – внутриутробной гипоксии, задержке развития. Нарушается работа почек и снижается выделение мочи, что становится причиной уменьшения объемов мочевого пузыря и появления маловодия. Последний фактор оказывает влияние на скорость развития тканей легких, замедляя формирование дыхательной системы. При отсутствии лечения происходит внутриутробная гибель плода по причине гипоксии и тяжелого недоразвития основных органов и систем.
Классификация
Выделяют несколько степеней развития фето-фетального трансфузионного синдрома, основываясь на тяжести состояния плодов и разнице их основных показателей (КТР, объем околоплодных вод). По мере прогрессирования ФФТС нарушения беременности нарастают таким образом, что каждая стадия включает в себя патологии всех предыдущих этапов заболевания. Современная классификация выделяет пять стадий развития синдрома:
Стадийность ФФТС не имеет четкой привязки к сроку беременности – при неблагоприятном и раннем развитии осложнения признаки 1-й стадии могут выявлять на 14-17 неделе. В акушерстве при синдроме считается важной границей срок в 25 недель гестации, так как появление нарушений ранее часто приводит к прерыванию беременности даже при лечении. Нередко принимается решение о сохранении только одного (более жизнеспособного) ребенка, тогда врачебное вмешательство может производиться в ущерб его близнецу.
Симптомы
Субъективных проявлений ФФТС не имеет, его обнаруживают при скрининговых ультразвуковых исследованиях. Беременные с такой патологией чаще, чем в норме, имеют гипертонус матки и другие состояния, угрожающие прерыванием вынашивания ребенка. Ряд исследователей допускает, что значительная часть самопроизвольных абортов при многоплодной беременности обусловлена ФФТС до его обнаружения. Осложнения патологии (внутриутробная смерть) могут проявляться болью в животе и груди, профузным маточным кровотечением либо появлением кровянистых выделений из влагалища. На поздних сроках признаком гибели близнецов является прекращение их движений (замирание).
Осложнения
Диагностика
Обнаружение ФФТС происходит при плановом УЗИ беременной, уже при выявлении монохориальной многоплодной беременности женщина вносится в группу риска. УЗИ-признаки заболевания обнаруживаются после 16-й недели (крайне редко – после 11-12-й), затем для подтверждения диагноза и мониторинга состояния плодов назначают дополнительные методы исследования. С их помощью определяют прогностические перспективы фето-фетального трансфузионного синдрома и собираются данные для возможного лечения.
Лечение ФФТС
Консервативное лечение ангиопротективными средствами и препаратами для коррекции микроциркуляции признано неэффективным и может использоваться только в качестве вспомогательной терапии. Аналогичной позиции специалисты придерживаются и в отношении гормональных (препараты прогестерона) и других лекарств, использующихся в акушерстве для сохранения беременности. Увеличивают выживаемость как минимум одного близнеца только методы фетальной хирургии:
Прогноз
Фето-фетальный трансфузионный синдром характеризуется неблагоприятным прогнозом – при отсутствии лечения и регулярного наблюдения у акушера-гинеколога это состояние практически всегда приводит к гибели плодов и самопроизвольному прерыванию беременности. Результативность хирургического вмешательства зависит от многих факторов: стадии развития ФФТС, срока беременности, наличия или отсутствия сопутствующих патологий у женщины. Довольно часто лечебные меры приходится производить в ущерб более пострадавшему ребенку для сохранения другого. Профилактика развития синдрома не разработана, так как неизвестны причины его возникновения.
Ультразвуковые и допплерографические критерии диагностики вариантов фето-фетальной трансфузии и селективной задержки роста одного из монозиготных близнецов
УЗИ сканер WS80
Идеальный инструмент для пренатальных исследований. Уникальное качество изображения и весь спектр диагностических программ для экспертной оценки здоровья женщины.
Введение
Хронический ФФТС необходимо дифференцировать с другими патологическими состояниями монозиготной многоплодной беременности, встречающимися реже: острой межблизнецовой трансфузией (ОМТ) и селективной задержкой роста (CЗР) одного из плодов. Несмотря на ряд схожих клинических проявлений, эти состояния имеют прогноз, отличный от прогноза при хроническом тяжелом ФФТС, требуют иной терапевтической тактики.
Хроническая форма ФФТС проявляется с середины II триместра гестации, имеет тяжелое течение, сопряжена с резко выраженным гемодинамическим дисбалансом между циркуляторными системами плодовблизнецов [9]. Клинически в течении хронического ФФТС различают 5 стадий (таблица). Критериями, на основании которых дифференцируется клиническая стадия синдрома, являются ультразвуковые и допплерографические изменения [10].
| Ультразвуковые критерии | Клиническая стадия ФФТС | ||||
|---|---|---|---|---|---|
| I | II | III | IV | V | |
| Полиолигогидрамнион | + | + | + | + | + |
| Мочевой пузырь донора | + | — | — | — | — |
| Патологические допплерограммы | — | — | + | + | + |
| Водянка реципиента | — | — | — | + | + |
| Внутриутробная гибель плода (плодов) | — | — | — | — | + |
Селективная задержка роста одного из близнецов (дискордантный рост монозиготных близнецов) характеризуется отставанием роста одного из плодов [15]. При этом межблизнецовая трансфузия незначительна либо отсутствует, патогенез нарушений связан преимущественно с проявлениями плацентарной дисфункции, либо функциональной патологией плода. Терапевтическая тактика в большинстве таких случаев выжидательноконсервативная [16]. При остром нарушении плацентарно-плодового кровообращения возможна антенатальная гибель одного из плодов-близнецов. В подобном случае показана фетоскопическая лазерная коагуляция его пуповины. При наличии соответствующего гестационного срока и адекватной перинатальной тактике прогноз для жизни и здоровья второго плода может быть благоприятным.
Очевидной представляется невозможность клинической диагностики ФФТС на антенатальном этапе без применения серийных ультразвуковых и допплерографических исследований.
Целью работы явилось выявление последовательности ультразвуковых и допплерографических изменений на разных стадиях некорригированного хронического ФФТС, при острой межблизнецовой трансфузии и селективной задержке роста одного из монозиготных близнецов.
Материалы и методы
Проведен сравнительный анализ перинатальных исходов, а также результатов патоморфологических исследований последов.
Результаты и обсуждение
У двух из 3 женщин с хроническим ФФТС имелись указания на наличие в анамнезе пороков развития плода, перинатальных потерь и преждевременных родов. Средний возраст женщин составил 27,8±0,8 лет.
На рис. 1-12 представлены ультразвуковые и допплерографические признаки разных клинических стадий тяжелой формы хронического прогрессирующего ФФТС.
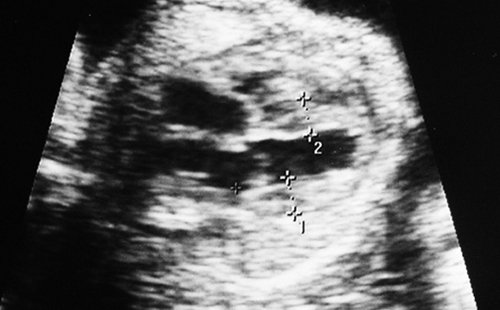
Рис. 1. Двуплодная монохориальная беременность, гестационный срок 25 нед. Выраженно дискордантный рост плодов: поперечное сечение туловища плода-донора (слева), аксиальное сечение головы плода-реципиента (справа). Отставание фетометрических показателей меньшего плода более чем на 3 SD.
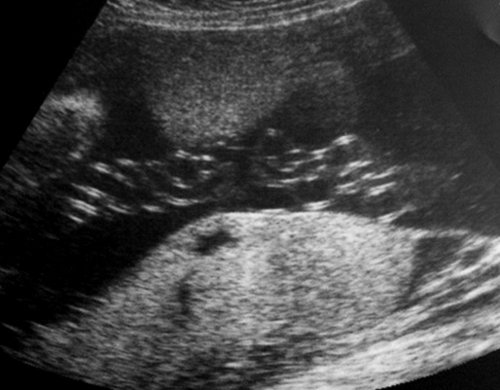
Рис. 3. Плод-реципиент, имеющий нормальные для срока гестации размеры.
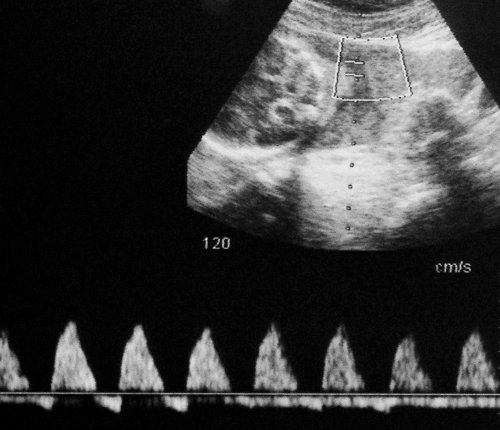
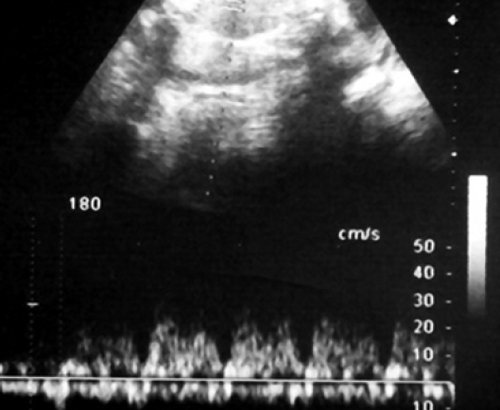
Рис. 5. Длительно регистрируемый постоянный нулевой диастолический кровоток, эпизоды реверсного диастолического кровотока в пуповинных артериях плода-донора. III стадия фето-фетального трансфузионного синдрома.
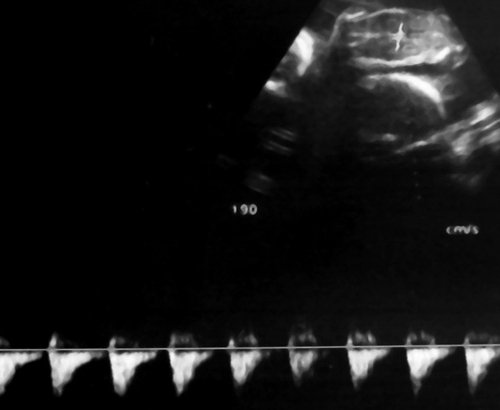
Рис. 6. Длительно регистрируемый нулевой диастолический кровоток в аорте близнеца-донора. Отсутствует визуализация мочевого пузыря плода.
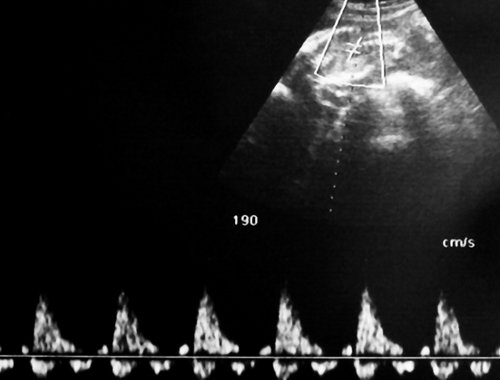
Рис. 7. Реверсный диастолический кровоток в торакальной аорте близнеца-донора. В условиях фето-фетальной трансфузии спектры, характерные для терминальной фетальной гемодинамики, могут регистрироваться до нескольких недель.
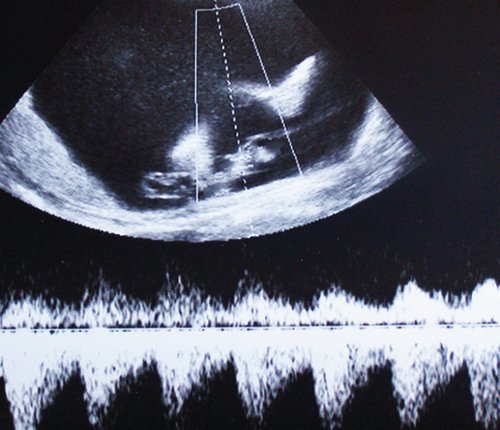
Рис. 8. Нормальная спектральная допплерограмма пуповинных артерий плода-реципиента сохраняется даже на фоне его терминального состояния, вплоть до внутриутробной гибели; выраженный полигидрамнион.
Рис. 9. Гипертрофическая компенсаторная кардиомегалия плода-реципиента (гестационный срок 26-27 нед): площадь сечения сердца занимает около 1/2 площади поперечного сечения грудной клетки, толщина миокарда желудочков и межжелудочковой перегородки сердца плода 6,5 и 6,8 мм соответственно.
Рис. 10. Пуповина плода-реципиента с признаками многократного «скручивания». Изменения зарегистрированы одновременно с допплерографическими признаками повышения резистентности венозного протока (см. рис. 11).
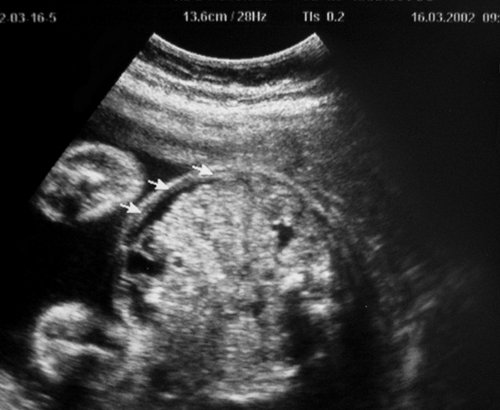
Рис. 12. Признаки развития сердечной недостаточности плода-реципиента вследствие гемодинамической перегрузки, начальный асцит (стрелки). IV, предтерминальная, стадия тяжелого хронического фето-фетального трансфузионного синдрома. Внутриутробная гибель обоих плодов наступила менее чем через 24 ч.
Межблизнецовые внутриплацентарные анастомозы были не единственным проявлением особенностей пуповинных сосудов. Для всех плодов при тяжелом хроническом ФФТС были характерны различные внеплацентарные изменения морфологии пуповин, выявленные антенатально в разных сочетаниях с помощью УЗИ: различная толщина пуповин близнецов за счет гипоплазии пуповинных сосудов меньшего плода, а также его гиповолемии; аномальное количество сосудов; децентрированное (краевое) отхождение пуповинных сосудов от плаценты; оболочечный ход сосудов пуповины; внеплацентарные межпуповинные анастомозы; многократно перекрученная, чрезмерно извитая пуповина большего плода; отсутствие спирального хода сосудов пуповины меньшего плода.
Патогномоничными для III клинической стадии тяжелой формы хронического ФФТС были гемодинамические изменения фетальных и пуповинных сосудов, регистрируемые с помощью спектральной допплерографии.
В то же время для пуповинных артерий плода-реципиента были характерны нормальные показатели кровотока, без повышения индексов сосудистой резистентности, регистрируемые вплоть до развития декомпенсированной трансфузии и гибели плодов. Особенностью плодовой гемодинамики близнеца-реципиента являлось нарастание объемной перегрузки с развитием застойной сердечной недостаточности, имевшей допплерографические проявления в виде повышения резистентности кровотока в субдиафрагмальных венозных сосудах плода прежде всего в венозном протоке. Ультразвуковым критерием позднего периода III клинической стадии ФФТС была регистрация допплерограммы венозного протока плода-реципиента с повышением систолодиастолического отношения (S/D) более 3,5. Таким образом, при тяжелом хроническом ФФТС именно патологические венозные допплерограммы реципиента свидетельствуют о скором развитии предтерминального состояния, что необходимо принимать во внимание при выработке акушерской тактики.
Вслед за регистрацией патологического спектра кровотока в венозном протоке быстро появлялись ультразвуковые признаки застойной сердечной недостаточности плода-реципиента: асцит, гидроторакс, гидроперикард либо анасарка, что отражало развитие IV клинической стадии тяжелого хронического ФФТС. Эта стадия в 2 случаях имела небольшую продолжительность (1-2 дня) и завершилась регистрацией внутриутробной гибели обоих пар плодов в 27 +4 и 28 +2 нед гестации; вес близнецов при рождении составил 690 и 1140 г и 810 и 1280 г, соответственно. В третьем случае при регистрации нарушений венозной гемодинамики реципиента было проведено оперативное родоразрешение в 30 +1 нед (вес при рождении составил 780 и 1630 г, меньший плод погиб интранатально, у большего плода имели место тяжелый интранатальный дистресс, полицитемия и неонатальные осложнения, связанные с недоношенностью).
Морфологическое исследование последа во всех случаях выявило наличие различных форм внутриплацентарных сосудистых анастомозов (артерио-артериальных, васкулярных цепей, артериовенозных, вено-венозных и сочетанных форм), а также внеплацентарных пуповинных аномалий.
В качестве иллюстрации синдрома острой межблизнецовой трансфузии и селективной задержки роста одного из плодов приводим клинические наблюдения.
Рис. 13. Беременность 31 нед. Монохориальная моноамниотическая двойня. Острая межблизнецовая трансфузия. Выраженное острое многоводие.
Рис. 14. Беременность 35-36 нед. Дискордантный рост монозиготных близнецов. Поперечные сечения туловищ плодов, имеющие разные диаметры и окружности. Допплерографически регистрировались признаки повышения резистентности в пуповинных артериях обоих плодов, венозная фетальная гемодинамика без изменений.
Выводы
В современной акушерской клинике сонография имеет безусловный приоритет как в первичной диагностике фето-фетального трансфузионного синдрома, так и в определении его клинической стадии, оценке гемодинамики фетоплацентарных систем плодов, их функционального состояния, прогнозировании перинатального исхода, дифференциальном диагнозе с другими вариантами осложнений монохориального многоплодия. Адекватный диагноз является необходимым условием выработки индивидуальной терапевтической тактики и cпособствует улучшению перинатальных результатов.
Литература
УЗИ сканер WS80
Идеальный инструмент для пренатальных исследований. Уникальное качество изображения и весь спектр диагностических программ для экспертной оценки здоровья женщины.
Фето фетальный синдром что
Фетофетальный трансфузионный синдром является крайне тяжелым осложнением монохориальной многоплодной беременности и встречается примерно в 10–15 % случаев. Причины его возникновения до конца не изучены, предполагают, что ФФТС связан с нарушением формирования плаценты, поздним разделением плодов, негативным влиянием внешних повреждающих факторов и дефицитом кровотока в матке беременной. ФФТС вызывает отклонения в развитии сердечно-сосудистой системы как во внутриутробном, так и в постнатальном периоде. Патологии, возникающие при этом, оказывают влияние на организм в целом и без своевременной диагностики и правильно подобранного метода лечения оказываются летальными до 100 % случаев.
Цель работы: анализ литературы, посвященной современным представлениям о влияния ФФТС на развитие сердечно-сосудистой системы монохориальной двойни во внутриутробном периоде. Раскрытие роли кардиоваскулярных нарушений в возникновении патологий организма в целом в постнатальном периоде.
Начиная со второй половины прошлого века в сфере научного исследования акушерства и гинекологии особое внимание уделялось закономерности повышенного риска развития сердечно-сосудистых патологий у монохориальных двоен в пре- и постнатальном периоде. Постепенно изучение данной проблемы привело ученых к выводу о существовании определенных процессов во внутриутробном периоде, которые нарушают поступление необходимых для развития сердечно-сосудистой системы веществ у близнецов. Такие процессы названы фетофетальным трансфузионным синдромом (ФФТС), который был впервые описан в конце XIX в. немецким гинекологом Фридрихом Шацом [1]. ФФТС является следствием развития глубоких анастомозов в сосудистой сети плаценты, в результате чего кровотоки плодов могут соединяться, вызывая диспропорцию в объёмах [2]. Таким образом, возникает нарушение в системе кровообращения двойни так, что один плод – «донор» испытывает недостаток пластических веществ и кислорода, а другой плод – «реципиент» подвержен действию избыточно поступающего объема крови. Этот процесс происходит из-за соединения сосудов плода и образования артериовенозного шунта. Выделяют два вида таких шунтов: поверхностные, которые находятся на основании стенки хориона – артерио-артериальные (АА) и вено-венозные (ВВ), и глубокие, расположенные в толще плаценты. Глубокие анастомозы обеспечивают поступление артериальной крови одного плода в венозную систему другого, образуя артериовенозные шунты (АВ) [2]. Существуют 5 степеней тяжести ФФТС, основанных на диаметре, количестве, направлении тока крови анастомозов и выраженности компенсаторных реакций двойни. Несмотря на то, что анастомозы между плодами имеются при всех монохориальных двойнях, ФФТС обычно формируется при диамниотических двойнях. Это связано с тем, что при моноамниотических беременностях больше двунаправленных поверхностных анастомозов, чем при диамниотических.
Основные особенности влияния ФФТС на организм человека могут быть изучены в результате сравнения протекания гестационного периода и родов беременных одним плодом и двойней, а также частоты постнатальных нарушений у детей. Согласно статистическим данным, частота преждевременных родов при одноплодной беременности составляет около 7 %, а при двуплодной – 49 %. Также масса тела при рождении, независимо от гестационного срока, будет 20 секунд. При этом существует вероятность перехода данного состояния в синдром внезапной детской смерти в постнатальном периоде [19].
Также у ребенка, который испытывал снижение ОЦК, после рождения возникают церебральные нарушения, связанные с рядом причин. Во-первых, с образованием кист белого вещества, формирующихся в результате длительной гипоксии и осложненной беременности, которыми могут стать арахноидальные кисты. Эти новообразования начинают оказывать давление на мозговые оболочки, что приводит к увеличению ликворопродукции. Следствием является увеличение внутричерепного давления и гидроцефалия, которые проявляются головной болью, срыгиванием, рвотой, потерей аппетита, вялостью, беспокойным сном, судорогами, гипотонусом и гипертонусом конечностей, неспособностью координировать движения, также возможны нарушения зрения и слуха. Во-вторых, церебральные патологии связаны с нарушением выделительной функции почек, что ведет к накоплению остаточных продуктов белкового обмена, оказывающих токсическое действие на головной мозг. Самые тяжелые поражения нервной системы могут проявляться такими аномалиями строения мозга, как агенезия борозд, агирия, недоразвитие серого вещества в больших полушариях головного мозга, полимикрогирия, гетеротопия [24]. По данным различных научных деятелей неврологические и нервно-психические расстройства встречаются среди 18–26 % выживших при ФФТС [25]. Таким образом, ФФТС оказывает значительное воздействие на организмы близнецов и в постнатальном периоде.
Заключение
ФФТС действительно вызывает отклонения сердечно-сосудистой системы как во внутриутробном, так и в постнатальном периоде. Патологии, возникающие при этом, оказывают влияние на организм в целом [26]. Поэтому необходимо проводить раннюю диагностику беременных с монохориальной двойней для выявления признаков нарушений и своевременного контроля над развитием ФФТС. В качестве рекомендаций для диагностики можно выделить следующие критерии УЗИ: наличие монохориальности (может быть определена с 4-й недели при использовании трансвагинального датчика) и максимального свободного кармана околоплодных вод одного плода менее 2,0 см и более 8,0 см второго плода [7]. С помощью классификации стадий ФФТС по Quintero и данных критериев возможно сравнивать различные способы лечения и прогнозировать выживаемость после врачебных вмешательств. При этом до установления типа хориальности все двуплодные беременности следует относить к группе риска ФФТС. Выбор тактики лечения ФФТС зависит от гестационного срока, анатомических особенностей матери, места прикрепления плаценты, возможности проведения фетоскопии, технического обеспечения. Консервативная терапия признана неэффективной, используются только хирургические методы: фетоскопическая коагуляция анастомозов плаценты, фетоскопическая лазерная коагуляция пуповины, амниоредукция или серийный амниодренаж, септостомия или прерывание беременности [2, 18, 27].