Применение ферросплавов для легирования различных сталей и сплавов
| В статье рассматривается процесс выплавки сталей с использованием для легирования различных ферросплавов. |
Обыкновенная сталь (железоуглеродистый сплав, содержащий более 45% железа и с объемом углерода до 2,14%) имеет определенную прочность, твердость, коррозионную стойкость, хладо- и жаростойкость, сопротивляемость нагрузкам. Когда же требуется получить сталь «особого назначения» с улучшенными характеристиками для конкретных условий эксплуатации, ей придают необходимые свойства. Для этого во время выплавки в состав стали вводят дополнительные химические элементы.
Процесс ввода добавок называют легированием (от немецкого «legieren» – «сплавлять»), а полученные стали – легированными. В современной металлургии используют разные способы легирования. Самым распространённым способом является введение в жидкий расплав металла специальных материалов в виде сплава железа с одним или несколькими химическими элементами. Такие материалы называются ферросплавами.
Производство ферросплавов
Ферросплавы получают из шихтовых материалов (руды или рудного концентрата) путём восстановления окислов основного химического элемента. Руду применяют в том случае, если содержание элементов для восстановления в ней достаточно высоко. Если в руде мало нужных элементов, то используют подготовленный рудный концентрат. Например, ферровольфрам (основные марки ФВ65, ФВ70, ФВ70Б) производится из вольфрамитового и шеелитового концентратов, содержащих свыше 55-65% триоксида вольфрама (WO3), а ферромолибден (основные марки ФМо52, ФМо55, ФМо58, ФМо60) – из молибденового концентрата, в состав которого входит не менее 53-58% молибдена (Mo).
Измельчённую руду или концентрат загружают в специальную ферросплавную электропечь, добавляя так называемый восстановитель (уголь, кокс, полукокс, торфяные брикеты и т.п.), более прочный и химически активный к базовому химическому элементу. В процессе плавки восстановитель извлекает ценный (ведущий) элемент из исходного сырья, а железо растворяет его, сплавляется с ним, выводит из зоны химической реакции, препятствуя обратным процессам. В итоге получается ферросплав с высоким содержанием нужного химического элемента. Конечная продукция может иметь вид кусков различных фракций, размер которых определен ГОСТами (в среднем 20-50 мм), а также блоков, чушек, гранул и т.п.
Производство стали
Как было упомянуто в начале статьи, сплав на основе железа называется сталью в том случае, если он содержит не более 2,14% углерода, плюс незначительное количество примесей, доля каждой из которых не превышает 1 % от общего объема металла. Таким образом, задача производства стали заключается в удалении из расплавленного исходного сырья (руды, чугуна, металлического лома, стружки и т.п.) лишнего углерода, а также минимизации вредных примесей – фосфора и серы, которые придают стали хрупкость и ломкость.
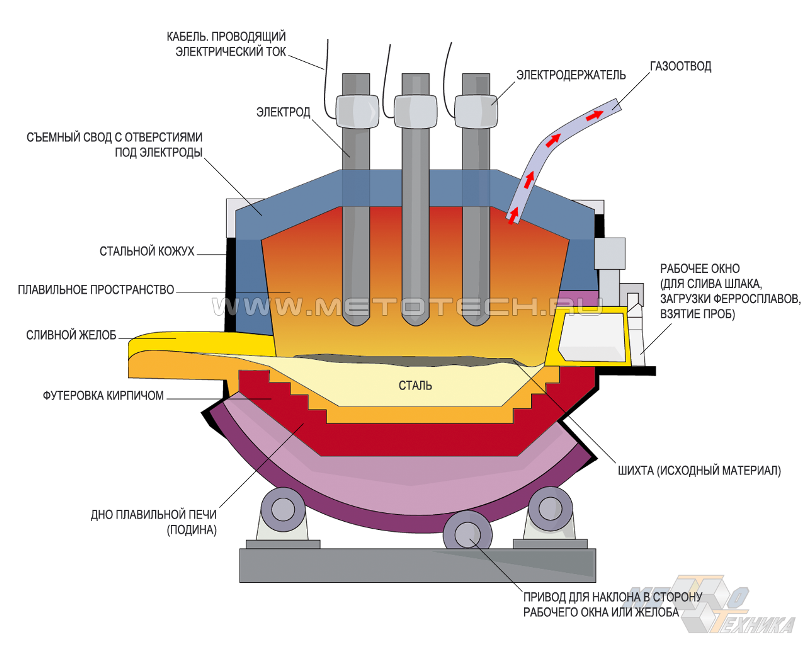
Процесс выплавки стали состоит из нескольких этапов. На первом, окислительном этапе, расплавляется шихта, происходит процесс окисления ряда химических элементов, включая углерод, фосфор превращается в первичный шлак, который удаляется из печи. На втором этапе расплав хорошо прогревается и закипает – сгорает лишний углерод и снова удаляют шлак. На третьем, восстановительном этапе, металл раскисляют (удаляют растворенный кислород), переводя серу в шлак, в расплав вводятся легирующие добавки для того, чтобы химический состав металла довести до заданного ГОСТами, и готовят к выпуску.
Рисунок 1. Конструкция печи для выплавки стали.
Легирование ферросплавами
Чтобы довести сталь до предусмотренного ГОСТом химического состава используют ферросплавы. Их вводят в разные периоды плавки стали. Например, ферроникель (основные марки ФН4 и ФН6) вводится в первый период – окислительный, из-за того, что никель не окисляется в печи, но содержит водород, который при нагреве превращается в газ. Этот газ и удаляется на втором этапе, в процессе кипения стали. В свою очередь феррониобий (основные марки ФН0, ФН1, ФН2, ФН3 и ФН4) и феррованадий (основные марки ФВд35 и ФВд50) хорошо окисляются, поэтому их вводят в конце плавки стали.
Рисунок 2. Ферросплавы.
Способы легирования и классификация стали
Помимо технологии легирования стали ферросплавами, в металлургической отрасли применяют еще ряд способов достижения в ней нужной концентрации химических элементов. Это может быть сделано путем сплавления стали с чистыми металлами, природными («сырыми») материалами, отходами производств, вторичным сырьем и т.д. После процесса легирования сталь классифицируют как низко-, средне- или высоколегированную, содержащую до 4%, до 11%, и свыше 11% легирующего элемента, соответственно.
Достоинства и недостатки легирования ферросплавами
Важным достоинством ферросплавов является то, что у большинства из них температура плавления ниже температуры плавления чистого металла. Благодаря этому окислы ведущего элемента ферросплава восстанавливаются при более низкой температуре, и происходит это полнее, быстрее, с меньшими энергетическими и финансовыми затратами. Техническая стоимость легирующего элемента в ферросплаве ниже, чем в чистом металле, что в определенной степени снижает и стоимость стали.
Кроме того, ферросплавы технологичнее чистого металла, они проще растворяются, что упрощает введение легирующего элемента в расплав, способствует минимизации угара и безвозвратных потерь массы легирующего элемента. К недостаткам ферросплавов относят высокую энерго-, трудо- и материалоемкость при их производстве, а также повышенные затраты на дробление, смешение и брикетирование перед отправкой готового продукта потребителю.
телефоны:
8 (800) 200-52-75
(495) 366-00-24
(495) 504-95-54
(495) 642-41-95
Ферросплавы
Кратко определяя, что такое ферросплавы и их применение, можно сказать – это категория соединений на основе или с присутствием железа, преимущественно используемых под легирование стали. Существует две причины востребованности подобных сплавов. Во-первых, технологически, легирование ферросплавами обходится дешевле, чем применение чистых металлов. Во-вторых, получаемые сплавы железа характеризуются более низкими температурами плавления, что упрощает процесс легирования стали. Ферросплавы (англ. – ferroalloys) очень востребованы в мировой металлургии.
Производство ферросплавов
Сырьевая база этого технологического процесса представляет собой разнообразные руды или концентраты. В частности, руда востребована в производстве следующих групп соединений:
Причина тому – высокий процент окислов элемента, подлежащего восстановлению в составе руд. Напротив, металлургия ферросплавов железа и тугоплавких металлов использует в качестве сырья рудные концентраты. Это связано с низкой концентрацией полезных элементов. Чтобы повысить эффективность, руду предварительно обогащают, получая из нее концентрат требуемого окисла.
Как видно, в основе производства ферросплавов лежит реакция восстановления. Это задает определенные требования по выбору реагентов:
Второе условие обусловлено способностью железа, понижать активность элементов, в частности препятствовать их окислению.
Ферросплавы
Ферросплавы
— сплавы железа с другими элементами (Cr, Si, Mn, Ti и др.), применяемые главным образом для раскисления и легирования стали (напр., феррохром, ферросилиций). К ферросплавам условно относят также некоторые сплавы, содержащие железо лишь в виде примесей (силикокальций, силикомарганец и др.), и некоторые металлы и неметаллы (Mn, Cr, Si) с минимальным содержанием примесей. Получают из руд или концентратов в электропечах или плавильных шахтах (горнах). Как правило, стоимость металла в виде ферросплава ниже, чем стоимость его в чистом виде. Это связано, в частности, с тем, что руда обычно содержит — в том или ином виде — железо, при переработке переходящее в сплав вместе с основным компонентом, и технологическая схема получения ферросплава оказывается одним из самых коротких и дешевых путей переработки сырья. В то же время для получения чистого сплава в технологию приходится вводить дополнительные этапы, усложняющие процесс и увеличивающие затраты. При этом получение железистого металла может быть либо полностью исключено либо являться одним из промежуточных этапов, когда получаемый передельный ферросплав перерабатывается на чистый металл. При восстановительной плавке железо, растворяя основной элемент, снижает его активность, понижает температуру плавления сплава. При легировании и раскислении стали и сплавов использование легирующего элемента в виде ферросплава повышает его усвоение расплавом, снижает угар.
Ферросплавное производство
Ферросплавное производство, получение ферросплавов на специализированных заводах чёрной металлургии. Наиболее распространён электротермический (электропечной) способ получения ферросплавов (т. н. электроферросплавов); по виду восстановителя он разделяется на углевосстановительный, которым получают углеродистые ферросплавы (5–8% С) и все кремнистые сплавы, и металлотермический (к нему условно относят и силикотермический), которым получают сплавы с пониженным содержанием углерода (0,01–2,5% С).Углевосстановительным процессом (см. Карботермия), осуществляемым главным образом в руднотермических печах мощностью 16,5–72 Мва, получают ферросилиций, кристаллический кремний, силикоалюминий, силикокальций, ферросиликокальций, силикомарганец, силикохром, углеродистый ферромарганец и феррохром, феррофосфор, комплексные сплавы на кремнистой основе, а также низкофосфористый марганцевый шлак; производство доменных ферросплавов очень незначительно по масштабам и постоянно сокращается (бедный ферросилиций и ферромарганец), т.к. они больше загрязнены примесями и стоят дороже электроферросплавов.
Низкоуглеродистые (рафинированные) ферросплавы получают в дуговых (рафинировочных) электропечах мощностью 2,5–5,5 Мва металлотермическим способом (см. Металлотермия). силикотермическим (см. Силикотермия) – низко- и безуглеродистые сплавы марганца и хрома, феррованадий (в шихту добавляют алюминий), ферровольфрам (в шихту добавляют коксик), силикоцирконий, алюминотермическим (см. Алюминотермия) – металлический хром, безуглеродистый феррохром, феррониобий, ферробор, силикоцирконий, различные лигатуры с редкими и редкоземельными металлами. Среднеуглеродистый феррохром получают также в конвертерах с кислородным дутьём (из углеродистого феррохрома). Для получения азотсодержащих (азотированных) сплавов марганца, хрома и ванадия применяют электропечи сопротивления и индукционные печи. Внепечным алюминотермическим способом выплавляют ферротитан, металлический хром и ванадий, внепечным силикотермическим способом – ферромолибден (в шихту добавляют алюминий).
По объёму производства разделяют так называемые «большие» и «малые» ферросплавы.
Кремнистые ферросплавы
Кремний — элемент главной подгруппы четвёртой группы третьего периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 14. Обозначается символом Si (лат. Silicium).
В промышленности кремний технической чистоты получают, восстанавливая расплав SiO2 коксом при температуре около 1800 °C в руднотермических печах шахтного типа. Чистота полученного таким образом кремния может достигать 99,9 % (основные примеси — углерод, металлы). Возможна дальнейшая очистка кремния от примесей.
Очистка в лабораторных условиях может быть проведена путём предварительного получения силицида магния Mg2Si. Далее из силицида магния с помощью соляной или уксусной кислот получают газообразный моносилан SiH4. Моносилан очищают ректификацией, сорбционными и др. методами, а затем разлагают на кремний и водород при температуре около 1000 °C.
Технический кремний находит следующие применения:
Cверхчистый кремний преимущественно используется для производства одиночных электронных приборов (нелинейные пассивные элементы электрических схем) и однокристальных микросхем. Чистый кремний, отходы сверхчистого кремния, очищенный металлургический кремний в виде кристаллического кремния являются основным сырьевым материалом для солнечной энергетики. Монокристаллический кремний — помимо электроники и солнечной энергетики используется для изготовления зеркал газовых лазеров. Соединения металлов с кремнием — силициды — являются широкоупотребляемыми в промышленности (например, электронной и атомной) материалами с широким спектром полезных химических, электрических и ядерных свойств (устойчивость к окислению, нейтронам и др.). Силициды ряда элементов являются важными термоэлектрическими материалами. Соединения кремния служат основой для производства стекла и цемента. Производством стекла и цемента занимается силикатная промышленность. Она также выпускает силикатную керамику — кирпич, фарфор, фаянс и изделия из них. Широко известен силикатный клей, применяемый в строительстве как сиккатив, а в пиротехнике и в быту для склеивания бумаги. Получили широкое распространение силиконовые масла и силиконы — материалы на основе кремнийорганических соединений.
Марганцевые ферросплавы
Ма́рганец — элемент побочной подгруппы седьмой группы четвёртого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 25. Обозначается символом Mn (лат. Manganum, ма́нганум, в составе формул по-русски читается как марганец, например, KMnO4 — калий марганец о четыре; но нередко читают и как манган). Простое вещество марганец (CAS-номер: 7439-96-5) — металл серебристо-белого цвета. Известны пять аллотропных модификаций марганца — четыре с кубической и одна с тетрагональной кристаллической решёткой
Распространённость в природе
Марганец — 14-й элемент по распространённости на Земле, а после железа — второй тяжёлый металл, содержащийся в земной коре (0,03 % от общего числа атомов земной коры). Весовое количество марганца увеличивается от кислых (600 г/т) к основным породам (2,2 кг/т). Сопутствует железу во многих его рудах, однако встречаются и самостоятельные месторождения марганца. В чиатурском месторождении (район Кутаиси) сосредоточено до 40 % марганцевых руд. Марганец, рассеянный в горных породах вымывается водой и уносится в Мировой океан. При этом его содержание в морской воде незначительно (10−7—10−6%), а в глубоких местах океана его концентрация возрастает до 0,3 % вследствие окисления растворённым в воде кислородом с образованием нерастворимого в воде оксида марганца, который в гидратированной форме (MnO2·xH2O) и опускается в нижние слои океана, формируя так называемые железо-марганцевые конкреции на дне, в которых количество марганца может достигать 45 % (также в них имеются примеси меди, никеля, кобальта). Такие конкреции могут стать в будущем источником марганца для промышленности. В России является остродефицитным сырьём, известны месторождения: «Усинское» в Кемеровской области, «Полуночное» в Свердловской, «Порожинское» в Красноярском крае, «Южно-Хинганское» в Еврейской автономной области, «Рогачёво-Тайнинская» площадь и «Северо-Тайнинское» поле на Новой Земле.
В промышленности марганец в виде ферромарганца применяется для «раскисления» стали при её плавке, то есть для удаления из неё кислорода. Кроме того, он связывает серу, что также улучшает свойства сталей. Введение до 12-13 % Mn в сталь (так называемая Сталь Гадфильда), иногда в сочетании с другими легирующими металлами, сильно упрочняет сталь, делает её твердой и сопротивляющейся износу и ударам (эта сталь резко упрочняется и становится тверже при ударах). Такая сталь используется для изготовления шаровых мельниц, землеройных и камнедробильных машин, броневых элементов и т. д. В «зеркальный чугун» вводится до 20 % Mn. Сплав 83 % Cu, 13 % Mn и 4 % Ni (манганин) обладает высоким электросопротивлением, мало изменяющимся с изменением температуры. Поэтому его применяют для изготовления реостатов и пр.Марганец вводят в бронзы и латуни.
Значительное количество диоксида марганца потребляется при производстве марганцево-цинковых гальванических элементов, MnO2 используется в таких элементах в качестве окислителя-деполяризатора. Соединения марганца также широко используются как в тонком органическом синтезе (MnO2 и KMnO4 в качестве окислителей), так и промышленном органическом синтезе (компоненты катализаторов окисления углеводородов, например, в производстве терефталевой кислоты окислением p-ксилола, окисление парафинов в высшие жирные кислоты). Цены на металлический марганец в слитках чистотой 95 % в 2006 году составили в среднем 2,5 долл/кг. Арсенид марганца обладает гигантским магнитокалорическим эффектом, усиливающимся под давлением. Теллурид марганца перспективный термоэлектрический материал(термо-э.д.с 500 мкВ/К).
Хромистые ферросплавы
Хром — элемент побочной подгруппы шестой группы четвёртого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 24. Обозначается символом Cr (лат. Chromium). Простое вещество хром (CAS-номер: 7440-47-3) — твёрдый металл голубовато-белого цвета.
Нахождение в природе
Хром является довольно распространённым элементом (0,02 масс. долей, %). Основные соединения хрома — хромистый железняк (хромит) FeO·Cr2O3. Вторым по значимости минералом является крокоит PbCrO4.
Хром встречается в природе в основном в виде хромистого железняка Fe(CrO2)2 (хромит железа). Из него получают феррохром восстановлением в электропечах коксом (углеродом): FeO · Cr2O3 + 4C → Fe + 2Cr + 4CO↑ Феррохром применяют для производства легированных сталей.
Чтобы получить чистый хром, реакцию ведут следующим образом:
Хром — важный компонент во многих легированных сталях (в частности, нержавеющих), а также и в ряде других сплавов. Используется в качестве износоустойчивых и красивых гальванических покрытий (хромирование). Хром применяется для производства сплавов: хром-30 и хром-90, незаменимых для производства сопел мощных плазмотронов и в авиакосмической промышленности.
Ферровольфрам
Ферровольфрам — сплав железа и вольфрама (ферросплав), используемый в чёрной металлургии для легирования стали и сплавов. Исходные материалы Основные минералы вольфрама, имеющие промышленное значение — ферберит FeWO4, гюбнерит MnWO4, вольфрамит (Fe,Mn)WO4 и шеелит CaWO44. Руды вольфрама обычно содержат 0,2-0,5 % WO3, часто в них присутствуют минералы молибдена, олова, меди, мышьяка и других элементов. Обогащают руды различными гравитационными методами — отсадкой, концентрацией на столах и в шлюзах. Получаемые концентраты обычно содержат 55-65 % WO3[2]. Высокожелезистые руды могут подвергаться дополнительному обогащению в магнитных сепараторах; для отделения шеелита, сульфидов, доводки концентратов применяют флотацию и электростатическую сепарацию. Шеелитовые руды обогащают флотацией в жирных кислотах (олеиновая кислота, олеат натрия, жидкое мыло) с использованием в качестве вспенивателя соснового масла или креозола.
Ферровольфрам используется в чёрной металлургии для легирования стали и сплавов. Вольфрам входит в состав быстрорежущих, жаропрочных, магнитных, некоторых конструкционных сталей, он увеличивает временное сопротивление разрыву и предел текучести стали, повышает её прочность и твёрдость при высоких температурах, увеличивает интенсивность намагничивания и улучшае т коэрцитивные свойства магнитных сталей.
Ферромолибден
Ферромолибден — ферросплав, содержащий 50-60 % молибдена.
Ферромолибден используют вместо чистого молибдена при легировании стали, чугуна и сплавов. Так, в стали содержание молибдена составляет от 0,1-0,3 % (легированная сталь) до 3-10 % (инструментальная сталь). Молибден улучшает закаливаемость и прокаливаемость стали, увеличивает её вязкость, ликвидирует отпускную хрупкость хромоникелевой стали, способствует сохранению свойств стали при высоких температурах. Добавка молибдена в чугун увеличивает его прочность и сопротивление износу.
Сырьем для производства ферромолибдена служат кварцево-молибденитовые, медно-молибденовые и молибдено-вольфрамовые руды, основным молибденсодержащим минералом которых является молибденит MoS2. Обогащают такое сырье преимущественно флотацией. В результате обогащения получают молибденовые концентраты, содержащие до 35 % серы — как в составе сульфида молибдена MoS2, так и в сульфидах прочих элементов — меди, железа и т. п.
Феррованадий
В чёрной металлургии феррованадий применяют при легировании стали, сплавов и чугунов для получения мелкокристаллической структуры, повышения ударной вязкости и устойчивости стали против знакопеременных нагрузок, повышения прокаливаемости. Феррованадий азотированный предназначен для легирования быстрорежущих, низколегированных, нержавеющих, морозостойких сталей ванадием и азотом. Поставляется в виде кусков массой 5-15 кг в стальных барабанах.
Cплавы щёлочноземельных металлов
Щё́лочноземе́льные мета́ллы — химические элементы 2-й группы периодической таблицы элементов: бериллий, магний, кальций, стронций, барий и радий. Названы так потому, что их оксиды — «земли» (по терминологии алхимиков) — сообщают воде щелочную реакцию. Соли щёлочноземельных металлов, кроме радия, широко распространены в природе в виде минералов.
Щёлочноземельные металлы имеют электронную конфигурацию внешнего энергетического уровня ns², и являются s-элементами, наряду с щелочными металлами. Имея два валентных электрона, щёлочноземельные металлы легко их отдают, и во всех соединениях имеют степень окисления +2 (очень редко +1). Химическая активность щёлочноземельных металлов растёт с ростом порядкового номера. Бериллий в компактном виде не реагирует ни с кислородом, ни с галогенами даже при температуре красного каления (до 600 °C, для реакции с кислородом и другими халькогенами нужна ещё более высокая температура, фтор — исключение). Магний защищён оксидной плёнкой при комнатной температуре и более высоких (до 650 °C) температурах и не окисляется дальше. Кальций медленно окисляется и при комнатной температуре вглубь (в присутствии водяных паров), и сгорает при небольшом нагревании в кислороде, но устойчив в сухом воздухе при комнатной температуре. Стронций, барий и радий быстро окисляются на воздухе, давая смесь оксидов и нитридов, поэтому их, так же и как щелочные металлы (и кальций), хранят под слоем керосина. Оксиды и гидроксиды щёлочноземельных металлов имеют тенденцию к усилению основных свойств с ростом порядкового номера: Be(OH)2 — амфотерный, нерастворимый в воде гидроксид, но растворим в кислотах (а также проявляет кислотные свойства в присутствии сильных щелочей), Mg(OH)2 — слабое основание, нерастворимое в воде, Ca(OH)2 — сильное, но малорастворимое в воде основание, Sr(OH)2 — лучше растворимо в воде, чем гидроксид кальция, сильное основание (щёлочь) при высоких температурах, близких к точке кипения воды (100 °C), Ba(OH)2 — сильное основание (щёлочь), по силе не уступающее KOH или NaOH, и Ra(OH)2 — одна из сильнейших щелочей, очень коррозионное вещество.
Нахождение в природе
Все щёлочноземельные металлы имеются (в разных количествах) в природе. Ввиду своей высокой химической активности все они в свободном состоянии не встречаются. Самым распространённым щёлочноземельным металлом является кальций, количество которого равно 3,38 % (от массы земной коры). Немногим ему уступает магний, количество которого равно 2,35 % (от массы земной коры). Распространены в природе также барий и стронций, которых соответственно 0,05 и 0,034 % от массы земной коры. Бериллий является редким элементом, количество которого составляет 6·10−4% от массы земной коры. Что касается радия, который радиоактивен, то это самый редкий из всех щёлочноземельных металлов, но он в небольшом количестве всегда содержится в урановых рудах. В частности, он может быть выделен оттуда химическим путём. Его содержание равно 1·10−10% (от массы земной коры)
Феррониобий
Феррониобий — ферросплав, содержащий около 60 % Nb (или Nb + Ta), 10-12,5 % Si, 2-6 % Al, 3-8 % Ti (остальное Fe и примеси); выплавляют электропечным алюминотермическим способом из пирохлорового концентрата или технической пятиокиси ниобия. Феррониобий применяют при выплавке конструкционной стали и жаропрочных сплавов.
Ферротитан и титансодержащие сплавы
Ферротитан — ферросплав, содержащий до 35 или более 60 % Ti, 1-7 % Al, 1-4,5 % Si, до 3 % Cu (остальное Fe и примеси).
Получают внепечным алюминотермическим способом из ильменитового концентрата и титановых отходов (низкопроцентный ферротитан) или сплавлением в электрической печи железных и титановых отходов (высокопроцентный ферротитан).
Ферротитан применяют для раскисления и легирования стали.
Тита́н (лат. Titanium; обозначается символом Ti) — элемент побочной подгруппы четвёртой группы, четвёртого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 22. Простое вещество титан (CAS-номер: 7440-32-6) — лёгкий металл серебристо-белого цвета. Существует в двух кристаллических модификациях: α-Ti с гексагональной плотноупакованной решёткой, β-Ti с кубической объёмно-центрированной упаковкой, температура полиморфного превращения α↔β 883 °C[1]. Температура плавления 1660±20 °C
Нахождение в природе
Титан находится на 10-м месте по распространённости в природе. Содержание в земной коре 0,57 % по массе, в морской воде 0,001 мг/л. В ультраосновных породах 300 г/т, в основных — 9 кг/т, в кислых 2,3 кг/т, в глинах и сланцах 4,5 кг/т. В земной коре титан почти всегда четырёхвалентен и присутствует только в кислородных соединениях. В свободном виде не встречается. Титан в условиях выветривания и осаждения имеет геохимическое сродство с Al2O3. Он концентрируется в бокситах коры выветривания и в морских глинистых осадках. Перенос титана осуществляется в виде механических обломков минералов и в виде коллоидов. До 30 % TiO2 по весу накапливается в некоторых глинах. Минералы титана устойчивы к выветриванию и образуют крупные концентрации в россыпях. Известно более 100 минералов, содержащих титан. Важнейшие из них: рутил TiO2, ильменит FeTiO3, титаномагнетит FeTiO3 + Fe3O4, перовскит CaTiO3, титанит CaTiSiO5. Различают коренные руды титана — ильменит-титаномагнетитовые и россыпные — рутил-ильменит-цирконовые.
Титановый памятник Гагарину на Ленинском проспекте в Москве.
Металл применяется в: химической промышленности (реакторы, трубопроводы, насосы, трубопроводная арматура), военной промышленности (бронежилеты, броня в авиации, корпуса подводных лодок), промышленных процессах (опреснительных установках, процессах целлюлозы и бумаги), автомобильной промышленности, сельскохозяйственной промышленности, пищевой промышленности, украшениях для пирсинга, медицинской промышленности (протезы, остеопротезы), стоматологических и эндодонтических инструментах, зубных имплантатах, спортивных товарах, ювелирных изделиях (Александр Хомов), мобильных телефонах, лёгких сплавах и т. д. Является важнейшим конструкционным материалом в авиа-, ракето-, кораблестроении. Титановое литье выполняют в вакуумных печах в графитовые формы. Также используется вакуумное литье по выплавляемым моделям. Из-за технологических трудностей, в художественном литье используется ограниченно. Первой в мировой практике монументальной литой скульптурой из титана является памятник Юрию Гагарину на площади его имени в Москве.
Титан является легирующей добавкой во многих легированных сталях и большинстве спецсплавов.
Нитинол (никель-титан) — сплав, обладающий памятью формы, применяемый в медицине и технике.
Алюминиды титана являются очень стойкими к окислению и жаропрочными, что в свою очередь определило их использование в авиации и автомобилестроении в качестве конструкционных материалов.
Ферробор, ферроборал и лигатуры с бором
Бор — элемент главной подгруппы третьей группы, второго периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 5. Обозначается символом B (лат. Borum). В свободном состоянии бор — бесцветное, серое или красное кристаллическое либо тёмное аморфное вещество. Известно более 10 аллотропных модификаций бора, образование и взаимные переходы которых определяются температурой, при которой бор был получен
Нахождение в природе
Среднее содержание бора в земной коре 4 г/т. Несмотря на это, известно около 100 собственных минералов бора; в «чужих» минералах он почти не встречается. Это объясняется прежде всего тем, что у комплексных анионов бора (а именно в таком виде он входит в большинство минералов) нет достаточно распространенных аналогов. Почти во всех минералах бор связан с кислородом, а группа фторсодержащих соединений совсем малочисленна. Элементарный бор в природе не встречается. Он входит во многие соединения и широко распространён, особенно в небольших концентрациях; в виде боросиликатов и боратов, а также в виде изоморфной примеси в минералах входит в состав многих изверженных и осадочных пород. Бор известен в нефтяных и морских водах (в морской воде 4,6 мг/л[4]), в водах соляных озёр, горячих источников и грязевых вулканов.
Бор (в виде волокон) служит упрочняющим веществом многих композиционных материалов. Также бор часто используют в электронике для изменения типа проводимости кремния. Бор применяется в металлургии в качестве микролегирующего элемента, значительно повышающего прокаливаемость сталей. Бор применяется и в медицине при бор-нейтронозахватной терапии (способ избирательного поражения клеток злокачественных опухолей)
Карбид бора применяется в компактном виде для изготовления газодинамических подшипников. Пербораты / пероксобораты (содержат ион [B2(O2)2(OH)4]2−) Технический продукт содержит до 10,4 % «активного кислорода», на их основе производят отбеливатели, «не содержащие хлор» («персиль», «персоль» и др.). Отдельно также стоит указать на то что сплавы бор-углерод-кремний обладают сверхвысокой твёрдостью и способны заменить любой шлифовальный материал (кроме алмаза, нитрида бора по микротвёрдости), а по стоимости и эффективности шлифования (экономической) превосходят все известные человечеству абразивные материалы.
Сплав бора с магнием (диборид магния MgB2) обладает, на данный момент, рекордно высокой критической температурой перехода в сверхпроводящее состояние среди сверхпроводников первого рода. Появление вышеуказанной статьи стимулировало большой рост работ по этой тематике. Борная кислота (H3BO3) широко применяется в атомной энергетике в качестве поглотителя нейтронов в ядерных реакторах типа ВВЭР (PWR) на «тепловых» («медленных») нейтронах. Благодаря своим нейтронно-физическим характеристикам и возможности растворяться в воде, применение борной кислоты делает возможным плавное (не ступенчатое) регулирование мощности ядерного реактора путем изменения её концентрации в теплоносителе — так называемое «борное регулирование». Нитрид бора активированный углеродом является люминофором с свечением в УФ от синего до жёлтого цвета и обладает самостоятельной фосфоресценцией в темноте и активируется органическими веществами при нагреве до 1000 °C. Изготовление люминофоров из нитрида бора, состава BN/C не имеет промышленного назначения, но являлся широкой любительской практикой в первой половине XX века.
Бороводороды и борорганические соединения
Ряд производных бора (бороводороды) являются чрезвычайно эффективными ракетными топливами (диборан B2H6, пентаборан, тетраборан и др.), а некоторые полимерные соединения с водородом и углеродом являются чрезвычайно стойкими к химическим воздействиям и высоким температурам (как широко известный пластик Карборан-22).
Боразон и его гексагидрид
Нитрид бора (боразон) подобен (по составу электронов) углероду. На его основе образуется обширная группа соединений, чем-то подобные органическим. Так, гексагидрид боразона (H3BNH3, похож на этан по строению) при обычных условиях твёрдое соединение с плотностью 0,78 г/см3, содержит почти 20 % водорода по весу. Его могут использовать водородные топливные элементы, питающие электромобили
Сплавы с алюминием
Алюми́ний — элемент главной подгруппы третьей группы третьего периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 13. Обозначается символом Al (лат. Aluminium). Относится к группе лёгких металлов. Наиболее распространённый металл и третий по распространённости химический элемент в земной коре (после кислорода и кремния). Простое вещество алюминий (CAS-номер: 7429-90-5) — лёгкий, парамагнитный металл серебристо-белого цвета, легко поддающийся формовке, литью, механической обработке. Алюминий обладает высокой тепло- и электропроводностью, стойкостью к коррозии за счёт быстрого образования прочных оксидных плёнок, защищающих поверхность от дальнейшего взаимодействия.
Современный метод получения был разработан независимо американцем Чарльзом Холлом и французом Полем Эру в 1886 году. Он заключается в растворении оксида алюминия Al2O3 в расплаве криолита Na3AlF6 с последующим электролизом с использованием расходуемых коксовых или графитовых электродов. Такой метод получения требует больших затрат электроэнергии, и поэтому оказался востребован только в XX веке. Для производства 1000 кг чернового алюминия требуется 1920 кг глинозёма, 65 кг криолита, 35 кг фторида алюминия, 600 кг анодной массы и 17 тыс. кВт·ч электроэнергии постоянного тока
Кусок алюминия широко применяется как конструкционный материал. Основные достоинства алюминия в этом качестве — лёгкость, податливость штамповке, коррозионная стойкость (на воздухе алюминий мгновенно покрывается прочной плёнкой Al2O3, которая препятствует его дальнейшему окислению), высокая теплопроводность, неядовитость его соединений. В частности, эти свойства сделали алюминий чрезвычайно популярным при производстве кухонной посуды, алюминиевой фольги в пищевой промышленности и для упаковки. Основной недостаток алюминия как конструкционного материала — малая прочность, поэтому для упрочнения его обычно сплавляют с небольшим количеством меди и магния (сплав называется дюралюминий). Электропроводность алюминия всего в 1,7 раза меньше, чем у меди, при этом алюминий приблизительно в 4 раза дешевле за килограмм, но, за счёт в 3,3 раза меньшей плотности, для получения равного сопротивления его нужно приблизительно в 2 раза меньше по весу. Поэтому он широко применяется в электротехнике для изготовления проводов, их экранирования и даже в микроэлектронике при изготовлении проводников в чипах. Меньшую электропроводность алюминия (37 1/ом) по сравнению с медью (63 1/ом) компенсируют увеличением сечения алюминиевых проводников. Недостатком алюминия как электротехнического материала является наличие прочной оксидной плёнки, затрудняющей пайку. Благодаря комплексу свойств широко распространён в тепловом оборудовании.
Алюминий и его сплавы сохраняют прочность при сверхнизких температурах. Благодаря этому он широко используется в криогенной технике. Высокий коэффициент отражения в сочетании с дешевизной и лёгкостью напыления делает алюминий идеальным материалом для изготовления зеркал. В производстве строительных материалов как газообразующий агент. Алитированием придают коррозионную и окалиностойкость стальным и другим сплавам, например клапанам поршневых ДВС, лопаткам турбин, нефтяным платформам, теплообменной аппаратуре, а также заменяют цинкование. Сульфид алюминия используется для производства сероводорода. Идут исследования по разработке пенистого алюминия как особо прочного и лёгкого материала.
Алюминиево-магниевые Al-Mg (серия 5ххх). Сплавы системы Al-Mg характеризуются сочетанием удовлетворительной прочности, хорошей пластичности, очень хорошей свариваемости и коррозионной стойкости. Кроме того, эти сплавы отличаются высокой вибростойкостью. В сплавах этой системы, содержащих до 6 % Mg, образуется эвтектическая система соединения Al3Mg2 c твердым раствором на основе алюминия. Наиболее широкое распространение в промышленности получили сплавы с содержанием магния от 1 до 5 %. Рост содержания Mg в сплаве существенно увеличивает его прочность. Каждый процент магния повышает предел прочности сплава на 30 МПа, а предел текучести — на 20 МПа. При этом относительное удлинение уменьшается незначительно и находится в пределах 30…35 %.
Сплавы с содержанием магния до 3 % (по массе) структурно стабильны при комнатной и повышенной температуре даже в значительно нагартованном состоянии. С ростом концентрации магния в нагартованном состоянии структура сплава становится нестабильной. Кроме того, увеличение содержания магния свыше 6 % приводит к ухудшению коррозионной стойкости сплава. Для улучшения прочностных характеристик сплавы системы Al-Mg легируют хромом, марганцем, титаном, кремнием или ванадием. Попадания в сплавы этой системы меди и железа стараются избегать, поскольку они снижают их коррозионную стойкость и свариваемость. Алюминиево-марганцевые Al-Mn (серия 3ххх). Сплавы этой системы обладают хорошей прочностью, пластичностью и технологичностью, высокой коррозионной стойкостью и хорошей свариваемостью.
Основными примесями в сплавах системы Al-Mn являются железо и кремний. Оба этих элемента уменьшают растворимость марганца в алюминии. Для получения мелкозернистой структуры сплавы этой системы легируют титаном. Присутствие достаточного количества марганца обеспечивает стабильность структуры нагартованного металла при комнатной и повышенной температурах.
Алюминиево-медные Al-Cu (Al-Cu-Mg) (серия 2ххх). Механические свойства сплавов этой системы в термоупрочненном состоянии достигают, а иногда и превышают, механические свойства низкоуглеродистых сталей. Эти сплавы высокотехнологичны. Однако у них есть и существенный недостаток — низкое сопротивление коррозии, что приводит к необходимости использовать защитные покрытия. В качестве легирующих добавок могут встречаться марганец, кремний, железо и магний. Причем наиболее сильное влияние на свойства сплава оказывает последний: легирование магнием заметно повышает предел прочности и текучести. Добавка кремния в сплав повышает его способность к искусственному старению. Легирование железом и никелем повышает жаропрочность сплавов второй серии. Нагартовка этих сплавов после закалки ускоряет искусственное старение, а также повышает прочность и сопротивление коррозии под напряжением.
Сплавы системы Al-Zn-Mg (Al-Zn-Mg-Cu) (серия 7ххх). Сплавы этой системы ценятся за очень высокую прочность и хорошую технологичность. Представитель системы — сплав 7075 является самым прочным из всех алюминиевых сплавов. Эффект столь высокого упрочнения достигается благодаря высокой растворимости цинка (70 %) и магния (17,4 %) при повышенных температурах, резко уменьшающейся при охлаждении. Однако существенным недостатком этих сплавов является крайне низкая коррозионная стойкость под напряжением. Повысить сопротивление коррозии сплавов под напряжением можно легированием медью.
Нельзя не отметить открытой в 60-е годы закономерности: присутствие лития в сплавах замедляет естественное и ускоряет искусственное старение. Помимо этого, присутствие лития уменьшает удельный вес сплава и существенно повышает его модуль упругости. В результате этого открытия были разработаны новые системы сплавов Al-Mg-Li, Al-Cu-Li и Al-Mg-Cu-Li. Алюминиево-кремниевые сплавы (силумины) лучше всего подходят для литья. Из них часто отливают корпуса разных механизмов.
Алюминий как добавка в другие сплавы
Алюминий является важным компонентом многих сплавов. Например, в алюминиевых бронзах основные компоненты — медь и алюминий. В магниевых сплавах в качестве добавки чаще всего используется алюминий. Для изготовления спиралей в электронагревательных приборах используют (наряду с другими сплавами) фехраль (Fe, Cr, Al).
Когда алюминий был очень дорог, из него делали разнообразные ювелирные изделия. Так, Наполеон III заказал алюминиевые пуговицы, а Менделееву в 1889 г. были подарены весы с чашами из золота и алюминия. Мода на них сразу прошла, когда появились новые технологии его получения, во много раз снизившие себестоимость. Сейчас алюминий иногда используют в производстве бижутерии. В Японии алюминий используется в производстве традиционных украшений, заменяя серебро.
В стекловарении используются фторид, фосфат и оксид алюминия.
Алюминий зарегистрирован в качестве пищевой добавки Е173.
Алюминий и его соединения в ракетной технике
Алюминий и его соединения используются в качестве высокоэффективного ракетного горючего в двухкомпонентных ракетных топливах и в качестве горючего компонента в твёрдых ракетных топливах. Следующие соединения алюминия представляют наибольший практический интерес как ракетное горючее: Порошковый алюминий как горючее в твердых ракетных топливах. Применяется также в виде порошка и суспензий в углеводородах.
Cплавы с редкоземельными металлами
Редкоземе́льные элеме́нты — группа из 17 элементов, включающая лантан, скандий, иттрий и лантаноиды. Все эти элементы — металлы серебристо-белого цвета, при том все имеют сходные химические свойства (наиболее характерна степень окисления +3).
Нахождение в природе
Как правило, редкоземельные элементы встречаются в природе совместно. Они образуют весьма прочные окислы, галоидные соединения, сульфиды. Для лантаноидов наиболее характерны соединения трёхвалентных элементов. Исключение составляет церий, легко переходящий в четырёхвалентное состояние. Кроме церия четырёхвалентные соединения образуют празеодим и тербий. Двухвалентные соединения известны у самария, европия и иттербия. По физико-химическим свойствам лантаноиды весьма близки между собой. Это объясняется особенностью строения их электронных оболочек. Суммарное содержание редкоземельных элементов составляет более 100 г/т. Известно более 250 минералов, содержащих редкоземельные элементы. Однако к собственно редкоземельным минералам могут быть отнесены только 60 — 65 минералов, в которых содержание Ме2О3 превышает 5 — 8 %. Главнейшие минералы редких земель — монацит (Ce, La)PO4, ксенотим YPO4, бастнезит Ce[CO3](OH, F), паризит Ca(Ce, La)2[CO3]3F2, гадолинит Y2FeBe2Si2O10, ортит (Ca, Ce)2(Al, Fe)3Si3O12(O, OH), лопарит (Na, Ca, Ce)(Ti, Nb)O3, эшинит (Ce, Ca, Th)(Ti, Nb)2O6. Наиболее распространён в земной коре церий, наименее — тулий и лютеций. Несмотря на неограниченный изоморфизм, в группе редких земель в определённых геологических условиях возможна раздельная концентрация редких земель иттриевой и цериевой подгрупп. Например, с щелочными породами и связанными с ними постмагматическими продуктами преимущественное развитие получает цериевая подгруппа, а с постмагматическими продуктами гранитоидов с повышенной щёлочностью — иттриевая. Большинство фторкарбонатов обогащено элементами цериевой подгруппы. Многие тантало-ниобаты содержат иттриевую подгруппу, а титанаты и титано-тантало-ниобаты — цериевую. Некоторая дифференциация редких земель отмечается и в экзогенных условиях. Изоморфное замещение редких земель между собой, несмотря на разницу в их порядковых номерах, обусловлено явлениями «лантаноидного сжатия»: с увеличением порядкового номера происходит достройка внутренних, а не внешних электронных орбит, в результате чего объём ионов не увеличивается.
Селективное накопление редкоземельных элементов в минералах и горных породах может быть обусловлено различиями в их радиусах ионов. Дело в том, что радиусы ионов лантаноидов закономерно уменьшаются от лантана к лютецию. Вследствие этого возможно преимущественное изоморфное замещение в зависимости от степени различия в размерах замещённых ионов редкоземельных элементов. Так, в скандиевых, циркониевых и марганцевых минералах могут присутствовать только редкие земли ряда лютеций — диспрозий; в урановых минералах преимущественно накапливаются минералы средней части ряда (иттрий, диспрозий, гадолиний); в ториевых минералах должны концентрироваться элементы цериевой группы; в состав стронциевых и бариевых минералов могут входить только элементы ряда европий — лантан.
Редкоземельные элементы используют в различных отраслях техники: в радиоэлектронике, приборостроении, атомной технике, машиностроении, химической промышленности, в металлургии и др. Широко применяют La, Ce, Nd, Pr в стекольной промышленности в виде оксидов и других соединений. Эти элементы повышают светопрозрачность стекла. Редкоземельные элементы входят в состав стекол специального назначения, пропускающих инфракрасные лучи и поглощающих ультрафиолетовые лучи, кислотно- и жаростойких стекол. Большое значение получили редкоземельные элементы и их соединения в химической промышленности, например, в производстве пигментов, лаков и красок, в нефтяной промышленности как катализаторы. Редкоземельные элементы применяют в производстве некоторых взрывчатых веществ, специальных сталей и сплавов, как газопоглотители. Монокристаллические соединения редкоземельных элементов (а также стёкла) применяют для создания лазерных и других оптически активных и нелинейных элементов в оптоэлектронике.
Ферроникель и феррокобальт
Ферроникель — сплав железа и никеля (ферросплав), получаемый, главным образом, при восстановительной электроплавке окисленных никелевых руд и используемый для легирования стали и сплавов.
Среди других методов получения ферроникеля из окисленных никелевых руд (некоторые из которых уже не применяются, а другие были лишь опробованы и пока не нашли применения) можно отметить кричный процесс, шахтную плавку на ферроникель, доменную плавку на ферроникель, плавку в агрегате с погруженным факелом, получение ферроникеля из штейна и необычные варианты электроплавки (двухстадийная плавка с ферросилицием в качестве восстановителя, электроплавка в печи со вспененной ванной).